سرطان، واقعیتها و آمار 2017
دکتر شاهرخ مستور تهرانی
توضیح مترجم: اطلاعات و آمار این مقاله مربوط به جامعه آمریکا میباشد اما با توجه به جامعیت آن و اینکه هیچ مقاله بدیلی بر مبنای آمار داخلی وجود ندارد لذا به نظر میرسد که بتواند از جنبههای مختلف برای پزشکان و محققان کشورمان مفید واقع گردد.
واقعیتهای اصلی سرطان
- سرطان چیست؟
سرطان به گروهی از بیماریها اطلاق میشود که مشخصه آنها رشد خارج از کنترل و پخش سلولهای غیرطبیعی میباشد. اگر پخش سلولها را نتوان کنترل کرد، نتیجه آن مرگ خواهد بود. علت ایجاد بسیاری از سرطانها بهویژه آنهایی که در دوران کودکی اتفاق میافتند ناشناخته است اما عوامل بیرونی همچون سبک زندگی و مصرف دخانیات و عوامل داخلی همچون موتاسیونهای ژنتیکی، هورمونها و شرایط ایمنی در آن دخیل هستند. عوامل خطرساز میتوانند بهطور همزمان عمل نمایند و یا اینکه به ترتیب موجب شروع و تسریع رشد سرطان شوند. بین مواجهه با عوامل بیرونی و ایجاد سرطان اغلب حدود 10 سال و بیشتر طول میکشد.
- آیا میتوان جلوی سرطان را گرفت؟
بخش قابل توجهی از سرطانها از جمله آنهایی که ناشی از مصرف دخانیات و الکل میباشند قابل پیشگیری هستند. بر اساس بررسیهای جدیدی که توسط اپیدمیولوژیستهای انجمن سرطان امریکا انجام شده است، از میان حدود 600920 مرگ ناشی از سرطان که تخمین زده میشود در سال 2017 در امریکا اتفاق بیفتد، 190500 مورد آن بهواسطه مصرف دخانیات اتفاق میافتد، علاوه بر این بر اساس برآورد بنیاد جهانی تحقیقات سرطان، حدود 20% سرطانها در آمریکا ناشی از افزایش وزن، عدم تحرک فیزیکی، مصرف زیاد الکل و تغذیه ناسالم است و لذا قابل پیشگیری میباشند. برخی از سرطانها که ناشی از عوامل عفونی همچون ویروس هپاتیت B، ویروس هپاتیت C، HIV، HPV و هلیکوباکتر پیلوری میباشند طبیعتاً با واکسیناسیون یا درمان عامل عفونی قابل پیشگیری خواهند بود. سالانه بیش از 5 میلیون مورد سرطان پوست شناسایی میشود که اکثر آنها با اجتناب از نور مستقیم خورشید و عدم استفاده از دستگاههای برنزه کننده پوست قابل پیشگیری هستند.
با غربالگری میتوان سرطانهای روده و دهانه رحم را در مراحل اولیه تشخیص داده و ضایعات پیشسرطانی را جراحی نمود، همچنین با غربالگری میتوان برخی از سرطانها را در مراحل اولیه که هنوز قابلیت درمان بیشتری دارند تشخیص داده و اقدامات لازم را به عمل آورد. غربالگری به کاهش تلفات ناشی از سرطانهای سینه، روده، رکتوم، دهانه رحم و ریه کمک میکند. همچنین افزایش آگاهی درخصوص تغییرات در قسمتهای خاصی از بدن همچون سینه، پوست، دهان، چشم یا دستگاه تناسلی میتواند به شناسایی زودهنگام سرطان کمک کند.
- چه تعداد بیماران سرطانی اکنون زنده هستند؟
در تاریخ اول ژانویه 2016 بیش از 15/5 میلیون نفر آمریکایی که سابقه ابتلا به سرطان را داشتهاند، در قید حیات بودند. بیماری برخی از این افراد اخیراً شناسایی شده و هنوز تحت درمان هستند اما بیشتر آنها سالهاست که هیچ علامتی از سرطان ندارند.
- در سال 2017 چه تعداد موارد جدید و چه تعداد مرگ ناشی از سرطان انتظار میرود؟
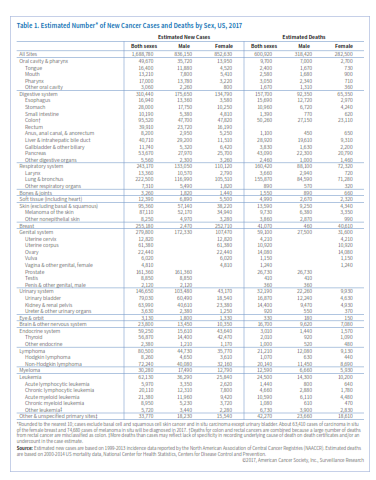
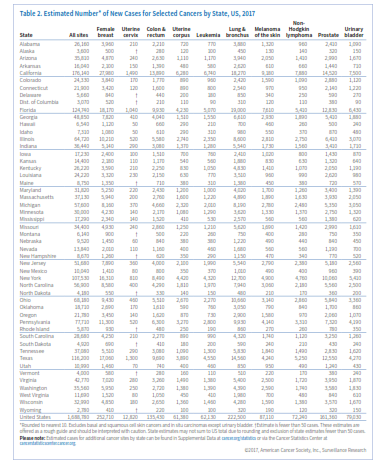
انتظار میرود حدود 1/688/780 مورد جدید سرطان در سال 2017 در امریکا شناسایی شود (جدول 1). البته سرطان درجا (in situ) در هرجای بدن بهجز مثانه و نیز سرطان سلولهای بازال و سلولهای سنگفرشی پوست شامل این آمار نمیشوند، چراکه گزارش این موارد به مراکز ثبت سرطان الزامی نیست. جدول 2 موارد جدید سرطان که انتظار میرود در سال 2017 شناسایی شود را برحسب ایالت مشخص کرده است.
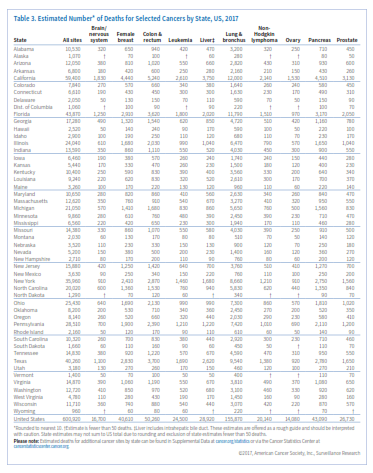
انتظار میرود که در سال 2017 حدود 600290 نفر آمریکایی براثر سرطان جان خود را از دست بدهند و این به معنی 1650 مرگ در روز است (جدول 1). سرطان بعد از بیماریهای قلبی دومین عامل مرگ در امریکا محسوب میشود و تقریباً از هر 4 مرگ یکی به علت سرطان است. جدول 3 میزان مرگ را برحسب ایالت در سال 2017 نشان میدهد.
- چه پیشرفتهایی علیه سرطان صورت گرفته است؟
بررسی روندهای مرگ بر اثر سرطان بهترین وسیله سنجش پیشرفت علیه سرطان میباشد. میزان مرگ بر اثر سرطان در اکثر اوقات در قرن بیستم افزایش نشان میدهد که قله آن در سال 1991 بود که 215 مرگ ناشی از سرطان در هر 100/000 نفر گزارش گردید و علت آن اپیدمی مصرف دخانیات بود.
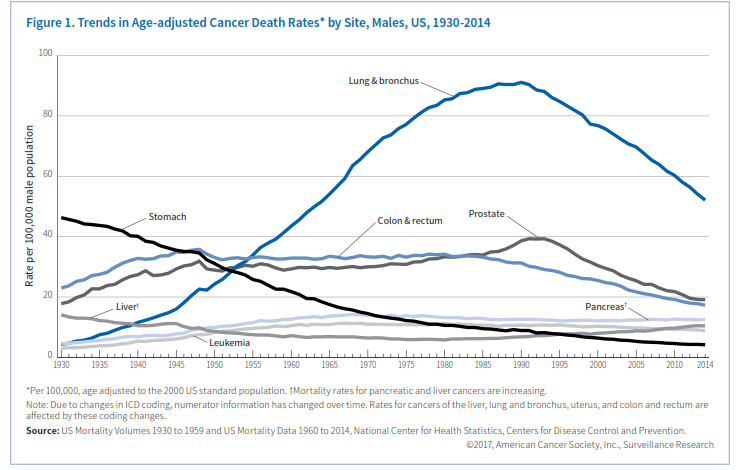
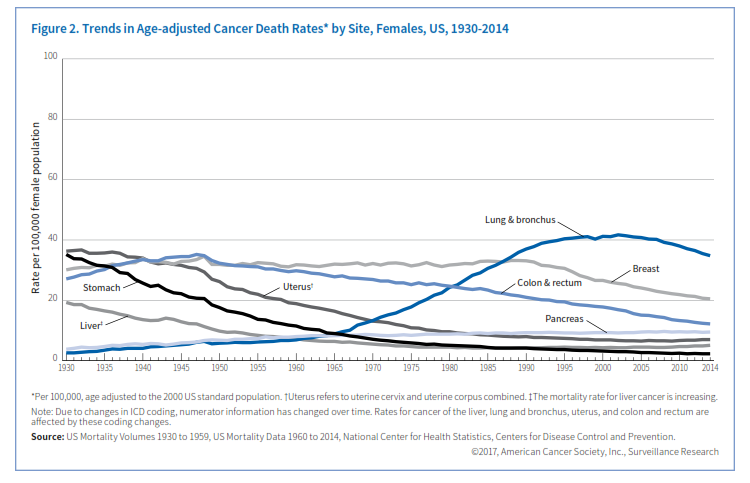
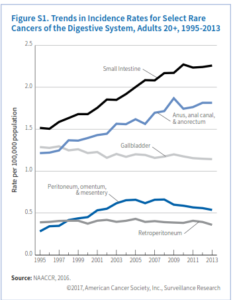
در سال 2014 این رقم به 161 مرگ به ازای هر 100/000 نفر کاهش پیدا کرد که تقریباً یک کاهش 25 درصدی است و بازهم علت کاهش مصرف دخانیات میباشد و علاوه بر آن بهبود روشهای شناسایی و درمان نیز در این کاهش نقش دارند، بعبارت دیگر در طی دو دهه اخیر 2/1 میلیون نفر از تعداد مرگهای ناشی از سرطان کاسته شده است که این پیشرفت ناشی از کاهش سریع در تعداد مرگ در اثر چهار سرطان متداول یعنی ریه، روده، سینه و پروستات میباشد (شکل 1 و 2).
- آیا میزان وقوع سرطان و مرگ ناشی از آن در ایالتهای مختلف متفاوت است؟
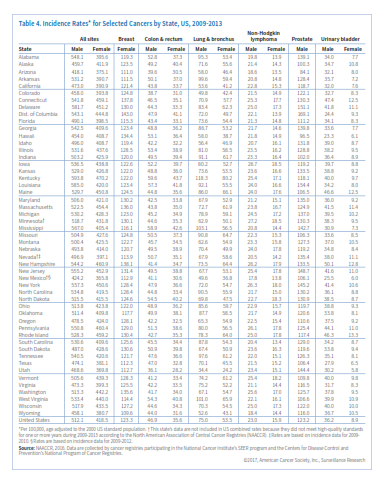
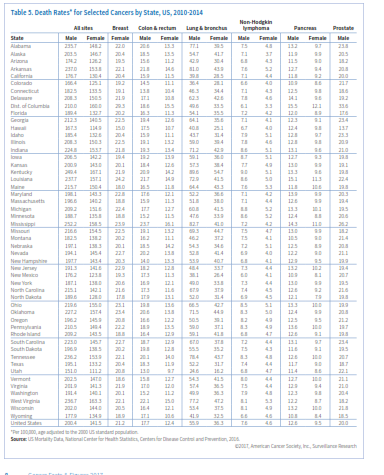
در جدول 4 و 5 میتوانید متوسط وقوع سالانه (موارد تشخیص دادهشده) سرطان و مرگ ناشی از آن را به تفکیک نوع سرطان و ایالت مشاهده کنید. در مورد برخی از سرطانها همچون سرطان ریه، نوسان در ایالتها بسیار زیاد است اما در مورد سرطانهای دیگر همچون لنفوم غیرهوچکینی این نوسان دیده نمیشود.
- چه کسی در معرض ابتلا به سرطان است؟
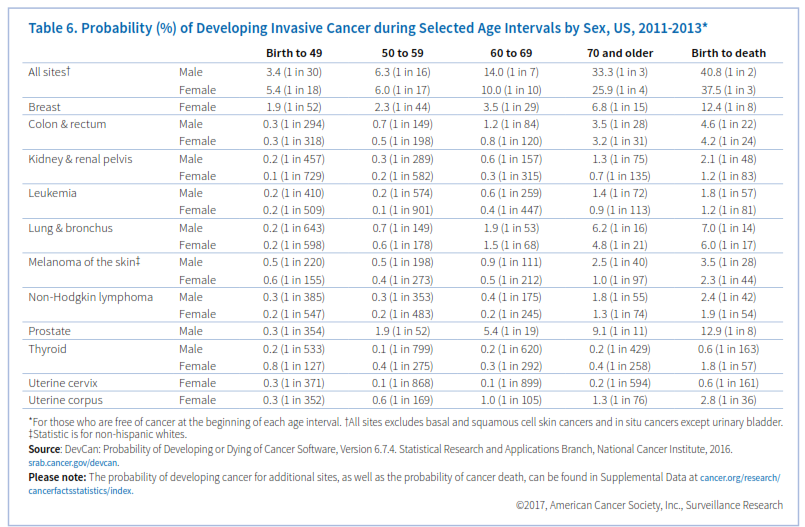
سرطان معمولاً در سنین بالا رخ میدهد. حدود 87% سرطانها در ایالت متحده در افراد بالای 50 سال شناسایی میگردد. برخی رفتارها همچون مصرف دخانیات، رژیم غذایی ناسالم و عدم تحرک نیز خطر ابتلا به سرطان را افزایش میدهد. در امریکا تقریباً از هر 100 مرد 41 نفر و از هر 100 زن 38 نفر در طی دوران زندگی خود به سرطان مبتلا خواهند شد (جدول 6).
این برآورد بر اساس وقوع سرطان در کل جمعیت است و در مورد تکتک افراد به لحاظ وجود عواملی چون مصرف دخانیات، سابقه خانوادگی و حساسیت ژنتیکی دقیق نیست.
رابطه بین مواجهه با یک عامل خطر و ایجاد سرطان را خطر نسبی مینامند. برای محاسبه آن وقوع سرطان را در افرادی که ویژگی خاصی دارند با میران وقوع سرطان در افرادی که آن ویژگی را ندارند مقایسه میکنند؛ بعنوان مثال زنان و مردان سیگاری 25 برابر افراد غیرسیگاری احتمال ابتلا به سرطان ریه را دارند، بنابراین خطر نسبی سرطان ریه در آنها 25 میباشد. در بیشتر موارد خطر نسبی به این بزرگی نیست؛ مثلاً زنانی که مادر یا خواهر یا دختر آنها سابقه سرطان سینه دارند در مقایسه با دیگران 2 برابر بیشتر احتمال دارد که به سرطان سینه مبتلا شوند، بعبارت دیگر خطر نسبی برای آنها 2 میباشد.
در مورد بیشتر سرطانها درصورتیکه سابقه ابتلای خانوادگی وجود داشته باشد، احتمال خطر بیشتر است. اکنون اعتقاد بر این است که بیشتر سرطانهای فامیلی ناشی از ژنتیک مشترک افراد و محیط زندگی مشابه آنها میباشد. تنها جزء کوچکی از سرطانها هستند که شدیداً ارثی میباشند و از طریق ژنتیک به ارث میرسند.
- چند درصد از افراد پس از سرطان زنده میمانند؟
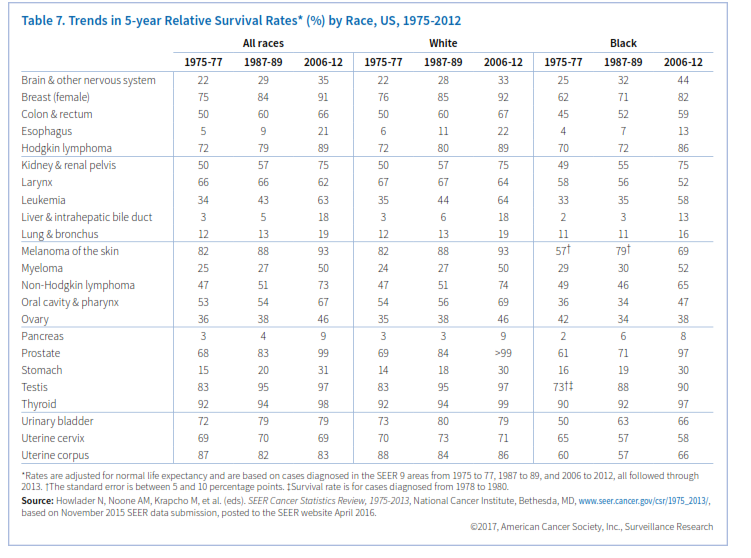
در دهه گذشته میزان بقای 5 ساله در میان سفیدپوستان 20% و در میان سیاهپوستان 24% افزایش یافته است، معذلک هنوز میزان بقای سیاهپوستان کمتر است (68% سفیدپوستان و 61% سیاهپوستان). پیشرفت در میزان بقا، ناشی از پیشرفت در درمان و تشخیص برخی انواع سرطان میباشد (جدول 7).
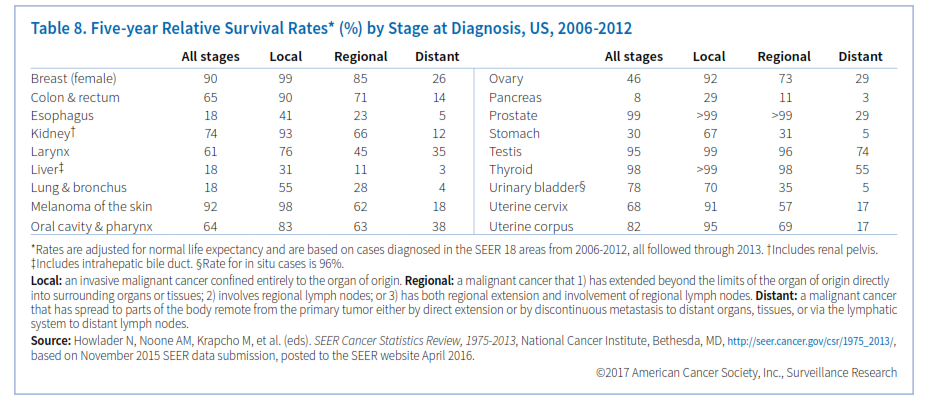
میزان بقا برحسب نوع سرطان و نیز مرحله تشخیص آن متفاوت است (جدول 8). بقای نسبی از تقسیم درصد افرادی که بعد از تشخیص سرطان برای یک مدت خاص (معمولاً 5 سال) زنده ماندهاند به درصد افرادی که بدون سرطان در طی این مدت زنده ماندهاند، بدست میآید. این نسبت بین بیمارانی که هیچ علامتی از سرطان ندارند با آنهایی که دچار عود بیماری شدهاند یا هنوز تحت درمان هستند تفاوت نمیگذارد و نیز بین بیماری که بهبود یافته است با آنکه پس از 5 سال فوت کرده است، تفاوت قائل نمیشود.
اگرچه نرخ بقای نسبی اطلاعاتی درخصوص بیماران سرطانی در یک جمعیت بیان میکند، اما باید با احتیاط تفسیر شود. نخست اینکه نرخ بقای 5 ساله پیشرفتهای اخیر را در تشخیص و درمان سرطان نشان نمیدهد، زیرا که بر اساس اطلاعات بیمارانی بیان میشود که سالها پیش تشخیص داده شدهاند. در ثانی عواملی را که در بقای بیمار دخالت دارند مانند درمان، سایر بیماریها و تفاوتهای بیولوژیک و رفتاری را در نظر نمیگیرد. نکته سوم آنکه بهبود در نرخ بقا همیشه نشانگر پیشرفت علیه سرطان نیست.
- سرطان چگونه مرحلهبندی staging میشود؟
مرحلهبندی (staging) یعنی مشخص کردن میزان گسترش سرطان به هنگام تشخیص. جهت بهینهسازی درمان و برآورد صحیح پیشآگهی، مرحلهبندی صحیح ضرورت دارد. مرحله سرطان به اندازه یا وسعت تومور اولیه و نیز دستاندازی آن به غدد لنفاوی اطراف و سایر نواحی بدن بستگی دارد. سیستمهای مختلفی برای مرحلهبندی سرطان مورد استفاده قرار میگیرند. یک سیستم مرحلهبندی خلاصه برای آنالیز تشریحی و آماری دادههای ثبت تومور بکار میرود و برای پیگیری تغییرات با گذشت زمان مفید است.
بر اساس این سیستم چنانچه سلولهای سرطانی صرفاً در همان محل پیدایش حضور داشته باشند و به اطراف گسترش نداشته باشند سرطان درجا یا (in situ) نامیده میشود. اگر سلولهای سرطانی از لایه بافت اولیه تجاوز کرده باشند، سرطان مهاجم تلقی شده و براساس وسعت تجاوز، محلی، ناحیهای و یا سراسری خواهد بود (پانوشت جدول 8 را ملاحظه کنید).
پزشکان اصولاً یک سیستم مرحلهبندی بنامTNM را به کار میبرند. سیستم TNM رشد و گسترش سرطان را از سه طریق بررسی میکند:
- وسعت تومور اولیه (T)
- درگیری غدد لنفاوی (N)
- وجود یا عدم وجود متاستاز (M)
وقتیکه طبقهبندی T،N و M مشخص شد، مرحلهبندی آنها به شکل 0، (I)، (II)، (III) و IV تعیین میگردد. مرحله 0، سرطان درجا، مرحله (I) مرحله ابتدایی و مرحله (IV) مرحله نهایی پیشرفت سرطان میباشد. بعضی سرطانها (مانند لنفوم) سیستم مرحلهبندی جداگانهای دارند. همزمان با شناسایی بهتر بیولوژی سرطان، شاخصههای توموری بیشتری در طرحهای درمانی و یا مرحلهبندی برخی سرطانها مشارکت داده میشوند.
هزینههای سرطان
براساس برآورد آژانس تحقیقات بهداشتی و کیفیت، هزینههای مستقیم پزشکی برای سرطان در آمریکا در سال 2014 بالغ بر 87/8 میلیارد دلار بوده است. 57% این مبلع برای بیماران سرپایی و 27% برای بیماران بستری هزینه شده است.
نداشتن بیمه خدمات درمانی و سایر موانع موجب محرومیت بسیاری از آمریکاییها جهت دسترسی به مراقبتهای بهداشتی بهینه شده است. 29 میلیون آمریکایی (9%) در سال 2015 تحت پوشش خدمات بیمه نبودهاند.
سرطانهای خاص
در این بخش درخصوص سرطانهای متداول صحبت میکنیم و اطلاعاتی همچون عوامل خطر، علائم، تشخیص زودهنگام، آمار وقوع، مورتالیتی و بقا ارائه خواهد شد. اطلاعات لازم در مورد سرطانهای خاص در بخش مربوطه ارائه خواهد شد.
سرطان سینه
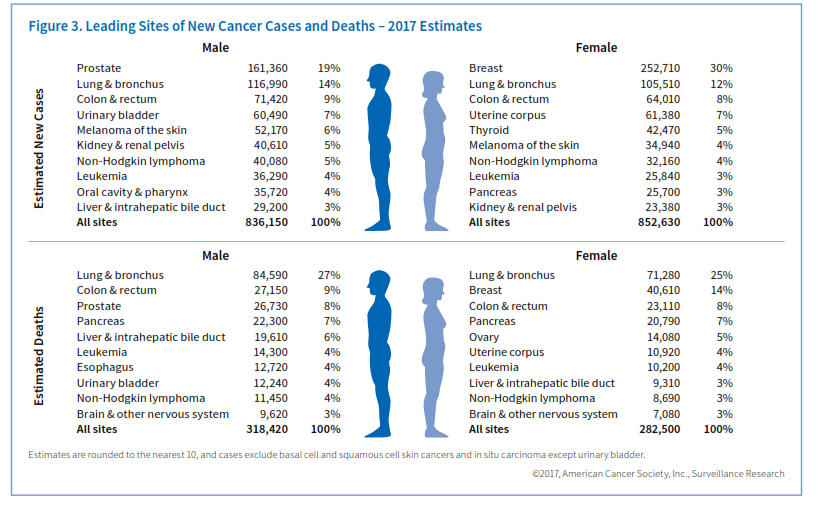
پیشبینی میشود که در سال 2017 حدود 252710 مورد سرطان مهاجم سینه در زنان و 2470 مورد در مردان در آمریکا تشخیص داده شود. علاوه بر این 63410 مورد سرطان درجای in situ سینه در زنان شناسایی خواهد شد. سرطان سینه متداولترین سرطان است که در زنان شناسایی میشود (شکل 3).
روند وقوع: از سال 2004 تا 2013 که آخرین دههای است که درخصوص آن اطلاعات در دسترس میباشد(اطلاعات هر دهه به طور جداگانه بررسی میشود و دهه مورد بررسی بعدی از سال 2014تا 2023 خواهد بود)، نرخ وقوع سرطان مهاجم سینه در زنان سفیدپوست ثابت مانده و در زنان سیاهپوست 0/5 درصد افزایش یافته است. این روند نشانگر همگرایی نرخها در دو گروه میباشد.
میزان موارد فوتی: تخمین زده میشود که 41070 مورد مرگ ناشی از سرطان سینه در سال 2017 اتفاق بیفتد که 40610 مورد آن مربوط به زنان و 460 مورد مربوط به مردان میباشد. سرطان سینه دومین عامل مرگ ناشی از سرطان در زنان میباشد
روند مورتالیتی: نرخ مرگ ناشی از سرطان سینه در زنان از اوج خود در سال 1989 تا سال 2014 حدود 38% کاهش یافته است که این امر ناشی از بهبود در تشخیص اولیه (از طریق افزایش آگاهی و غربالگری) و درمان میباشد. بعبارت دیگر در طی این مدت 297/300 مورد از مرگ ناشی از سرطان سینه کم شده است. برخلاف میزان وقوع، نرخ مرگ ناشی از سرطان سینه در بین زنان سفیدپوست و سیاهپوست یکسان است و از سال 2005 تا 2014 همهساله حدود 1/8% کاهش یافته است.
علائم و نشانهها: معمولترین علامت سرطان سینه وجود یک توده در پستان است. علائم دیگر که کمتر شایع هستند عبارت از افزایش ضخامت، تورم، اعوجاج، درد، حساسیت پوستی، قرمزی، زبر شدن و تغییرات غیرطبیعی نوک پستان یا ترشحات خودبخود میباشد.
عوامل خطرساز: بسیاری از عوامل خطرساز سرطان سینه آنهایی هستند که مواجهه بافت سینه را با هورمونها بهطور مستمر تحت تأثیر قرار میدهند. عوامل خطرسازی که قابل اجتناب هستند عبارتند از افزایش وزن بعد از 18 سالگی و یا چاقی، استفاده از هورمونها (استروژن و پروژسترون) بعد از یائسگی، فقدان تحرک فیزیکی و مصرف الکل. تحقیقات اخیر نشان داده است که مصرف طولانی مدت و زیاد دخانیات بهویژه اگر شروع مصرف قبل از تولد اولین نوزاد باشد، خطر ابتلا به سرطان سینه را افزایش میدهد. کار شیفتی بهویژه شیفت شب که الگوی خواب را مختل میسازد نیز ممکن است سبب افزایش خطر ابتلا گردد.
افزایش سن، سابقه خانوادگی سرطان سینه و تخمدان، موتاسیونهای ارثی در ژنهای BRCA1،BRCA2 یا سایر ژنهای مرتبط با سرطان سینه، برخی تغییرات خوشخیم سینه (مثل هیپرپلازی آتیپیک)، سابقه کارسینوم درجای مجاری یا لوبها، تابش اشعه قوی به سینه در سنین پایین (مثلاً برای درمان لنفوم)، بالا بودن تراکم بافت سینه و دیابت نوع 2 از جمله عوامل خطرساز غیرقابل پیشگیری سرطان سینه محسوب میشوند. فاکتورهای تولیدمثل مانند طولانی بودن دوره قاعدگی، استفاده اخیر از ضدحاملگیهای خوراکی، بدنیا نیاوردن بچه، تولد اولین نوزاد بعد از سی سالگی و بالا بودن هورمونهای جنسی نیز میتوانند از عوامل خطرساز سرطان سینه باشند.
شیر دادن بچه حداقل به مدت یک سال، ورزش متوسط و یا شدید بهطور منظم و کنترل وزن بدن از عوامل کاهش خطر بهحساب میآیند. برای کاهش خطر در زنانی که احتمال خطر ابتلا به سرطان سینه در آنها بالاست دو داروی tamoxifen و raloxifene مورد تأیید قرار گرفتهاند.
رالوکسیفن عوارض جانبی کمتری دارد و تنها دارویی است که استفاده از آن در زنان یائسه مورد تائید است. نوع دیگری از داروها موسوم به مهارکنندههای aromatase هم اخیراً مشخص شده که در پیشگیری از سرطان سینه مؤثر هستند.
تشخیص زودهنگام: ماموگرافی یک روش تصویربرداری با دوز پایین است که برای تشخیص زودهنگام سرطان سینه بکار میرود. مطالعات متعددی نشان دادهاند که تشخیص زودهنگام با استفاده از ماموگرافی میتواند به نجات زندگی بیمار کمک کند، اما مانند هر وسیله غربالگری دیگر، ماموگرافی هم کامل و بدون نقص نیست؛ بهعنوان مثال احتمال دریافت نتیجه منفی کاذب بهویژه در زنانی که بافت سینه آنها متراکم است وجود دارد. همچنین ماموگرام میتواند بهطور کاذب مثبت شود.
یک نفر از هر ده زن ماموگرام غیرطبیعی دارد که 95% آنها سرطان ندارند. ضمناً ماموگرافی برخی سرطانها را که غیرمهاجم هستند، نشان میدهد که این سرطانها هیچگاه موجب آسیب به فرد نخواهند شد، اما با توجه به ماموگرافی، مورد درمان غیرضروری ممکن است قرار گیرند. دستورالعمل اخیر انجمن سرطان آمریکا درخصوص غربالگری زنانی که با خطر متوسط مواجهند به این ترتیب است که زنان 40 تا 44 ساله در صورت تمایل میتوانند ماموگرافی را شروع کنند و زنان 45 تا 54 سال باید سالی یک مرتبه ماموگرافی کنند. زنان بالای 55 سال مختارند در فواصل زمانی یک یا دو سال این آزمایش را انجام دهند. تا زمانی که انتظار 10 سال طول عمر میرود و وضعیت کلی سلامت فرد خوب است باید ماموگرافی ادامه یابد. در زنانی که احتمال خطر در آنها بالاست باید علاوه بر ماموگرافی سالانه یک بار هم MRI بعمل آید و شروع این اقدام از سی سالگی میباشد.
درمان: برحسب تمایل بیمار و نوع تومور (اندازه، وضعیت گیرندههای هورمونی و وسعت دستاندازی آن) بخشی از سینه (شامل تومور و بافتهای اطراف) و یا کل سینه برداشته میشود که اولی را lumpectomy و دومی را ماستکتومی مینامند. به اکثر بیمارانی که سینه بهطور کامل در آنها برداشته نمیشود توصیه میگردد که اشعهدرمانی را هم بکار بگیرند. مطالعات نشان میدهند در سرطان اولیه پستان (که پوست، دیواره سینه و اعضای دیگر درگیر نشدهاند) جراحی lumpectomy به اضافه اشعهدرمانی نتایجی مشابه یا بهتر از ماستکتومی دارد. معمولاً غدد لنفاوی زیربغل هم برای بررسی وسعت انتشار تومور برداشته میشوند. بعد از ماستکتومی میتوان با استفاده از مواد مختلف به بازسازی پستان پرداخت و حتیالامکان شکل و ظاهر آن را حفظ کرد. این عمل را میتوان همزمان با ماستکتومی و یا بعد از آن انجام داد ولی معمولاً برای تکمیل فرآیند بازسازی بیش از یک مورد جراحی لازم است.
اگر وسعت تومور زیاد باشد و یا به غدد لنفاوی دستاندازی کرده باشد توصیه میشود که بعد از ماستکتومی پرتودرمانی هم انجام شود. درمان میتواند شامل شیمیدرمانی (قبل یا بعد از جراحی)، هورمون درمانی و یا درمان هدفمند هم باشد. در مراحل اولیه سرطان سینه که تستهای رسپتورهای هورمونی مثبت باشد درمان با هورمون به مدت 5 سال یا بیشتر مؤثر خواهد بود. درصورتیکه پروتئین HER2 بیش از اندازه بیان شود درمانهای هدفمند متعددی در دسترس میباشند.
میزان بقا: نرخ بقای نسبی 5 و 10 ساله در سرطان سینه مهاجم به ترتیب 90 و 83 درصد میباشد. بیشتر بیماران (61%) در مرحلهای تشخیص داده میشوند که تومور لوکالیزه است و به غدد لنفاوی، بافتهای اطراف و سایر مناطق بدن دستاندازی نکرده است. در این افراد نرخ بقای 5 ساله 99% است (جدول 8). نرخ بقا هم برای زنان سفیدپوست و هم سیاهپوست در حال افزایش است اما بهطور مطلق در زنان سیاهپوست 11% کمتر میباشد (جدول 7).
سرطانهای اطفال (14-0 سال)
موارد جدید: برآورد میشود که در سال 2017 تعداد 10270 مورد سرطان در کودکان زیر 14 سال در آمریکا شناسایی گردد.
روند وقوع: میزان وقوع سرطان کودکان از سال 1975 هرساله به مقدار 0/6 درصد افزایش یافته است.
مرگ: برآورد میشود که در سال 2017 تعداد 1190 مورد مرگ ناشی از سرطان کودکان در امریکا اتفاق بیفتد. در کودکان 14-1 سال پس از تصادفات، سرطان دومین عامل مرگ میباشد.
روند مورتالیتی: مرگ ناشی از سرطان اطفال از سال 1969 تا سال 2014 به میزان دوسوم کاهش یافته و از 5/6 مرگ در صدهزار نفر به 2 مرگ در صدهزار نفر رسیده است. عمدهاین پیشرفت مرهون بهبود روشهای درمانی و مشارکت گسترده در کارآزماییهای بالینی میباشد.
علائم و نشانهها: ازآنجاکه علائم سرطان میتواند مشابه بیماریهای معمولی دورهی کودکی باشد، تشخیص زودهنگام آن دچار تأخیر میگردد. والدین باید بهطور مرتب نسبت به چکاپ فرزندانشان اقدام نموده و نسبت به علائم مستمر غیرمعمول هشیار باشند. این علائم شامل ایجاد توده غیرمعمول در بدن، رنگپریدگی یا کاهش سطح انرژی، کبودی یا خونریزی ناگهانی، درد لوکالیزه یا لنگ زدن، تب طلانی بدون علت مشخص، سردرد مکرر که اغلب همراه استفراغ است، تغییر ناگهانی در وضعیت دید و کاهش وزن شدید و ناگهانی میباشند. انواع عمده و اصلی سرطان اطفال به شرح ذیل میباشد:
- لوسمی (شامل 29% همه سرطانهای اطفال) با علائمی همچون درد استخوان و مفاصل، ضعف، رنگپریدگی، خونریزی و کبودی، تب و عفونت تظاهر میکند.
- سرطان مغز و سایر سرطانهای سیستم اعصاب مرکزی (26%)، با علائم سردرد، تهوع، استفراغ، تاری دید و دوبینی، تشنج، گیجی و اشکال در راه رفتن و برداشتن اشیاء ظاهر میشود.
- نوروبلاستوما (6%) یک سرطان سیستم اعصاب مرکزی است که در بچههای زیر 5 سال شایعتر است و معمولاً بهصورت بزرگ شدن شکم تظاهر میکند.
- تومور ویلمز (5%) نوعی سرطان کلیه است که به آن نفروبلاستوما هم میگویند و بهصورت ایجاد یک توده در شکم بروز میکند.
- لنفوم غیرهوچکینی شامل لنفوم بورکیت (5%) و لنفوم هوچکین (3%) که در دوران نوجوانی بیشتر دیده میشود و علائم آن شامل تورم غدد لنفاوی گردن و زیربغل و کشاله ران به همراه خستگی، کاهش وزن و تب میباشد.
- رابدومیوسارکوم (3%)، سارکوم بافت نرم است که در ناحیه سر و گردن، تناسلی، تنه و دست و پاها ایجاد میشود و همراه با درد و تورم میباشد.
- استئوسارکوم (2%)، یک نوع سرطان استخوان است که اغلب در دوره نوجوانی رخ میدهد و عموماً به شکل درد پراکنده در استخوان تظاهر میکند که ممکن است در شب و یا به هنگام فعالیت تشدید شود و نهایتاً ایجاد یک تورم و توده در محل میکند.
- رتینوبلاستوم (2%) یک نوع سرطان چشم است که در کودکان زیر 15 سال دیده میشود و معمولاً به هنگام عکس گرفتن یا معاینه چشم و زدن فلاش، مردمک به رنگ سفید یا صورتی درمیآید.
- سارکوم اوینگ (1%)، نوع دیگری از سرطان استخوان است که اغلب در نوجوانی دیده میشود و به شکل درد در محل تومور خود را نشان میدهد.
عوامل خطرساز: عوامل خطر شناخته شده در خصوص سرطان اطفال بسیار محدود میباشند. قرار گرفتن در معرض اشعه یونیزان احتمال لوسمی و شاید سایر سرطانها را در اطفال افزایش میدهد. بخش کوچکی از سرطانهای اطفال توسط موتاسیون ژنتیکی که ارثی هستند ایجاد میگردند. برخی از سندرمهای ژنتیکی مانند سندرم داون خطر ابتلا به سرطان را افزایش میدهند.
درمان: برحسب نوع و مرحله سرطان از جراحی، شیمیدرمانی، اشعهدرمانی و درمان هدفمند استفاده میشود. تیم درمانی شامل انکولوژیست اطفال، پرستار، مددکار اجتماعی، روانشناس و سایر افراد آموزشدیده میباشند که به درمان طفل و حمایت از خانواده وی اقدام میکنند. درصورتیکه درمان در یک مرکز تخصصی اطفال انجام شود، نتیجه بهتری عاید خواهد شد. در کودکان واجد شرایط کارآزماییهای بالینی که درمانهای جدید را با درمانهای فعلی مقایسه میکنند باید مدنظر باشد.
بقا: میزان بقا در تمامی سرطانهای مهاجم اطفال طی سی سال گذشته به لطف پیشرفت در روشهای درمانی افزایش یافته است. میزان بقای نسبی 5 ساله در آخرین دوره مورد بررسی (2012-2006) حدود 83% بوده است، گرچه بسته به نوع سرطان، سن بیمار و سایر عوامل، نوسانات زیادی مشاهده میشود. بهعنوان مثال میزان بقای 5 ساله برای لنفوم هوچکین 98%، رتینوبلاستوما 95%، تومور ویلمز 92%، لنفوم غیرهوچکین 91%، لوسمی 86% (90% برای لوسمی لنفوئید حاد و 64% برای لوسمی میلوئید حاد)، نوروبلاستوما 80%، سارکوم اوینگ 79%، تومور مغز و سایر تومورهای سیستم اعصاب مرکزی (بهجز تومورهای خوشخیم مغز) 73%، استئوسارکوم 70% و رابدومیوسارکوم 70% میباشد.
اطفالی که از سرطان جان سالم بدر میبرند ممکن است مدتها بعد دچار عواقب سوء درمان شامل اختلال در عضو خاص (مثلاً اختلالات شناختی) و سرطانهای ثانویه شوند. گروه انکولوژی اطفال دستورالعملهایی را برای غربالگری و درمان عوارض دیرهنگام در کودکان درمانشده تدوین کرده است.
روده بزرگ و رکتوم
موارد جدید: برآورد میشود که در سال 2017، تعداد 95520 مورد سرطان کولون و 39910 مورد سرطان رکتوم در آمریکا تشخیص داده شوند. سرطان کولورکتال سومین سرطان شایع در هر دو جنس زن و مرد میباشد.
روند وقوع: وقوع سرطان کولورکتال به دلیل تغییر الگوی فاکتورهای خطرساز و انجام غربالگری طی چند دهه اخیر کاهش یافته است، اما این تغییرات وابسته به سن میباشد.
در دهه مورد بررسی اخیر (2013-2004) میزان وقوع در افراد بالای پنجاه سال همهساله حدود 3% کاهش نشان میدهد، اما در افراد زیر 50 سال، هرسال 2% افزایش را شاهد هستیم که بیشتر آن هم مربوط به سرطان رکتوم است.
مرگ: برآورد مرگ ناشی از سرطان کولورکتال در امریکا در سال 2017 قریب به 50260 مورد میباشد. سرطان کولورکتال دومین عامل مرگ ناشی از سرطان در مردان و سومین عامل در زنان میباشد و درمجموع مردان و زنان نیز دومین عامل مرگ ناشی از سرطان محسوب میگردد. متأسفانه آمار دقیقی که مرگ ناشی از سرطان کولون را از سرطان رکتوم تفکیک کرده باشد وجود ندارد و موارد بالایی از مرگ ناشی از سرطان رکتوم بهطور اشتباهی بهحساب سرطان کولون گذاشته میشود. بخش عمدهای از این اشتباه ناشی از این است که در مطالب آموزشی واژه سرطان کولون هم بجای سرطان کولون و هم بجای سرطان رکتوم استعمال میشود.
روند مورتالیتی: میزان مرگ ناشی از سرطان کولورکتال در سال 2014 (14 در صدهزار) نصف میزان آن در سال 1975 (28 در صدهزار) بود. از سال 2005 تا سال 2014 همهساله 2/5درصد از نرخ مرگ در سال کم شده است.
علائم و نشانهها: مرحله اولیه سرطان کولورکتال هیچ علامتی ندارد، به همین دلیل غربالگری این سرطان ضروری میباشد. علائم در صورت وجود میتوانند شامل خونریزی از مقعد، وجود خون در مدفوع، تغییر عادات دفع یا شکل مدفوع (باریک شدن مدفوع)، احساس عدم دفع کامل، درد شکم در قسمت پایین، کاهش اشتها و کاهش وزن میباشند. در برخی موارد دفع خون از ضایعه سرطانی موجب کمخونی شده و علائمی چون ضعف و خستگی بروز میدهد. ارزیابی بهموقع این علائم در همه بزرگسالان ضروری است.
عوامل خطرساز: عوامل خطری که قابل پیشگیری هستند شامل چاقی، کمتحرکی، مصرف دخانیات، مصرف زیاد گوشت قرمز و فرآوری شده، کمبود مصرف کلسیم، مصرف زیاد الکل و مصرف کم میوه و سبزیجات میباشند. مصرف غلات سبز کامل این خطر را کاهش میدهد. عوامل ارثی و طبی که موجب افزایش خطر سرطان کولورکتال میشوند عبارتند از: وجود سابقه سرطان یا پولیپ در خانواده، برخی ناهنجاریهای ژنتیکی (مثل سندرم Lynch، پولیپوز آدنوماتوز ارثی، بیماریهای التهابی روده و دیابت نوع دو).
مصرف منظم و طولانی مدت داروهای ضدالتهابی غیراستروئیدی مانند آسپرین مقدار خطر سرطان را کاهش میدهد اما ممکن است عوارض شدیدی همچون خونریزی معده داشته باشد.
جامعه سرطان آمریکا این داروها را بهعنوان پیشگیری از سرطان توصیه نکرده است اما برمبنای یک مطالعه که توسط یک نهاد حکومتی آمریکا صورت گرفته است مصروف روزانه دوز پایین آسپرین برای پیشگیری از بیماریهای قلبی عروقی و سرطان کولورکتال در افراد خاص که ریسک بالایی دارند در دهه 50 و 60 عمر توصیه شده است. تصمیمگیری درخصوص مصرف آسپرین باید با مشورت پزشک باشد.
تشخیص زودهنگام: مردان و زنانی که ریسک متوسط دارند با شروع دهه پنجاه عمر باید مورد غربالگری قرار بگیرند. در صورت وجود ضایعات پیشسرطانی یا سرطان اولیه با انجام غربالگری میتوان اقدام عاجل بعمل آورده و جلوی خسارات بعدی را گرفت. دستورالعملهای متعددی درخصوص موارد مختلف غربالگری کولورکتال وجود دارد که در صورت لزوم میتوان به آنها مراجعه کرد.
درمان: برای سرطان کولورکتال که هنوز منتشر نشده است جراحی معمولترین اقدام بهحساب میآید، کولستومی دایمی (ایجاد یک سوراخ در شکم برای دفع مدفوع) معمولاً در سرطان رکتوم لازم نیست و بندرت باید برای سرطان کولون انجام شود. در مواردی که سرطان به غدد لنفاوی و سایر قسمتهای شکم دستاندازی کرده است، شیمیدرمانی و رادیوتراپی نیز انجام میشود. در سرطان متاستاتیک، درمان عمدتاً شامل شیمیدرمانی و یا درمان هدفمند خواهد بود.
بقا: نرخ بقای نسبی 5 و 10 ساله در سرطان کولورکتال به ترتیب 65% و 58% میباشد. حدود 39% از بیماران در مرحله لوکالیزه تشخیص داده میشوند که میزان بقای 5 ساله در آنها 90% میباشد(جدول 8). بقای 5 ساله در گسترش ناحیهای 71% و در متاستاز دوردست 14% است.
کلیه و لگنچه
موارد جدید: برآورد میزان موارد جدید سرطان کلیه و لگنچه در سال 2017 در آمریکا بالغ بر 63990 مورد تخمین زده میشود. این موارد در درجه اول شامل کارسینوم سلولهای کلیوی و سپس سرطانهای لگنچه (5%) و تومور ویلمز (1%) میباشند. میزان ابتلا در مردان دو برابر زنان است.
روند وقوع: نرخ وقوع سرطان کلیه در دهههای اخیر افزایشی را تجربه کرده است که عمدتاً ناشی از تشخیص اتفاقی به هنگام رادیوگرافی شکم بوده است، اما بنظر میرسد در سالهای اخیر نرخ آن ثابت مانده باشد.
مرگ: تخمین زده میشود که در سال 2017، تعداد 14400 نفر براثر ابتلا به سرطان کلیه در آمریکا فوت شوند.
روند مورتالیتی: از سال 2002 تاکنون همهساله 1% از میزان مرگ براثر سرطان کلیه کم شده است.
علائم و نشانهها: مراحل اولیه سرطان کلیه معمولاً هیچ علامتی ندارد. با پیشرفت بیماری علائمی چون وجود خون در ادرار، درد یا وجود یک توده در قسمت پایین کمر یا شکم، خستگی، کاهش وزن، تب و یا تورم در ساق و مچ پا دیده میشود.
عوامل خطرساز: چاقی و استعمال دخانیات عوامل خطرساز قوی برای سرطان کلیه محسوب میشوند. فشارخون بالا، نارسایی مزمن کلیه و مواجهه شغلی با برخی مواد همچون تریکلرواتیلن هم موجب افزایش ریسک میشوند. قرار گرفتن در معرض تشعشع (مثلاً در درمان سرطان) نیز اندکی باعث افزایش ریسک میشود. بخش کوچکی از سرطانهای کلیه زمینه ارثی دارند.
درمان: جراحی درمان اولیه برای اکثر سرطانهای کلیه محسوب میشود. در مواردی که تومور کوچک باشد ممکن است نظارت فعال بجای جراحی اعمال گردد. در بیمارانی که داوطلب جراحی نیستند برداشتن تومور بهوسیله حرارت یا سرما نیز میتواند مدنظر باشد. تاکنون ادجوانتدرمانی توفیقی در درمان سرطان کلیه نداشته است. در سرطان متاستاتیک درمان هدفمند روش اصلی درمان خواهد بود که گاهی با جراحی کلیه توأم میگردد.
بقا: بقای 5 ساله در سرطان کلیه و لگنچه 74% است. دوسوم این سرطانها در مرحله لوکال تشخیص داده میشوند که بقای پنجساله این دسته به 93% هم میرسد (جدول 8).
لوسمی
موارد جدید: برآورد میشود که تعداد موارد جدید لوسمی در سال 2017 در آمریکا بالغ بر 62130 نفر گردد. گرچه لوسمی اغلب بهعنوان بدخیمی کودکان قلمداد میگردد، اما 92% موارد آن در افراد بالای 20 سال مشاهده میشود. معمولترین لوسمیها در بزرگسالان CLL (37%) و AML (31%) میباشند، درحالیکه ALL در افراد زیر 20 سال معمولتر است و 75% لوسمیهای افراد زیر بیست سال را تشکیل میدهد. گرچه در این گزارش CLL همچنان جزو لوسمیها طبقهبندی شده است، اما اکنون بیشتر در رده لنفومها درنظر گرفته میشود چراکه به اصولا شبیه (SLL) Small Lymphocitic Lymphoma میباشد.
تفاوت عمده این دو سرطان این است که در CLL بیشتر سلولهای سرطانی در جریان خون قرار دارند، درحالیکه در SLL در غدد لنفاوی جای گرفتهاند.
روند وقوع: از سال 2004 تا 2013 وقوع کلی لوسمی همهساله حدود 2% افزایش یافته که عمدتاً ناشی از افزایش وقوع AML است که از 3/4 در صدهزار در سال 2004 به 5/1 در سال 2013 افزایش یافته است. رشد وقوع ALL و CML به ترتیب 1 و 2 درصد در سال بوده درحالیکه CLL، 0/5 درصد افزایش یافته است.
مرگ: برآورد تعداد مرگ ناشی از لوسمی در سال 2017 در آمریکا 24/500 مورد میباشد.
روند مورتالیتی: برخلاف تعداد وقوع، میزان مرگ ناشی از لوسمی از سال 2004 تا 2014 همهساله برای ALL، CLL و CML حدود 1% کاهش یافته ولی در مورد AML تغییری نکرده است.
علائم و نشانهها: خستگی، رنگپریدگی، کاهش وزن، عفونت مکرر، تب، خونریزی یا کبودی، درد استخوان و مفصل و تورم غدد لنفاوی یا شکم از جمله علائم لوسمی هستند.
در لوسمی حاد شروع علائم ناگهانی میباشد. لوسمی مزمن معمولاً در طی آزمایش روتین خون تشخیص داده میشود و پیشرفت علائم در آن تدریجی میباشد.
عوامل خطرساز: قرار گرفتن در معرض اشعه یونیزان خطر ابتلا به انواع لوسمی را افزایش میدهد. اشعه درمانی (مثلاً در درمان سرطان) معمولترین منبع قرار گرفتن در معرض اشعه میباشد. شیمیدرمانی و همچنین برخی بیماریهای ژنتیکی چون سندرم داون احتمال ابتلا به لوسمی را افزایش میدهند. برخی عوامل شغلی همچون صنایع لاستیکسازی نیز خطر را افزایش میدهند.
برخی از عوامل خطرساز ارتباط نزدیک با نوع خاصی از لوسمی دارند؛ بهعنوان مثال زمینه خانوادگی عامل خطرساز قوی در ابتلا به CLL میباشد. مصرف سیگار عامل افزایش خطر ابتلا به AML در بزرگسالان است و شواهد متعددی نشان میدهند که مصرف سیگار توسط والدین قبل و بعد از تولد نوزاد نیز میتواند موجب لوسمی در فرزند گردد. شواهد محدودی حکایت از آن دارد که قرار گرفتن مادر در معرض بخارات رنگ ممکن است ابتلا به لوسمی در فرزند را افزایش دهد. مواجهه با برخی مواد شیمیایی خاص همچون فرمالدئید و بنزن خطر ابتلا به لوسمی میلوئید را افزایش میدهد. آلودگی به ویروس (HTLV-1) میتواند مسبب ایجاد یک لوسمی نادر بنام لوسمی/ لنفوم سلول T بزرگسالان گردد. عفونت با (HTLV-1) در جنوب ژاپن و جزایر کارائیب معمولتر است و افراد آلودهشده در آمریکا، مهاجرین این مناطق و یا از نسل آنها میباشند. به نظر میرسد که چاقی خطر ابتلا به برخی از انواع لوسمی را افزایش میدهد.
تشخیص زودهنگام: در حال حاضر هیچ برنامه غربالگری برای تشخیص زودهنگام لوسمی وجود ندارد، اما گاهی دیدن نتایج غیرطبیعی به هنگام آزمایش خون به علت پیگیری سایر بیماریها به کشف زودهنگام لوسمی میانجامد.
درمان: برای درمان بیشتر لوسمیهای حاد از شیمیدرمانی استفاده میشود. داروهای ضد سرطان متعددی بهصورت منفرد یا ترکیبی مورد استفاده قرار میگیرند. داروهای هدفمند متعددی (همچون imatinib) برای درمان CML بکار میروند. این داروها به سلولهای حاوی کروموزوم فیلادلفیا (که شاخصه CML میباشد) حمله میکنند. بعضی از این داروها برای درمان نوعی از ALL که اختلال ژنتیکی مشابهی دارد نیز بکار میروند. در بیماران مبتلا به CLL که بیماری پیشرونده نیست و علامتی نیز وجود ندارد، اقدام درمانی ضرورتی ندارد. برای آن دسته از مبتلایان CLL که اقدام درمانی ضرورت دارد در سالهای اخیر داروهای هدفمند جدید و امیدوارکنندهای بکار گرفته شده است.
در برخی انواع لوسمی ابتدا با دوز بالا شیمیدرمانی انجام میدهند و سپس اقدام به پیوند سلول بنیانی مینمایند.
درمانهای تجربی جدیدتر که سیستم ایمنی بدن را تقویت میکنند نظـــیر درمان
Chimeric Antigen Receptor (CAR) T-cell حتی علیه برخی لوسمیهای مقاوم به درمان اثرات امیدوارکنندهای را نشان داده است.
بقا: میران بقا برحسب نوع لوسمی شدیداً متغیر است؛ بهعنوان مثال بقای 5 ساله در دوره (2012-2006) برای مبتلایان AML، 27% و برای بیماران CLL، 83% بوده است. پیشرفتهای درمانی سبب شده که نرخ بقا برای اکثر انواع لوسمی بهطور قابلتوجهی افزایش یابد (جدول 7)، بهعنوان مثال نرخ بقای 5 ساله مبتلایان ALL از سالهای 77-1975 تا 2012-2006 از 41% به 71% افزایش یافته است. در مورد CML نرخ بقای 5 ساله در اوایل دهه 1990 حدود 31% بود که در سالهای 2012-2006 به 66% رسید؛ به عبارت دیگر بیش از دو برابر افزایش یافت که عمدتاً ناشی از بکارگیری درمانهای هدفمند جهت درمان این لوسمی بود.
کبد
موارد جدید: تخمین زده میشود که در سال 2017 حدود 40710 مورد جدید سرطان کبد در امریکا تشخیص داده شود که حدود سهچهارم آن کارسینوم هپاتوسلولار خواهد بود. شیوع سرطان کبد در مردان سه برابر بیشتر از زنان است.
روند وقوع: میزان وقوع سرطان کبد از سال 1980 تاکنون سه برابر شده است و نرخ رشد آن از سال 2004 تا 2013 هرساله حدود 4% بوده است.
مرگ: تخمین زده میشود که در سال 2017 تعداد 28920 مورد مرگ ناشی از سرطان کبد در آمریکا رخ دهد.
روند مورتالیتی: نرخ رشد مرگ ناشی از سرطان کبد از سال 2000 همهساله حدود 3% رشد داشته است.
علائم و نشانهها: علائم معمولاً تا مراحل پیشرفته سرطان ظهور نمیکنند و شامل درد و تورم شکم، کاهش وزن، ضعف، کاهش اشتها، یرقان و تب میباشند. بزرگ شدن کبد مهمترین نشان فیزیکی میباشد.
عوامل خطرساز: مهمترین عوامل خطرساز ابتلا به سرطان کبد در امریکا شامل عفونت مزمن با ویروس هپاتیت B و هپاتیت C، مصرف بیش از حد الکل، چاقی، دیابت، مصرف دخانیات و برخی اختلالات ژنتیکی همچون هموکروماتوز میشود.
پیشگیری: واکسن هپاتیت B از سال 1982 به بازار عرضه شد. برای هپاتیت C هنوز واکسنی وجود ندارد اما درمانهای ترکیبی ضدویروس قادرند در حد قابلتوجهی عفونت را از بین ببرند و احتمال خطر ابتلا به سرطان کبد را کاهش دهند. مرکز کنترل و پیشگیری بیماریها (CDC) توصیه کرده است که در افرادی که بین سالهای 1947 تا 1965 متولد شدهاند حتماً آزمایش هپاتیت C انجام شود چراکه سهچهارم افراد آلوده در آمریکا در این بازه سنی قرار دارند. اقدامات پیشگیرانه درخصوص HCV شامل غربالگری داوطلبان اهدای خون، عضو و بافت، تقید به کنترل عفونت در حین عملهای پزشکی و دندانپزشکی، تعویض سوزن در معتادان تزریقی و رعایت نکات ایمنی در تماس جنسی میباشد.
تشخیص زودهنگام: گرچه غربالگری سرطان کبد اثری بر کاهش مورتالیتی نداشته است، اما بسیاری از مراکز بهداشتی با سونوگرافی و آزمایش خون نسبت به غربالگری افراد پرخطر اقدام میکنند.
درمان: گاهی پس از تشخیص زودهنگام سرطان کبد میتوان با جراحی بخش سرطانی را جدا نمود اما بیماران معدودی را میتوان یافت که بخش باقیمانده کبد در آنها کفایت لازم را داشته باشد. در افرادی که تومور محدود دارند و امکان هپاتکتومی نسبی در آنها وجود ندارد پیوند کبد را میتوان مدنظر داشت. سایر درمانها شامل تخریب تومور یا مسدود کردن جریان خون به آن میباشند. در بیمارانی که در مراحل پیشرفته بیماری تشخیص داده میشوند امکانات درمانی محدودتری وجود دارد.
در مبتلایان به کارسینوم هپاتوسلولار که کاندیدای جراحی نیستند و دچار سیروز هم نشدهاند مصرف داروی sorafenib تأیید شده است.
بقا: نرخ بقای 5 ساله مبتلایان به سرطان کبد 18% است. 43% از بیماران در مرحله لوکال سرطان تشخیص داده میشوند که نرخ بقای 5 ساله برای آنها 31% است (جدول 8).
ریه و نایژهها
موارد جدید: سرطان ریه دومین سرطان متداول مردان و زنان در امریکا میباشد. برآورد موارد جدید سرطان ریه در سال 2017 در امریکا قریب 222500 مورد میباشد که حدود 25% کل سرطانهای تشخیص داده شده میباشد.
روند وقوع: نرخ وقوع سرطان ریه از اواسط 1980 در مردان و از اواسط دهه 2000 در زنان شروع به کاهش کرده است. علت این تفاوت در الگوهای تاریخی اعتیاد و ترک دخانیات در این دو جنس است.
از سال 2004 تا 2013 نرخ وقوع سرطان ریه در مردان سالانه 2% و در زنان سالانه 1% کاهش یافته است.
مرگ: سرطان ریه اولین عامل مرگ ناشی از سرطان در هر دو جنس مرد و زن میباشد. تخمین تعداد فوت ناشی از این سرطان در سال 2017 در امریکا 155870 نفر میباشد که درواقع از هر 4 مرگ ناشی از سرطان یک مورد مربوط به سرطان ریه است.
روند مورتالیتی: نرخ مرگ ناشی از سرطان ریه از سال 1990 در مردان 43% کاهش یافته است و این نرخ در زنان از سال 2002، 17% بوده است که علت آن کاهش مصرف دخانیات میباشد که با سرعت گرفتن ترک دخانیات در سالهای اخیر از سال 2010 تا 2014 کاهش 3/5% در سال در مردان و کاهش 2% در سال در زنان مشاهده میشود.
علائم و نشانهها: معمولاً تا زمان پیشرفت سرطان علائمی بروز نمیکند. علائم شامل سرفه مستمر، خلط خونآلود، درد سینه، تغییرات در صدا، تنگی نفس و پنومونی یا برونشیت مکرر میباشند.
عوامل خطرساز: مصرف سیگار مهمترین عامل خطر ابتلا به سرطان ریه است و 80% مرگهای ناشی از سرطان ریه در آمریکا ناشی از مصرف سیگار است. با افزایش مصرف و طول مدت مصرف، خطر افزایش مییابد. مصرف سیگار برگ و پیپ هم خطر را افزایش میدهد. دومین عامل ایجاد سرطان ریه در آمریکا تنفس گاز رادون است که از خاک و مواد ساختمانی متصاعد میشود. سایر عوامل خطرساز شامل مواجهه شغلی یا محیطی با دود (دست دوم) سیگار، آزبست، فلزات خاص (کروم، کادمیوم، آرسنیک)، برخی مواد شیمیایی آلی، اشعه، آلودگی هوا و دود دیزل میباشند. کار کردن در کارخانههای لاستیکسازی، کاشیکاری، ایزوگام سقف، نقاشی و پاک کردن دوده بخاری از مشاغل خطرساز هستند. خطر ابتلا احتمالاً در افراد مسلول افزایش مییابد. زمینه ژنتیک بهویژه در کسانی که در سنین پایین دچار بیماری میشوند احتمالاً در پیدایش سرطان ریه نقش دارد.
تشخیص زودهنگام: غربالگری در بین کسانی که در حال حاضر 30 بسته در سال ســــــــیگار میکشـــــــند و یا قبلاً سیـــــــگاری بوده و در پانــــــــزده ســال اخیــر تـــــرک کردهاند بهوسیله
Low- Dose Spiral Computed Tomography (LDCT) در مقایسه با عکس ساده قفسه سینه، 20% مرگ ناشی از سرطان ریه را کاهش میدهد.
دستورالعملهای انجمن سرطان امریکا برای تشخیص بهموقع سرطان ریه بر تعامل بین پزشک و بیمار تأکید دارند. افرادی که در سنین 55 تا 74 سال بوده، در حال حاضر سیگاری هستند و یا در 15 سال گذشته ترک کردهاند، مصرف سیگار آنها حداقل 30 پاکت در سال بوده و سلامت خوبی دارند کاندیدای غربالگری میباشند. تصمیم در مورد غربالگری باید با توجه به مذاکره درخصوص منافع آن، عدم قطعیت و مضار آن موردبحث قرار گیرد.
درمان: درمان مناسب سرطان ریه بســتگی بــه خصـــــــــــــــــوصیات تومور و نوع آن
{small cell(13%) و non-small cell (84%)} دارد. برحسب نوع، مرحله و ویژگیهای مولکولی تومور درمان ممکن است شامل جراحی، اشعهدرمانی، شیمیدرمانی، ایمونوتراپی و یا درمان هدفمند باشد.
در سرطان non-small cell جراحی معمولاً انتخاب اول است، شیمیدرمانی (گاهی توأم با اشعهدرمانی) هم ممکن است بکار برود. مراحل پیشرفته تومور non-small cell معمولاً با شیمیدرمانی، داروهای هدفمند (یا ترکیب هردو) و یا ایمونوتراپی درمان میشوند. در سرطان سلولهای کوچک، شیمیدرمانی بهتنهایی یا همراه با اشعه درمانی روش معمول است که درصد زیادی از بیماران، فروکش بیماری را تجربه میکنند اما در اغلب موارد سرطان بازمیگردد.
بقا: نرخ بقای 5 ساله برای مردان 15% و برای زنان 21% است. تنها 16% سرطانهای ریه در مرحله لوکال شناسایی میشوند که نرخ بقای 5 ساله آنها 55% میباشد (جدول 8).
لنفوم
موارد جدید: میزان برآورد تعداد موارد لنفوم در سال 2017 در امریکا 80500 مورد میباشد. این سرطان از برخی سلولهای ایمنی شروع میشود و به دو دسته لنفوم هوچکین (8/260 مورد) و لنفوم غیرهوچکین (72240 مورد) تقسیم میشود. برحسب نوع سلولها، ویژگیهای مولکولی، محل آناتومیک، عفونتهای خاص و سایر خصوصیات، خود لنفومهای هوچکین (HL) و غیرهوچکین (NHL) به زیرگروههایی تقسیمبندی میشوند. متداولترین زیرگروههای NHL شاملdiffuse large B-cell lymphoma و لنفوم فولیکولار میشوند (CLL به لحاظ مشابهت باsmall lymphatic lymphoma جزء NHL طبقهبندی میشود ولی در این مقاله CLL در بخش لوسمی ها موردبحث قرار گرفته است).
روند وقوع: نرخ وقوع لنفوم هوچکین و غیرهوچکین درمجموع از سال 2004 تا 2013 ثابت مانده است گرچه این نرخ در زیرگروهها متفاوت است.
مرگ: تعداد مرگ ناشی از لنفوم هوچکین 1070 و برای NHL، 20140 مورد در سال 2017 برآورد میشود.
روند مورتالیتی: با پیشرفت روشهای درمانی، نرخ مرگ ناشی از لنفوم هوچکین از سال 1975 و برای NHL از اواسط دهه 1990 کاهشی بوده است. از سال 2005 تا 2014 نرخ کاهش مرگ ناشی از لنفوم هوچکین سالانه حدود 4% و برای NHL سالانه 2% بوده است.
علائم و نشانهها: متداولترین علائم لنفوم بهواسطه بزرگ شدن غدد لنفاوی بروز میکنند و شامل غدد لنفاوی برآمده، درد سینه، تنگی نفس، احساس پری در شکم و کاهش اشتها میشوند. سایر علائمی که ممکن است بروز کنند عبارتند از: خارش، تعریق شبانه، خستگی، کاهش وزن و تب متناوب.
عوامل خطرساز: مانند بیشتر سرطانها وقوع NHL با افزایش سن بالا میرود، اما در لنفوم هوچکین میزان خطر ابتلا در نوجوانی و ابتدای بزرگسالی افزایش مییابد و در میانسالی کاهش یافته و سپس در کهنسالی مجدداً افزایش مییابد.
بیشتر عوامل خطرساز لنفوم آنهایی هستند که سیستم ایمنی را شدیداً تضعیف میکنند، بهعنوان مثال در افرادی که بخاطر پیوند عضو داروهای مضعف ایمنی دریافت میکنند خطر ابتلا به لنفوم افزایش مییابد. برخی عوامل عفونی (نظیر ویروس اپشتینبار) خطر ابتلا به برخی از زیرگونههای لنفوم را افزایش میدهند، علاوه بر این عفونت مزمن با میکروبهای مضعف سیستم ایمنی (نظیر HIV) و یا عفونت با میکروبهایی که سبب برانگیختگی مستمر سیستم ایمنی میشوند (نظیر H. pylori و HCV) نیز ابتلا به لنفوم را افزایش میدهند. برخی از بیماریهای خودایمنی (نظیر سندرم شوگرن، لوپوس و رماتیسم مفصلی) نیز موجب افزایش ابتلا به لنفوم میشوند.
سابقه خانوادگی هم خطر ابتلا به همه زیرگروههای لنفوم هوچکین و غیرهوچکین را افزایش میدهد و تغییرات ژنتیکی شناختهشدهای که موجب افزایش خطر ابتلا به لنفوم میشوند بهطور فزایندهای در حال شناسایی هستند.
برخی مطالعات، برای عوامل رفتاری همچون وزن بدن و نیز مواجهه با برخی از عوامل محیطی در ایجاد لنفوم نقش قائل هستند.
درمان: NHL معمولاً با شیمیدرمانی یا اشعه درمانی بهتنهایی یا بهطور توأمان درمان میشوند. برای برخی زیرگروههای NHL، ایمونوتراپی هدفمند نیز استفاده میشود. اینها آنتیبادیهایی هستند که به یک داروی شیمیدرمانی یا اتم رادیواکتیو متصل شدهاند. اگر بعد از درمان استاندارد NHL بهبود نیابد یا عود کند پیوند سلولهای بنیانی را هم میتوان مدنظر قرار داد.
لنفوم هوچکین را بسته به مرحله بیماری و نوع سلول معمولاً بهوسیله شیمیدرمانی، پرتودرمانی و یا ترکیب هر دو درمان میکنند. درصورتیکه این درمان مؤثر نباشد، پیوند سلول بنیانی و یا درمان با آنتیبادی منوکلونال متصل به دارو درنظر گرفته میشود.
بقا: میزان بقا بستگی به زیرگونههای لنفوم و مرحله آن دارد و در زنان اندکی بهتر از مردان است. میزان بقای 5 ساله برای لنفوم هوچکین در مردان 85% و در زنان 87% و برای NHL در مردان 69% و در زنان 72% میباشد.
حفره دهان و حلق
موارد جدید: موارد جدید سرطان حفره دهان و حلق در سال 2017 در امریکا 49670 مورد برآورد میشود. میزان وقوع در مردان نسبت به زنان بیش از دو برابر بالاتر است.
روند وقوع: نرخ وقوع از سال 2004 تا 2013 در میان سیاهپوستان سالانه 2% کاهش و در سفیدپوستان 1% افزایش نشان میدهد که این افزایش عمدتاً ناشی از انواعی از سرطان زبان، اروفارنکس و لوزههاست که بهواسطه HPV بوجود میآیند.
مرگ: بالغ بر 9700 مورد مرگ ناشی از این سرطان در سال 2017 در امریکا تخمین زده میشود.
روند مورتالیتی: روند طولانی کاهش نرخ مرگ براثر سرطان حفره دهان و حلق در سالهای اخیر متوقف شده است و نرخ آن بین سالهای 2005 تا 2014 ثابت مانده است.
علائم و نشانهها: علائم شامل ضایعهای در حلق یا گلو که بهراحتی خونریزی میکند و بهبود نمییابد، لکه قرمز یا سفید پایدار، وجود یک توده یا ضخیم شدن بخشی از دهان یا حلق، گوش درد، توده گردنی و سرفه خونآلود میباشند. اشکال در جویدن، تورم یا اشکال در حرکت زبان و فک از علائم دیررس محسوب میشوند.
عوامل خطرساز: عوامل خطرساز شناخته شده مصرف دخانیات والکل میباشند. در افرادی که هم الکل و هم دخانیات مصرف میکنند این خطر تا 30 برابر افزایش مییابد. عفونت HPV دهان و حلق که احتمالاً ناشی از تماس جنسی است هم این خطر را افزایش میدهد.
پیشگیری: گرچه در کارآزماییهای بالینی اثرات پیشگیرانه واکسن HPV تنها بر بیماریهای جنسی احراز شده است، اما احتمالاً این واکسن جلوی برخی از موارد سرطان حلق و دهان ناشی از HPV را میگیرد. متأسفانه در مقایسه با کشورهای دیگر مصرف واکسن HPV در آمریکا کمتر بوده و تنها در 28% پسران و 42% دختران بین 13 تا 17 سال این واکسن در سه دوز توصیه شده در سال 2015 مورد استفاده واقع شده است.
تشخیص زودهنگام: هر بخش از حفره دهان شامل لبها، زبان، دهان و حلق ممکن است مبتلا به سرطان گردد. معاینه چشمی توسط دندانپزشک و پزشک میتواند ضایعات پیشسرطانی را در زمانی که هنوز قابلیت بیشتری برای درمان دارند، شناسایی کند.
درمان: پرتودرمانی و جراحی بهطور منفرد یا توأمان راهکار استاندارد درمانی هستند که در موارد پیشرفته شیمیدرمانی هم اضافه میگردد. درمان هدفمند را میتوان در مرحله اول همراه پرتودرمانی بکار گرفت و یا اینکه در عود سرطان مورد استفاده قرار داد. ایمونوتراپی راهکار جدیدی برای موارد پیشرفته یا عود سرطان محسوب میگردد.
بقا: نرخ بقای 5 ساله برای سرطانهای حفره دهان و حلق در سفیدپوستان 66% و در سیاهپوستان 47% میباشد. حدود یکسوم موارد در مرحله لوکال تشخیص داده میشود که نرخ بقا برای آنها 83% در سفیدپوستان و 79% در سیاهپوستان میباشد. مطالعات نشان میدهد درصورتیکه تست HPV مثبت باشد میزان بقا افزایش خواهد داشت.
تخمدان
موارد جدید: برآورد وقوع موارد جدید در سال 2017 در آمریکا تعداد 22440 مورد سرطان تخمدان میباشد.
روند وقوع: در طی دو دهه اخیر نرخ وقوع سرطان تخمدان در زنان سفیدپوست 1% و در زنان سیاهپوست 0/4 درصد در هرسال کاهش یافته است.
مرگ: در سال 2017 تعداد 14080 مورد مرگ ناشی از سرطان تخمدان در امریکا رخ خواهد داد. 5% مرگهای ناشی از سرطان در زنان مربوط به سرطان تخمدان میشود که در بین سرطانهای قسمت تناسلی از همه بالاتر است.
روند مورتالیتی: مرگ ناشی از سرطان تخمدان از سال 1975 به بعد کاهش یافته است. از سال 2005 تا 2014 میزان این کاهش در سفیدپوستان سالانه 2% و در سیاهپوستان سالانه 1% بوده است.
علائم و نشانهها: سرطان تخمدان در مراحل اولیه معمولاً هیچ علامت مشخصی ندارد، اما برخی مطالعات نشان میدهد که در عدهای از زنان مبتلا ماهها قبل از تشخیص بیماری علائم غیراختصاصی همچون نفخ، درد لگن یا شکم، مشکل در غذا خوردن و یا زود سیر شدن و فوریت یا تکرر ادرار مشاهده میشود. زنانی که بیش از چند هفته با چنین علائمی مواجه میشوند باید سریعاً به پزشک مراجعه کنند.
متداولترین نشانه سرطان تخمدان ورم شکم است که بهواسطه تجمع مایعات ایجاد میشود. خونریزی غیرطبیعی مهبلی یکی از علائم نادر سرطان تخمدان است که همچنین ممکن است در سرطان دهانه رحم و رحم مشاهده شود.
عوامل خطرساز: مهمترین عامل خطر، وجود سابقه ابتلا به سرطان تخمدان و سینه در خانواده است. زنانی که سابقه ابتلا به سرطان سینه داشتهاند و یا آزمایش ژنهایی همچون BRCA1 و BRCA2 در آنها مثبت شده است، در معرض خطر بیشتری هستند. جراحی پیشگیرانه تخمدان و لولههای فالوپ در این زنان خطر را کاهش میدهد.
بیماری التهاب لگن و سندرم Lynch نیز موجب افزایش خطر میشوند. آژانس بینالمللی تحقیقات سرطان اخیراً اعلام کرده که چاقی نیز خطر سرطان تخمدان را افزایش میدهد. استفاده از هورمون بعد از یائسگی (استروژن بهتنهایی و یا استروژن و پروژسترون بهطور توأمان) نیز با افزایش خطر همراه است. مصرف دخانیات خطر ابتلا به نوع نادری از سرطان تخمدان (موسینی) را افزایش میدهد. حاملگی، مصرف طولانی مدت ضدحاملگیهای خوراکی و بستن لوله فالوپ یا جراحی آن خطر ابتلا را کاهش میدهند. استفاده از پودر تالک در ناحیه تناسلی ممکن است اندکی خطر ابتلا را افزایش دهد که هنوز این استنتاج قطعی نشده است.
تشخیص زودهنگام: هنوز هیچ روش غربالگری دقیقی برای بررسی زنانی که ریسک متوسط دارند پیدا نشده است. معاینه لگن که گاهی همراه با سونوگرافی واژینال انجام میشود برای بررسی زنانی که علامتدار هستند بکار میرود، ولی بندرت میتواند سرطان تخمدان را شناسایی کند و اگر هم چنین اتفاقی بیفتد معمولاً در مرحله پیشرفته سرطان میباشد. در زنانی که ریسک بالایی دارند معاینه لگنی همراه با سونوگرافی واژینال و آزمایش CA125 پیشنهاد میگردد، گرچه این استراتژی در زنانی که ریسک متوسط دارند اثر ثابتشدهای در کاستن مورتالیتی ناشی از سرطان تخمدان نداشته است.
شواهدی در دست است که نشان میدهد تغییر مقدار CA125 در طی زمان بیشتر از نتیجه یک آزمایش تکی قدرت پیشبینی خطر را دارد.
درمان: درمان شامل جراحی و اغلب شیمیدرمانی میشود. جراحی شامل برداشتن هردو تخمدان، لولههای فالوپ، رحم و بافت چربی اطراف میشود و از پریتونئوم (لایه داخل شکم) بیوپسی بعمل میآید. در زنان جوان که در مراحل ابتدایی تشخیص داده میشوند و مایل به حفظ باروری هستند ممکن است فقط تخمدان گرفتار و لوله فالوپ آن سمت برداشته شوند. در بیمارانی که زودهنگام تشخیص داده میشوند مرحلهبندی جراحی دقیق (شامل آزمایش میکروسکوپی بافت قسمتهای مختلف لگن و شکم) به بهبود نتیجه درمان کمک میکند.
در برخی بیماران در مرحله پیشرفته تزریق مستقیم داروی شیمیدرمانی به داخل شکم میزان بقا را بهبود میبخشد، اما در سال 2012 تنها نیمی از این افراد واجد شرایط به این طریق درمان شدند که احتمالاً بخاطر ترس از عواقب خطرات جانی آن بوده است. در برخی موارد پس از آنکه تومور را با درمانهای دیگر کوچک کردند و یا درمواردی که رشد سرطان کند است از داروهای هدفمند استفاده میشود.
بقا: بقای 5 ساله مبتلایان به سرطان تخمدان نسبتاً کم است (46%) چراکه بیشتر بیماران (60%) در مرحلهای تشخیص داده میشوند که بیماری به نقاط دور متاستاز داده است که در این افراد شانس بقای 5 ساله 29% است. برای آن دسته از بیماران که در مرحله لوکال تشخیص داده میشوند (15%) شانس بقای 5 ساله 92% میباشد. نرخ بقای 5 ساله به سن بیماران هم بستگی دارد و در زنان پایینتر از 45 سال حدود 77% و در افراد بالای 75 سال حدود 20% میباشد.
پانکراس
موارد جدید: تعداد موارد جدید تشخیص سرطان پانکراس در سال 2017 در امریکا قریب به 53670 مورد میباشد. اکثر این موارد (94%) در بافت اگزوکرین پانکراس هستند که آنزیمهای لازم را برای هضم غذا ترشح میکند. تومورهای بافت اندوکرین (6%) در سلولهایی ایجاد میشوند که وظیفه تولید هورمونها را برعهده دارند. این تومورها پیشآگهی بهتری داشته و در سنین پایینتر ایجاد میشوند.
روند وقوع: نرخ وقوع سرطان پانکراس از سال 2004 تا 2013 در سفیدپوستان سالانه 1% افزایش یافته ولی در سیاهپوستان ثابت مانده است.
مرگ: سرطان پانکراس چهارمین علت مرگ ناشی از سرطان در مردان و زنان میباشد و تخمین زده میشود که تعداد 43090 نفر در سال 2017 براثر این بیماری در آمریکا فوت کنند.
روند مورتالیتی: از سال 2005 تا 2014، میزان مرگ براثر سرطان پانکراس در مردان سفیدپوست سالانه 0/3 درصد افزایش یافته، در زنان سفیدپوست ثابت مانده و در زنان و مردان سیاهپوست 0/5 درصد افزایش یافته است.
علائم و نشانهها: تا زمان پیشرفت بیماری معمولاً علامتی ظاهر نمیشود و در آن هنگام علائمی همچون کاهش وزن، درد شکمی که به پشت تیر میکشد و بندرت ایجاد دیابت، نمایان میگردند. تومورهایی که نزدیک مجرای صفرای اصلی رشد میکنند گاهی سبب یرقان میگردند که این امر به تشخیص زودهنگام کمک میکند. نشانههای مراحل پیشرفته بیماری شامل درد شدید شکمی، تهوع و استفراغ میباشند.
عوامل خطرساز: خطر سرطان پانکراس در افراد سیگاری دو برابر کسانی است که هرگز سیگار نکشیدهاند. سایر عوامل خطرساز شامل سابقه ابتلا در خانواده، سابقه پانکراتیت مزمن، یا دیابت در خود فرد و چاقی میباشند. مصرف بیش از حد الکل هم موجب افزایش خطر میشود. مبتلایان به سندرم Lynch و برخی سندرمهای ژنتیکی دیگر مانند ناقلین موتاسیونهای BRCA1و BRCA2 نیز در معرض افزایش خطر هستند.
درمان: جراحی، پرتودرمانی و شیمیدرمانی روشهایی هستند که ممکن است طول عمر را افزایش دهند و یا علائم را کمتر سازند ولی بندرت بهبودی کامل حاصل میشود. کمتر از 20% بیماران کاندیدای جراحی هستند زیرا که اکثر موارد سرطان پانکراس به هنگام تشخیص در اعضای دیگر متاستاز دادهاند و قابل جراحی نمیباشند. در کسانی که جراحی میشوند شیمیدرمانی و گاهی پرتودرمانی ممکن است به کاهش ریسک عود بیماری کمک نماید. در مراحل پیشرفته بیماری، شیمیدرمانی (و گاهی به همراه داروهای هدفمند) ممکن است طول عمر بیمار را افزایش دهد. در حال حاضر کارآزماییهای بالینی متعددی در حال آزمایش داروهای جدید برای بهبود طول عمر این بیماران میباشند.
بقا: میزان بقای 5 ساله برای همه مراحل بیماری درمجموع 8% است. حتی برای آن عده اندکی (9%) که بیماری در مرحله لوکال تشخیص داده میشود، میزان بقای 5 ساله 29% است. حدود نیمی (52%) از بیماران در مرحلهای تشخیص داده میشوند که سرطان به نقاط دوردست متاستاز داده است که در این افراد نرخ بقای 5 ساله 3% میباشد.
پروستات
موارد جدید: برآورد تعداد موارد جدید سرطان پروستات در سال 2017 در آمریکا 161/360 مورد میباشد. سرطان پروستات در کنار سرطان پوست بیشترین موارد سرطان مردان را تشکیل میدهد. خطر ابتلا در سیاهپوستان 74% بیشتر از سفیدپوستان است که علت آن نامشخص است و احتمالاً به زمینه ژنتیکی مربوط میشود.
روند وقوع: با بکارگیری آزمایش PSA جهت غربالگری گسترده سرطان پروستات در اواخر دهه 1980 و اوایل دهه 1990، نرخ وقوع این بیماری شدیداً افزایش یافت. در حوالی سال 2000 این رشد کاهش یافت و در سالهای اخیر کاهش رشد شدت گرفت که این امر نیز احتمالاً بخاطر توصیههایی بود که در سال 2008 علیه بکارگیری روتین PSA در تشخیص سرطان پروستات بعمل آمده است. از سال 2009 تا 2013 نرخ وقوع سالانه 8% کاهش یافته است.
مرگ: تعداد مرگ ناشی از سرطان پروستات در سال 2017 در آمریکا 26730 مورد برآورد میشود که با این حساب سرطان پروستات سومین عامل مرگ ناشی از سرطان در مردان محسوب میگردد.
روند مورتالیتی: مرگ ناشی از سرطان پروستات از اوایل دهه 1990 در همه نژادها کاهش یافته، گرچه هنوز در مردان سیاهپوست دو برابر بقیه نژادها میباشد (جدول 10). درمجموع از سال 1999 مرگ ناشی از سرطان پروستات سالانه 3% کاهش نشان میدهد.
علائم و نشانهها: سرطان پروستات در مراحل اولیه معمولاً هیچ علامتی ندارد. با پیشرفت بیماری علائمی همچون ضعیف شدن یا قطع جریان ادرار، اشکال در شروع یا خاتمه دفع ادرار، نیاز به دفع مکرر به ویژه در شب، خون در ادرار یا درد و سوزش بهنگام ادرار ظاهر میشوند. سرطان پیشرفته معمولاً به استخوان متاستاز داده و در لگن و ستون فقرات، دندهها و سایر نواحی ایجاد درد میکند.
عوامل خطرساز: فاکتورهای خطرساز شناخته شده محدود به افزایش سن، نژاد آفریقایی، سابقه خانوادگی و برخی تغییرات ژنتیکی ارثی میباشند. مردان سیاهپوست آمریکایی و مردان جزایر کارائیب که نژاد آفریقایی دارند بیشترین نرخ وقوع سرطان پروستات را دارا میباشند. مطالعات ژنتیکی نشان میدهند که استعداد خانوادگی میتواند مسئول 5 تا 10 درصد موارد سرطان پروستات باشد. سندرم Lynch، موتاسیون BRCA1 و BRCA2 هم سبب افزایش خطر میشوند. مصرف دخانیات ممکن است نوع کشنده سرطان پروستات را افزایش دهد.
پیشگیری: پیشگیری از سرطان پروستات با استفاده از داروها و مواد شیمیایی بشدت تحت مطالعه و بررسی میباشد. دو داروی موردتوجه یعنی finasteride و dutasteride مقدار برخی از هورمونها را در بدن کاهش میدهند و مصرف آنها در هیپرپلازی خوشخیم پروستات مجاز میباشد. گرچه بنظر میرسد این داروها موجب کاهش سرطان پروستات میشوند، اما بهواسطه اثرات سوئی که دارند استفاده از آنها برای پیشگیری از سرطان پروستات مجاز نیست.
تشخیص زودهنگام: در حال حاضر هیچ نهادی غربالگری روتین سرطان پروستات را در مردان با ریسک متوسط حمایت نمیکند، زیرا خطر تشخیص بیش از حد وجود دارد؛ به این معنی که سرطانهایی شناسایی میشوند که هیچگاه مهاجم نخواهند شد و ایجاد علامت نخواهند کرد، اما شناسایی و درمان آنها موجب خسارات فراوانی میگردد. انجمن سرطان آمریکا توصیه میکند که مردان با ریسک متوسط در شروع 50 ســــــالگی و انتظار عمر (life expectancy) حداقل 10 ساله با پزشک خود درخصوص انجام یا عدم انجام آزمایش PSA مذاکره کنند و آگاهانه با توجه به منافع و مضار آن تصمیم به انجام آزمایش یا عدم انجام آن بگیرند. مردانی که ریسک بالاتری جهت ابتلا به سرطان پروستات دارند (سیاهپوستان یا کسانی که یکی از نزدیکان آنها قبل از 65 سالگی سرطان پروستات گرفته است) باید این مذاکره را قبل از 45 سالگی انجام دهند و در کسانی که خطر از این هم بالاتر است (مثل کسانی که چندین نفر از افراد فامیل آنها در سنین پایین تشخیص سرطان پروستات داشتهاند) باید در 40 سالگی اقدام به مذاکره با پزشک خود نمایند.
درمان: انتخاب درمان به عواملی چون سن، مرحله بیماری، درجه سرطان و ترجیحات خود بیمار بستگی دارد. در مورد بسیاری از بیماران زیر نظر داشتن بیماری در طی زمان نسبت به انجام جراحی اولویت دارد، بهویژه چنانچه هنوز مراحل اولیه بیماری باشد و یا تومور مهاجم نباشد و یا اینکه سن بیمار خیلی بالا باشد. روشهای درمانی شامل جراحی، تابش اشعه از بیرون و براکیتراپی میباشد. در موارد پیشرفتهتر در کنار جراحی و پرتودرمانی استفاده از درمان هورمونی هم امکانپذیر است. این درمانها معمولاً کیفیت زندگی فرد را کاهش میدهند و اثرات جانبی آن مانند اختلال ادرار و نعوظ (دائم یا موقت) موجب آزار بیمار میگردد. تحقیقات جاری درصدد یافتن مارکرهای بیولوژیک جدیدی هستند که بتوانند بین سرطان مهاجم و غیرمهاجم افتراق قائل شوند تا از درمان غیرضروری اجتناب گردد.
در موارد دستاندازی سرطان به نقاط دوردست، درمان هورمونی، شیمیدرمانی، پرتودرمانی و سایر درمانها مورد استفاده قرار میگیرد. درمان هورمونی در سرطان پیشرفته پروستات با کوچک کردن تومور و محدود کردن رشد آن میتواند به مدت طولانی به رفع علائم درد و سایر علامتها کمک کند.
غالباً اگر درمان هورمونی کفایت نکند، شیمیدرمانی شروع میشود، گرچه مطالعات اخیر نشان دادهاند که اگر از همان اول همراه با درمان هورمونی شیمیدرمانی هم شروع شود طول عمر بیمار بیشتر افزایش مییابد. در مردانی که سرطان متاستاتیک دارند و به درمان هورمونی جواب نمیدهند انتخاب دیگر استفاده از واکسنی است که سیستم ایمنی فرد را علیه سلولهای سرطانی تحریک میکند.
اَشکال جدید درمان هورمونی برای درمان سرطانهای متاستاتیک که به هورمون درمانی اولیه و شیمیدرمانی مقاوم بودهاند تأثیر مثبتی نشان دادهاند. داروهای دیگری هم هستند که در متاستاز سرطان پروستات به ا ستخوان مورد استفاده قرار میگیرند.
بقا: 92% موارد سرطان پروستات در مرحله لوکال شناسایی میشوند که برای این گروه شانس بقای 5 ساله 100% است. درصورتیکه متاستاز به نقاط دور انجام شده باشد شانس بقای 5 ساله 29% میباشد. نرخ بقای 10 و 15 سال برای سرطان پروستات به ترتیب 98% و 96% است.
پوست
موارد جدید: متداولترین سرطانی که در آمریکا تشخیص داده میشود سرطان پوست است، اما تعداد واقعی بسیاری از این سرطانها (شامل سرطان سلولهای بازال و سنگفرشی) که به آنها سرطان غیرملانومی هم میگویند مشخص نیست چرا که گزارش آنها اجباری نمیباشد. آخرین مطالعه درخصوص کارسینوم کراتینوسیت در سال 2012 نشان میدهد که 5/4 میلیون مورد وقوع سرطان در 3/3 میلیون نفر شناسایی شده است (به عبارت دیگر در برخی افراد بیش از یک مورد کارسینوم کراتینوسیت وجود داشته است).
ملانوم مهاجم حدود 1% از تمام انواع سرطانهای پوست را تشکیل میدهد اما بیشترین موارد مرگ ناشی از سرطان پوست مربوط به ملانوم میباشد. برآورد میشود که تعداد موارد جدید ملانوم در سال 2017 در امریکا بالغ بر 87110 مورد باشد. بیشترین وقوع آن در سفیدپوستان غیراسپانیاییتبار میباشد (26 در صدهزار) درحالیکه این عدد در سفیدپوستان اسپانیایی 5 و در سیاهپوستان 1 در صدهزار است. میزان وقوع قبل از 50 سالگی در زنان بیشتر است اما در 65 سالگی در مردان به دو برابر زنان و در هشتاد سالگی سه برابر زنان میشود.
روند وقوع: وقوع ملانوم در طی سی سال گذشته سریعاً افزایش یافته است اما درحال حاضر روند وقوع به سن بستگی دارد. از سال 2004 تا 2013، نرخ وقوع 2 تا 3 درصد در سال در میان مردان و زنان بالای 50 سال افزایش داشته است اما در افراد زیر 50 سال ثابت مانده است.
مرگ: برآورد تعداد مرگ ناشی از ملانوم در سال 2017 در امریکا بالغ بر 9730 مورد میباشد.
روند مورتالیتی: روند مورتالیتی برحسب سن متفاوت است. از سال 2005 تا 2014، نرخ مرگ در افراد بالاتر از 50 سال ثابت مانده اما در افراد کمتر از 50 سال سالانه 2/6% کاهش یافته است.
علائم و نشانهها: علائم هشداردهنده همه انواع سرطان پوست شامل تغییر در اندازه، شکل یا رنگ یک خال یا ضایعه پوستی و یا رشد و ایجاد ضایعه جدید و یا زخمی که خوب نمیشود، میباشد. تغییراتی که یک ماه یا بیشتر بطول میانجامد باید توسط پزشک بررسی شود. کارسینوم سلول بازال بهصورت ضایعهای تخت یا اندکی برآمده به رنگ صورتی یا قرمز و براق که با مختصر جراحتی خونریزی میکند، تظاهر مینماید. کارسینوم سلولهای سنگفرشی به شکل یک توده رشدیابنده، اغلب با سطح زبر و یا یک ضایعه تخت قرمز که به آهستگی رشد میکند نمایان میشود.
عوامل خطرساز: وجود سابقه فردی یا خانوادگی ابتلا به ملانوم یا حضور بیش از 50 خال بزرگ و آتیپیک از عوامل خطرساز برای ملانوم محسوب میگردند. قرار گرفتن در معرض اشعه ماوراء بنفش اعم از نور خورشید یا سیستمهای برنزهکننده برای همه انواع سرطان عامل خطرساز هستند. در افرادی که به نور حساس هستند یا سابقه مواجهه طولانی با نور خورشید را دارند و نیز در بیماریها یا درمانهایی که سیستم ایمنی سرکوب میگردد و نیز سابقه ابتلای قبلی به سرطان پوست، ریسک ابتلا افزایش مییابد.
پیشگیری: با اقداماتی همچون اجتناب از مواجهه با نور خورشید، استفاده از سایهبان، لباس بلند، کلاه لبهدار، عینک آفتابی و کرمهای ضدآفتاب میتوان خطر ابتلا به سرطان پوست را کاهش داد. کودکان را بهویژه باید از نور خورشید محافظت نمود چراکه آفتابسوختگی احتمال ابتلا به ملانوم را افزایش میدهد. در ژولای 2014 جراحان عمومی آمریکا فراخوانی برای اقدام بر پیشگیری سرطان پوست صادر کردند چرا که تعداد آن رو به افزایش بود. هدف از این فراخوان افزایش آگاهی آمریکاییها و درگیر کردن آنها در رفتارهای پیشگیرانه از سرطان پوست بود.
تشخیص زودهنگام: بهترین راه شناسایی زودهنگام سرطان پوست توجه به تغییرات پوستی بهویژه موارد غیرمعمول آن میباشد. هر ضایعه جدید و نیز تغییرات پیشرونده در ضایعات قدیمی (تغییر در اندازه، شکل، رنگ و …) باید فوراً توسط پزشک بررسی شود.
درمان: سرطانهای نوپای پوست بهوسیله جراحی برداشته میشوند. مراحل اولیه کارسینوم کراتوسیت را میتوان بهوسیله جراحی، electrodesiccation و کورتاژ یا کرایوسرجری درمان کرد. پرتودرمانی و برخی داروهای موضعی هم ممکن است مورد استفاده قرار بگیرند. در مورد ملانوم، بافت سرطانی به همراه بخشی از بافت سالم اطراف برداشته میشود و گاهی هم غدد لنفاوی مسیر جهت بررسی متاستاز برداشته میشوند. اگر غدد لنفاوی مجاور سرطانی باشند ممکن است غدد لنفاوی دورتر هم برداشته شوند. ملانومی که به عمق پوست دستاندازی کرده یا به غدد لنفاوی سرایت نموده را با جراحی، ایمونوتراپی، شیمیدرمانی و یا پرتودرمانی تحت درمان قرار میدهند. درمان ملانوم پیشرفته در سالهای اخیر تغییرات زیادی کرده است چراکه FDA روشهای متعدد جدیدی را مبتنی بر ایمونوتراپی و داروهای هدفمند برای ملانوم تأیید کرده است که میتوانند بسیاری از ملانومها را تخریب کنند. شیمیدرمانی را هم میتوان به کار گرفت اما تأثیر آن از درمانهای جدید کمتر است.
بقا: تقریباً تمام موارد کارسینوم کراتوسیت بهویژه د مراحل اولیه آن قابل درمان میباشند. گرچه ملانوم هم در مراحل اولیه بشدت قابل درمان است، اما احتمال گسترش آن به سایر نقاط بدن بیش از کارسینوم کراتوسیت میباشد. در مراحل لوکال نرخ بقای 5 ساله 98% و در موارد تهاجم محلی 62% و متاستاز به نقاط دوردست 18% میباشد.
تیروئید
موارد جدید: برآورد تعداد موارد جدید تیروئید در سال 2017 در امریکا 56870 مورد میباشد که سهچهارم آن در زنها خواهد بود. سرطان تیروئید متداولترین سرطان در بین زنان 20 تا 34 سال میباشد.
روند وقوع: در چند دهه گذشته میزان وقوع سرطان تیروئید در جهان افزایش یافته است و تقریباً سریعترین رشد وقوع سرطان را در آمریکا دارد که این موضوع تا حدود زیادی به خاطر پیشرفت در روشهای حساس تشخیصی است که ممکن است حتی موجب تشخیص بیش از حد (overdiagnosis) شوند. از سال 2004 تا 2013 تعداد موارد سرطان تیروئید در آمریکا سالانه حدود 5% در زنان و مران افزایش یافته است که به نظر میرسد از شدت این افزایش در سالهای اخیر کاسته شده باشد.
مرگ: پیشبینی میشود که 2010 مورد مرگ براثر ابتلا به سرطان تیروئید در سال 2017 در آمریکا اتفاق بیفتد.
روند مورتالیتی: نرخ مرگ ناشی از سرطان تیروئید از سال 2005 تا 2014 مختصری افزایش یافته و از 0/48 در صدهزار به 0/5 در صدهزار رسیده است.
علائم و نشانهها: مهمترین علامت سرطان تیروئید وجود یک توده در گردن است که توسط خود فرد یا پزشک کشف میشود. سایر علائم شامل احساس پری و سفتی در گردن، اختلال در تنفس و بلع، خشونت صدا، تورم غدد لنفاوی و درد مستمر در گلو و گردن میباشند. بسیاری از سرطانهای تیروئید بهطور تصادفی در عکس رادیولوژی شناسایی میشوند.
عوامل خطرساز: جنسیت مؤنث، سابقه گواتر یا ندولهای تیروئید، سابقه سرطان تیروئید در خانواده و قرار گرفتن در معرض اشعه در دوران کودکی از عوامل خطرساز تیروئید محسوب میشوند.
افرادی که دارای موتاسیون در ژن موسوم بهRET هستند در معرض نوع خاصی از سرطان تیروئید میباشند که با برداشتن تیروئید بهوسیله جراحی میتوانند این خطر را کاهش دهند.
برخی سندرمهای ژنتیکی نادر نظیر پولیپوز آدنوماتوز فامیلی (FAP) هم خطر ابتلا را افزایش میدهند. چاقی نیز خطر ابتلا را اندکی افزایش میدهد.
درمان: بیشتر سرطانهای تیروئید قابلیت درمان بسیار بالایی دارند اما برخی از انواع آن (نوع مدولاری و آناپلاستیک) که 5% موارد را شامل میشوند مهاجمتر بوده و احتمال گسترش به سایر اعضاء را دارند. نوع درمان به نوع سلول، اندازه تومور و وسعت بیماری بستگی دارد. انتخاب اولیه جراحی است که بخشی یا تمام تیروئید را برمیدارند و گاهی غدد لنفاوی اطراف را نیز جراحی میکنند. در مورد تومورهای بزرگ یا وجود متاستاز بعد از جراحی استفاده از ید رادیواکتیو (I-131) برای از بین بردن بقایای سلولهای سرطانی توصیه میشود. پس از جراحی تیروئید جهت حفظ عملکرد طبیعی بدن، هورمونهای تیروئیدی بهطور مستمر تجویز میشود. در مورد برخی انواع پیشرفته سرطان تیروئید داروهای هدفمند جهت کمک به کوچک کردن تومور مورد استفاده قرار میگیرند.
بقا: میزان بقای 5 ساله در سرطان تیروئید 98% است، معذلک نرخ بقا به مرحله بیماری، سن بیمار و زیرگروه سرطان بستگی دارد (جدول 8).
مثانه
موارد جدید: پیشبینی میشود موارد جدید سرطان مثانه در سال 2017 در امریکا بالغ بر 79030 مورد باشد. وقوع سرطان مثانه در مردان چهار برابر زنان و در سفیدپوستان دو برابر سیاهپوستان میباشد.
روند وقوع: بعد از چند دهه افزایش آهسته وقوع سرطان مثانه، میزان وقوع آن در سفیدپوستان شروع به کاهش کرده اما در سیاهپوستان چنین اتفاقی نیفتاده است. از سال 2009 تا 2013 همهساله رخداد سرطان مثانه در زنان و مردان سفیدپوست 1% کاهش، در مردان سیاهپوست 0/5 درصد افزایش داشته و در زنان سیاهپوست ثابت مانده است.
مرگ: انتظار میرود در سال 2017 تعداد 16870 مرگ ناشی از سرطان مثانه در آمریکا اتفاق بیفتد.
روند مورتالیتی: برخلاف تعداد وقوع، نرخ مرگ ناشی از سرطان مثانه از سال 2005 تا 2014 در زنان سیاهپوست 1% کاهش و در زنان سفیدپوست 0/3 درصد کاهش داشته و در مردان سفیدپوست ثابت مانده است.
علائم و نشانهها: بهواسطه مشاهده خون در ادرار یا علائمی چون تکرر ادرار و فوریت ادرار یا درد و ناراحتی به هنگام دفع ادرار، سرطان مثانه معمولاً زود تشخیص داده میشود.
عوامل خطرساز: استعمال دخانیات عامل خطرساز شناخته شده برای سرطان مثانه است که نیمی از موارد این بیماری را شامل میگردد. کار کردن در صنایع لاستیک، چرم، آلومینیوم، نقاشی و رنگرزی و نیز استفاده از آب آشامیدنی حاوی مقادیر بالای آرسنیک هم خطر ابتلا به سرطان مثانه را افزایش میدهد. برخی اختلالات مادرزادی مثانه نیز خطرساز هستند.
تشخیص زودهنگام: برای افرادی که ریسک متوسط دارند در حال حاضر هیچ آزمایش غربالی توصیه نشده است. تشخیص سرطان مثانه با آزمایش میکروسکوپی سلولهای بدست آمده از ادرار یا بافت مثانه و معاینه دیواره مثانه با سیستوسکوپ انجام میشود. برای افرادی که در معرض خطر بالا هستند و نیز پیگیری پس از درمان، این آزمایشها بهمراه آزمایشهای دیگر میتوانند جهت غربالگری استفاده شوند.
درمان: جراحی بهتنهایی یا در ترکیب با روشهای دیگر در 90% موارد سرطان مثانه مورد استفاده قرار میگیرد. در مراحل اولیه بیماری پس از برداشت تومور میتوان داروهای شیمیدرمانی و ایمنیدرمانی را مستقیماً به داخل مثانه تزریق کرد و در موارد پیشرفته بیماری ممکن است که برداشت کل مثانه بهوسیله جراحی ضرورت داشته باشد. استفاده از شیمیدرمانی بهتنهایی یا همراه با پرتودرمانی قبل از سیستکتومی نتایج عمل را بهبود میبخشد. پایش بهموقع پس از جراحی نهایت اهمیت را دارد چراکه احتمال عود سرطان مثانه بسیار بالاست. در موارد متاستاتیک، شیمیدرمانی درمان انتخابی است که گاهی همراه با پرتودرمانی انجام میشود. درصورتیکه شیمیدرمانی نتیجهبخش نباشد ایمنیدرمانی یک انتخاب جدید خواهد بود.
بقا: نرخ بقای 5 ساله در سرطان مثانه 79% برای مردان سفیدپوست و 74% برای زنان سفیدپوست، 69% برای مردان سیاهپوست و 54% برای زنان سیاهپوست میباشد.
دهانه رحم
موارد جدید: رخداد موارد جدید سرطان دهانه رحم در سال 2017 در امریکا بالغ بر 12820 مورد برآورد میشود.
روند وقوع: نرخ وقوع سرطان دهانه رحم بین سالهای 1975 (14/8 درصدهزار) و 2013 (6/5درصدهزار) از نصف هم کمتر شده است که عمدتاً به دلیل غربالگری با آزمایش پاپ اسمیر میباشد. معذلک سرعت این کاهش در سالهای اخیر بهویژه در میان زنان سفیدپوست کمتر شده است. نرخ وقوع سرطان دهانه رحم بین سالهای 2004 تا 2013 در میان زنان کمتر از 50 سال سفیدپوست ثابت مانده اما در سیاهپوستان سالانه 3% کاهش یافته است ولی در زنان بالاتر از 50 سال در سفیدپوستان 2% و در سیاهپوستان 4% در سال کاهش یافته است.
مرگ: برآورد مرگ ناشی از سرطان دهانه رحم در سال 2017 در آمریکا حدود 4/210 مورد میباشد.
روند مورتالیتی: نرخ مرگ ناشی از سرطان دهانه رحم در سال 2014 (2/3 در صدهزار) کمتر از نصف این کمیت در سال 1975 (5/6 در صدهزار) بوده است که این کاهش عمدتاً ناشی از کاهش در میزان وقوع و تشخیص زودهنگام با آزمایش پاپ اسمیر میباشد. نرخ مرگ در سالهای 2005 تا 2014 در زرنان کمتر از 50 سال ثابت بود و در زنهای بالاتر از 50 سال سالیانه 0/9 درصد کاهش داشت.
علائم و نشانهها: ضایعات اولیه دهانه رحم اغلب هیچ علامتی ندارند. وقتیکه سلولهای دهانه رحم بدخیم شده و به بافتهای اطراف تهاجم کردند، مهمترین علامت خونریزی غیرطبیعی از واژن است که در فواصل عادت ماهیانه یا پس از مقاربت و یا دوش واژینال و یا معاینه لگن اتفاق میافتد. در این افراد خونریزی ماهیانه ممکن است طولانیتر و شدیدتر از معمول باشد. در افراد یائسه خونریزی و افزایش ترشحات واژینال هم ممکن است علامتی از این بیماری باشد.
عوامل خطرساز: بیشتر سرطانهای دهانه رحم ناشی از عفونت مزمن با انواع خاصی از ویروس پاپیلومای انسانی (HPV) میباشند. معذلک باید توجه داشت که عفونت با HPV در زنان سالم هم معمول بوده و بندرت موجب سرطان سرویکس میگردد. گرچه شروع روابط جنسی زودهنگام و داشتن ارتباطات متعدد به افزایش خطر عفونت HPV منجر میشود، اما این عفونت در زنانی که تنها یک شریک جنسی هم دارند ممکن است مشاهده شود. مصرف سیگار، سرکوب سیستم ایمنی و حاملگیهای متعدد میتوانند خطر عفونت با HPV و ابتلا به سرطان سرویکس را افزایش دهند. استفاده طولانی مدت از ضدحاملگیهای خوراکی نیز همین نقش را دارد.
پیشگیری: برای انواع متداول که ممکن است منجر به سرطان سرویکس شوند، واکسن HPV تهیه شده که باید در سنین 9 تا 26 سال تلقیح گردد. در اکتبر 2016، CDC تعداد دفعات تزریق واکسن را برای سنین 9 تا 14 سال به دوبار کاهش داد، اما برای سنین 15 تا 26 سال تزریق واکسن همچنان در سه دوز توصیه میشود. متأسفانه پوشش واکسن HPV در آمریکا در مقایسه با سایر کشورهای پردرآمد پایین است. در سال 2015 تنها 42% از دختران نوجوان آمریکا تحت پوشش این واکسن بودند درحالیکه این رقم در استرالیا 77% بود.
واکسن HPV علیه عفونت مستقر و نیز همه انواع HPV مؤثر نیست، به همین دلیل زنانی که توسط این واکسن ایمن میشوند بازهم باید مورد غربالگری سرطان سرویکس قرار بگیرند.
با متداولتر شدن غربالگری، ضایعات پیشسرطانی سرویکس بیش از ضایعات سرطانی شناسایی میگردند. آزمایش پاپ اسمیر یک آزمایش ساده است که طی آن بخشی از سلولهای دهانه رحم بر روی لام منتقل شده و توسط مشاهده میکروسکوپی بررسی میشوند. آزمایش HPV که عفونتهای HPV (در ارتباط با سرطان سرویکس) را بررسی میکند میتواند خطر ابتلا به سرطان سرویکس را از سالها قبل پیشبینی کند و لذا توصیه میشود که در زنهای 30 تا 65 سال و نیز در مواردی که نتیجه پاپ اسمیر مبهم است آزمایش HPV نیز انجام شود.
ضمناً آزمایش HPV میتواند خطر ابتلا به نوعی از سرطان سرویکس (آدنوکارسینوم) که اغلب در پاپ اسمیر از قلم میافتد را شناسایی کند. این سرطان 28% موارد سرطان سرویکس را در آمریکا تشکیل میدهد.
بیشتر موارد پیشسرطانی سرویکس به آهستگی رشد میکنند، لذا اگر فرد بهطور منظم تحت نظارت غربالگری باشد، این سرطانها قابل پیشگیری خواهند بود. ضروری است که همه زنان و حتی آنها که واکسن HPV را دریافت کردهاند مقید به پیروی از دستورالعملهای غربالگری سرطان سرویکس باشند.
تشخیص زودهنگام: غربالگری میتواند سرطان سرویکس را در مراحل اولیه که هنوز درمان آن امکانپذیر است شناسایی کند. در بیشتر زنانی که سرطان سرویکس تشخیص داده میشود آنهایی هستند که اخیراً مورد غربالگری قرار نگرفتهاند. جامعه سرطان آمریکا با همکاری انجمن کولپوسکوپی و پاتولوژی سرویکس و نیز انجمن کلینیکال پاتولوژی آمریکا غربالگری را در زنان 21 تا 65 سال بهوسیله آزمایش پاپ اسمیر توصیه میکنند و تأکید دارند که در زنان 30 تا 65 سال آزمایش HPV نیز انجام شود.
درمان: ضایعات پیش سرطانی را میتوان با Loop Electrosurgical Excision Procedure (LEEP)، کرایوتراپی، لیزر یا جراحی از میان برداشت. سرطان مهاجم را با جراحی یا پرتودرمانی به همراه شیمیدرمانی معالجه میکنند. در موارد پیشرفته اغلب از شیمیدرمانی ممکن است استفاده شود. در زنانی که سرطان متاستاتیک، عودکننده یا پایدار سرویکس دارند در کنار شیمیدرمانی استفاده از درمان هدفمند میتواند به بهبود بقا کمک کند.
بقا: نسبت بقای 5 ساله در زنان سفیدپوست 69% و در سیاهپوستان 57% میباشد. 46% بیماران در مرحله لوکال بیماری تشخیص داده میشوند که بقای 5 ساله آنها 91% است. شانس بقای 5 ساله وقتیکه سرطان در مرحله ناحیهای و متاستاز دوردست است به ترتیب به 57% و 17% کاهش مییابد (جدول 8).
جسم رحم (اندومتر)
موارد جدید: رخداد موارد جدید در سال 2017 در آمریکا 61380 مورد برآورد میشود. سرطان جسم رحم اغلب به سرطان اندومتر اطلاق میشود چراکه 92% موارد آن در آندومتر اتفاق میافتد.
روند وقوع: نرخ وقوع از سال 2004 تا 2013 در زنان سفیدپوست 1% و در سیاهپوستان 3% در هر سال افزایش یافته است.
مرگ: برآورد ناشی از سرطان اندومتر در سال 2017 در آمریکا حدود 10920 مورد میباشد
روند مورتالیتی: از سال 2005 تا 2014 نرخ مرگ سرطان رحم حدود 1% در زنان سفید و 2% در سال در زنان سیاهپوست افزایش یافته است.
علائم و نشانهها: خونریزی غیرطبیعی رحم و یا لکه بینی (بهویژه در زنان یائسه) معمولترین نشانه اولیه این سرطان میباشد. درد به هنگام ادرار و مقاربت و یا درد در ناحیه لگن نیز میتواند علامت این سرطان باشد.
عوامل خطرساز: چاقی و چربی اطراف شکم خطر سرطان رحم را افزایش میدهد. این کار احتمالاً با افزایش مقدار استروژنهای خون انجام میشود. سایر عوامل خطرساز عبارتند از: استفاده از استروژن پس از یائسگی، تأخیر در یائسگی، حامله نشدن و سابقه سندرم تخمدان پلیکیستیک.
استفاده از استروژن به همراه پروژسترون بعد از دوران یائسگی احتمالاً موجب افزایش ریسک ابتلا نمیشود. تاموکسیفن که برای درمان سرطان سینه استفاده میشود از طریق اعمال اثرات مشابه استروژن بر روی رحم اندکی خطر ابتلا به سرطان را بالا میبرد. سندرم Lynch و دیابت نیز موجب افزایش خطر میشوند. حاملگی، استفاده از ضدحاملگیهای خوراکی یا دستگاه داخل رحمی و فعالیت فیزیکی از خطر ابتلا به سرطان رحم میکاهند.
تشخیص زودهنگام: برای زنانی که ریسک متوسط دارند هیچ روش استاندارد و روتین غربالگری وجود ندارد، معالوصف 67% موارد بهواسطه مشاهده خونریزی پس از یائسگی بهموقع شناسایی میشوند. هرگونه خونریزی یا لکهبینی غیرمعمول باید به پزشک گزارش شود. براساس توصیه انجمن سرطان آمریکا، زنان مشکوک به سندرم Lynch باید بهطور سالانه با بیوپسی رحم و یا سونوگرافی داخل واژینال از شروع 35 سالگی مورد غربالگری قرار بگیرند.
درمان: برحسب مرحله بیماری از جراحی، پرتودرمانی، هورمونها و یا شیمیدرمانی استفاده میشود.
بقا: نرخ بقای 5 ساله برای زنان سفیدپوست 84% و برای زنان سیاهپوست 62% میباشد.
سرطانهای نادر در بزرگسالان
مقدمه
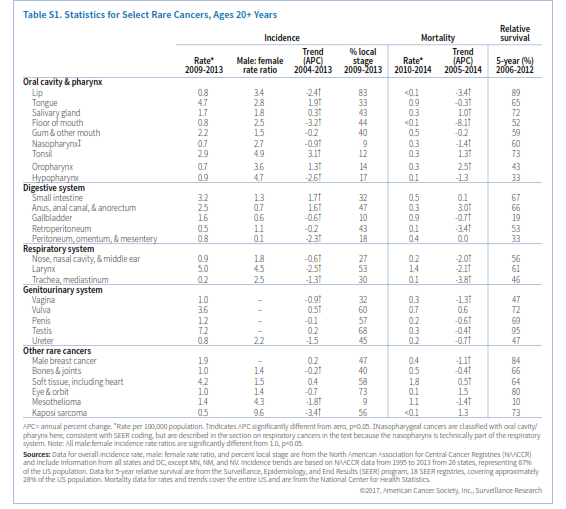
تشخیص هر نوع سرطانی مشکل است اما درخصوص سرطانهای نادر چالشهای بیشتری برای بیمار، کارکنان بهداشتی و حتی پزشکان وجود دارد. برای بیشتر سرطانهای نادر، تحقیق درخصوص علل ایجاد و استراتژی پیشگیری یا تشخیص بهموقع بسیار دشوار میباشد. از طرفی تشخیص این سرطانها نیز بسیار دشوار است و اغلب با معاینه توسط پزشکان مختلف، تشخیص اشتباه و تأخیر در تشخیص همراه است. پس از تشخیص نیز بیمار و همراهانش برای کسب اطلاعات درخصوص نوع سرطان در فشار هستند و امکانات درمانی معمولاً محدودتر و کماثرتر از سرطانهای متداول میباشد. بخشی از این محدودیت ناشی از فقدان کارآزماییهای بالینی کافی برای سرطانهای نادر میباشد، درنتیجه سرطانهای نادر باید از اولویت خاص برای محققین و سیستمهای بهداشت و درمان برخوردار باشند. در این گزارش نرخ وقوع و مورتالیتی، روندها، مرحله تشخیصی و نرخ بقا را در مورد 28 سرطان نادر در افراد بالای 20 سال در آمریکا شرح میدهیم و علاوه بر آن مروری بر علائم و عوامل خطرساز را در بخشی از این سرطانها خواهیم داشت.
- سرطان نادر چیست؟
هیچ تعریف پذیرفتهشده جهانی برای توصیف سرطان نادر وجود ندارد.
بنابر تعریف مؤسسه ملی سرطان، آن دسته از سرطانها که در سال کمتر از 15 نفر در هر صدهزار نفر را مبتلا میسازند سرطان نادر خوانده میشوند. اخیراً کنسرسیومی از اتحادیه اروپا این حد را 6 در هر صدهزار نفر تعریف کرده که ما نیز در این گزارش بر این تعریف پایبند خواهیم بود. برای مقایسه توجه داشته باشید که نرخ وقوع سرطان سینه و پروستات که معمولترین سرطانها در زنان و مردان است هر دو حدود 123 مورد در هر صدهزار نفر میباشد.
به لحاظ تاریخی سرطانها برحسب محل درگیر (در بدن) و نوع بافت منشأ تقسیمبندی میشوند. امروزه اطلاعات ژنتیکی بهطور فزایندهای در گروهبندی سرطانها مورد استفاده واقع میشوند و درنتیجه برخی سرطانهای معمول به زیرگروههای نادر تقسیم میشوند، اما به لحاظ محدودیت اطلاعات مولکولی سرطانهای ثبتشده، در اینجا ما براساس محل سرطان آن را گروهبندی میکنیم. درخصوص سرطان بیضه که شیوع آن اندکی بیشتر از حد آستانهای است که برای سرطانهای نادر در نظر گرفتهایم اما ازآنجاکه معمولاً آن را جزو سرطانهای نادر محسوب میکنند در اینجا نیز ما آن را جزو سرطانهای نادر مورد بررسی قرار دادهایم. بیشتر زیرگروههای لوسمی و لنفوم هوچکین و نیز سرطانهای دهان و حلق برحسب تعریف سرطان نادر محسوب میشوند اما چون آنها را قبلاً شرح دادهایم در اینجا مورد بحث قرار نمیگیرند.
- انتظار میرود چه تعداد سرطان نادر در سال 2017 تشخیص داده شوند؟
حدود 13% (یک مورد از 8 مورد) سرطانی که در افراد بالای 20 سال تشخیص داده میشود برحسب تعریف سرطان نادر است که به عبارت دیگر انتظار میرود تعداد 208/000 مورد جدید در سال 2017 در امریکا سرطان نادر شناسایی شود (که این رقم شامل 8850 مورد سرطان بیضه نمیشود).
برخی سرطانهای نادر منتخب
سیستم گوارشی
معمولترین سرطان نادر سیستم گوارشی سرطان روده کوچک است (جدول S1). روده کوچک شامل سه قسمت عمده بنام دئودنوم، ژئوژنوم و ایلئوم میباشد. با اینکه 75% طول و 90% سطح مخاطی سیستم گوارشی را روده کوچک تشکیل میدهد، اما فقط 4% سرطانهای گوارشی در این بخش رخ میدهد.
بیشترین بخش سرطانهای روده کوچک در قسمت فوقانی آن که به معده متصل است یعنی دئودنوم ایجاد میشود. چهار نوع عمده سرطان روده کوچک شامل تومورهای کارسینوئید (با منشأ سلولهای نورواندوکرین) (48%)، آدنوکارسینوم (با منشأ سلولهای غدهای) (28%)، لنفوم (با منشأ بافت لنفاوی) (13%) و سارکوم (با منشأ بافت استروما) (9%) میباشند. داشتن سابقه ابتلا به سرطان کولورکتال، بیماری کرون، بیماری سلیاک، سندرم Lynch و پلیپوز آدنوماتوز فامیلی از جمله عوامل خطرساز ابتلا به سرطان روده کوچک میباشند.
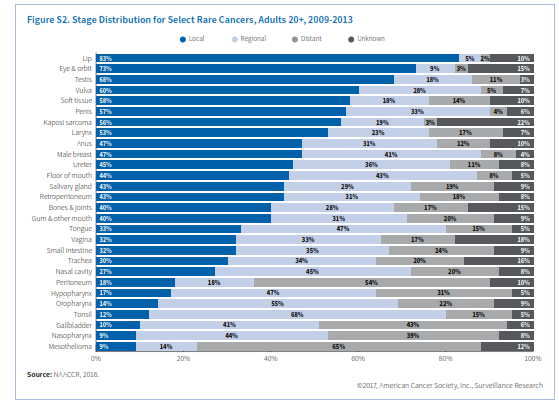
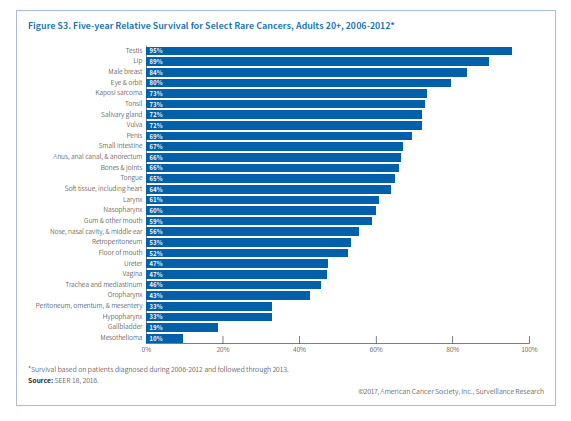
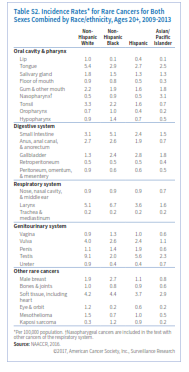
بعضی مطالعات پیشنهاد میکنند که عوامل خطرساز سرطان روده بزرگ همچون چاقی و مصرف الکل در اینجا هم میتوانند خطرساز باشند. سرطان روده کوچک در مردان اندکی بیشتر از زنان است (1/3 برابر) و در سیاهپوستان (5/1 نفر در هر صدهزار نفر) هم کمی بالاتر از سفیدپوستان غیراسپانیایی (3/1 در هر صدهزار نفر) میباشد (جدول S2). نرخ وقوع سرطان روده کوچک از سال 1995 تا 2010 هرساله 2/8% افزایش یافت اما از آن به بعد تا سال 2013 ثابت ماند (شکل S1). این ثبات شاید بیشتر به خاطر تأخیر در گزارش باشد. در مورد سرطان روده کوچک هم معمولاً تا مرحله پیشرفته بیماری علائم ظاهر نمیشوند و علائم ظاهرشده هم غیراختصاصی بوده به شکل دلدرد و کاهش وزن بروز میکنند. 59% سرطانهای روده در مرحله متاستاز ناحیهای یا متاستاز دور تشخیص داده میشوند (شکل S2). بقای نسبی 5 ساله با تشخیص در مرحله لوکال 83%، مرحله ناحیهای 73% و متاستاز دوردست 43% میباشد.
دومین سرطان نادر دستگاه گوارش سرطان مقعد (anus) میباشد. مقعد، کانال مقعدی و بخش آنورکتوم سه سانتیمتر انتهای لوله گوارش را تشکیل میدهند که مدفوع از آن طریق به خارج دفع میشود. بیش از90% سرطان مقعد ناشی از عفونت با HPV میباشد. سرطان مقعد یکی از محدود سرطانهایی است که وقوع آن در زنها بیشتر از مردان است، اما برحسب نژاد و سن الگوی وقوع آن تفاوت میکند. درمجموع زنان سفیدپوست غیراسپانیاییتبار و مردان سیاهپوست بالاترین نرخ ابتلا را در آمریکا دارند (3/3 و 2/8 در صدهزار نفر). در میان سفیدپوستان، ابتلای زنان در همه گروههای سنی بالاتر است ولی در سیاهپوستان ابتلای مردان قبل از 60 سالگی بالاتر بوده اما در بالای 60 سالگی نسبت برعکس میشود. نرخ وقوع سرطان مقعد از سال 2004 تا 2013 هرسال 1/6% افزایش یافته است (شکل S1). نرخ مرگ ناشی از این سرطان هم از سال 1998 تا 2014 همهساله 3% افزایش یافته است. در افراد مبتلا به HIV خطر ابتلا به سرطان مقعد 32 برابر افراد عادی میباشد. بنظر میرسد که سالمند شدن افراد مبتلا به HIV در افزایش رشد سرطان مقعد در آمریکا نقش دارد. معمولاً خونریزی از مقعد اولین نشانه بیماری است و بیش از نیمی از موارد در مرحله لوکال تشخیص داده میشوند که شانس بقای 5 ساله آنها 81% میباشد. درمجموع نرخ بقای 5 ساله برای سرطان مقعد 66% است (شکل S3).
کیسه صفرا عضو کوچکی در پایین کبد است که موجب تغلیظ و ذخیره صفرا میگردد. نرخ وقوع سرطان کیسه صفرا در زنان 66% بیشتر از مردان است. وجود سنگ صفرا و چاقی از عوامل خطرساز سرطان کیسه صفرا محسوب میگردند. وقوع آنها در اسپانیایی تبارها (2/8 در هر صدهزار نفر) و سیاهپوستان (2/4 در هر صدهزار نفر) 1/5 تا دو برابر سفیدپوستان غیراسپانیایی تبار (1/3 در هر صدهزار نفر) میباشد. نرخ وقوع مرگ ناشی از سرطان کیسه صفرا طی دهه گذشته همهساله به ترتیب 0/6 درصد و 0/7درصد کاهش یافته است. سرطان کیسه صفرا معمولاً تا مراحل پیشرفته بیماری علامتی نشان نمیدهد به همین جهت تنها 10% از مبتلایان در مرحله لوکال تشخیص داده میشوند و لذا درمجموع نرخ بقای 5 ساله سرطان کیسه صفرا 19% است (جدول S1).
سیستم تنفسی
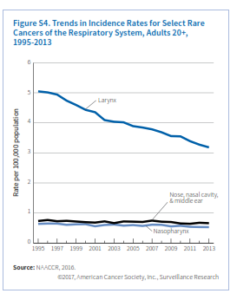
سرطانهای نادر دستگاه تنفسی عمدتاً در حنجره، نازوفارنکس، بینی و حفره بینی رخ میدهند. مهمترین عامل خطرساز برای سرطان حنجره مصرف تنباکو و الکل میباشد. مطالعات نشان میدهد که 20% سرطانهای حنجره در ارتباط با عفونت HPV میباشد. نرخ وقوع سرطان حنجره در مردان 5-4 برابر زنان است. بالاترین نرخ وقوع در سیاهپوستان (6/7 در هر صدهزار نفر) و کمترین آن در آسیاتبارها (1/6 در هر صدهزار نفر) میباشد (جدول S2). نرخ وقوع و مرگ ناشی از سرطان حنجره طی دهه اخیر سالانه حدود 2% کاهش یافته است که عمدتاً ناشی از کاهش مصرف دخانیات است. نزدیک 48% موارد منشأ سرطان حنجره در تارهای صوتی است که اغلب آنها (79%) در مرحله لوکال تشخیص داده میشوند چراکه تغییرات محسوسی در صدای فرد ایجاد میشود. سرطانهایی که منشأ آنها سایر قسمتهای حنجره است علائم غیراختصاصی مانند گلودرد و سرفه ایجاد میکنند و لذا احتمال تشخیص آنها در مراحل اولیه کم است.
نرخ بقای 5 ساله سرطان حنجره درمجموع 61% است.
نازوفارنکس قسمت فوقانی گلو است و در پشت بینی واقع شده است. عوامل خطرساز برای ابتلا به سرطان نازوفارنکس شامل مصرف ماهی نمکسود و سابقه ارثی میباشد. نرخ وقوع در میان آسیاتبارهای آمریکایی (3/1 در صدهزار) بیش از شش برابر سفیدپوستان و اسپانیایی تبارها (0/5 در صدهزار) میباشد. همچنین نرخ وقوع در میان برخی اقوام آسیایی بهویژه در جنوب چین و جنوب غربی آسیا بالاست. همچنین در بومیان آلاسکا این نرخ نسبتاً بالاست. در طی دهه اخیر نرخ وقوع و مرگ ناشی از سرطان نازوفارنکس به ترتیب 0/9 درصد و 1/4 درصد در سال نزول کرده است. بیشتر سرطانهای نازوفارنکس (83%) در مرحله ناحیهای و متاستاز دوردست شناسایی میشوند (شکل S2). درمجموع نرخ بقای 5 ساله در سرطان نازوفارنکس 60% است (شکل S3)
برخی سرطانهای بینی، حفره بینی و گوش میانی در ارتباط با مسائل شغلی مانند گردوغبار ناشی از چوب و چرم در صنایع مبلمان و کابینت و کفش میباشند. برخی دیگر نیز بعلت عفونت با HPV ایجاد میشوند.
این سرطانها نیز در مردان دو برابر زنان میباشند. از دهه 1990 نرخ وقوع سالانه 0/6 درصد (شکل S4) و نرخ مرگ سالانه 2% کاهش یافته است. نرخ بقای نسبی 5 ساله برای سرطانهای بینی، حفره بینی و گوش میانی درمجموع 56% است.
65% این سرطانها در مرحله ناحیهای یا متاستاز دوردست شناسایی میشوند که نرخ بقای 5 ساله برای آنها به ترتیب 49% و 37% میباشد.
سیستم ادراری تناسلی
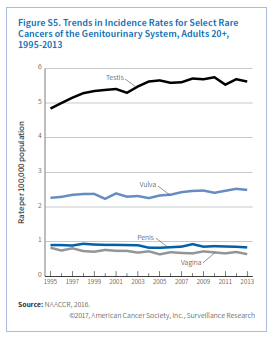
سرطانهای نادر سیستم ادراری تناسلی شامل سرطانهای ولوا، واژن، پنیس و بیضه میباشند. عفونت با HPV و مصرف دخانیات از عوامل خطرساز سرطانهای واژن و ولوا هستند. یک مطالعه اخیر نشان میدهد که 75% سرطانهای واژن و 69% سرطانهای ولوا که بین سالهای 2008 تا 2012 در امریکا شناسایی شدهاند با عفونت HPV مرتبط بودهاند. برخلاف سرطان سرویکس که اوج ابتلا به آن در دهه 30 و 40 عمر اتفاق میافتد، درخصوص سرطان واژن و ولوا، با افزایش سن نرخ ابتلا افزایش مییابد. نرخ ابتلا به سرطان ولوا در زنان سفیدپوست غیر اسپانیاییتبار و نرخ سرطان واژن در زنان سیاهپوست بالاتر از بقیه گروههای نژادی میباشد (جدول S2). از دهه 1990 نرخ وقوع و مرگ ناشی از سرطان واژن سالانه 1% کاهش یافته ولی در مورد سرطان ولوا ثابت مانده یا اندکی افزایش داشته است (شکل S5). در بیشتر زنانی که سرطان واژن یا ولوا دارند علائم بهطور زودهنگام ظاهر میشوند. این علائم درخصوص سرطان واژن شامل خونریزی غیرطبیعی، ترشح یا درد به هنگام مقاربت میباشد. علائم سرطان ولوا بهصورت وجود یک توده یا برآمدگی، خارش مداوم و درد نمایان میشود. احتمال تشخیص سرطان ولوا در مرحله اولیه در مقایسه با سرطان واژن بیشتر است (60% در برابر 32%)، به همین جهت نرخ بقای سرجمع 5 ساله در سرطان ولوا 72% و در سرطان واژن 47% میباشد.
سرطان پنیس هم اکثراً (63%) ناشی از عفونت با HPV است. دخانیات هم خطر ابتلا به سرطان پنیس را 4 برابر افزایش میدهد، درحالیکه ختنه کردن این خطر را پایین میآورد. نرخ وقوع سرطان پنیس در مردان اسپانیاییتبار 1/9 در صدهزار، سیاهپوستان 1/4در صدهزار، سفیدپوستان 1/1 در صدهزار و آسیاتبارها 0/6 در صدهزار میباشد. نرخ وقوع از سال 2004 تا 2013 نسبتاً ثابت مانده و نرخ مرگ سالانه 0/6 درصد کاهش یافته است (جدول S1). سرطان پنیس به شکل تغییر رنگ یا ضخامت پوست تظاهر کرده و بهتدریج به زخم یا جوش تبدیل میشود. 57% موارد سرطان پنیس در مرحله لوکال تشخیص داده میشوند که نرخ بقای 5 ساله در این مرحله 81% است.
سرطان بیضه متداولترین سرطان مردان در سن 15 تا 44 سال میباشد. 97% سرطانهای بیضه از منشأ سلولهای زایا میباشند که این سلولها بهطور طبیعی باید اسپرمها را تولید کنند. دو زیرگروه اصلی این سرطان سمینوماها و غیرسمینوماها هستند. سیمنوماها تومورهای کندرشدی هستند که در اواخر دهه 20 تا اواخر دهه 40 سن ظهور میکنند.
تومورهای غیرسمینوما معمولاً در اواخر دهه 20 تا اوایل دهه 40 ظهور کرده و مهاجمتر هستند. مهمترین عوامل خطرساز سرطان بیضه کریپتوکیدیسم (نهانخایگی)، سابقه شخصی یا خانوادگی سرطان بیضه (بهویژه در برادر) و نژاد اروپای شمالی میباشد. مطالعات نشان میدهد که آتشنشانها و کسانی که در معرض حشرهکشهای ارگانوکلراید هستند احتمال بیشتری برای ابتلا به سرطان بیضه دارند. نرخ وقوع در مردان سفیدپوست 9/1 در صدهزار، مردان اسپانیاییتبار، 5/6 درصدهزار، سیاهپوستان 2 درصدهزار و آسیاتبارها 2/3 در صدهزار میباشد. در سطح جهان نیز بالاترین نرخ سرطان بیضه مربوط به کشورهای اسکاندیناوی و پایینترین نرخ مربوط به کشورهای آفریقایی و آسیایی است. نرخ وقوع سرطان بیضه در آمریکا و سایر کشورهای غربی طی 40 سال گذشته افزایش یافته است، اما نرخ مرگ از سال 1990 تا 2014 همهساله 0/4 درصد کاهش نشان میدهد. وجود یک توده در بیضه نخستین نشان سرطان است و همین باعث میشود که 68% موارد سرطان بیضه در مرحله اولیه تشخیص داده شود. پیشآگهی سرطان بیضه درمجموع بسیار خوب است. نرخ بقای نسبی 5 ساله 95% میباشد (شکل S3). حتی سرطان متاستاتیک آن هم نرخ بقای 5 ساله بالغ بر 73% دارد.
سایر سرطانهای نادر
استخوان و مفاصل
دو نوع متداول سرطان استخوان و مفصل در بزرگسالان کندروسارکوم (35%) و استئوسارکوم (22%) میباشد که اولی از غضروف منشأ میگیرد و دومی معمولاً از انتهای استخوانهای طویل سرچشمه میگیرد.
عوامل خطرساز برای سرطان استخوان، پرتودرمانی بهویژه در جوانی و با دوز بالا و نیز برخی شرایط ارثی (سندرم Li-Fraumeni، رتینوبلاستوم) میباشند. نشانه اولیه سرطان استخوان، درد و تورم ناحیه مبتلا است. از سال 1995 نرخ وقوع و نرخ مرگ ناشی از سرطان استخوان اندکی کاهش یافته است (سالانه 0/2 تا 0/4 درصد). حدود 45% موارد سرطان استخوان در مرحله لوکال تشخیص داده میشود که نرخ بقای 5 ساله برای این گروه 85% میباشد. نرخ بقای سرجمع سرطان استخوان در بزرگسالان 66% است که برای کندروسارکوم (80%) بیشتر از استئوسارکوم (54%) میباشد.
بافت نرم
سارکومهای بافت نرم گروه متنوعی از سرطانها هستند که منشأ آنها سلولهای چربی (لیپوسارکوم)، عضلات اسکلتی (رابدومیوسارکوم)، عضلات صاف (لیومیوسارکوم) و سلولهای پوشاننده سطح عروق (آنژیوسارکوم) هستند. سارکوم بافت نرم میتواند بیش از یک نوع بافت بدن را مبتلا سازد یا اینکه منشأ آن اصلاً مشخص نباشد. بیش از 70 نوع مختلف سارکوم بافت نرم وجود دارد. بیشتر آنها در اطراف بازوها یا ساق پا ظاهر میشوند، اما بهطورکلی در هرکجای بدن از جمله تنه، سر و گردن، اعضای داخلی و ناحیه پشت شکم میتوان انتظار ظهور آنها را داشت. نادر بودن و تنوع تعداد آنها بررسی آنها را مشکل کرده است. اطلاعات کمی درخصوص عوامل ایجاد سرطان بافت نرم وجود دارد اما همانند استخوان پرتودرمانی و برخی شرایط ارثی (مانند نوروفیبروماتوز، سندرم گاردنر و سندرم Li-Fraumeni ) احتمال خطر ابتلا را افزایش میدهند. نرخ وقوع سرجمع سارکوم بافت نرم در سیاهپوستان در بالاترین حد و در آسیاتبارها در پایینترین حد میباشد (جدولS2). نرخ وقوع سرطان بافت نرم از سال 1995 تا 2009 سالانه 1/3 درصد افزایش یافت و سپس ثابت ماند (شکلS6 ). نرخ مرگ از سال 2001 تا 2014 همهساله 0/5 درصد افزایش نشان میدهد. سارکوم بافت نرم اغلب به شکل یک توده بدون درد تظاهر میکند که در 58% موارد در مرحله لوکال تشخیص داده میشود.
پیشآگهی سرطان بافت نرم برحسب زیرگروههای آن بسیار متغیر است و میزان بقای 5 ساله درمجموع 64% است اما اگر در مرحله لوکال تشخیص داده شود تا 80% میرسد.
چشم و حدقه
بیشتر سرطانهای چشم و حدقه ملانومای چشمی هستند. (لنفوم هم ممکن است در چشم ایجاد شود اما تحت عنوان لنفوماها طبقهبندی میشود). همانند ملانومای پوستی، خطر ابتلا به ملانومای چشم در سفیدپوستان بهویژه آنهایی که پوست لطیف و چشمان روشن دارند، بیشتر است. اما هنوز مشخص نیست که مواجهه با نور خورشید و اشعه فرابنفش موجب افزایش خطر میگردد یا نه. نرخ وقوع سرطان چشم و حدقه نسبتاً ثابت مانده اما نرخ مرگ از سال 1990 تا 2004 سالانه 2/8% کاهش یافته و سپس ثابت مانده است. علائم سرطانهای چشم و حدقه شامل اختلال دید و یا شکل چشم است که در معاینه توسط چشمپزشک مشخص میگردد. قریب به سهچهارم سرطانهای چشم و حدقه در مرحله لوکال تشخیص داده میشود (شکل S2) که نرخ بقای 5 ساله برای آنها 85% میباشد.
سرطان پستان در مردان
گرچه سرطان پستان عموماً یک بیماری زنانه تلقی میشود، اما در مردان هم رخ میدهد. چاقی، ژنیکوماستی، دیابت و سندرم کلینفیلتر ازجمله عوامل خطرساز مستقل برای این سرطان هستند. پرتودرمانی، موتاسیون ژن BRCA2/1 و سابقه فامیلی ابتلا به سرطان سینه در مردان و زنان نیز موجب افزایش خطر میگردند. نرخ وقوع آن در مردان سیاهپوست 2/7 در صدهزار و در مردان سفیدپوست 1/9 در صدهزار میباشد (جدول S2).
نرخ وقوع این سرطان از سال 1995 تا 2013 ثابت مانده اما نرخ مرگ ناشی از آن از سال 1993 همهساله 1/2% کاهش یافته است. معمولاً اولین نشانه سرطان سینه در مردان وجود یک توده در سینه است. مشاهده مراحل پیشرفته سرطان سینه در مردان بیشتر از زنان است چراکه مردان مورد غربالگری قرار نمیگیرند و آگاهی لازم در این زمینه وجود ندارد. نرخ بقا در زنان و مردانی که در مرحله مشابه میباشند ثابت است، اما ازآنجاکه احتمالاً سرطان مردان در مراحل پیشرفتهتر شناسایی میشود نرخ بقای 5 ساله برای مردان 84% و برای زنان 90% است.
مزوتلیوما
سلولهای مزوتلیال سطح برخی حفرههای بدن را پوشش میدهند. بیشتر موارد مزوتلیوما در پلور (81%) و پریتوان (90%) رخ میدهد. مهمترین عامل خطرساز جهت ابتلا به مزوتلیوما مواجهه با آزبست بهویژه در محیطهای کاری میباشد. قوانین ایمنی جدید و روشهای کاری روزآمد خطر ابتلای کارگران را کاهش داده است. سایر مواجهههای محیطی شامل برخی الیاف معدنی نیز به ایجاد مزوتلیوم بهویژه در پریتوان منجر میشوند.
نرخ وقوع مزوتلیوم در مردان 4 برابر زنان است که نشاندهنده تأثیر مواجهه شغلی میباشد. در مردان غیر اسپانیاییتبار، نرخ وقوع دو برابر سیاهپوستان است (1/5 در صدهزار در برابر 0/7 در صدهزار) (جدول S2). نرخ وقوع مزوتلیوم تا اواسط دهه 1990 در حال افزایش بود، سپس چند سالی ثابت ماند و در سال 2005 کاهش یافت (شکل S6). از سال 2005 تا 2013 نرخ وقوع در زنان ثابت ماند اما در مردان سالانه 2/6% کاهش یافت که نشانگر کاهش مواجهه با آزبست در محیطهای کاری میباشد. نرخ مرگ هم از سال 1999 تا 2014 در مردان سالانه 1/5 درصد کاهش یافت، اما در زنان ثابت باقی ماند. علائم مزوتلیوما میتواند شامل تنگی نفس، خسخس و خشونت صدا، سرفه مداوم و درد سینه یا قسمت پایین کمر باشد. افرادی که در مواجهه با آزبست بودهاند باید این علائم را بشناسند و در صورت بروز به پزشک مراجعه کنند.
بین مواجهه با آزبست تا تشخیص مزوتلیوما معمولاً بین 20 تا 50 سال فاصله وجود دارد. نرخ بقای 5 ساله برای مزوتلیوما فقط 10% است، چراکه بیماری معمولاً در مرحله پیشرفته تشخیص داده میشود که درمان در این مرحله دشوار است.
سارکوم کاپوسی
چهار نوع سارکوم کاپوسی (KS) وجود دارد. سارکوم کاپوسی کلاسیک عمدتاً در افراد مسن با نژاد مدیترانهای و کلیمی رخ میدهد. نوع آندمیک آن در میان افرادی که نزدیک خط استوا هستند و اغلب کمتر از 40 سال سن دارند پدیدار میگردد. نوع ایاتروژنیک بر اثر تضعیف سیستم ایمنی فرد با دارو به هنگام دریافت عضو حادث میشود و نوع دیگر آن توسط عفونت ایدز ایجاد میشود که به آن سارکوم کاپوسی اپیدمیک میگویند.
سارکوم کاپوسی توسط هرپس ویروس ایجاد میشود و بیشترین موارد آن در امریکا ناشی از عفونت ایدز میباشد. در افراد مبتلا به HIV درمان ترکیبی ضد روتروویروس خطر ایجاد بیماری ایدز و سارکوم کاپوسی را توأمان کاهش میدهد. میزان سارکوم کاپوسی در امریکا در مردان 10 برابر زنان است و در سیاهپوستان و اسپانیاییتبارها بیشتر از سایر گروههای نژادی میباشد (جدولS2 ). اوج وقوع سارکوم کاپوسی اوایل دهه 1990 و همزمان با اوج اپیدمی ایدز در آمریکا بود که پس از آن بهسرعت کاهش یافت (شکل S6). وقوع سارکوم کاپوسی از سال 1993 تا 2013 همهساله 3/4% کاهش یافته است. ضایعات پوستی (به رنگ ارغوانی، قرمز یا قهوهای) اولین نشانههای سارکوم کاپوسی هستند. این ضایعات میتوانند در سطوح مخاطی همچون دهان و حلق یا سایر نقاط بدن مانند ریه، معده و روده ظاهر شوند. مبتلایان به HIV باید بهطور مرتب توسط پزشکان ورزیده در تشخیص سارکوم کاپوسی و سایر بیماریهای مرتبط با ایدز معاینه شوند. مبتلایان به سارکوم کاپوسی معمولاً بهواسطه سایر بیماریهای ناشی از ایدز فوت میکنند و نرخ بقای 5 ساله برای آنها 73% میباشد.
نتیجهگیری
در این بخش چشماندازی از سرطانهای نادر را در میان بزرگسالان آمریکا ارائه کردیم. برآورد میشود که در سال 2017 تعداد 208/000 مورد سرطان نادر تشخیص داده شود. به لحاظ توجه و سرمایهگذاری محدود در خصوص این سرطانها، اطلاعات محدودی درخصوص این گروه متنوع وجود دارد. در سالهای اخیر همکاریهای ملی و بینالمللی برای روشن نمودن برخی از چالشهای این بیماریهای نادر انجام پذیرفته است. در اروپا پروژهای تحت عنوان RARECARE به راه افتاد که هدف آن مشخص نمودن تعداد موارد سرطانهای نادر و ایجاد یک شبکه جهت افزایش آگاهی و بهبود سرانجام مبتلایان به این بیماریها میباشد. در آمریکا هم در سال 2013 مؤسسه ملی سرطان طرح تومورهای نادر را منتشر ساخت که براساس آن همکاری دانشمندان، حمایتگران و متخصصین صنعتی بهمنظور پیشبرد تحقیقات و درمان سرطانهای نادر شکل گرفت. علاوه بر آن یکی از اهداف برنامه کارآزمایی بالینی توسعه ملی سرطان، بهبود مراقبت از بیمارانی است که سرطانهای نادر دارند.
تلاشهای مستمر برای تشخیص زودهنگام سرطان سرطانهای نادر و بهبود بقای بیماران همچنان ضرورت دارد.
برای دانلود پی دی اف بر روی لینک زیر کلیک کنید
ورود / ثبت نام