بیومارکرهای پروگنوستیک در سندرمهای کرونری حاد
دکتر سید مهدی زرگریان: دکترای علوم آزمایشگاهی
علی مرادی: کارشناس ارشد بیوشمی
چکیده
هدف مطالعه. ترپونین قلبی (cTn) نقش مهمی در ارزیابی سرانجام سندرم کرونری حاد (ACS) ایفا میکند، معذلک ارزش پروگنوستیک cTn مطلق نیست. در این مقاله نقش بیومارکرهای اختلال بطن چپ، استرس همودینامیک، التهاب و اختلال کلیوی را در پیشبینی سرانجام ACS بررسی خواهیم کرد.
یافتههای اخیر. تنها چند بیومارکر توانستهاند اطلاعات پیشبینی کنندهای بیش از cTn ارائه کنند. در این بین (NPs) B-type Natriuretic Peptides و (GDF-15)Growth – Differentiation Factor 15 از امیدوارکنندهترین موارد در این خصوص بودهاند، اما درخصوص نقش این بیومارکرها در اتخاذ تصمیمات درمانی و همچنین فایده پروگنوستیک آنها در مقایسه با cTn HS تردیدهایی وجود دارد.
خلاصه. NPs و GDF-15 ارزش پروگنوستیک بیشتری نسبت به CTn در سندرم کرونری حاد دارند، اما نقش آنها در تصمیمسازی بالینی با توجه به امکانات فعلی هنوز تعریف نشده است.
مقدمه
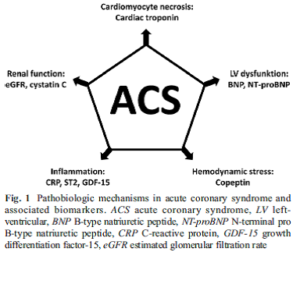
وقتی که کاردیومایوسیتها در معرض ایسکمی شدید قرار میگیرند به نحوی که تخریب غیرقابل برگشت سلولی ایجاد میشود، تروپونین قلبی یا همان cTn آزاد میگردد (1). در مدیریت بیمارانی که مشکوک به ACS هستند، سنجشcTn نقش حیاتی دارد و پیششرط تشخیص انفارکتوس میوکارد (MI)، افزایش cTn میباشد (2). در بیمارانی که علائم ACS را دارند، افزایش cTn بیانگر وجود ضایعات کرونروی ناپایدار و افزایش خطر حملات ایسکمیک راجعه میباشد. هرچه میزان cTn بالاتر باشد بیانگر بزرگتر بودن وسعت انفارکتوس و در نتیجه افزایش خطر مرگ خواهد بود (4،3)، به همین دلیل سنجش cTn در ارزیابی خطر کوتاهمدت و بلندمدت کاربرد دارد و در انتخاب بیمار جهت جراحی قلب یا درمان با آنتیکوآگولانها، میزان cTn از ملاکهای معمول است (6،5)، معذلک ارزش پروگنوستیک cTn مطلق نیست؛ بهعنوان مثال در (STEMI) ST-Segment MI مقدار cTn تحت تأثیر خونرسانی مجدد قرار میگیرد، علاوه بر این در برخی پروسههای پاتولوژیک که به ACS مرتبطند مانند اختلال بطن چپ، استرس همودینامیک، التهاب و یا اختلال کلیه، مقدار cTn تغییر نمیکند (شکل 1). این موضوع سبب گردیده تا تمایل به یافتن بیومارکرهایی که در کنار cTn بتوانند در موارد ACS پیشبینی خطر را بهبود بخشند، افزایش یابد. در دهه اخیر بهطور مستمر شاهد معرفی چنین بیومارکرهایی بودهایم. در این مقاله تلاش کردهایم که شواهد مربوط به این موضوع را بهطور خلاصه جمعآوری و ارائه کنیم. بهمنظور فراهم ساختن اطلاعاتی که برای پزشکان معالج مفید باشد، دامنه این مرور را به بیومارکرهایی محدود کردهایم که با امکاناتی که در حال حاضر در بازار وجود دارند، قابل سنجش باشند.
بیومارکرهای اختلال بطن چپ
پپتـیدهای ناتریورتـیک نوع بBNP و پیــــــــــشهورمون آن NT-pro BNP در پاسخ به کشش ایجاد شده توسط حجم یا فشار وارده اضافه به سلولهای دهلیز و بطن آزاد میشــوند. نقش فیزیولوژیـــک پپتیدهای ناتریورتیک، افزایش دفــــــع سدیم از ادرار، گشـــادی عروق و مهـــار اثـــرات سیســـــتم اعصــــــاب سمـــــپاتیک و سیستم (RAAS) Renin– Angiotensin- Aldosterone میباشد.
این عملکرد سبب ایجاد تعادل در احتباس مایعات شده و احتمالاً از هیپرتروفی ناهنجار و فیبروز بطن چپ پیشگیری میکند (7).
در ایسکمی میوکارد اغلب یک افزایش موقت فشار و کشش در دیواره بطن چپ ایجاد میشود که این امر بهنوبه خود سبب افزایش پپتید ناتریورتیک میگردد.
مقدار پپتید ناتریورتیک در ACS متناسب با وسعت ایسکمی میباشد و از طرفی نشاندهنده اختلال عملکرد بطن چپ در هنگام حمله ACS و قبل از آن میباشد که در مجموع پیشبینی کننده مهمی از عواقب سوء ACS تلقی میگردد (13-8). مقدار پپتید ناتریورتیک بهتدریج طی چند هفته پس از ACS کاهش مییابد (14). در برخی بیماران بهویژه آنهایی که نهایتاً دچار نارسایی قلبی میشوند، افزایش مجدد پپتید ناتریورتیک بعد از چند روز مشاهده میگردد که بیانگر بازسازی نامطلوب بطن چپ میباشد (8).
صرفنظر از یافتههای اکوکاردیوگرافی و cTn در بیماران ACS، چه افزایش ST-Segment داشته باشند و چه نداشته باشند، پپتیدهای ناتریورتیک پیشگوییکننده قوی مرگ و نارسایی قلبی میباشند
(12-9،15،16).
مشخص نیست که این گزاره در سنجش خیلی حساس cTn هم مصداق داشته باشد. پپتیدهای ناتریورتیک اطلاعات پروگنوستیک حاصله از درجهبندی GRACE (18،17) را تقویت کرده و نیز بهبود عملکرد بطن چپ را پس از ACS پیشبینی میکند (13)، اما ارتباط بین پپتیدهای ناتریورتیک و رخدادهای ایسکمیک راجعه در بررسیهای تعدیلشده ضعیف است یا اصلاً وجود ندارد. با توجه به ارتباط نزدیک میزان پپتید ناتریورتیک با شدت بیماری عروق کرونری، این مسئله عجیب بنظر میرسد (19) معذالک هیچ رابطه علت و معلولی بین میزان پپتید ناتریورتیک و آتروترومبوز وجود ندارد.
بهترین زمان برای اندازهگیری پپتید ناتریورتیک جهت ارزیابی ریسک مشخص نیست. نمونههایی که در طی بستری شدن یا در دوران پایش بیماری گرفته میشوند در مقایسه با نمونههایی که خیلی زود تهیه میشوند ارتباط قویتری با عواقب بعدی بیماری نشان میدهند (20،16،14،8)، اما هنوز مشخص نیست که تغییرات موقت میزان پپتید ناتریورتیک موجب تغییر پیشآگهی هم میشود یا خیر (20،16،14).
مطالعات متعددی به بررسی نقش سنجش پپتید ناتریورتیک در بیماران NSTE- ACS پرداختهاند. گرچه نتایج متناقضی (10،9) در طی برخی از این مطالعات رخ نموده اما یک متاآنالیز که اخیراً بر روی 8125 بیمار از پنج گروه مورد مطالعه انجام شده، نشان میدهد که در گروهی از این بیماران که پپتید ناتریورتیک بالاست انجام مداخله تهاجمی از میزان مرگ بهطور قابلتوجهی میکاهد (21).
از آنجائی که مقدار پپتید ناتریورتیک بیانگر میزان اختلال عملکرد بطن چپ میباشد، لذا منطقی است بپذیریم که میتواند راهنمایی جهت درمان دارویی تغییرات بطن چپ باشد.
بیومارکرهای استرس همودینامیک- Copeptin
Copeptin بخش ترمینال– C از پروهورمون آرژنین- وازوپرسین میباشد که در استرس اندوژن از نووروهیپوفیز آزاد میشود (26). مقدار Copeptin در اختلالات حاد متعددی از جمله انفارکتوس میوکارد سریعاً افزایش مییابد اما این بیومارکر مختص قلب نیست. علاوه بر MI در سایر بیماریهای قلبی نظیر میوکاردیت و نارسایی قلب هم افزایش مییابد اما در آنژین ناپایدار تغییر نمیکند (27).
در بیماریهای غیرقلبی مانند سکته مغزی، عفونت خون، عفونت دستگاه تنفسی و رفلاکس گاستروازوفاژ هم مقدار آن افزایش مییابد (28،26).
با توجه به افزایش سریع آن در بیماریهای حاد، برای رد تشخیص سریع انفارکتوس قلبی مورد توجه واقع شده است (27،26). از طرفی مقدار Copeptin همانند پپتیدهای ناتریورتیک در اختلال عملکرد بطن چپ هم افزایش مییابد (29). Copeptin یک پیشبینی کننده قوی برای مرگ و نارسایی قلبی در بیماران ACS میباشد (31-29،32).
بیومارکرهای التهابی
CRP
CRP پروتئینی است که در پاسخ به التهاب سیستمیک ایجاد میشود (34). این پروتئین شاخصی شناختهشده برای شناسایی عفونت و التهاب و نکروز میباشد. در طی بیست سال اخیر نقش CRP در ارزیابی ACS بهطور وسیع مورد مطالعه واقع شده است (25). در انفارکتوس میوکارد CRP در عرض 6 ساعت پس از شروع علائم افزایش یافته و در طی 4-2 روز به اوج خود میرسد (36). افزایش CRP در پاسخ به آسیب میوکارد است و متناسب با وسعت آسیب مقدار CRP نیز تغییر میکند (37). در پلاکهای آترواسکلروتیک CRP شناسایی شده است اما رابطه علت و معلولی بین وقایع عروق کرونر و CRP بسیار نامحتمل است (38).
اینکه سنجش CRP میتواند اطلاعاتی بیشتر از سایر بیومارکرها ارائه کند محل مناقشه است و مطالعات مختلف نتایج مختلفی نشان دادهاند (15،44-41). نکته قابلتوجه این است که تاکنون هیچ مطالعه وسیعی در مقایسه با Hs-cTn بعمل نیامده است، همچنین باید گفت که نقش ثابتشدهای برای CRP در انتخاب درمان ACS اظهار نشده است (45).
ST2
ST2 عضوی از خانواده رسپتور اینترلوکین -1 میباشد که محلول بوده و در پاسخ به استرس مکانیکی ترشح میشود (46). ST2 بهعنوان شاخصی برای التهاب، فیبروز و تغییر شکل نامطلوب میوکارد هم پیشنهاد شده است (48،47). تناسب ST2 با سایر بیومارکرها همچون cTn و پپتیدهای ناتریورتیک ضعیف است و لذا بنظر میرسد که راه تحریک و آزاد شدن آن متفاوت میباشد (49). ST2 در نارسایی قلبی بهطور گسترده مطالعه شده و مشخص گردیده که بهطور مستقل و قوی با مرگ رابطه دارد (47). FDA سنجش ST2 برای پیشآگهی نارسایی قلبی را تأئید کرده است.
در بیماران ACS، نقش ST2 کمتر بررسی شده است و بهطور قطع هیچ نقشی در تشخیص انفارکتوس میوکارد ندارد (50). مشخص نیست که سنجش ST2 بتواند در انتخاب درمان ACS مؤثر باشد، اما طی یک مطالعه مشخص شده که افزایش ST2 در انفارکتوس میوکارد نشان میدهد که استفاده از آنتاگونیستهای رسپتور مینرالوکورتیکوئید برای درمان مفید خواهد بود (55).
(GDF-15) Growth – Differentiation Factor 15
GDF-15 عضوی از فوقخانواده transforming growth factor β است که عملاً در همه بافتها وجود دارد و این نشاندهنده اهمیت آن در عملکرد سلولی میباشد، گرچه عملکرد دقیق بیولوژیک آن هنوز بهخوبی مشخص نیست (56).
GDF-15 در تنظیم روندهای التهابی و آپوپتیک نقش دارد و در موارد پاتولوژیک متعدد از جمله بیماریهای قلبی عروقی افزایش مییابد (56).
میزان GDF-15 پیشبینی کننده مستقل و مستحکمی برای میزان مرگومیر و پیشرفت بیماری در ACS است.
در طی یک بررسی متاآنالیز شامل 8903 بیمار ACS مشخص گردید که میزان GDF-15 اگر کمتر از ng/L 1200 باشد خطر حوادث قلبی عروقی در آینده کم است اما اگر بیشتر از ng/L 1800 باشد این خطر قابلتوجه خواهد بود.
بیومارکرهای کارکرد کلیه
(eGFR) Estimated Glomerular Filtration Rate
بیماران ACS که مبتلا به نارسایی مزمن کلیه هم هستند بسیار آسیبپذیر تلقی میگردند. تخمین دقیق عملکرد کلیوی در این افراد به لحاظ پیشگویی آینده بیماری، اخذ تصمیم برای استراتژی درمانی و دوز دارو بسیار حائز اهمیت خواهد بود. ازآنجاکه سنجش مستقیم فیلتراسیون کلیوی ممکن نیست، لذا از کراتینین سرم یا فرمولهای مبتنی بر کراتینین برای تخمین عملکرد کلیه استفاده میشود. متأسفانه کراتینین سرم حساسیت لازم را برای تشخیص کاهش متوسط عملکرد کلیه دارا نیست و لذا قابلاعتماد نمیباشد و از عوامل متعددی همچون سن، جنس، توده عضلانی، فعالیت فیزیکی و رژیم غذایی تأثیر میپذیرد.
متداولترین روش محاسبه eGFR مبتنی بر روش معرفیشده توسط MDRD و فرمـــــــــول Cockroff- Gault میباشد (63،62). هنوز هم در مورد اینکه کدامیک از این دو فرمول به حقیقت نزدیکتر میباشند جای شک و شبهه وجود دارد. هیچکدام از این دو فرمول در بیماران قلبی اعتبارسنجی نشدهاند. علاوه بر این متغیرها و ضرایب آنها نیز با هم فرق میکنند. نتایج eGFR با استفاده از فرمول Cockroff- Gault در افراد مسن و کسانی که توده عضلانی کمتری دارند (یعنی درواقع کسانی که بیشتر در معرض بیماریهای قلبی عروقی هستند) کمتر است (65،64). لذا فرمول Cockroff- Gault در پیشبینی خطر بر فرمول MDRD برتری دارد (65،64).
صرفنظر از معادله مورد استفاده، در بیماران ACS، هرچه میزان eGFR کمتر باشد خطر مرگ بیشتر خواهد بود (68،67،65،64،15). ارتباط eGFR با حوادث ایسکمیک راجعه ضعیف بوده و معمولاً پس از در نظر گرفتن فاکتورهای بالینی ارتباطی ملاحظه نمیشود، البته در بیشتر این مطالعات بیمارانی که نارسایی شدید کلیوی داشته و یا دیالیز میشدهاند، کنار گذاشته شدهاند.
مطالعات معدودی به بررسی ارزش پروگنوستیک eGFR نسبت به cTn پرداختهاند (15،67،68). این بررسیها نشان میدهد که در بیماران ACS بررسی عملکرد کلیوی هم باید جزئی از مراحل مدیریت بیماری باشد. بر اساس این مطالعات ارزش پروگنوستیک eGFR اضافه بر cTn تاحدودی مشخص میشود (67).
در بیمارانی که نارسایی شدید کلیوی دارند مقدار cTn اندکی افزایش مییابد و این باعث میشود که همبستگی پروگنوستیک بین cTn و eGFR پیچیده گردد.
Cystatin c
نگرانیهای مربوط به معادلات مختلف محاسبه eGFR سبب شد تا پژوهشگران به دنبال شاخص مطمئنتری برای عملکرد کلیه باشند. یکی از این شاخصها، سیستاتین Cمیباشد. این پروتئین که 13 کیلودالتون وزن دارد در تمام سلولهای هستهدار تولید میشود و توسط گلومرولهای کلیه فیلتر میگردد بیآنکه ترشح یا بازجذبی متعاقب آن انجام شود (73). سیستاتین C در برآورد عملکرد کلیه از کراتینین حساستر بوده و حداقل در حد eGFR حساسیت دارد (74). دلیل دیگر موردتوجه بودن Cystatin c این است که مهارکننده cytokine– activated elastolytic cystain proteasae است که آنزیم مذکور در تشکیل پلاکهای آترواسکلروتیک و بیثبات کردن آنها نقش دارد (75). بنابراین سیستاتین C در مسیرهای مختلف ACS نقش دارد و این موضوع به لحاظ تئوریک نقش پروگنوستیک آن را در مقایسه با سایر راههای برآورد عملکرد کلیه پررنگتر میسازد.
مشخص شده که سیستاتین C یک پیشگوی مستقل برای مرگ در ACS میباشد. در برخی مطالعات قدرت پیشگویی سیستاتین C درخصوص عوارض ناخواسته از کراتینین سرم یا eGFR بیشتر بوده است (78-76).
خلاصه و چشمانداز
تحقیقات بیشماری جهت یافتن بیومارکرهایی انجام پذیرفته که بتواند در کنار cTn اطلاعات پروگنوستیک بیشتری در اختلالات قلبی عروقی ارائه کنند. برخی از این بیومارکرها جهت مصرف در سطوح بالینی توصیه شدهاند، معذلک هنوز ناشناختههای بسیاری باقی مانده است. تنها تعداد معدودی از این مطالعات درخصوص بیومارکرهای مذکور در مقایسه با روش فوق حساس سنجش cTn یعنی cTn- hs انجام پذیرفتهاند، لذا این سؤال وجود خواهد داشت که مطالعات قبلی که همراه با سنجش cTn به روش بسیار حساس نبودهاند آیا وقتی با این روش همراه شوند اعتبار خود را حفظ خواهند کرد؟ اگرچه بسیاری از بیومارکرهایی که در این مقاله به آنها اشاره شد میتوانند روشهای موجود در پیشبینی سرانجام ACS را تکمیل کنند، اما مقایسه جزء به جزء در این خصــــوص بســــیار اندک بوده است.
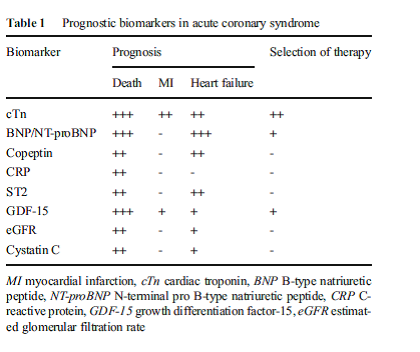
در تحـــقیق موســـوم به PLATO و MERLIN– TIMI 36 نشان میدهند که بیومارکرهای التهاب وقتیکه فاکتورهای بالینی و نتایج cTn هم در بررسی لحاظ شوند ارزش پیشبینی نسبتاً کمی دارند. پپتیدهای ناتریورتیک و GDF-15 شاخصهای برآورد ریسک قویتری هستند (67،44،23،22) و ارزش افزوده پروگنوستیک نسبت به GRACE score دارند (18). در جدول یک خلاصهای از ویژگیهای بیومارکرهای موردبحث در این مقاله آمده است.
معذلک وجود حتی یک رابطه قوی با سرانجام بیماری بندرت جهت مفید بودن بالینی یک بیومارکر کفایت میکند. یک بیومارکر باید اطلاعاتی به دست دهد که مستقیماً بر مدیریت بالینی بیمار تأثیرگذار باشد، بنابراین کارآیی یک بیومارکر خوب در این نکته نهفته است که وقتی مقدار آن بالا باشد یک اقدام درمانی خاص بتواند در سرنوشت بیمار تغییر مثبت ایجاد کند. همچنین باید در تحقیقات مشخص شود که آیا با کاهش سطح بیومارکر خطر تبعات منفی نیز کاهش مییابد یا نه.
گرچه اطلاعات مربوط به بیومارکرهای پیشنهادی در مقالات متعدد آورده شده است، اما تا استفاده روتین بالینی از این بیومارکرها راه درازی در پیش است. اکنون این سؤال مطرح میشود که آیا رویکردهای دیگری که الزاماً تمرکز بر روی یک بیومارکر نباشد، میتوانند در پیشبینی سرانجام بیماری مفید واقع شوند؟ در بحث ژنومیک مطالعاتی در حال انجام است که هدف آنها شناسایی بیومارکرهایی است که نشانگر یک مسیر بخصوص در ACS میباشند (80،79). ارزیابی micro RNAs گزینه دیگری است که توجه زیادی را به خود جلب کرده است. میکروآرانایها، آرانایهای کوچک غیرکدکنندهای هستند که تنظیمکنندههای کلیدی در فرآیندهای بیولوژیک پیچیدهای هستند که این فرآیندها در ایجاد بیماریهای مختلف قلبی عروقی نقش دارند. شواهد زیادی به نقش میکروآرانایها در تشخیص ACS و احتمالاً نقش پروگنوستیک آنها تأکید دارند (81). رویکرد متفاوت دیگر جهت غنی کردن اطلاعات حاصله از بیومارکرها این است که بجای تکیه بر یک بیومارکر، مجموعهای از آنها را در یک مدل پیچیده مورد ارزیابی قرار دهند (83،82). این اقدام بر محدودیتهای فردی هر بیومارکر منفرد فائق خواهد آمد و استفاده از چنین رویکردی در بیماریهای قلبی عروقی بهطور مستمر در حال افزایش میباشد.
نتیجهگیری
گرچه بیومارکرهای متعددی سالهای اخیر جهت پیشبینی عواقب ACS معرفی شدهاند، اما تنها تعداد محدودی از آنها در مقایسه با cTn ارزش بیشتری ایجاد کردهاند. پپتیدهای ناتریورتیک و GDF-15 دو بیومارکری هستند که در این خصوص امیدوارکننده میباشند، اما نقش آنــــــــــها بهویژه باید در شرایط حاضر که استفاده از Hs- cTn رواج یافته، باید مشخص شود.
ترجمه همراه با تلخیص از :
منابع:
Papers of particular interest, published recently, have beenhighlighted as:
- Of importance
- • Of major importance
- White HD. Pathobiology of troponin elevations: do elevations occur with myocardial ischemia as well as necrosis? J Am Coll
Cardiol. 2011;57:2406–8. doi:10.1016/j.jacc.2011.01.029. Erratum in J Am Coll Cardiol 2011;58:2356.
- Thygesen K, Alpert JS, Jaffe AS, Simoons ML, Chaitman BR, White HD, et al. Third universal definition of myocardial infarction. J Am Coll Cardiol. 2012;60:1581–98. doi:10.1016/j.jacc.2012.08.001.
- Lindahl B, Diderholm E, Lagerqvist B, Venge P, Wallentin L. FRISC II (Fast Revascularization during InStability in CAD) Investigators. Mechanisms behind the prognostic value of troponin T in unstable coronary artery disease: a FRISC II substudy. J Am Coll Cardiol. 2001;38:979–86.
- Hallén J. Troponin for the estimation of infarct size: what have we learned? Cardiology. 2012;121:204–12. doi:10.1159/000337113.
- Morrow DA, Cannon CP, Rifai N, Frey MJ, Vicari R, Lakkis N, et al. Ability of minor elevations of troponins I and T to predict
benefit from an early invasive strategy in patients with unstable angina and non-ST elevation myocardial infarction: results from a
randomized trial. JAMA. 2001;286:2405–12.
- James SK, Lindbäck J, Tilly J, Siegbahn A, Venge P, Armstrong P, et al. Troponin-T and N-terminal pro-B-type natriuretic peptide predict mortality benefit from coronary revascularization in acute coronary
syndromes: a GUSTO-IV substudy. J Am Coll Cardiol. 2006;48:1146–54. doi:10.1016/j.jacc.2006.05.056.
- Daniels LB, Maisel AS. Natriuretic peptides. J Am Coll Cardiol. 2007;50:2357–68. doi:10.1016/j.jacc.2007.09.021.
- Talwar S, Squire IB, Downie PF, Mccullough AM, Campton MC, Davies JE, et al. Profile of plasma N-terminal proBNP following acute myocardial infarction; correlation with left ventricular systolic dysfunction. Eur Heart J. 2000;21:1514–21. doi:10.1053/euhj.1999.2045.
- Morrow DA, de Lemos JA, Sabatine MS, Murphy SA, Demopoulos LA, DiBattiste PM, et al. Evaluation of B-type natriuretic
peptide for risk assessment in unstable angina/non-ST-elevation myocardial infarction: B-type natriuretic peptide and prognosis
in TACTICS-TIMI 18. J Am Coll Cardiol. 2003;41:1264–72. Erratum in: J Am Coll Cardiol 2003;41:1852.
- Jernberg T, Lindahl B, Siegbahn A, Andren B, Frostfeldt G, Lagerqvist B, et al. N-terminal pro-brain natriuretic peptide in relation to inflammation, myocardial necrosis, and the effect of an invasive strategy in unstable coronary artery disease. J Am Coll
Cardiol. 2003;42:1909–16.
- Mega JL, Morrow DA, De Lemos JA, Sabatine MS, Murphy SA, Rifai N, et al. B-type natriuretic peptide at presentation and prognosis in patients with ST-segment elevation myocardial infarction: an ENTIRE-TIMI-23 substudy. J Am Coll Cardiol. 2004;44:335–9. doi:10.1016/j.jacc.2004.04.033.
- Björklund E, Jernberg T, Johanson P, Venge P, Dellborg M, Wallentin L, et al. Admission N-terminal pro-brain natriuretic peptide and its interaction with admission troponin T and ST segment resolution for early risk stratification in ST elevation myocardial infarction. Heart. 2006;92:735–40. doi:10.1136/hrt.2005.072975.
- Mayr A, Mair J, Schocke M, Klug G, Pedarnig K, Haubner BJ, et al. Predictive value of NT-pro BNP after acute myocardial infarction: relation with acute and chronic infarct size and myocardial function. Int J Cardiol. 2011;147:118–23. doi:10.1016/j.ijcard.2009.09.537.
14.• Lindahl B, Lindbäck J, Jernberg T, Johnston N, Stridsberg M, Venge P, et al. Serial analyses of N-terminal pro-type natriuretic
peptide in patients with non-ST-segment elevation acute coronary syndromes: a Fragmin and fast Revascularisation during In
Stability in Coronary artery disease (FRISC)-II substudy. J Am Coll Cardiol. 2005;45:533–41. doi:10.1016/j.jacc.2004.10.057.
One of the few studies investigating the prognostic implications of changes in NT-proBNP levels after NSTEACS and the optimal timing of measurements.
15.•• James SK, Lindahl B, Siegbahn A, Stridsberg M, Venge P, Armstrong P, et al. N-terminal pro-brain natriuretic peptide and
other risk markers for the separate prediction of mortality and subsequent myocardial infarction in patients with unstable coronary
artery disease: a Global Utilization of Strategies To Open occluded arteries (GUSTO)-IV substudy. Circulation. 2003;108:275–81.
doi:10.1161/01.CIR.0000079170.10579.DC. A large analysis that confirmed the prognostic value of NT-proBNP as a mortality
predictor independent of cTnT, CRP or estimates of renal dysfunction.
- Morrow DA, de Lemos JA, Blazing MA, Sabatine MS, Murphy SA, Jarolim P, et al. Prognostic value of serial B-type natriuretic peptide testing during follow-up of patients with unstable coronary artery disease. JAMA. 2005;294:2866–71. doi:10.1001/jama.294.22.2866.
- Khan SQ, Narayan H, Ng KH, Dhillon OS, Kelly D, Quinn P, et al.
N-terminal pro-B-type natriuretic peptide complements the
GRACE risk score in predicting early and late mortality following
acute coronary syndrome. Clin Sci (Lond). 2009;117:31–9. doi:10.
1042/CS20080419.
18.•• Widera C, Pencina MJ, Bobadilla M, Reimann I, Guba-Quint A,
Marquardt I, et al. Incremental prognostic value of biomarkers beyond
the GRACE (Global Registry of Acute Coronary Events)
score and high-sensitivity cardiac troponin T in non-ST-elevation
acute coronary syndrome. Clin Chem. 2013;59:1497–505. doi:10.
1373/clinchem.2013.206185. One of the few analyses
investigating the incremental value of multiple biomarkers to
an established risk prediction tool in NSTE-ACS.
- Sadanandan S, Cannon CP, Chekuri K, Murphy SA, Dibattiste PM,
Morrow DA, et al. Association of elevated B-type natriuretic peptide
levels with angiographic findings among patients with unstable
angina and non-ST-segment elevation myocardial infarction. J Am
Coll Cardiol. 2004;44:564–8. doi:10.1016/j.jacc.2004.03.072.
- Squire IB, Ørn S, Ng LL,Manhenke C, Shipley L, Aarsland T, et al.
Plasma natriuretic peptides up to 2 years after acute myocardial
infarction and relation to prognosis: an OPTIMAAL substudy. J
Card Fail. 2005;11:492–7. doi:10.1016/j.cardfail.2005.05.004.
21.•• Dong SY, Dong MS, Chen ZH, Sun J, Yang X, Zeng Q. Dynamic
use of B-type natriuretic peptide-guided acute coronary syndrome
therapy. Am J Med Sci. 2014;348:283–7. doi:10.1097/MAJ.
- 0000000000000245. This meta-analysis confirmed the prognostic
benefit of early coronary revascularization in ACS patients
with higher NP levels.
- Wallentin L, Lindholm D, Siegbahn A, Wernroth L, Becker RC,
Cannon CP, et al. Biomarkers in relation to the effects of ticagrelor in
comparison with clopidogrel in non-ST-elevation acute coronary syndrome
patients managed with or without in-hospital revascularization:
a substudy from the Prospective Randomized Platelet Inhibition and
Patient Outcomes (PLATO) trial. Circulation. 2014;129:293–303. doi:
10.1161/CIRCULATIONAHA.113.004420.
- Squire I, Quinn P, Narayan H, Khan S, Dhillon O, Ng K, et al.
Identification of potential outcome benefit from ACE inhibition after
acute coronary syndrome: a biomarker approach using N-terminal
proBNP. Heart. 2010;96:831–7. doi:10.1136/hrt.2009.184614.
- Scirica BM, Morrow DA, Bode C, Ruzyllo W, Ruda M, Oude
Ophuis AJ, et al. Patients with acute coronary syndromes and elevated
levels of natriuretic peptides: the results of the AVANT
GARDE-TIMI 43 Trial. Eur Heart J. 2010;31:1993–2005. doi:10.
1093/eurheartj/ehq190.
- Morrow DA, Scirica BM, SabatineMS, de Lemos JA, Murphy SA,
Jarolim P, et al. B-type natriuretic peptide and the effect of
ranolazine in patients with non-ST-segment elevation acute coronary
syndromes: observations from the MERLIN-TIMI 36
(Metabolic Efficiency With Ranolazine for Less Ischemia in Non-
ST Elevation Acute Coronary-Thrombolysis In Myocardial
Infarction 36) trial. J Am Coll Cardiol. 2010;55:1189–96. doi:10.
1016/j.jacc.2009.09.068.
- Morgenthaler NG. Copeptin: a biomarker of cardiovascular and
renal function. Congest Heart Fail. 2010;16 Suppl 1:S37–44. doi:
10.1111/j.1751-7133.2010.00177.x.
- Reichlin T, Hochholzer W, Stelzig C, Laule K, Freidank H,
Morgenthaler NG, et al. Incremental value of copeptin for rapid
rule out of acute myocardial infarction. J Am Coll Cardiol.
2009;54:60–8. doi:10.1016/j.jacc.2009.01.076.
- Stallone F, Twerenbold R,Wildi K, Reichlin T, Rubini Gimenez M,
Haaf P, et al. Prevalence, characteristics and outcome of non-cardiac
chest pain and elevated copeptin levels. Heart. 2014;100:1708–14.
doi:10.1136/heartjnl-2014-305583.
- Kelly D, Squire IB, Khan SQ, Quinn P, Struck J,Morgenthaler NG,
et al. C-terminal provasopressin (copeptin) is associated with left
ventricular dysfunction, remodeling, and clinical heart failure in
survivors of myocardial infarction. J Card Fail. 2008;14:739–45.
doi:10.1016/j.cardfail.2008.07.231.
- Khan SQ, Dhillon OS, O’Brien RJ, Struck J, Quinn PA, Morgenthaler
NG, et al. C-terminal provasopressin (copeptin) as a novel and prognostic
marker in acute myocardial infarction: Leicester Acute
Myocardial Infarction Peptide (LAMP) study. Circulation. 2007;115:
2103–10. doi:10.1161/CIRCULATIONAHA.106.685503.
- Voors AA, von Haehling S, Anker SD, Hillege HL, Struck J,
Hartmann O, et al. C-terminal provasopressin (copeptin) is a strong
prognostic marker in patients with heart failure after an acute myocardial
infarction: results from the OPTIMAAL study. Eur Heart J.
2009;30:1187–94. doi:10.1093/eurheartj/ehp098.
32.•• O’Malley RG, Bonaca MP, Scirica BM, Murphy SA, Jarolim P,
Sabatine MS, et al. Prognostic performance of multiple biomarkers
in patients with non-ST-segment elevation acute coronary syndrome:
analysis from the MERLIN-TIMI 36 trial (Metabolic
Efficiency With Ranolazine for Less Ischemia in Non-STElevation
Acute Coronary Syndromes-Thrombolysis In
Myocardial Infarction 36). J Am Coll Cardiol. 2014;63:1644–53.
doi:10.1016/j.jacc.2013.12.034. Erratum in: J Am Coll Cardiol
2014;63:2642. This large analysis confirmed that biomarkers
reflective of hemodynamic stress including copeptin add to
the prognostic value obtained from cTnT in NSTE-ACS.
- Balmelli C,Meune C, Twerenbold R, Reichlin T, Rieder S, Drexler
B, et al. Comparison of the performances of cardiac troponins,
including sensitive assays, and copeptin in the diagnostic of acute
myocardial infarction and long-term prognosis between women and
men. Am Heart J. 2013;166:30–7. doi:10.1016/j.ahj.2013.03.014.
- PepysMB. C-reactive protein fifty years on. Lancet. 1981;1:653–7.
- He LP, Tang XY, LingWH, ChenWQ, Chen YM. Early C-reactive
protein in the prediction of long-term outcomes after acute coronary
syndromes: a meta-analysis of longitudinal studies. Heart. 2010;96:
339–46. doi:10.1136/hrt.2009.174912.
- de Beer FC, Hind CR, Fox KM, Allan RM, Maseri A, Pepys MB.
Measurement of serum C-reactive protein concentration in myocardial
ischaemia and infarction. Br Heart J. 1982;47:239–43.
- Smith SJ, Bos G, Esseveld MR, Van Eijk HG, Gerbrandy J. Acutephase
proteins from the liver and enzymes from myocardial infarction;
a quantitative relationship. Clin Chim Acta. 1977;81:75–85.
- Wensley F, Gao P, Burgess S, Kaptoge S, Di Angelantonio E, Shah
T, et al. Association between C reactive protein and coronary heart
disease: mendelian randomisation analysis based on individual participant
data. BMJ. 2011;342:d548. doi:10.1136/bmj.d548.
- Liuzzo G, Biasucci LM, Gallimore JR, Grillo RL, Rebuzzi AG,
Pepys MB, et al. The prognostic value of C-reactive protein and
serum amyloid a protein in severe unstable angina. N Engl J Med.
1994;331:417–24.
40.• James SK, Armstrong P, Barnathan E, Califf R, Lindahl B, Siegbahn
A, et al. Troponin and C-reactive protein have different relations to
subsequent mortality and myocardial infarction after acute coronary
syndrome: a GUSTO-IV substudy. J Am Coll Cardiol. 2003;41:916–
- This large analysis demonstrated that CRP levels add prognostic
increment to cTnT regarding the prediction of mortality in
NSTE-ACS whereas there was no added value regarding the prediction
of recurrent ischemic events.
- Morrow DA, Rifai N, Antman EM, Weiner DL, McCabe CH,
Cannon CP, et al. C-reactive protein is a potent predictor of mortality
independently of and in combination with troponin T in acute
coronary syndromes: a TIMI 11A substudy. Thrombolysis in
Myocardial Infarction. J Am Coll Cardiol. 1998;31:1460–5.
- Lindahl B, Toss H, Siegbahn A, Venge P, Wallentin L. Markers of
myocardial damage and inflammation in relation to long-term mortality
in unstable coronary artery disease. FRISC Study Group.
Fragmin during Instability in Coronary Artery Disease. N Engl J
Med. 2000;343:1139–47. doi:10.1056/NEJM200010193431602.
- Bogaty P, Boyer L, Simard S, Dauwe F, Dupuis R, Verret B, et al.
Clinical utility of C-reactive protein measured at admission, hospital
discharge, and 1 month later to predict outcome in patients with
acute coronary disease. The RISCA (recurrence and inflammation
in the acute coronary syndromes) study. J Am Coll Cardiol.
2008;51:2339–46. doi:10.1016/j.jacc.2008.03.019.
- Scirica BM, Sabatine MS, Jarolim P, Murphy SA, de Lemos JL,
Braunwald E, et al. Assessment of multiple cardiac biomarkers in
non-ST-segment elevation acute coronary syndromes: observations
from the MERLIN-TIMI 36 trial. Eur Heart J. 2011;32:697–705.
doi:10.1093/eurheartj/ehq468.
- Biasucci LM, KoenigW, Mair J, Mueller C, Plebani M, Lindahl B,
et al. How to use C-reactive protein in acute coronary care. Eur
Heart J. 2013;34:3687–90. doi:10.1093/eurheartj/eht435.
- Weinberg E, Shimpo M, De Keulenaer G, MacGillivray C,
Tominaga S, Solomon S, et al. Expression and regulation of ST2,
an interleukin-1 receptor family member, in cardiomyocytes and
myocardial infarction. Circulation. 2002;106:2961–6.
- Januzzi Jr JL. ST2 as a cardiovascular risk biomarker: from the
bench to the bedside. J Cardiovasc Transl Res. 2013;6:493–500.
doi:10.1007/s12265-013-9459-y.
- Kohli P, Bonaca MP, Kakkar R, Kudinova AY, Scirica BM,
Sabatine MS, et al. Role of ST2 in non-ST-elevation acute coronary
syndrome in theMERLIN-TIMI 36 trial. Clin Chem. 2012;58:257–
- doi:10.1373/clinchem.2011.173369.
- Richards AM, Di Somma S, Mueller T. ST2 in stable and unstable
ischemic heart diseases. Am J Cardiol. 2015;115(7 Suppl):48B–58.
doi:10.1016/j.amjcard.2015.01.041.
- Aldous SJ, Richards AM, Troughton R, Than M. ST2 has diagnostic
and prognostic utility for all-cause mortality and heart failure in
patients presenting to the emergency department with chest pain. J
Card Fail. 2012;18:304–10. doi:10.1016/j.cardfail.2012.01.008.
- Sabatine MS, Morrow DA, Higgins LJ, MacGillivray C, GuoW, Bode
C, et al. Complementary roles for biomarkers of biomechanical strain
ST2 and N-terminal prohormone B-type natriuretic peptide in patients
with ST-elevation myocardial infarction. Circulation. 2008;117:1936–
- doi:10.1161/CIRCULATIONAHA.107.728022.
- Shimpo M, Morrow DA,Weinberg EO, Sabatine MS,Murphy SA,
Antman EM, et al. Serum levels of the interleukin-1 receptor family
member ST2 predict mortality and clinical outcome in acute
myocardial infarction. Circulation. 2004;109:2186–90. doi:10.
1161/01.CIR.0000127958.21003.5A.
- Dhillon OS, Narayan HK, Khan SQ, Kelly D, Quinn PA, Squire IB,
et al. Pre-discharge risk stratification in unselected STEMI: is there
a role for ST2 or its natural ligand IL-33 when compared with
contemporary risk markers? Int J Cardiol. 2013;167:2182–8. doi:
10.1016/j.ijcard.2012.05.073.
54.• O’Donoghue ML, Morrow DA, Cannon CP, Jarolim P, Desai NR,
Sherwood MW. Multimarker risk stratification in patients with acute
myocardial infarction. J Am Heart Assoc. 2016;5:e002586. doi:10.
1161/JAHA.115.002586. In this head-to-head analysis of 11 biomarkers
reflective of different pathobiological pathways, ST2 together
with myeloperoxidase and cTnT were the only biomarkers
that independently predicted adverse outcome in STEMI.
- Weir RA, Miller AM, Murphy GE, Clements S, Steedman T, Connell
JM, et al. Serum soluble ST2: a potential novel mediator in left ventricular
and infarct remodeling after acute myocardial infarction. J Am
Coll Cardiol. 2010;55:243–50. doi:10.1016/j.jacc.2009.08.047.
- Unsicker K, Spittau B, Krieglstein K. The multiple facets of the
TGF-beta family cytokine growth/differentiation factor-15/macrophage
inhibitory cytokine-1. Cytokine Growth Factor Rev.
2013;24:373–84. doi:10.1016/j.cytogfr.2013.05.003.
- Zhang S, Dai D, Wang X, Zhu H, Jin H, Zhao R, et al. Growth
differentiation factor-15 predicts the prognoses of patients with
acute coronary syndrome: a meta-analysis. BMC Cardiovasc
Disord. 2016;16:82. doi:10.1186/s12872-016-0250-2.
58.•• HagstromE, James SK, BertilssonM, Becker RC, Himmelmann A,
Husted S, et al. Growth differentiation factor-15 level predicts major
bleeding and cardiovascular events in patients with acute coronary
syndromes: results from the PLATO study. Eur Heart J.
2016;37:1325–33. doi:10.1093/eurheartj/ehv491. This study
confirmed the strong value of GDF-15 as a predictor of global
risk independent of hs-cTnT levels.
- Bonaca MP, Morrow DA, Braunwald E, Cannon CP, Jiang S,
Breher S, et al. Growth differentiation factor-15 and risk of recurrent
events in patients stabilized after acute coronary syndrome:
observations from PROVE IT-TIMI 22. Arterioscler Thromb Vasc
Biol. 2011;31:203–10. doi:10.1161/ATVBAHA.
- Wollert KC, Kempf T, Lagerqvist B, Lindahl B,Olofsson S, Allhoff
T, et al. Growth differentiation factor 15 for risk stratification and
selection of an invasive treatment strategy in non-ST-elevation
acute coronary syndrome. Circulation. 2007;116:1540–8. doi:10.
1161/CIRCULATIONAHA.107.697714.
- Lindholm D, James SK, Bertilsson M, Becker RC, Cannon CP,
Giannitsis E. Biomarkers and coronary lesions predict outcomes
after revascularization in non-ST-elevation acute coronary syndrome.
Clin Chem. 2016. doi:10.1373/clinchem.2016.261271.
- Cockcroft DW, Gault MH. Prediction of creatinine clearance from
serum creatinine. Nephron. 1976;16:31–41.
- Levey AS, Greene T, Kusek JW, Beck GJ,MDRD Study Group. A
simplified equation to predict glomerular filtration rate from serum
creatinine. J Am Soc Nephrol. 2000;11:155A.
- Melloni C, Peterson ED, Chen AY, Szczech LA, Newby LK,
Harrington RA, et al. Cockcroft-Gault versus modification of diet
in renal disease: importance of glomerular filtration rate formula for
classification of chronic kidney disease in patients with non-STsegment
elevation acute coronary syndromes. J Am Coll Cardiol.
2008;51:991–6. doi:10.1016/j.jacc.2007.11.045.
- Szummer K, Lundman P, Jacobson SH, Schön S, Lindbäck J,
Stenestrand U, et al. Relation between renal function, presentation,
use of therapies and in-hospital complications in acute coronary
syndrome: data from the SWEDEHEART register. J Intern Med.
2010;268(1):40–9. doi:10.1111/j.1365-2796.2009.02204.x.
- Levey AS, Stevens LA, Schmid CH, Zhang YL, Castro 3rd AF,
Feldman HI, et al. A new equation to estimate glomerular filtration
rate. Ann Intern Med. 2009;150:604–12. Erratum in: Ann Intern
Med 2011;155:408.
67.•• Åkerblom A, Wallentin L, Larsson A, Siegbahn A, Becker RC,
Budaj A, et al. Cystatin C- and creatinine-based estimates of renal
function and their value for risk prediction in patients with acute
coronary syndrome: results from the PLATelet Inhibition and
Patient Outcomes (PLATO) study. Clin Chem. 2013;59:1369–75.
doi:10.1373/clinchem.2012.200709. The so far largest study
investigating the prognostic value of estimates of renal
dysfunction in ACS, including cystatin C.
- Mueller C, Neumann FJ, Perruchoud AP, Buettner HJ. Renal function
and long term mortality after unstable angina/non-ST segment
elevation myocardial infarction treated very early and predominantly
with percutaneous coronary intervention. Heart. 2004;90:902–7.
doi:10.1136/hrt.2003.021741.
- Freda BJ, Tang WH, Van Lente F, Peacock WF, Francis GS.
Cardiac troponins in renal insufficiency: review and clinical implications.
J Am Coll Cardiol. 2002;40:2065–71.
- Parikh RH, Seliger SL, deFilippi CR. Use and interpretation of high
sensitivity cardiac troponins in patients with chronic kidney disease
with and without acute myocardial infarction. Clin Biochem.
2015;48:247–53. doi:10.1016/j.clinbiochem.2015.01.004.
- Diris JH, Hackeng CM, Kooman JP, Pinto YM, Hermens WT, van
Dieijen-Visser MP. Impaired renal clearance explains elevated troponin
T fragments in hemodialysis patients. Circulation. 2004;109:
23–5. doi:10.1161/01.CIR.0000109483.45211.8F.
- Melloni C, Alexander KP, Milford-Beland S, Newby LK, Szczech LA,
Pollack CV, et al. Prognostic value of troponins in patients with non-
ST-segment elevation acute coronary syndromes and chronic kidney
disease. Clin Cardiol. 2008;31:125–9. doi:10.1002/clc.20210.
- Newman DJ, Cystatin C. Ann Clin Biochem. 2002;39:89–104.
- Laterza OF, Price CP, ScottMG. Cystatin C: an improved estimator
of glomerular filtration rate? Clin Chem. 2002;48:699–707.
- Liu J, Sukhova GK, Sun JS, Xu WH, Libby P, Shi GP. Lysosomal
cysteine proteases in atherosclerosis. Arterioscler Thromb Vasc Biol.
2004;24:1359–66. doi:10.1161/01.ATV.0000134530.27208.41.
- Jernberg T, Lindahl B, James S, Larsson A, Hansson LO,Wallentin
- A novel predictor of outcome in suspected or confirmed non-STelevation
acute coronary syndrome. Circulation. 2004;110:2342–8.
doi:10.1161/01.CIR.0000145166.44942.E0.
- Kilic T, Oner G, Ural E, Yumuk Z, Sahin T, Bildirici U, et al.
Comparison of the long-term prognostic value of Cystatin C
to other indicators of renal function, markers of inflammation
and systolic dysfunction among patients with acute coronary
syndrome. Atherosclerosis. 2009;207:552–8. doi:10.1016/j.
atherosclerosis.2009.05.015.
- García Acuña JM, González-Babarro E, Grigorian Shamagian L,
Peña-Gil C, Vidal Pérez R, López-Lago AM, et al. Cystatin C
provides more information than other renal function parameters
for stratifying risk in patients with acute coronary syndrome. Rev
Esp Cardiol. 2009;62:510–9.
- Van Eyk JE. Overview: the maturing of proteomics in cardiovascular
research. Circ Res. 2011;108:490–8. doi:10.1161/
CIRCRESAHA.110.226894.
- Stastna M, Van Eyk JE. Secreted proteins as a fundamental source
for biomarker discovery. Proteomics. 2012;12:722–35. doi:10.
1002/pmic.201100346.
- Navickas R, Gal D, Laucevičius A, Taparauskaitė A, Zdanytė M,
Holvoet P. Identifying circulating microRNAs as biomarkers of
cardiovascular disease: a systematic review. Cardiovasc Res.
2016;111:322–37. doi:10.1093/cvr/cvw174.
- Hijazi Z, Lindbäck J, Alexander JH, Hanna M, Held C, Hylek EM,
et al. The ABC (age, biomarkers, clinical history) stroke risk score:
a biomarker-based risk score for predicting stroke in atrial fibrillation.
Eur Heart J. 2016;37:1582–90. doi:10.1093/eurheartj/ehw054.
- Lindholm D, Lindback J, James SK, Becker RC,
Himmelmann A, Siegbahn A, et al. Biomarker-based prediction
model for recurrent ischemic events in revascularised
patients with acute coronary syndromes. Eur Heart J.
2015;36((Abstract Supplement)):10–1.
تست فرا- حساس تروپونین: چالشها و فرصتها برای آزمایشگاهها و پزشکان
معرفی آزمایش N-Termnal Pro B-type Natriuretic Peptide (NT-Pro BNP)
برای دانلود فایل pdf بر روی لینک زیر کلیک کنید
ورود / ثبت نام