خانواده سودوموناداسه
زکیه نظری کارشناس ارشد میکروبیولوژی zakiye.nazari1987@gmail.com
دکتر مهدی قیامی راد دکترای تخصصی میکروبیولوژی
تاريخچه:
اجداد مشترك سودوموناد (pseudomonad) صدها ميليون سال پيش زندگي ميكردند، با اين حال آنها در پايان قرن نوزدهم توسط انسانها طبقه بندي شدند. نام عمومي سودوموناس بوســـــــــيله walter migula در سال 1894 تا 1900 به عنوان يك جنس از باكتريهاي گرم منفي، ميلهاي شكل، قطبي و داراي تاژك تعيين شد و براي اولين بار در نسخه 7 كتابچه راهنماي Bergey به زبان يوناني اينچنين بيان شد كه pseudes به معناي كاذب (false) وmonas به معناي تك واحد است كه ميتواند معني واحد كاذب (false unit) را بدهد.
بعدها سودوموناس آئروژينوزا بطور فزايندهاي به عنوان پاتوژن فرصت طلب در حال ظهور، به رسميت شناخته شد.
مقدمه:
خانواده سودوموناداسه متشكل از گروه بزرگي از باسيلهاي گرم منفي است كه با انتشار وسيع در خاك، مواد معدني، گياهان و آب يافت ميشود و تاكنون بيش از 87 گونه از آن شناسايي شده است. چندين گونه از اعضاي اين جنس بيماريزاي حيوانات و گياهان هستند. اغلب ارگانيسمهاي جنس سودوموناس، انسان را آلوده نميكنند، اما بعضي از آنها بيماريزاي فرصت طلب مهم براي ميزبانهايي هستند كه سيستم دفاعي آنها ضعيف شده باشد.
سودوموناس آئروژينوزا مهمترين پاتوژن انساني در اين گروه است كه به عنوان دومين عامل عفونتهاي سوختگي است، همچنين اين باكتري در محيطهاي بيمارستاني و در مناطق مرطوب يافت ميشود. سودوموناسها همچنين فاكتورهاي ساختماني، آنزيمها و توكسينهاي بسياري به منظور افزايش ويرولانس و مقاومت به آنتيبيوتيكهاي معمول توليد ميكنند.
طبقه بندي:
دامنه: باكتري
شاخه: Proteobacteria
كلاس: Gammaproteobacteria
راسته: Pseudomonadales
نام خانوادگي: Pseudomonadaceae
جنس: Pseudomonas
خانواده سودوموناداسه بر پايه همساني rRNA به پنج گروه تقسيم ميشوند:
گروه يك از سايرين مهمتر است و خود به دو گروه فلورسانت و غير فلورسانت تقسيم ميشود. سودوموناسهاي فلورسنت شامل aeroginosa، flurescens و putida و سودومونــــــــاسهاي غير فلورسنت شامل alcaligenes، pseudoalcaligenes و stutzeri ميباشند.
گروه دو Burkholderia، گروه سهDelftia ، گروه چهار Brevundimonas و گروه پنج Stenotrophomonas ميباشد. سودوموناس آئروژينوزا، بورخلدريا سودومالئي، بورخلدريا مالئي، بورخلدريا سپاسيا و استنوترفوموناس (گزانتوموناس) مالتوفيليا گونههاي مهم و بيماريزاي آن ميباشد كه در ادامه به آنها ميپردازيم.
خصوصيات كلي:
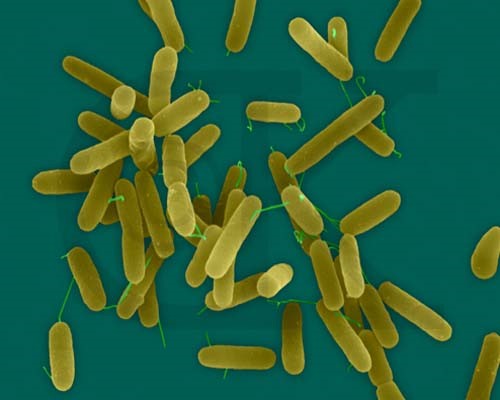
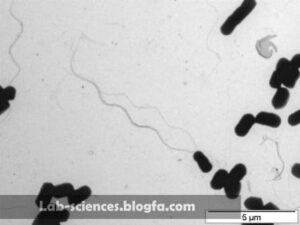
سودوموناس باسيل مستقيم يا كمي خميده و گرم منفي است به ابعاد (0/5 تا 1 ميكرومتر در 5 /1تا 5 ميكرومتر) و متحرك با فلاژلهاي قطبي و پيلي ميباشد. ارگانيسم غير تخميري و اكسيژن پذيرنده نهايي الكترون بوده و اكسيداز و كاتالاز مثبت است. گرچه اين ارگانيسمها هوازي اجباري محسوب ميشوند ولي با استفاده از نيترات به عنوان پذيرنده نهايي الكترون بجاي اكسيژن ميتوانند بصورت بيهوازي رشد كنند.
برخي از محصولات سودوموناس، پيگمان منتشر شونده است مثل پيوسيانين (آبي)، فلورسئين (زرد) و پيوروبين (قرمز- قهوهاي) كه توليد پيوسيانين مختص سودوموناس آئروژينوزا است. تشكيل گاز در سودوموناس و همچنين تستهاي ايندول، متيل-رد و VP منفي است و تست سيترات آن مثبت است.
شكل كلنيهاي سودوموناس:
Flat diffuse colonies with an irregular edge: در محيط آگار و دماي 37 درجه سانتيگراد بيشتر جدايهها كلنيهاي تخت و منتشر با لبههاي نامنظم پديد ميآورند.
Colliform in appearance: پارهاي از كلنيها نمودي همانند كوليفرم دارند.
Dry pepper-corn colonies: كلنيهاي ديگر مثل كلنيهاي دانه فلفلي خشك، كمياب هستند.
Dwarf colonies: كلنيهاي موكوئيد و بسيار ريز دارند.
كلنيها ممكن است فرمهاي s (صاف و درخشان) يا R (خشن و دانهدار) و آتيپيك M داشته باشند. بعضي از سويهها كلنيهاي براق فلزي دارند.
خصوصيات سودوموناس آئروژينوزا:
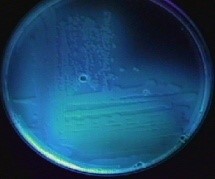
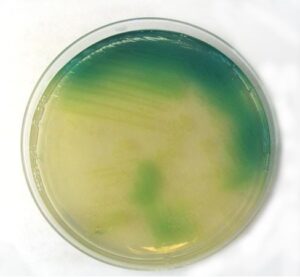
سودوموناس آئروژينوزا يك باسيل هوازي گرم منفي با اندازهاي در حدود (0/5 تا 1 ميكرون در 3 تا 4 ميكرون) ميباشد. اين باسيلها بصورت تك تك، جفت و گاه به صورت زنجيرههاي كوتاه مشاهده ميشوند و فاقد اسپور هستند. اغلب سلولها يك فلاژل قطبي دارند، اما گاهي ممكن است 2 يا 3 فلاژل داشته باشند. اغلب ارگانيسمهايي كه از نمونههاي باليني جدا شدهاند حاوي پيلي هستند. سودوموناي آئروژينوزا از نظر آزمون سيمون سيترات و آرژنين دهيدرولاز مثبت و از نظر ليزين دكربوكسيلاز و اورنيتين دكربوكسيلاز منفي است. سودوموناس آئروژينوزا داراي كلنيهاي گرد، درشت، خزنده، صاف و نامنظم است كه به علت توليد پيگمان سبز در محيط كشت، آن را به رنگ سبز درميآورد.
بعضي سويهها رنگ فلورسانت فلورسئين را توليد ميكنند. بطور معمول كشتهاي سودوموناس آئروژينوزا داراي خاصيت بوي معطر ميوهاي و يا شبيه انگور ميباشد. هنگامي كه نمونههاي باليني بر روي پليتهاي آگار خوندار رشد ميكنند غالباً بتا هموليتيك هستند.
خصوصيات بورخلدريا سودومالئي:
گونههاي بورخلدريا در گذشته در جنس سودوموناس دسته بندي ميشدند و اينك خود جنس جداگانهاي هستند و مهمترين گونههاي آن مالئي و سودومالئي ميباشد. بورخلدريا سودومالئي يك باسيل گرم منفي، كوچك، هوازي و متحرك است، كلونيهاي مخاطي يا صاف تا زبر و چين و چروك خورده را با رنگ كرم تا نارنجي تشكيل ميدهد. در رنگ آميزي بصورت دو قطبي نمايان ميشود و اين حالت به باكتري در آزمايش ميكروسكوپي ظاهري شبيه به سنجاق سر ميدهد.
در محيط ژلوز خوندار ابتدا هموليز ناقص است ولي بعد كامل ميگردد. درجه حرارت مناسب رشد 37 درجه سانتيگراد است ولي در 42 درجه سانتيگراد نيز رشد ميكند. اين باكتري اكسيداز مثبت بوده و نيترات را به نيتريت احيا ميكند. اين باكتري در آگار TSI پس از 24 ساعت در قسمت شيبدار حالت اسيدي و در عمق حالت خنثي (پس از 72 ساعت انكوباسيون به حالت اسيدي تغيير ميكند) ايجاد ميكند.
خصوصيات بورخلدريا مالئي:
باسيل گرم منفي كوچك، بدون حركت، بدون پيگمان و هوازي، بدون كپسول و هاگ است. در محيط ژلوز گليسرول به فاصله چند روز پوشش كرم رنگ در سطح محيط كه صاف، مرطوب و چسبناك است بوجود ميآيد. درجه حرارت مناسب رشد 37 درجه سانتيگراد و مدت زمان انكوباسيون 48-24 ساعت است. در اين شرايط پرگنههاي صاف، سفيد تا كرم رنگ با قطر 2-1 ميليمتر رشد ميكنند.
خصوصيات مهم سودوموناس آئروژينوزا، بورخلدريا سودومالئي و بورخلدريا مالئي
| خصوصيات | سودوموناس آئروژنز | بورخلدريا سودومالئي | بورخلدريا مالئي |
| توليد رنگدانه | ++ | — | — |
| بو | بوي ميوه مشابه انگور | بوي فساد | — |
| رشد در آگار مككانكي | + | + | — |
| رشد در 5 درجه سانتيگراد | — | — | — |
| رشد در 42 درجه سانتيگراد | + | + | — |
| اكسيداسيون گلوكز | + | + | + |
| اكسيداسين لاكتوز | — | + | — |
| احياء نيترات به نيتريت | + | + | + |
| احياء نيترات به گاز N2 | متغير | + | — |
| حركت | + | + | — |
خصوصيات بورخلدريا سپاسيا:
بورخلدريا سپاسيا قبلاً تحت عنوان EO-1، سودوموناس كينگي و سودوموناس مولتي وورانس طبقه بندي ميشد. باسيل گرم منفي است و براي كشت آن ميتوان از محيط كشت داراي كوليستين نيز استفاده كرد. اين باكتري آهستهتر از ديگر باكتريهاي گرم منفي رشد ميكند و كلنيهاي آن معمولاً بعد ازسه روز مشاهده ميشود.
خصوصيات استنوترفوموناس (گزنتوموناس) مالتوفيليا:
از باسيلهاي غير تخميري و گرم منفي است. اين ارگانيسم قبلاً در گروه سودوموناسها طبقه بندي ميشد، سپس در جنس گزانتوموناس قرار گرفت و نهايتاً به جنس استنوترفوموناس منتقل شد. اين باكتري كلنيهايي را به رنگ خاكستري يا سبز متمايل به بنفش كمرنگ در روي محيط بلاد آگار ايجاد ميكند. اكسيداز منفي بوده و ليزين دكربوكسيلاز مثبت است.
اپيدميولوژي سودوموناس آئروژينوزا:
سودوموناسها پاتوژنهاي فرصت طلبي هستند كه در محيطهاي مختلفي يافت ميشوند. سودوموناسها احتياجات غذايي سادهاي داشته و طيف وسيعي از دما را تحمل ميكنند. رويداد فصلي خاصي براي بيماري وجود ندارد. كلنيزاسيون گذرا در مجراي تنفسي و معده- رودهاي بيماران بستري به ويژه آنهايي كه با آنتيبيوتيكهاي وسيعالطيف درمان ميشوند و يا در معرض ابزار كمك تنفسي قرار دارند يا به مدت طولاني در بيمارستان بستري هستند، وجود دارد. سودوموناس آئروژينوزا در آب، خاك و سبزيجات يافت ميشود.
اين باكتري به روي پوست و درون دستگاه گوارشي و گلوي 3% از كل جمعيت حمل ميشود، اما درجه ناقليت بين كارمندان بيمارستان ممكن است تا 20% هم افزايش يابد. عموماً عفونتها در نقاطي از بدن شكل ميگيرد كه رطوبت فراوان وجود دارد كه شامل حفره دهاني- ناي، پوست سوخته، گوش خارجي و زخمهاي جلدي ميباشد. تحقيقات اپيدميولوژي نشان داده است كه سودوموناس آئروژينوزا، 10% از عفونتهاي بيمارستاني و 11% از نمونههاي خون را به خود اختصاص ميدهد، اما فقط 4% از اپيدميهاي بيمارستاني را موجب شده است. به علت اهميت وجود اين باكتري در آب، مؤسسه استاندارد و تحقيقات صنعتي ايران آزموني را بنام كيفيت آب- شناسايي و شمارش سودوموناس آئروژينوزا به روش صاف كردن غشايي- تعيين كرده است كه اين استاندارد انواع مختلف آب، آب معدني و آب استخرهاي شنا را شامل ميشود.
اپيدميولوژي عفونتهاي بيمارستاني و زخمهاي سوختگي ناشي از سودوموناس آئروژينوزا:
سودوموناس آئروژينوزا پاتوژن فرصت طلبي است كه در سالهاي اخير به عنوان يكي از مهمترين پاتوژنهاي بيمارستاني شناسايي شده است. اين باكتري مسئول 11 تا 13 درصد از عفونتهاي بيمارستاني به ويژه در بيماران فيبروز سيستيك، اشخاص دچار سوختگي يا داراي نقص ايمني و افرادي كه هوادهي مصنوعي ميشوند، است. با وجود پيشرفتهاي زيادي كه در درمان بيماران سوخته بوجود آمده است، هنوز هم سوختگيها به عنوان يكي از مهمترين عوامل مرگ و مير در جوامع بشري محسوب ميشود؛ بطوري كه گفته ميشود عفونت، عامل بيش از 75% مرگ و مير بعد از سوختگي است.
سپسيس ناشي از اين باكتري يك عارضه جدي متعاقب عفونت سوختگي است. از دست دادن سد دفاعي پوست، سركوب سيستم ايمني، تعلل در ارجاع بيمار به بيمارستان، طول مدت اقامت در بيمارستان و اقدامات عملي- درماني عواملي هستند كه باعث ميشوند افراد دچار سوختگي در اغلب موارد در معرض خطر به عفونتهاي متعدد گردند. سودوموناس آئروژينوزا به عنوان دومين بيماريزاي بسيار رايج در جراحيها و سومين باكتري مطرح در پزشكي است. طي نتايج بدست آمده تمام 150 سويه بدست آمده از عفونت سوختگي داراي ژن oprI و oprL بوده است. 94/7 درصد سويهها داراي توكسين A،65/4 درصد داراي اگزو آنزيم و 12/66درصد داراي نورآمينيداز I (nanI) بودند.
فراواني عفونت سوختگي باكتريال در مراجعين به بخش سوختگي بيمارستان بعثت همدان به ترتيب شيوع، سودوموناس آئروژينوزا 72/7%، استاف اورئوس 14/4% و استافيلوكوك اپيدرميديس 7/8% گزارش شد. طي تحقيقاتي، اساتيد دانشگاه علوم پزشكي تبريز گزارش دادند 63/3درصد عوامل باكتريايي در عفونتهاي سوختگي از نوع سودوموناس است. طي بررسيهايي به اين نتيجه رسيدند كه آنتيباديهاي ضد فلاژلي سودوموناس با مهار تهاجم باكتري و اوپسونيزه كردن آن ميتوانند در برابر عفونت ناشي از زخم سوختگي اثر حفاظتي داشته باشند كه براي درمان سوختگي كمك كننده است.
در مطالعه وضعيت عفونتهاي سودوموناسي و استافيلوكوكي مقاوم به دارو در بخش سوانح سوختگي بيمارستان زارع ساري مشخص شده كه 51/4 درصد از نمونههاي باليني و 37/3 درصد از لوازم و تجهيزات پزشكي به سودوموناس آئروژينوزا آلوده بودهاند.
طي تحقيقات به عمل آمده سودوموناس آئروژينوزا از گوجه، تربچه، كرفس، كلم، خيار و پياز در آشپزخانه يك بيمارستان عمومي ايزوله شده است. اين باكتري در دست پرسنل آشپزخانه بيمارستان و تخته برش كه با برخورد سبزيجات آلوده شده است، وجود دارد. سبزيجات منبع و ناقل مهم سودوموناس آئروژينوزا است.Shooter و همكارانش طي آزمايشات خود در غذاهاي آشپزخانه بيمارستان، اشريشيا كولي، سودوموناس و كلبسيلا را يافتند و مشخص شد سبزيجات نپخته در آشپزخانه بيمارستان منبع سودوموناس آئروژينوزا است.
اپيدميولوژي مقاومت آنتيبيوتيكي سودوموناس آئروژينوزا:
سودوموناس آئروژينوزا مقاومت زيادي نسبت به بسياري از مواد ضد ميكروبي و ضد عفوني كننده نظير تركيبات آمونيوم، هگزا كلروفن، صابونها و محلولهاي يد دارد. افزون بر اين، استفاده گسترده از آنتيبيوتيكها در سالهاي اخير موجب شده است كه اين باكتري نسبت به آنتيبيوتيكهاي وسيعالطيف از گروههاي مختلف آنتيبيوتيكي مقاوم شود. مصرف رو به ازدياد بيوسايدها در فراوردههاي بهداشتي كه از اواسط دهه 1990 ميلادي آغاز شد و همچنان ادامه دارد، نگراني ميكروب شناسان و متخصصان بهداشت و سلامت را تشديد كرده است.
وجود سويههاي با مقاومت چندگانه دارويي مشكل اصلي در درمان باكتري در بخشهاي مهم بيمارستاني چون سوختگي و مراقبتهاي ويژه است. با توجه به توانايي ذاتي و اكتسابي اين باكتري در ايجاد مقاومت به بسياري از عوامل ضد ميكروبي، شناسايي الگوي مقاومت آن در كنترل باكتري اهميت بالايي دارد. طي مطالعاتي بر روي سويههاي توليد كننده متالوبتالاكتاماز (تجزيه كننده آنتيبيوتيكهاي بتالاكتام) در سودوموناس آئروژينوزاي جدا شده از سوختگي به اين نتيجه رسيدند كه سودوموناس آئروژينوزا داراي اين آنزيم، به آنتيبيوتيكهاي ايميپنم، كاربنيسيلين، آميكاسين، توبرامايسين، تيكارسيلين، پلي ميكزين B و لكتين سولفات مقاوم است.
طي بررسيهاي خانم آهني آذري بر روي سودوموناس آئروژينوزاي جدا شده از بيمارستان طالقاني گرگان، بخش تالاسمي با 38/5% آلودهترين بخش و شيرهاي آب با 61/1% آلودهترين محل از نظر نمونه برداري شناسايي شدند كه 20% آنها به سفتازيديم و 32/7% به پيپراسيلين مقاومت داشته و 10/9% از آنها مقاومت همزمان به هر دو آنتيبيوتيك داشتند. ريسك فاكتورها در عفونتهاي تنفسي مقاومت چند دارويي سودوموناس آئروژينوزا (MDR- PA) در بيماران بستري شده در بيمارستان علاوه بر سوندهاي ادراري، لولههاي تغذيه هستند. طي بررسي حساسيت دارويي و اپيدميولوژي مولكولي سودومونوس آئروژينوزاي جدا شده از بيماران سوخته، بيشترين مقاومت نسبت به آنتيبيوتيك سفيزوكسيم (87%) و بيشترين حساسيت نسبت به ايميپنم (65/5 %) بود.
مكانيزم مقاومت آنتيبيوتيكي در سودوموناس آئروژينوزا
| آنتيبيوتيك | مكانيسم مقاومت |
| بتالاكتام | هيدروليز بتالاكتام، كاهش نفوذ پذيري، تغيير پروتئينهاي اتصالي |
| آمينوگليكوزيد | هيدروليز آنزيمي با استيلاسون، آدنيلاسيون يا فسفريلاسيون، كاهش نفوذ پذيري، تغيير هدف ريبوزومي |
| كلرامفنيكل | هيدروليز آنزيمي از طريق استيل ترانسفراز، كاهش نفوذ پذيري |
| فلوروكوئينولون | تغيير هدف (DNA جيراز)، كاهش نفوذ پذيري |
اپيدميولوژي بورخلدريا سودومالئي:
يك باكتري با زندگي آزاد است كه در آب گرم و خاك مرطوب نواحي اندميك، عمدتاً در جنوب شرقي آسيا يافت ميشود. اين باكتري به ويژه در جنوب تايلند و ويتنام شايع است، ولي مواردي از بيماري در فرانسه، ايران، چين و آمريكا گزارش شده است. در شاليزارهاي برنج رشد كرده و باعث ايجاد يك بيماري بنام مليوئيدوز يا شبه مشمشه ميشود. در جريان جنگ ويتنام 150 مورد ابتلا در نظاميان آمريكايي وجود داشته كه تقريباً 30 درصد از موارد ابتلا در سرنشينان هليكوپتر اتفاق افتاده است. بيماري در جوندگان، خرگوش، كبوتر، انسان و حيوانات باغ وحش مثل گوزن، سگ، گربه، گوسفند و بز و شتر گزارش شده است.
پخش عفونت از طريق مصرف آب و غذاي آلوده، گزش حشرات، زخمهاي جلدي و احتمالاً از طريق استنشاق مواد آلوده است. گرسنگي و استرسهاي ديگر حساسيت حيوان آزمايشگاهي را در مقابل عفونت افزايش ميدهد. در گذشته بورخلدريا سودومالئي، باسيل وتيمورBacillus of whitmore)) اطلاق ميشد. بورخلدريا سودومالئي به عنوان سلاح بيولوژيك استفاده ميشود، در نتيجه كار روي اين باكتري محدوديتهايي دارد و در آزمايشگاههايي كه مجوز لازم دارند تحقيقات انجام ميشود.
اپيدميولوژي بورخلدريا مالئي:
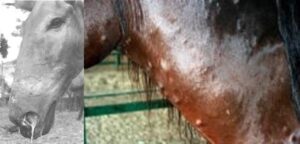
بورخلدريا مالئي عامل مشمشه و فرم پوستي آن يعني سراجه در تك سميها (اسب، قاطر، الاغ) است. انسان و بعضي از گربهسانان مثل شير مستعد ابتلا به بيماري هستند و عفونت گاهي در سگ، گوسفند، بز و شتر اتفاق ميافتد. گاو، خوك، موش صحرايي و پرندگان در مقابل عفونت مقاوم ميباشند. در انسان اغلب كشنده است و موارد آن در افرادي كه در تماس نزديك با دام آلوده هستند مثل پرورش دهندگان اسب اتفاق ميافتد.
بورخلدريا مالئي يك انگل اجباري در دام است و در طبيعت يافت نميشود. انتقال بيماري از طريق بلع مواد آلوده و به ميزان كمتري از طريق استنشاق مواد آلوده است. علائم عمومي مشمشه شامل تب، درد عضله، سردرد، اسهال و كاهش وزن است. بوسيله جراحت پوست و غشاي مخاطي مشخص ميشود و بدون كنترل ممكن است وارد جريان خون شود و به سراسر بدن منتقل شود.
اپيدميولوژي بورخلدريا سپاسيا:
ارگانيسمي است كه در محيط اطراف يافت شده و قادر به رشد در آب، خاك، گياهان، حيوانات و سبزيجات در حال پوسيدگي است. در بيمارستان از منابع مختلفي از آب و محيط اطراف جدا شده است كه از آن طريق ميتواند به بيماران انتقال يابد. بيماران مبتلا به فيبروز سيستيك به عفونت با بورخلدريا سپاسيا مستعد هستند.
اپيدميولوژي استنوترفوموناس مالتوفيليا:
در اپيدميهاي بيمارستاني ردپايي از اين باكتري در محلولهاي ضد عفوني كننده، دستگاههاي درماني تنفسي و تجهيزات نمايشگر و ماشينهاي يخ ديده ميشود.
فاكتورهاي بيماريزايي
سودوموناس آئروژينوزا:
سودوموناس آئروژنز ويرولانس فاكتورهاي متعددي دارد كه شامل تركيبات ساختماني، توكسين و آنزيمهاي مختلف است.
- فاكتورهاي باكتريايي درگير در بيماريزايي عفونتهاي سودوموناس آئروژينوزا:
الف) اندوتوكسين: اندوتوكسين ليپوپليساكايد در سودوموناس آنتيژن اصلي ديواره سلولي ميباشد. قسمت ليپيد A ليپوپليساكاريد، فعاليت اندوتوكسيك دارد. شوك اندوتوكسيك در بيماراني كه دچار باكتريمي سودوموناس هستند رخ ميدهد. بيش از يك نوع آنتيژن O ممكن است بطور همزمان بيان شود.
ب)پروتئازهاي خارج سلولي: حملهوري و حدّت اين باكتري براي انسان و حيوانات، بيشتر مربوط به اين پروتئازها و اگزوتوكسين A است. حداقل سه پروتئاز خارج سلولي حائز اهميت توسط سودوموناس آئروژينوزا توليد ميشود كه شامل الاستاز، آلكالين پروتئاز و پروتئاز IV ميباشد. الاستاز باعث تخريب بافتهاي حاوي الاستين (مانند رگهاي خوني، بافت ريه، پوست) كلاژن، ايمونوگلوبولينها و فاكتورهاي كمپلمان ميشود. الاستاز از طريق تجزيه كلاژنهاي نوع IV، V و VI باعث صدمه به چشم شده و در نهايت موجب كراتيت ميشود.
آلكالين پروتئاز منجر به اختلال بافتي و انتشار سودوموناس آئروژينوزا ميشود. اين آنزيم غالباً برهم زننده پاسخهاي ايمني ميزبان است.
پروتئاز IV ناشناخته باقي مانده است، اما تحقيقات در خرگوش نشان داده است كه فعاليت پروتئاز IV به چشم آسيب ميرساند و با ايجاد كراتيت در ارتباط است.
ج) اگزوتوكسينهاي ADP– ريبوزيل ترانسفراز:
شامل اگزوتوكسين A، اگزوآنزيم S و لكوسيدين با وزن مولكولي بالا ميباشد.
اگزوتوكسين A يكي از مهمترين فاكتورهاي ويرولانس توليد شده است؛ آنزيمي كه از طريق غير فعال كردن فاكتور طويل كننده2 (EF-2) باعث توقف سنتز پروتئين و در نهايت مرگ سلول ميشود. اگزوتوكسين A از طريق تجزيه نيكوتين آميد دينوكلئوتيد (NAD) به ADP- ريبوزيلات EF2 عمل ميكند. اگزوتوكسينA داراي سه قسمت است؛ بخش I به گيرندههاي سلولي ميزبان متصل ميشود و اندوسيتوز را پيريزي ميكند. بخش II موجـــــب انتقال توكسين به درون سيتوپلاسم سلول ميشود و بخش III، ADP- ريبوزيل فاكتور طويل كننده 2 را كاتاليز ميكند.
اگزوآنزيم S (EXOS) پروتئينهاي سلولي ميزبان را در مقايسه با EF-2، ADP- ريبوزيله ميكند. در ميان پروتئينهاي هدف اين آنزيم ميتوان به ويمنتين و چندين پروتئين ديگر كه به GTP متصل ميگردند اشاره كرد. به دليل اينكه پروتئينهاي متصل شونده به GTP در حركت ليزوزومها نقش دارند، اگزوآنزيمها ممكن است سودوموناس آئروژينوزا را از كشته شدن توسط لوكوسيتهاي پليمرفونوكلئر و ماكروفاژها محافظت كنند. به نظر ميرسد كه اگزوآنزيم S عامل مهمي براي گسترش عفونتهاي سودوموناس آئروژينوزا در بيماراني باشد كه دچار سوختگي شدهاند.
لكوسيدين باعث آغاز ADP- ريبوزيلاسيون شده و موجب فعال شدن پروتئين كيناز C ميشود كه عليه لكوسيتهاي پليمرفونوكلئر مؤثر است.
د) سيدروفورها: سودوموناس آئروژينوزا از دو سيدروفور براي كسب آهن سه ظرفيتي ترانسفرين استفاده ميكند. به دليل اينكه باكتري به آهن نياز دارد، باكتريهايي كه نميتوانند آهن را كسب كنند قادر نخواهند بود به بافت ميزبان هجوم ببرند.
ه) پيلي: بسياري از ايزولههاي سودوموناس آئروژينوزا تعداد زيادي از پيلي نوع IV هستند.
اين پيلي اتصال به موسين و سلولهاي اپيتليال را واسطهگري ميكند و در بيماران فيبروز سيستيك اين موسينها به مقدار فراوان توليد ميشوند. در بيماران فيبروز سيستيك بنظر ميرسد كه عفونتهاي سودوموناسي در ريه بوسيله باكتريهاي پيليداري كه ترجيحاً به اپيتليوم تنفسي و موسين فراوان ميچسبند، تثبيت ميشود.
سودوموناس آئروژينوزا همچنين نورآمينيداز توليد ميكند كه باعث افزايش اتصال باكتري به سلولهاي اپيتليال ميشود.
و) رامنوليپيد: يك هموليزين مقاوم به حرارت است كه باعث از بين رفتن لكتين موجود درسطح بافتهاي بدن ميشود. اين هموليزين منجر به مهار فعاليت مژههاي دستگاه تنفسي ميشود. سودوموناس آئروژينوزا دو نوع گليكوليپيد كه مشابه مواد دترجنت هستند را با نام رامنوليپيد توليد ميكند. مونو رامنوليپيد، رامنوزي است كه به ديمر بتا- هيدروكسي دكانوئيك اسيد متصل ميشود و دي رامنوليپيد يك دايمر رامنوز است كه به ديمر بتا- هيدروكسي دكانوئيك اسيد متصل ميشود. رامنوليپيد موجب ترشح موسين ميشود و همچنين سبب از بين رفتن ماكروفاژهاي مشتق شده در منوسيتها، ممانعت از فعاليت فاگوسيتي ماكروفاژها و موجب اختلال يون در سلولهاي اپيتليال ميشود.
ز) فسفوليپاز C: در مقابل حرارت ناپايدار است. دو نوع فسفوليپاز (PLC) توسط سودوموناس آئروژينوزا توليد ميشود؛ فسفوليپاز با وزن مولكولي بالا كه هموليتيك است (PLC-H)، در حالي كه فسفوليپاز با وزن مولكولي پايين غير هموليتيك (PLC-N) ميباشد. باعث تجزيه سولفيدريل كولين ميشود كه موجب آزاد شدن ديآسيل گليسرول و كولين ميشود كه اين مواد باعث اتلاكتازي، تحريك بيشتر توليد PLC-H و در نهايت موجب تشكيل محصولات متابوليسم آراشيدونات ميشوند. همچنين باعث توليد محافظت كننده اسموتيك ميشوند كه باكتري را از فشار بالاي اسموتيك در ريه اين بيماران محافظت ميكند. اين آنزيم با شكستن ليپيدها و لسيتين انهدام بافتي را تسهيل ميكند.
ح) سيتوتوكسين: توانايي كشتن لكوسيتهاي پليمرفونوكلئر را داراست. به غشاي سلولهاي ميزبان متصل شده و موجب بيثباتي قوام غشايي ميگردد.
ط) كپسول: سودوموناس آئروژينوزا كپسول پليساكاريدي توليد ميكند (غالباً به عنوان اگزوپليساكاريد موكوئيدي، لايه آلژينات يا گليكوكاليس شناخته شده) كه چندين نقش دارد. اين لايه پليساكاريدي به عنوان لنگر باكتري به سلول اپيتليال و موسين ترانكوبرونشيال است. كپسول باعث حفاظت باكتري در برابر فاگوسيتوز شده و خاصيت ضد آنتيبيوتيكي مثل آمينوگليكوزيد دارد. 80% بيماراني كه دچار فيبروز سيستيك هستند به علت سويههاي سودوموناس آئروژينوزاي توليد كننده آلژينات به طرف عفونتهاي تنفسي پيشرفت ميكنند. سيگنالهاي تنظيمي مهم براي سنتز آلژينات NaCl، KCl و عوامل خشك كننده هستند.
ساير فاكتورهاي بيماريزايي:
لكتين PA-1 قادر به كشتن يا جلوگيري از رشد سلولهاي اپيتليال دستگاه تنفسي است. پيگمانهاي فنازين (فنل پيوسيانين) ميتوانند به عنوان عوامل بازدارنده رشد مژهها، احياي آهن سه ظرفيتي به آهن دو ظرفيتي، جلوگيري از پاسخ بلاستوژنيك سلولهاي T به ميتوژن و آنتيژنهاي اختصاصي عمل ميكنند.
- فاكتورهاي ميزبان درگير در بيماريزايي عفونتهاي سودوموناس آئروژينوزا:
الف) كراتيت: زماني رخ ميدهد كه سودوموناس آئروژينوزا از طريق ضربه به چشم، عفونتهاي هرپس سيمپلكس يا استفاده طولاني مدت از لنزهاي تماسي نرم، كلونيزه شود. باكتري ممكن است از طريق محلولهاي شستشوي آلوده به داخل چشم وارد شود.
ب) عفونتهاي ريوي در بيماران فيبروز سيستيك (FC): بيماراني كه از كاهش عملكرد ريه براي مدت سه سال يا بيشتر رنج ميبرند، به طرف عفونتهاي دورهاي سودوموناس آئروژينوزا كه از 6 ماه تا 2 سال به طول ميانجامد، سير ميكنند و همين دليل باعث بوجود آمدن عفونتهاي مزمن تنفسي با سويههاي موكوئيد سودوموناس آئروژينوزا ميشود.
آسيب تنفسي كه به علت عفونتهاي استافيلوكوك اورئوس و هموفيلوس آنفلوانزا ايجاد ميشود موجب در معرض قرار گرفتن گيرندههاي گانگليوزيدي براي ادهسينهاي سودوموناس ميشود. ريهها نه تنها از طريق توليدات سودوموناس آئروژينوزا، بلكه بوسيله فاكتورهاي ميزبان نيز آسيب ميبينند. به نظر ميرسد كه واكنش ازدياد حساسيت نوع سوم به عنوان يك فاكتور محوري در صدمه ريوي مطرح ميشود.
ج) نكروز بافتي و سپسيس در بيماراني كه دچار سوختگي هستند:
تحقيقات نشان ميدهد كه وجود سودوموناس آئروژينوزا توليد كننده پروتئاز قادر خواهد بود كه فعاليت پروتئوليتيكي را در بافت افزايش دهد. عفونتهاي سودوموناس آئروژينوزا در بيماراني كه دچار سوختگي شدهاند تنها زماني كشنده خواهد بود كه اين بيماران با سويههاي توليد كننده مقادير زياد پروتئاز آلوده شده باشند. اگزوآنزيم S هم در ايجاد عفونتهاي سوختگي دخالت دارد.
بورخلدريا سودومالئي:
بورخلدرا سودومالئي تركيب سمي درمونكروتيك كه براي موش كشنده است را توليد ميكند. اين باكتري داراي يك ليپوپليساكاريد اندوتوكسيك است و همچنين پروتئاز، ليپاز، PLC و هموليزين توليد ميكند ولي الاستاز توليد نميكند.
اين باكتري مولد توكسيني ميباشد كه شامل عامل كشنده با فعاليت ضد انعقادي و يك عامل پروتئوليتيك نكروز دهنده پوست است. توكسين كشنده يك زنجير پليپپتيدي ميباشد كه قادر است با يك مكانيسم مشابه توكسين ديفتري و اگزوتوكسين A سودوموناس آئروژينوزا، سنتز پروتئين و DNA را در ماكروفاژها مهار كند. اين ارگانيسم ميتواند بطور درون سلولي در گلبولهاي سفيد تك هستهاي و پليمورفونوكلئر زنده مانده و تكثير كند.
بورخلدريا سپاسيا:
در صاف شدههاي كشت بورخلدريا سپاسيا يك پروتئاز خارج سلولي جداسازي شده است كه خصوصياتي مشابه با آنزيم الاستاز در سودوموناس آئروژينوزا دارد. همانند ساير عفونتهاي ريوي، عفونت بورخلدريا سپاسيا سطح ويرولانس پاييني داشته و منجر به مرگ نميشود.
سندرمهاي كلينيكي:
سودوموناس آئروژينوزا:
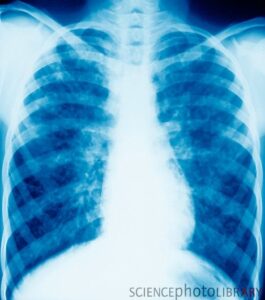
سودوموناس آئروژينوزا يك پاتوژن متحرك است كه با طيف وسيعي از عفونتها در انسان ارتباط دارد. عفونتهاي سودوموناس آئروژينوزا در دستگاه تنفسي تحتاني ميتواند كلونيزاسيون بدون علامت يا تراكئوبرونشيت خوشخيم تا برونكوپنوموني نكروز دهنده شديد را در بر گيرد. كلونيزه شدن باكتري در مبتلايان به FC با بيماريهاي زمينهاي مثل بيماريهاي تهاجمي پارانشيم ريه همراه است.
شرايطي كه بيماران داراي نقص ايمني را مستعد عفونت با سودوموناس ميكند:
- درمان قبلي با آنتيبيوتيكهاي وسيعالطيف كه باعث اختلال در جمعيت باكتريهاي نرمال و حفاظتي ميشود.
- استفاده از تجهيزات درماني تنفسي كه ممكن است باعث عرضه باكتري به مجاري تنفسي تحتاني شود. بيماري تهاجمي در اين گروه با برونكوپنوموني دو طرفه منتشر همراه با آبسههاي كوچك و نكروز بافتي مشخص ميشود. سودوموناس آئروژينوزا عامل غير عادي پنوموني اكتسابي از جمع (Community-Acquired Pneumonia)، اما يك عامل عادي پنوموني اكتسابي از بيمارستان است.
پنوموني ناشي از سودوموناس آئروژينوزا در چندين مورد اتفاق ميافتد:
- معمولاً در بيماران با بيماري مزمن ريه
- معمولاً در ICU اتفاق ميافتد.
- معمولاً در ميزبان نوتروپني اتفاق ميافتد.
1- پنوموني بدون باكتريمي: معمولاً زماني كسب ميشود كه بيماران دچار بيماري مزمن ريوي يا دچار نقص ايمني در عملكرد قلب باشند و توسط تجهيزات تهويه و نيبوليزرهاي آلوده شده تحت درمان قرار گيرند. اين بيماران از يك برونكوپنوموني شديد همراه با تب، ديسپنه، خلط چركي فراوان، سيانوز، ترشحات پرده جنب، ميكرو آبسهها و خونريزيهاي كانوني رنج ميبرند. 2- پنوموني همراه با باكتريمي اوليه: اين بيماري اغلب در بيماراني كه مبتلا به سرطان و نوتروپني هستند ديده ميشود.
در ريه اين بيماران زخمهاي نكروتيك توسعه مييابد. 3- عفونتهاي مزمن تنفسي: اين بيماري در بيماران سالخوردهاي كه به FC مبتلا هستند رخ ميدهد. بيماران چركي شدن مزمن و كنده شدن موكوس مسير تنفسي، برونكواكتازي، آتلكتازي و فيبروزيس را بروز ميدهند. اين بيماران از تنفس سريع، خسخس سينه، سرفه همراه با خلط، كاهش در اشتها و وزن رنج ميبرند.
2- عفونتهاي بافت نرم و پوست: عفونت زخمهاي حاصل از سوختگي بيشترين مورد مشاهده شده محسوب ميشود. كلونيزه شدن آئروژينوزا در زخمهاي سوختگي با آسيب عروق محلي، نكروز بافتي و باكتريمي دنبال ميشود و تا غلظت بيش از 10 به توان 5 باكتري به ازاي هر گرم بافت رشد ميكنند. بيمار بيقراري، تب يا كاهش درجه حرارت بدن، درد شكم همراه استفراغ و اسهال و لكوپني را بروز ميدهد. به محض اينكه عفونت نكروتيك تثبيت شد سودوموناسها ميتوانند به سرعت در خون انتشار يابند و موجب سپسيس برقآسا شوند.
از عفونتهاي شايع ديگر كه توسط سودوموناس در نتيجه شناور شدن آبهاي آلوده رخ ميدهند، فوليكوليت ميباشد. عفونت ثانويه سودوموناس آئروژينوزا در مبتلايان به آكنه و كساني كه موي پاي خود را ميكنند روي ميدهد. همچنين سودوموناس آئروژينوزا در افرادي كه دستهايشان تماس مداوم با آب دارد منجر به بروز عفونتهاي ناخن ميشود.
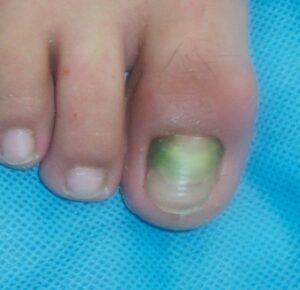
سودوموناس آئروژينوزا ميتواند باعث درماتيت وان گرم در افرادي باشد كه از وانهاي آلوده شده به باكتري استفاده ميكنند، همچنين اين باكتري مي تواند موجب بيماري پاي گنديده حارهاي در بيماراني شود كه به بيماري قارچي پاي ورزشكاران مبتلا هستند. سندرم ناخن سبز مشكي به علت التهاب اطراف ناخن است كه توسط اين باكتري ايجاد ميشود. استفاده از كيسههاي آب گرم عاملي براي افزايش عفونتهاي پوستي سودوموناس آئروژينوزا است.
3- عفونت دستگاه ادراري: سويههاي اشريشيا كولي، انتروكوكوس و سودوموناس آئروژينوزا عامل شايع عفونتهاي دستگاه ادراري بيمارستاني هستند. عفونت دستگاه ادراري بطور اوليه در بيماراني كه كاتترهاي ادراري دارند ديده ميشود.
بطور معمول اين بيماران تحت درمان چند آنتيبيوتيكي هستند كه باعث گزينش گونههاي سودوموناس مقاوم به آنتيبيوتيك ميشود.
پيلونفريت يك عارضه شايع عفونتهاي بالا رونده ميباشد. شرايط زمينهاي ميزبان كه ممكن است به استفاده طولاني سوند ادراري نياز داشته باشد از بهبودي عفونتها ممانعت ميكند.
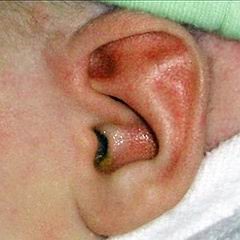
4- عفونت گوش: عفونت گوش خارجي به وفور توسط سودوموناس آئروژينوزا در شناگران (گوش شناگران) به عنوان يك ريسك فاكتور مهم روي ميدهد. عفونت بدخيم گوش خارجي حالت شديد بيماري است كه در افراد ديابتيك و افراد مسن ديده ميشود. اين عفونت ميتواند بافتهاي زيرين را مورد تهاجم قرار داده و باعث آسيب اعصاب و استخوان جمجمه شود.
تظاهرات تيپيك شامل كانال گوش متورم و حساس بوده و با تخليه چرك و گرانوله شدن ابتدا و انتهاي ديواره كانال همراه است. گاهي اوقات بيماران از تريسموس (گرفتگي) و كاهش شنوايي شكايت دارند و نيز ممكن است سپسيس رخ دهد. درجه مرگ و ميري حدود 20-15% در بيماران درمان شده گزارش شده است. سودوموناس آئروژينوزا ممكن است عامل عفونت گوش مياني در نوزادان تازه متولد شده باشد. همچنين اين باكتري شايعترين عامل عفونتهاي مزمن چركي گوش مياني در كودكان و بالغين است.
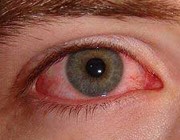
5- عفونت چشم: عفونتهاي چشم در پي تروماي اوليه در قرنيه چشم رخ ميدهند (خراشيدگي ناشي از زخم روي سطح چشم) و سپس نسبت به ورود سودوموناس آئروژينوزا از آب آلوده آسيب پذير ميشوند. زخمهاي قرنيه توسعه يافته و ميتوانند به سوي بيماريهاي وخيمتر چشمي پيش رود.
لايه اپيدرم و استروما نكروز شده و در زخم، ترشحات چركي جمع ميشود. ممكن است چشم سرشار از چرك شود (هايپوپيون) و عملكرد آن به سرعت از بين برود.
6- باكتريمي: در حالي كه اشريشيا كولي، كلبسيلا و انتروباكتر سه عامل مهم باكتريمي كسب شده بيمارستاني اوليه هستند، سودوموناس آئروژينوزا در مقام چهارم قرار دارد. باكتريمي اغلب موارد در بيماران مبتلا به نوتروپني، ديابت، سوختگيهاي وسيع و بدخيميهاي هماتولوژيك رخ ميدهد. بيشتر موارد باكتريمي سودوموناسي از عفونت دستگاه تنفسي تحتاني، دستگاه ادراري، پوست و بافتهاي نرم مخصوصاً زخمهاي سوختگي منشأ ميگيرد.
زخمهاي مشخص پوستي بنام اكتيماگانگروزوم در تعداد كمي از بيماران توسعه مييابد. بيماراني كه دچار باكتريمي ناشي از سودوموناسها هستند از يك سپسيس تيپيك گرم منفي رنج ميبرند. بطور معمول اين بيماران تب، افزايش ضربان قلب، به شدت نفس زدن، اشكال در تنفس، كاهش فشار خون و ازوتمي را بروز ميدهند. ممكن است سپسيس منجر به شوك مهار نشدني و انسداد كليوي شود.
7- اندوكارديت: سودوموناس آئروژينوزا مسئول دو سوم از تمام موارد اندوكارديتهاي عفوني است. اندوكارديت سودوموناسي به وفور در موارد استعمال نادرست داروهاي داخل وريدي مشاهده ميشود. دريچه سه لختي قلب اغلب درگير شده و بيماري سير مزمن دارد.
اندوكارديت يكي از عوارض باكتريمي است كه با بيشترين شيوع در مصرف كنندگان مواد مخدر داخل وريدي ديده ميشود. بيماراني كه دچار اندوكارديت تحت حاد دريچه سه لختي هستند از تب، مورمور شدن و آمبولي پنومونيايي سپتيك رنج ميبرند. اين آمبولي بطور معمول با سرفه پروداكتيو، ترشحات پرده جنب و انفيلتراسيون ريوي همراه است. بيماراني كه دچار اندوكارديت حاد دريچه دو لختي يا آئورت هستند ممكن است از نقص انسدادي قلب و آمبولي آرتريال سيستميك رنج ببرند.
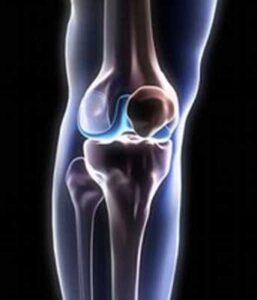
8- عفونت استخوان و مفصل: ممكن است كه استخوانها و مفاصل بيماران به وسيله سودوموناس آئروژينوزا از طريق انتشار خوني باكتري از جايگاه عفونت اوليه يا از طريق انتشار مستقيم عفونت از قسمتهاي مجاور آلوده شوند. افرادي كه براي انتشار عفونت مستقيم در معرض خطر قرار دارند شامل بيماران با زخمهاي باز و بيماران با سلوليت هستند. گاهي درد در اين مكانها با تب و كاهش تحرك همراه ميشود.
9- عفونت سيستم اعصاب مركزي: سودوموناس آئروژينوزا موجب مننژيت و آبسههاي مغزي در بيماراني ميشود كه داراي نقص ايمونولوژيكي زمينهاي يا ضربه مغزي هستند. ممكن است كه باكتري از طريق ضربه، انتشار خوني يا انتشار مستقيم از يك عفونت مزمن گوش يا سينوس به درون سيستم اعصاب مركزي وارد شود. مننژيت ناشي از اين باكتري اغلب در بيماران سرطاني رخ ميدهد و معمولاً با تب، سردرد، خشكي گردن، گيجي و ساير علائم نورولوژيكي مننژيت همراه است.
10- عفونت دستگاه گوارشي: در درجه اول در نوزادان تازه متولد شده و بيماراني كه دچار نقص سيستم ايمني هستند رخ ميدهد. بيماري در برخي از نوزادان تازه متولد شده به طرف انتروكوليت گسترش مييابد. بيماري در بيماران نوتروپني كه به انتروكوليت مبتلا هستند به طرف زخمهاي نكروتيك و خونريزي دهنده در لايه مخاطي روده توسعه مييابد.
11- عفونتهاي عمومي: ناشي از انتقال عفونت زخمها به وسيله جريان خون است و هنگامي كه عروق و بافتها مورد تهاجم قرار ميگيرند منجر به نوتروپني ميشود.
12- بيماريزايي در حيوانات: سودوموناس آئروژينوزا از تورم پستان در گاو جدا شده است و علت آن را تزريق مواد آلوده داخل پستاني ذكر كردهاند. دام مبتلا به علت اندوتوكسمي تلف ميگردد. عفونتهاي رحمي ناشي از اين باكتري ممكن است منجر به عقيمي شود. مواردي از سقط جنينهاي تك گير ناشي از اين باكتري گزارش شده است.
در گوسفندان علاوه بر تورم پستان و پنوموني بيماري، بيماري گنديدگي پشم (Fleece-rot) يا پشم سبز (green wool) نيز حائز اهميت است. گنديدگي پشم متعاقب رشد باكتري در پشم گوسفنداني كه در معرض رطوبت طولاني مدت قرار ميگيرند بروز ميكند. در اسب علاوه بر تورم رحم و آبسههاي ريوي، عفونت چشم معمول است.
بورخلدريا سودومالئي:
بورخلدريا سودومالئي عامل بيماري مليوئيدوز يا شبه مشمشه است.
ابتلا به بيماري ممكن است در يكي از چهار شكل حاد، تحت حاد، مزمن و يا نهفته بروز كند.
در شكل حاد، سپتيسمي و همراهي با تشكيل آبسه تقريباً در هر يك از اندامهاي بدن اتفاق ميافتد.
شكل تحت حاد بيماري توسط طولانيتر بودن دوره علامتدار، تشكيل آبسه در اندامهاي مختلف، باكتريمي ملايمتر و پنوموني مشخص ميشود. شكل مزمن بيماري علائم ريوي خفيفي دارد.
شواهد سرولوژيك نشان ميدهد كه در نواحي اندميك و در 30% از جمعيت بالغين، آنتيبادي ضد بورخلدريا سودومالئي وجود دارد. اين آنتيباديها نمايشگر ابتلا به عفونت نهفته و يا بدون علامت هستند. هر دو شكلهاي مزمن و نهفته ممكن است بعد از چندين سال به شكل علامتدار بيماري تغيير يابند. اين رفتار بيماري موجب شده است تا به آن بمب ساعتي ويتنام لقب داده شود، زيرا افرادي كه در ويتنام از عفونت مزمن تنفسي و بدون علامت رنج ميبرند چندين سال پس از يك عفونت بورخلدريا سودومالئي، ناگهان سپتيسمي كشندهاي را بروز ميدهند.
دوره كمون بيماري ميتواند كوتاه تا حدود 2 تا 3 روز و يا طولانيتر باشد، ولي ممكن است عفونت نهفته ماهها تا سالها طول بكشد. عفونت چركي موضعي در مكان ورود باكتري در خراش پوستي مشاهده ميشود.
شايعترين شكل مليوئيدوز، عفونتهاي ريوي بوده كه ممكن است بصورت پنومونيت اوليه باشد. در بيمار ممكن است تب و لوكوسيتوز همراه با سفت شدن لوب فوقاني ريه ظاهر شود. ضايعات مشخص بيماري حضور ندولهاي پنيري ميباشد. ندولها ممكن است به هم بپيوندند و يك ناحيه وسيع را فراگيرند يا امكان دارد تبديل به آبسه شوند. ندولها و آبسههاي چندگانه در اغلب اندامها از جمله عقدههاي لنفاوي، طحال، ريه، كبد، مفاصل و حفره بيني تشكيل ميشوند. در گوسفند اين آبسهها حاوي چرك سبز و ضخيم پنيري است.
اگر شرايط ضعيف شدن يا سركوب ايمني مانند ديابت مليتوس و سيروز كبدي باشد، يك حمله كشنده مليوئيدوز حاد ميتواند براي اين افراد مهلك باشد.
بورخلدريا مالئي:
يك بيماريزاي اختصاصي حيوانات است كه عامل بيماري مشمشه يا گلاندرز (Glandrrs) در اسب و الاغ ميباشد. انسان از طريق تماس مستقيم و يا از وراي خراشهاي پوستي و استنشاق ارگانيسم، آلوده ميشود.
نامهاي ديگر مشمشه كه كمتر شناخته شدهاند equinia، malleus و droes ميباشد.
اين بيماري در اسب با گرفتار شدن واضح ريه، لزيونهاي زخمي زير پوستي و ضخيم شدن لنفاتيكها همراه ايجاد ندول بروز ميكند. بيماري سيستميك هم گاهي ديده ميشود.
الاغ به فرم حاد، قاطر بيشتر به فرم تحت حاد و اسب بيشتر به فرم مزمن دچار ميگردند.
عفونت انساني معمولاً با يك زخم پوستي يا غشايي و گاه پنوموني آغاز ميشود و به لنفانژيت و سپتيسمي ميانجامد.
اشكال بيماري در تك سميان:
شكل سپتيسميك:
با تب، تراوشات موكوسي و چركي از بيني و علائم تنفسي همراه، و كشنده است.
اشكال مزمن بيماري:
فرم بينياي Nasal: با ندولهاي اولسراتيو روي مخاط تيغههاي مياني بيني و پايينتر از بوقكهاي بيني، تراوشات چركي خونآلود از بيني، لنفادنوپاتي موضعي، زخم در بيني و بافتهاي اسكار ستارهاي شكل پس از بهبود همراه است.
فرم تنفسي يا ششي Pulmonary: با آسيبهاي شبه سلي همراه است.
فرم پوستي Cutanous: اين فرم از بيماري سراجه يا Farcy ناميده ميشود و با لنفانژيت و پيدايش ندول در طول رگهاي لنفاوي اندامهاي حركتي، زخم شدن ندولها و خروج چرك متمايل به زرد زعفراني شناخته ميشود.
اين بيماري به آساني به انسان قابل سرايت ميباشد و 95% منجر به مرگ ميشود. بيماري در اسب مزمن و تحليل برنده است و واكنش ازدياد حساسيت در بدن پديد ميآورد كه براي آزمايش، مالئين مورد استفاده قرار ميگيرد.
سراجه فرم جلدي مشمشه است و قبل از سال 1882 بر اين باور بودند كه جدا از بيماري اسب است. روند بيماري در سراجه يا فارسي به اين صورت است كه بعد از بروز عفونت، باكتري به مخاط ناحيه بيني- حلقي و روده نفوذ ميكند و وارد جريان لنف موضعي ميگردد و از آنجا در قسمتهاي مختلف بدن موضع ميگيرد. ندولها ممكن است در كانالهاي لنفي تشكيل و سپس ضخيم گردند.
ندولهاي متورم زخم ميشوند و از آنها ترشحات چركي زرد رنگ عسل مانند خارج ميگردد كه حاوي سودوموناس مالئي است. به عبارتي ديگر در اين فرم، آبسه ندولار (Farcy pipes) و تراوش چرك ژلاتيني زرد- سبز شاخص بيماري است. بعد از پخش باكتري از طريق جريان لنفي، باكتري وارد جريان خون شده و در ريهها جاي ميگيرد.
علت مرگ ببر مازندران در پارك ارم تهران شيوع بيماري مشمشه در باغ وحش ارم اعلام شده است.
بورخلدريا سپاسيا:
عفونتهاي حاصل از اين ارگانيسم شامل:
1- عفونتهاي تنفسي در مبتلايان به FC يا بيماريهاي گرانولوماتوز مزمن 2- عفونت دستگاه ادراري در بيماران استفاده كننده از كاتتر و سپتيسمي خصوصاً در بيماراني كه از كاتترهاي آلوده درون رگي استفاده ميكنند.
بيشترين موارد عفونتها در بيماراني اتفاق ميافتد كه ضعيف باشند و نقص ايمني داشته باشند. شدت بيماري زمينهاي، مصرف آنتيبيوتيكهاي آمينوگليكوزيدي و داشتن برادر يا خواهر مبتلا يه FC، فاكتورهاي خطر براي لانه گزيني و تكثير بورخلدريا مالئي هستند.
همچنين باعث ايجاد سندرم سپاسيه، كونژونكتويت، اندوكاديت، گنديدگي جنگل (عفونت پا) و مننژيت نوزادان ميشود.
استنوترفوموناس (گزانتوموناس) مالتوفيليا:
طيف عفونتهاي بيمارستاني حاصل از اين ارگانيسم وسيع بوده و شامل باكتريمي، پنوموني، مننژيت، عفونتهاي زخمي و عفونتهاي مجاري ادراري ميباشد.
تشخيص آزمايشگاهي:
سودومونا آئروژينوزا:
نمونهها از ترشحات زخمهاي عفوني، چرك، ادرار، خون، مايع نخاعي، خلط و مواد ديگري ميباشند.
باسيلهاي گرم منفي را اغلب ميتوان در نمونههاي رنگ آميزي شده مشاهده كرد. مورفولوژي كلني به همراه نتايج تستهاي سريع بيوشيميايي براي تشخيص اوليه بكار ميرود؛ به عنوان مثال سودوموناس آئروژينوزا رشد ميكند و هموليز بتا و كلنيهاي مسطح با لبههاي منتشر به همراه پيگمان ناشي از پيوسيانين آبي و فلورسين (زرد) داشته و اكسيداز مثبت است و داراي بوي شيريني شبيه به انگور ميباشد.
نمونه را روي بلاد آگار يا مككانكي آگار و محيطهاي كشت افتراقي كه اغلب جهت كشت باسيلهاي گرم منفي رودهاي استفاده ميشود، كشت ميدهند.
سودوموناس لاكتوز را تخمير نكرده و به آساني از باكتريهايي كه لاكتوز را تخمير نميكنند قابل شناسايي است.
سودوموناس در محيط PPLO رشد ميكند و رنگ سبز مايل به آبي توليد ميكند. در محيط سه قندي آهندارTriples Suger Iron Agar (TSI) بدون واكنش است. سودوموناس آئروژينوزا به سيتريميد مقاوم است و در حضور آن رشد ميكند و كشت در محيط داراي سيتريميدو اسيد ناليديكسيك ميتواند براي تشخيص نمونهها مورد استفاده قرار گيرد.
در محيط كشت CHROMagar pseudomonas كلني سبز- آبي مشخصه سودوموناس است.
محيط سيتريمايد آگار: كلني درشت كه حاشيه آن كمرنگ تر از وسط آن بوده و نقطه سياه در وسط كلني نشانه اكسيداز مثبت بودن آن است.
محيط TSI: به علت غير تخميري بودن آن در اين محيط بدون واكنش است. اين محيط داراي سه قند گلوكز (1%)، لاكتوز و سوكروز (هر كدام 1%)، پپتون (2%)، تيوسولفات سديم، سيترات آمونيوم فريك و فنلرد است (با تخمير گلوكز قسمت عمق و با تخمير لاكتوز سطح محيط زرد رنگ ميشود).
در آزمايش احياي نيترات سودوموناس آئروژينوزا نيترات را احيا نميكند.
در آزمايش استفاده از سيترات، سودوموناس سيترات مثبت است
بورخلدريا سودومالئي:
زماني به مليوئيدوز مشكوك ميشويم كه بيمار نشانههاي باليني، تاريخچه بيماري و آنتيبيوتيكهاي ضد اين باكتري را دارا باشد. نمونههاي ترشحات و گرانولوما بايد رنگ آميزي شوند و به منظور حضور باسيلهاي گرم منفي كه سنجاق سري شكل هستند مورد بررسي قرار گيرند. با وجود آزمايشهاي سرم شناسي، هماگلوتيناسيون غير مستقيم IHA و تثبيت عامل كمپلمان CFT، تشخيص بيماري مليوئيدوز بر اساس جداسازي باكتري و تزريق به خوكچه هندي نر (واكنش اشتراس) است.
آزمايش پادتن درخشان براي نشان دادن باكتري در گسترش بافتي سودمند است. براي تشخيص سريع ميتوان از روش آنتيبادي ايمونوفلوئورسانس، الايزا، آگلوتيناسيون لاتكس و PCR كمك گرفت. در بررسيهاي سرمي بايستي افزايش تيتر را مد نظر قرار داد.
تشخيص قطعي مليوئيدوز بر جداسازي باكتري از مايعات بدن، خون، ادرار و خلط استوار است.
در شرايط هوازي در 37 درجه سانتيگراد به مدت 48-24 ساعت به خوبي بر روي نوترينت آگار، آگار خوندار يا مككانكي (با اكسيداسيون لاكتوز) رشد ميكند و مورفولوژي پرگنهها از صاف و موكوئيدي تا خشن متفاوت است كه با گذشت زمان قهوهاي مايل به زرد ميشود و بوي خاص كهنگي و كپك ميدهد. باكتري در 42 درجه سانتيگراد نيز رشد ميكند. باكتري گلوكز را در محيـــــــــــــــــــــط Hughand Leison Medium اكسيده ميكند و آرژنين را به آمونياك احيا ميكند. نشاسته، ژلاتين و توئين 80 را نيز ميشكند. در پي رنگ آميزي با متيلنبلو يا رايت از كشتهاي تازه، باكتري به شكل دوقطبي سنجاق سري ديده ميشود.
بورخلدريا مالئي:
تشخيص بيماري ممكن است با روشهاي جداسازي عامل بيماري، تزريق به حيوان آزمايشگاهي حساس (خوكچه هندي) و يا آزمايشهاي سرم شناسي و آزمايش مالئين صورت گيرد.
- جداسازي بورخلدريا مالئي: نمونه برداري جهت كشت بهتر است از قسمتهايي از اعضايي كه هنوز باز نشده و آلوده نيست صورت گيرد. بورخلدريا مالئي به آساني در محيط غني از گليسرول رشد ميكند. اين باكتري هوازي است و بهترين درجه حرارت رشد 37 درجه سانتيگراد است.
- تزريق به خوكچه هندي: مواد آلوده مشكوك به اين باكتري را ميتوان در داخل صفاق خوكچه هندي تزريق كرد. خوكچه آلوده به شدت دچار پريتونيت و تورم پردههاي بيضه ميگردد. بروز اين نشانهها به فاصله 3-2 روز بعد از تزريق را نشانه اشتراس (straus reaction) مينامند. بورخلدريا مالئي از موارد مترشحه از ضايعات بصورت خالص جدا ميگردد.
- آزمايشهاي سرم شناسي: در بيماري مشمشه هر دو نوع ايمني هومورال وابسته به سلول در دفاع در برابر اين باكتري فعال ميشود. مشخص شده است كه چهار نوع آزمايش سرم شناسي جهت تشخيص بيماري مفيد و قابل استفاده ميباشد:
الف) تثبيت عناصر مكمل CF-T: سرم دام مبتلا پس از يك هفته از ابتلاي آن قابل آزمايش ميباشد و تا مدتهاي طولاني در اشكال مزمن بيماري همچنان سرم مثبت باقي ميماند. عيار يك بيستم به عنوان مورد مشكوك و عيار يك چهلم به عنوان مثبت تلقي ميشود.
ب) آزمايش آگلوتيناسيون: اين روش يك اشكال دارد آن هم اينكه در موارد مزمن بيماري اسبهاي مبتلا معمولاً نتيجه منفي ميدهد.
ج) هماگلوتيناسيون غير مستقيم: عيار بالاتر از يك صد و شصتم به عنوان مورد مثبت تلقي ميگردد.
د) ايمونو الكتروفورز معكوس (CIEP): اين روش سادهترين روش با سريعترين و اقتصاديترين آزمايش تشخيصي براي تعداد زيادي نمونه سرم است.
- آزمايشهاي مالئين: اساس آزمايشهاي مالئين نشان دادن ازدياد حساسيت ناشي از عفونت با بورخلدريا مالئي است. مالئين گليكوپروتئيني است كه از اين باكتري استخراج ميشود. استفاده از مالئين جهت انجام آزمايش ازدياد حساسيت به سه روش انجام ميگيرد:
الف) زير جلدي: در موارد مثبت افزايش درجه حرارت و تورم سخت و دردناك در محل تزريق به فاصله 24 ساعت پس از تزريق ايجاد ميشود. ميزان تزريق مالئين 5 /2 ميليليتر است.
ب) آزمايش چشمي: با تجويز چند قطره مالئين در گوشه چشم دام، در صورت آلودگي، آماس و واكنش چركي در چشم به فاصله 12-6 ساعت مشاهده ميگردد.
ج) آزمايش داخل پلك: 0/1 ميليليتر از مالئين را در داخل پلك پايين دام مورد نظر تزريق كرده، پس از 48-24 ساعت نتيجه آزمايش قرائت ميشود. در صورتي كه تورم قابل ملاحظهاي در پلك چشم مشاهده شود دليل بر مثبت بودن آزمايش خواهد بود.
درمان
سودوموناس آئروژينوزا:
درمان عفونتهاي ناشي از سودوموناس آئروژينوزا مشكل است زيرا كه اين باكتري بطور معمول به داروهاي متعددي مقاوم است و همچنين برخي از سويهها سفالوسپورينازها را توليد ميكنند كه ميتوانند سفالوسپورينهاي نسل سوم را تجزيه كنند. به درمان تركيبي و يك عامل بتالاكتام ضد سودوموناسي نياز است تا زماني كه ميزان قابليتهاي دارو تعيين شود.
ارگانيسمهاي حساس ممكن است در طي درمان آنتيبيوتيكي با توليد آنزيمهاي خنثي كننده فعاليت آنتيبيوتيك و يا با انتقال پلاسميدهاي مقاومت از سويههاي حساس و يا با موتاسيون در ژن كد كننده پورينهاي منافذ غشاي خارجي مقاوم شوند. انتقال ايمونوگلوبولين و گرانولوسيت به منظور بهبود سيستم ايمني ميتواند در بيماران مبتلا به عفونت سودوموناسي و داراي نقص ايمني مفيد واقع شود.
براي درمان معمولاً يكي از انواع پنيسيلينهاي فعال عليه سودوموناس نظير تيكارسيلين يا پيپراسيلين همراه با يك آمينوگليكوزيد نظير توبرامايسين تجويز ميگردد. كوئينولونها و كارباپنمها دو نوع از آنتيبيوتيكهاي جديد با فعاليت ضد سودوموناسي هستند. سيپروفلوكساسين مثالي از يك كوئينولون با فعالين خوب ضد سودوموناسي است.
در موارد سوختگي، كاربرد موضعي كرم سولفامايلون، كرم سيلور سولفاديازين و يا محلول شستشوي نيترات نقره پذيرفته شدهترين شكل درمان است. در بيماران سرطاني، درمان ايمونولوژيك در شكل گاماگلوبولين هيپرايميون و ترانسفورماسيون گرانولوسيت با موفقيت همراه بوده است.
سفتازيديم در درمان اوليه عفونتهاي سودوموناس آئروژينوزا به كار ميرود.
از عصاره سير در درمان عفونت سوختگي ناشي از سودوموناس آئروژينوزا ميتوان استفاده كرد، همچنين عصاره خام الكلي و آبي اكاليپتوس بخوبي ميتواند از رشد سودوموناس آئروژينوزا جلوگيري كند.
عصاره Ruta graveolens (روتا گراوئولنس) بر سودوموناس آئروژنزا اثر ضد ميكروبي دارد.
عسل طبيعي داراي اثرات ضد ميكروبي روي سودوموناس آئروژينوزا است و با توجه به مقاومت اين باكتري نسبت به طيف وسيعي از آنتيبيوتيكها ميتواند به عنوان جايگزين آنتيبيوتيك قرار گيرد.
بورخلدريا سودومالئي:
سولفاديازين تا حدود 50% ميزان مرگ و مير را كاهش ميدهد. درمــــــــان انتخابي بيماري، تريمتوپريم- سولفامتوكسازول و نيز نووبيوسين- تتراسايكلين ميباشد كه براي مدت زمان طولاني تجويز ميشود.
بورخلدريا سودومالئي به كارباپنم، پنيسيلينهاي ضد سودوموناسي (مانند پيپراسيلين، آزوسين) و داكسيسيلين حساس است. معمولاً به انواع مختلفي از آنتيبيوتيكها نظير تتراسايكلين، سولفوناميد، كلرامفنيكل، آموكسيسيلين يا تيكارسيلين همراه با اسيد كلاوولانيك و سفالوسپورينهاي نسل سوم حساس است.
بورخلدريا مالئي:
موارد انساني را ميتوان بطور مؤثر با تتراسايكلين همراه با يك آمينوگليكوزيد درمان كرد.
بورخلدريا مالئي در مقابل سولفوناميدها و تتراسايكلينها حساس است. دوره درمان 20 روز است. سولفاديازين به عنوان داروي انتخابي توصيه شده است.
بورخلدريا سپاسيا:
به لحاظ اينكه بورخلدريا سپاسيا در برابر اغلب آنتيبيوتيكها مقاومت ذاتي دارد لذا درمان عفونتهاي آن مشكل است. سفتازيديم يك آنتيبيوتيك نسل سوم سفالوسپورينها است كه به عنوان يك عامل مؤثر اميدبخش بوده است.
استنوترفوموناس (گزانتوموناس) مالتوفيليا:
تريمتوپريم- سولفامتوكسازول فعالترين دارو عليه اين ارگانيسم بوده و فعاليت خوب در مورد كلرامفنيكل و سفتازيديم، تيكارسيلين و اسيد كلاوولانيك ديده شده است.
كنترل و پيشگيري:
سودوموناس آئروژينوزا:
كوشش براي ريشه كني سودوموناسها از بيمارستانها بيفايده است. استفاده بيرويه آنتيبيوتيكها نيز بايد كنترل شود تا مانع از بين رفتن فلور نرمال و ايجاد سويههاي مقاوم به آنتيبيوتيك شود. پيشگيري مشكل است اما با كنترل بهداشتي و دقيق هوا دهندهها و فيلترها در واحدهاي احتراق، ممنوع كردن مصرف ميوه و سبزيجات خام، استريليزاسيون تجهيزات تنفسي درماني و سرانجام در برخي افراد حساس واكسيناسيون امكان پذير است.
حداقل دو كارخانه مختلف واكسنهايي را از فرآوردههاي ديواره سلولي سودوموناس آئروژينوزا تهيه كردهاند. موفقيت اين واكسنها متناقض بوده است.
واكسنهايي كه از فرآورده خالص شدهتر به همراه اگزوتوكسين ضعيف شده يا توكسوئيد A هستند مقادير بيشتري از آنتيبادي را براي مدتهاي طولانيتر تحريك ميكنند. بقيه محققين واكسنهايي را تكميل كردهاند كه با استفاده از پروتئين F غشاي خارجي، فلاژله و يا گليكوكاليس سودوموناس بوده است. بعضي از محققين اعتقاد دارند كه بجاي واكسينه كردن بيماران به عفونتهاي سودوموناسي، بهتر است از ايمونيزاسيون غير فعال استفاده شود.
در مورد باكتري سودوموناس آئروژينوزا مانند باكتري كزاز ميتوان سم آن را جدا و غير فعال كرد تا از آن در درمان استفاده شود. واكسني به اين منظور ساخته شده است، بنابراين سم اين باكتري را جدا و غير فعال كرده و از خاصيت ايمنيزايي آن ميتوان بهره برد. سم ضعيف شده از اگزوتوكسين A از سوشهاي سمزاي سودوموناس آئروژينوزا تهيه شد و ثابت شد كه از اين واكسن ميتوان در جلوگيري از مرگ افراد در شغلهاي پرخطري كه دچار سوختگي ميشوند استفاده كرد.
بورخلدريا سودومالئي:
بهترين راه كنترل بيماري حذف دامهاي آلوده و ضد عفوني وسائل و محل زندگي دام است.
بورخلدريا مالئي:
اين بيماري با كشتار اسبها و قاطرهاي آلوده پيشگيري شده و امروزه فوقالعاده نادر است. در بعضي كشورها عفونتهاي آزمايشگاهي تنها منبع عفونت هستند.
برنامه كنترل بيماري بايستي بطور كامل اجرا شود:
1) قرنطينه كامل دامهاي آلوده و مشكوك
2) كنترل بهداشت محل پرورش دام
3) كنترل نقل و انتقال دام
4) موارد مشخص بيماري را بايستي از بين برد و دامهاي باقيمانده را به فاصله هر سه هفته تحت آزمايش مالئين قرار داد تا زماني كه راكتورها مشخص و نابود شوند.
كنترل بيولوژيك بوسيله سودوموناسها:
توليد متابوليتهاي ضد ميكروبي توسط ريزوباكترهاي آنتاگونيست به عنوان يك عامل مهم در كاهش بسياري از بيماريهاي ريشه ميباشد. در سالهاي اخير بحث امكان كنترل بيولوژيكي خاكزاد مورد توجه جدي محققين قرار گرفته است كه در اين مورد ميتوان از باكتريهاي آنتاگونيست، بخصوص از باكتريهاي گروه سودوموناسهاي فلورسنس در كنترل بيماريهاي قارچي و باكتريهاي ريشه گياهان زراعي استفاده كرد.
ميكروارگانيسمهايي كه در ناحيه ريزوسفر گياهان زندگي ميكنند گزينه مناسي براي استفاده در روشهاي كنترل بيولوژيكي هستند، زيرا ريزوسفر خط مقدم دفاعي ريشهها عليه بيماريهاي خاكزي ميباشد؛ به عنوان مثال سودوموناسهاي فلورسنــس باعــث ممــانعت از رشـــــــــــــد قارچ Pythium ulimum trow، عامل پوسيدگي بذر لوبيا ميشوند و امكان جوانهزني بذر لوبيا در محيط كشت را موجب ميشوند.
اين توانايي در سودوموناسهاي فلورسنس مربوط به توليد سيانيد هيدروژن، پروتئاز، سيدروفور و تعدادي تركيبات آنتيبيوتيكي ميشود.
در موردي ديگر با تهيه جهش يافتههاي مقاوم به آنتيبيوتيك باكتري سودوموناس فلورسنس، بر خواص آنتاگونيستي باكتري افزوده و باعث ممانعت از رشد قارچRhizoctonia solani ، عامل بيماري مرگ گياهچه پنبه ميشوند.
كاربردهاي صنعتي و بيولوژيك از سودوموناس:
تجزيه علفكش آترازين: تجزيه زيستي آترازين بوسيله باكتريها به عنــوان يكي از روشهاي مهم زيست پالايي مطرح است. باكتريها معمولاً از آترازين به عنوان منبع كربن و نيتروژن استفاده ميكنند. سودوموناس آئروژينوزا و سودوموناس فلورسنس توان تجزيه آترازين را دارند، با اين تفاوت كه حضور نيتروژن عامل محدود كننده در تجزيه آترازين بوسيله سودوموناس فلورسنس است.
افزايش مقدار جذب عناصر غذايي در گندم: مايهزني گندم با سويههاي مختلف سودوموناس فلورسنس موجب بهبود جذب عناصر غذايي توسط گندم ميشود و بيشترين جذب براي عناصر آهن و منگنز گزارش شده است.
تحريك رشد و افزايش تارهاي كشنده ريشه گندم: سودوموناس پوتيدا موجب افزايش عملكرد بسياري از گياهان ميشود. باكتري مذكور قادر به توليد انواع هورمونهاي گياهي (مانند هورمون اكسين) است كه باعث تأثير آنها بر سيستم ريشهاي گياه ميشود. برخي از اين تغييرات شامل افزايش جذب مواد غذايي از طريق تكثير تارهاي كشنده و افزايش ريشههاي جانبي ميباشد.
توسعه كشت جلبك بوسيله باكتري سودوموناس فلورسنس: باكتري سودوموموناس فلورسنس تأثير قوي و مثبتي بر رشد جلبكهاي پرورشي نشان داده است كه اين جلبكها مورد استفاده در آبزي پروري هستند (از قبيل: كتوسروس، اسكلتونما، تتراسلميس و كلرلا) به گونهاي كه ميتوان به تنهايي از سودوموناس فلورسنس در تكثير جلبك استفاده كرد و اين امر يك رهآورد جديد در پرورش جلبك تلقي ميشود.
تجزيه تركيبات آروماتيك سمي و فنل: شناسايي باكتريهاي هوازي تجزيه كننده مواد سمي، گامي مهم در روند تكامل سيستمهاي تصفيه فاضلاب محسوب ميشود.
سودوموناس توانايي تجزيه غلظت 500 ميليگرم بر ليتر فنل در 48 ساعت را دارد.
سودوموناس آئروژينوزا و سودوموناس پوتيدا باعث حذف آلايندهها و رسوبات آلوده نفتي مثل نفتالين ميشوند.
سودوموناس آلكاليژنز، سودوموناس آئروژينوزا، بروانديوموناس وسيكالريس باعث تجزيه فنل در سيستم بيوفيلتر و لجن فعال ميشوند.
همچنين سودوموناس سويه SA.r كه سويه بومي كشف شده توسط پژوهشگر ايراني است، توانايي تجزيه تركيبات آروماتيك مانند فنل در ميزان حدود يك كيلوگرم بر ليتر را دارد.
سولفورزدايي: وجود گوگرد در سوختهاي فسيلي و انتشار دياكسيد گوگرد ناشي از احتراق سوختها، سبب ايجاد مشكلات جدي مثل بارانهاي اسيدي و مسموم شدن آب درياچهها براي محيط زيست شده است. سودوموناس آئروژينوزا سويه PG201 توانايي حذف گوگرد به ميزان 90% را داراست و اين سويه يكي از فراوانترين ميكروارگانيسمهاي موجود در نفت خام است و مقاومت بالايي به فلزات سنگين موجود در نفت خام دارد و از طرفي توانايي توليد بيوسورفاكتانت را داراست.
توليد بيوسورفاكتانت: مهمترين بيوسورفاكتانت توليد شده توسط سودوموناسها، رامنوليپيد است كه توسط سودوموناس آئروژينوزا توليد ميشود و جهت كاربردهاي غذايي، شيميايي، دارويي و بهداشتي از سويه جهش يافته M34 آن استفاده ميشود.
از بيوسورفاكتانتهاي مؤثر ديگر ميتوان به اورنيتين ليپيدها اشاره كرد كه توسط سودوموناس روبسنس توليد ميشود.
سورفاكتانتهاي توليد شده توسط سودوموناس سويه PG-1 باعث افزايش حلاليت هيدروكربنها ميشود و در استخراج نفت كاربرد دارد.
بيوسورفاكتانت توليد شده توسط سودوموناس سويه MEOR171,172 در ونزوئلا در صنعت نفت، در مواد آرايشي، غذا و دارو كاربرد دارد.
سودوموناس آئروژينوزا بيوسورفاكتانتي را توليد ميكند كه باعث حلاليت پروتئينها ميشود.
منابع:
1- آهني آذري.الف، دانش.الف، فراواني و حساسيت آنتيبيوتيكي سودوموناس آئروژينوزاي جدا شده از بيمارستان طالقاني گرگان، مجله علمی دانشگاه علوم پزشکی گرگان، دوره9، شماره3، صفحه 69 تا 73
2- اخي.م، حسنزاده.ع، باكتريهاي دخيل در عفونتهاي سوختگي و الگوي حساسيت آنها
3- ارزنلو.م، عرب.ر، علايي.ر، اثر درماني سير (Allium sativa) در مقابل عفونت سوختگي ناشي از سودوموناس آئروژينوزا، Biological Science Research Journal.
4- ارزنلو.ه، ستاري.م، زواران حسيني.الف، فائزي.س، بررسي آثار حفاظتي آنتيباديهاي ضد فلاژلي سودوموناس آئروژينوزا به عفونت سوختگي ناشي از آن در موش BALB/C.
5- استوارت واكر، ميكروب شناسي (باكتري شناسي پزشكي)، ترجمه رنجبر.ر و همكاران، (1386)، انتشارات ارجمند، صفحه 130 تا 146.
6- اصلاني.م و همكاران، تشخيص مولكولي و تعيين فاكتورهاي ويرولانس سويههاي سودوموناس آئروژينوزا جدا شده از عفونتهاي زخم و سوختگي، مجله پژوهشي پژوهنده دانشگاه علوم پزشكي شهيد بهشتي، سال 15، شماره6، 1389، صفحه 287 تا 292.
7- اميني.ف و همكاران، بررسي شرايط توليد رامنوليپيد حاصل از سويههاي مختلف سودوموناس آئروژينوزا، مجله علوم تغذيه و صنايع غذايي ايران، سال 4، شماره 1،1388.
8- اوليا.پ، صادري.ح، طباطبايي نژاد.الف، ناصر.م، رضايي.م، مقايسه اثر ضدميكروبي عصاره Ruta graveolens و جنتامايسين بر سودوموناس آئروژينوزا.
9- ايماني.غ، ستاري.م، گودرزي.غ، شناسايي ژنflic (فلاژلين) در سودوموناس آئروژينوزاهاي جدا شده از نمونههاي باليني با استفاده از واكنش زنجيرهاي پليمراز PCR، مجله علوم آزمايشگاهي، دوره سوم، شماره 1، 1388.
10- بروكس، گئاف، ميكروب شناسي پزشكي جاوتز، (1387)، انتشارات حيان، صفحه 322 تا 326.
11- تاجبخش.ح، باكتري شناسي عمومي، (1383)، انتشارات دانشگاه تهران، 700 تا 703.
12- جاكليك، ويلت، آموس، ويلفرت، ميكروب شناسي زينسر، ترجمه رحيمي.م و همكاران، (1387)، انتشارات آييژ، چاپ سوم، صفحه 295 تا 307.
13- جانسون، زيگلر، فيتزجرارد، لوكا سويكز، هالي، ميكروبيولوژي و ايمونولوژي، ترجمه شهيدي.ف، محبي.ح، عدالتيان.م، انتشارات دانشگاه فردوسي مشهد، شماره 357، صفحه 119 تا 122.
14- جنيدي.الف، موحديان عطار.ح، پرورش.ع، شكوهي.ر، شناسايي باكتريهاي هوازي تجزيه كننده فنل در سيستم تركيبي بيوفيلتر و لجن فعال، (1384).
15- جهاني فر.ه، صبوري.الف، حسنزاده.ن، نراقي.ل، تهيه جهش يافتههاي مقاوم به آنتيبيوتيك باكتري سودوموناس فلورسنس و بررسي فعاليت و مكانيسمهاي آنتاگونيستي آنها بر عليه قارچ Rhizoctonia solani عامل بيماري مرگ گياهچه برگ، فصلنامه تحقيقات بيماريهاي گياهي، سال اول، شماره1، تابستان 90، صفحه 67 تا 76.
16- حسننيا.م، نقش باكتري سودوموناس فلورسنس در توسعه جلبك، (1381).
17- حسنی طباطبایی.ع، فیروزی.ر، بیماریهای باکتریایی دام، انتشارات دانشگاه تهران، (1380).
18- رضايي.د، حقنیا.غ، لکزیان.الف، حسنزاذه خیاط.م، نصیرلی.ح، مطالعه تجزيه علفكش آترازين بوسيله باكتريهاي سودوموناس فلورسنس و سودوموناس آئروژينوزا به عنوان منبع نيتروژن و كربن در شرايط آزمايشگاهي، نشريه آب و خاك (علوم و صنايع كشاورزي)، جلد 25، شماره4،1390، صفحه 779 تا 806.
19- رضايي.ر ، ميكروبيولوژي پزشكي، (1373)، مركز انتشارات علمي دانشگاه آزاد اسلامي، صفحه 167 تا 173.
20- سپهري.س، نجار پيرايه.ش، ستاري.م، آهنگرزاده.م، ارزيابي توليد بتالاكتاماز توسط پلاسميد در سويههاي سودوموناس آئروژينوزاي جدا شده از سوختگيها، مجله پژوهشي حكيم، بهار 86، دوره دهم، شماره اول، صفحه 61 تا 65.
21- ستاري.م، شهبازي.ن، نجار پيرايه.ش، ارزيابي اثر باكتريايي عصاره آبي و الكلي اكاليپتوس بر سودوموناس آئروژينوزا، (1384).
22- سليمي.خ، اوليا.پ، يخچالي.ب، رستگار لاري.ع، بررسي حساسيت دارويي و اپيدميولوژي مولكولي سودوموناس آئروژينوزاي جدا شده از بيماران سوخته.
23- شاهيان.م،گلبانگ.ن، امتيازي.گ، بررسي امكان تصفيه زيستي فنل و مشتقات فنلي از پساب صنايع سنگين با استفاده از مخمرهاي تجزيه كننده فنل، چهارمين همايش ملي بيوتكنولوژي جمهوري اسلامي ايران، كرمان، مرداد 1384.
24- شريفي تهراني.ع و همكاران، بررسي تأثير سودوموناس هايفلورسنس روي قارچ Pythium Ulimum Trow عامل پوسيدگي بذر لوبيا، مجله علوم كشاورزي ايران، دوره 34، شماره4.
25- صفاري.م، نقي زاده.م، پوربابايي.م، مطالعه اثر انواع مختلف عسل بر رشد سويه استاندارد سودوموناس آئروژينوزا در شرايط برون تني.
26- صفاهيه.ع، موجودي.ف، ذولقرنين.ح، ارزيابي و مقايسه توانايي باكتريهاي سودوموناس بومي منطقه خورموسي در حذف تركيبات آروماتيك حلقوي، محيط شناسي، سال37، شماره 58، 1390، صفحه 149 تا 158.
27- طالب جهرمي.خ، شريفي تهراني.ع، احمدزاده.م، مطالعه توليد برخي از متابوليتهاي ضد ميكروبي بوسيله تعدادي از سودوموناسهاي فلورسنت، پايگاه نشريات الكترونيكي دانشگاه تهران، مجله علوم كشاورزي ايران، دوره 35، شماره 3.
28- عسكريان.م، حسيني.ر، خيرانديش.پ، بررسي ميزان بروز عفونتهاي بيمارستاني و تعيين عامل ميكروبي آنها در بيمارستان سوختگي قطبالدين شيراز، مجله علمي دانشگاه علوم پزشكي و خدمات بهداشتي درماني همدان، سال چهاردهم، شماره3.
29- عطائي.ن، خاوازي.ك، قرباني. ش، تأثير جدايههاي سودوموناس پوتيدا توليد كننده هورمون اكسين بر تحريك رشد و افزايش تارهاي كشنده ريشه گندم، مجموعه مقالات يازدهمين كنگره علوم خاك ايران، گرگان، تير 1388.
30- غفاري.ش، راهب.ج، اكبرزاده.س، ابراهيمي پور.غ، سولفورزدايي سودوموناس آئروژينوزا PG201 در حضور بيوسورفاكتانت، مركز بينالمللي علوم و تكنولوژي پيشرفته و علوم محيطي، چهارمين همايش ملي بيوتكنولوژي جمهوري اسلامي ايران، كرمان. مرداد 84.
31-فقري.ج، بررسي علل عفونتهاي باكتريال بيماران دچار سوختگي بستري در بيمارستان سوانح و سوختگي اصفهان طي سالهاي 1384-1383، مجله علمي دانشگاه علوم پزشكي و خدمات بهداشتي درماني همدان، دوره 14، شماره3، 1386.
32- مالكنژاد.پ، عليقلي.م، موسوي.س، بررسي مقاومت سودوموناس آئروژينوزا به پنيسيلين، سفالوسژورين و آمينوگليكوزيدها.
33- مبين.ه و همكاران، بررسي فراواني عوامل باكتريايي در عفونتهاي سوختگي، مجله پژوهشي علوم پزشكي تبريز، شماره1، سال 1378.
34- متحدين.پ، صعودي.م، بررسي مقاومت به مواد ضد ميكروبي در سويههاي سودوموناسي جدا شده از فرآوردههاي بهداشتي، مجله زيست شناسي ايران، جلد1، شماره1، بهار 1385.
35- محمدي.م، ريحاني تبار.ع، عليخاني.ح، صالح راستين.ن، اثرات كاربرد سويه بومي سودوموناس آئروژينوزا بر مقدار جذب عناصر غذايي، پايگاه نشريات الكترونيكي دانشگاه تهران، مجله علوم كشاورزي ايران، دوره 33، شماره 4.
36- مماني.م و همكاران، فراواني عفونت باكتريال زخمهاي سوختگي و مقاومت دارويي آنها در مراجعين به بخش سوختگي بيمارستان بعثت همدان، نشريه جراحي ايران، دوره17، شماره 1، 1388.
37- مورايي،روزنتال،فالر، ميكروب شناسي پزشكي، ترجمه اسلامي و همكاران، انتشارات آييژ، صفحه 425 تا 435.
38- مؤسسه استاندارد و تحقيقات صنعتي ايران، چاپ اول، كيفيت آب- شناسايي و شمارش سودوموناس آئروژينوزا به روش صاف كردن غشايي.
39- مهرباني.د، واكسن پيشگيري از عفونتهاي سوختگي،Medical journal of microbiology british
40- ميرصالحيان.الف و همكاران، فراواني سويههاي توليد كننده متالوبتالاكتاماز در سودوموناس آئروژينوزاي جدا شده از بيماران سوختگي، مجله دانشكده پزشكي، دانشگاه علوم پزشكي تهران، دوره 68، شماره 10، دي 1389، صفحه 563 تا 569.
41- ناصري رازليقي.ع، ناصري رازليقي.آ، ميكروبيولوژي مواد غذايي، (1388)، انتشارات آييژ، صفحه41 تا 47.
42- نعمتي.الف، مظفري.ن، نصيري.الف، بررسي وضعيت عفونتهاي سودوموناسي و استافيلوكوكي مقاوم به دارو در بخش سوانح و سوختگي بيمارستان زارع، مجله دانشگاه علوم پزشكي مازندران، دوره17، شماره 59، 1389، صفحه 134 تا 135.
43-Bridget Carr Gregory, DVM, MPH, AND David M.Waag, text books of military medicin-chapter 6, 2007, pag 121-146.
44- Charles wright, Spyros D.Komlnos and Robert B.yee, entrobacteriaceae and pseudomonas aeroginosa recovered from vegetable salads, printed in U.S.A (MAY 1976).
45-C.M.C.Carrea, Tibana, P.P.Gontijofilho, vegetables as a sours of infection whith pseudomonas aeroginosa in a university and ancology hospital of Rio dejaneria (april 2004).
46- H.M.Ehrnardtand , H.S.Rehm, phenol degradation by microorganism adsorbed on activated carbon, institud kir microbiologie universifit miinster.
47-K.G.Kerr,Am.Snelling, pseudomonas aeroginosa aformidable and ever-present adversary(17may 2010) journal of hospital infecton pages 338-344.
48-N Bouziges, A Gouby. A monamat. J.P Daures,A Sotto,Risk factors for multidrug-resistant pseudomonas aeroginosa nosocomial infection, juornal of hospital infection ,page 209-216.
49- N.G.K.Karanth, P.G.Deo and N.K.Veenandig,microbial production of biosurfactants and their importance Department of biochemistri, india.
50-shigeki fuji tani, H sin-yun sun, victor L.Yo, jeremy A.weingarten pneumonia Due to pseudomonas aeroginosa, 17th world congress for bronchology and interventional pulmonology.
51-Spyros D.Komlnos, Charls E.copeland,Barbara Grosiak, and Bosko Posiic, introduction of pseudomonas aeroginosa, intoa hospital via vegetables, Departments of pathology and General surgery(1972).
52- V.M.Kokis, B.M.Moreira,F.L.P.C.Pellegrino, indentification of an imipenem – resistant pseudomonas aeroginosa clon among patients in a hospital in rio de janeiro, journal of hospital infection, page 16-26
https://en.wikipedia.org/wiki/Pseudomonas
مکانیزمهای مقاومت آنتیبیوتیکی در سودوموناس آئروجینوز
برای دانلود پی دی اف بر روی لینک زیر کلیک کنید
ورود / ثبت نام