بررسی سرواپیدمیولوژی آنتیبادیهای SARS-COV-2 IgG, IgM در مراجعین بیمارستان غیاثی- شهرک ولیعصر (منطقه 18 تهران) در همه گیری COVID-19
(تیرماه تا اسفندماه 1399)
دکتر فریبا فیاض: دکترای علوم آزمایشگاهی، هیئت علمی دانشکده پزشکی دانشگاه علوم پزشکی شهید بهشتی
لیلا عاطف مهر: کارشناس ارشد زیستشناسی سلولی و مولکولی، دانشگاه آزاد واحد علوم تحقیقات تهران
دکتر محمدجواد نصیری: PhD میکروبشناسی پزشکی، استادیار بخش میکروبشناسی دانشکده پزشکی دانشگاه علوم پزشکی شهید بهشتی
چکیده
این تحقیق برمبنای یک مطالعه سرواپیدمیولوژیک تشخیص آنتیبادیهای SARS-COV-2 IgG, IgM در 1000 نفر از مراجعین بیمارستان غیاثی شهرک ولیعصر و در سه فصل تابستان، پائیز و زمستان 1399 پس از شیوع بیماری در اثر ویروس SARS-CoV-2 و در موجهای دوم، سوم و شروع چهارم این بیماری در ایران به منظور دستیابی به آمار اپیدمیولوژیک یک جامعه کوچک (شهرک ولیعصر) در جنوب غرب تهران بزرگ صورت پذیرفت. در این پژوهش تعداد 1000 نمونه خون مراجعین که همه از ساکنین شهرک ولیعصر تهران بوده اند و درخواست اندازه گیری آنتیبادیهای SARS-COV-2 IgG ,IgM را داشتند، توسط آزمایش الایزا با اندازه گیری SARS-CoV-2 IgM بر اســـــاس روش Antibody capture و SARS-CoV-2 IgG بر مبنای الایزای غیرمستقیم مورد بررسی قرار گرفت. IgG با اختلاف معنیدار 95% بیشترین میزان خود را نسبت به میانگین (برابر با 2/7) در موج سوم (بازه زمانی اوایل مهر 1399 تا اواخر آذر 1399) و IgM بیشترین میزان خود را نسبت به میانگین (برابر با 0/77) در موج دوم (بازه زمانی اواخر تیر 1399 تا اواخر مرداد 1399) در مراجعین نشان میدهد. در طی پاندمـــــــی حاصل از SARS-COV-2، بدست آوردن کلیه اطلاعات اپیدمیولوژیک در جوامع مختلف از هر منطقه، روستا، شهر، کشور و قاره از اهمیت ویژه ای برخوردار است، زیرا با دستیابی به هرگونه اطلاعات و تحقیقات بدست آمده در رویارویی با ایمنی حاصل شده قبل و بعد از واکسیناسیون میتوان برای برنامه ریزی های آینده در جوامع و مناطق کوچک و در طی آن در جهت تصمیمات کلان بهداشتی در سطوح جمعیتی بالاتر اقدام نمود.
کلمات کلیدی: SARS-COV-2 IgG, IgM، COVID-19، الایزا، موج، پیک
مقدمه
از دسامبر سال 2019 که شیوع و انتقال ویروس (SARS-CoV-2) از کشور چین آغاز گردیده تا به امروز همچنان ویروس حضور دارد و شمار قربانیان خود را در ورقهای تاریخ در قرن 21 میلادی و سال 1400 خورشیدی به ثبت میرساند. توسعه سریع رشد این پاندمی و موجهای مختلف آن در اقصی نقاط گیتی، استانداردهای همیشگی کادر درمان خصوصاً آزمایشگاهیان را درهم شکسته و آنها را به سمت انجام آزمایشهای غربالگری و تشخیصی سریعتر و دقیق تر سوق داده است (2 و 3).
همه گیری جهانی بیماری COVID-19 در حال حاضر برقراری قوانین بهداشتی خاصی را در دنیا رقم زده است. حفظ فاصله اجتماعی، استفاده از پوشش ماسک، شرایط قرنطینه در شهرها و مناطق مختلف، تعطیلی کسب و کار و … همه نشانگر آن است که هر روز مقررات خاصی وضع میشوند که این قوانین بر مبنای آمار مبتلایان، بهبودیافتگان، مرگ و میر، بستری و حتی ایمونیزاسیون با واکسن اجرا میگردند (9 و 4). این قوانین و پروتکلها تغییر مییابند و به تبعیت آن تقاضا برای تستهای آزمایشگاهی به منظور غربالگری و تشخیص نیز افزایش مییابد (12).
استفاده از کیتهای مختلف تشخیصی و روی آوردن به ابداع و استفاده از روشهای جدید با حساسیت و ویژگی بالا از اهداف اولیه و همیشگی آزمایشگاهیان در رویارویی با این تقاضاها است. در مواقعی شاهد آن بوده ایم که آزمایشهای استاندارد تصدیقی(Gold Standard) بهطور مثال PCR در SARS-CoV-2 قادر به پاسخگویی تمام نیازهای شیوع در یک جامعه نیستند، لذا در این زمان تستهای سرولوژیک در مطالعات اپیدمیولوژی و ارزیابی میزان شیوع و طول عمر ایمنی ایجادشده در اثر بیماری یا به دنبال واکسیناسیون نقش بارز خود را نشان میدهند (4 و 8).
جهت ارزیابی میزان چرخش ویروس در اجتماع، محافظت از احتمال عفونت مجدد، سنجش میزان ایمنی در صورت ابتلا به ویروس و پس از واکسیناسیون علیه SARS-CoV-2 و پیگیری افراد مبتلا پس از بهبودی، انجام آزمایشهای سرولوژیک و ارزیابی سرواپیدمیولوژی علیه SARS-CoV-2 را ضروری میسازد (4 و 5). تحقیقات نشان داده است که در کلیه بیماران مبتلا به این ویروس، چه آنها که علائم خفیف نشان داده اند و یا در بیمارستان بستری شدهاند و یا حتی بدون علامت بوده اند و تنها به خاطر آگاهی از وضعیت خود به آزمایشگاه مراجعه نموده اند، پدیده seroconversion وجود دارد. همه آنها بعد از 18-10 روز روند تولید و تغییرات آنتیبادی را داشته اند و پیدایش آنتیبادی در فرد در صورتی که نقص سیستم ایمنی نداشته باشد حتمی است (7 و 16).
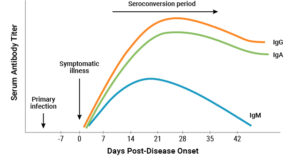
شکل 1- پیدایش و تغییرات آنتیبادیها در ابتلا به ویروس SARS-CoV-2
Reference: SARS-CoV-2 and the Antibody Response in COVID-19 Patients, By: Emily A. Teslow, Ph.D., Medical Affairs • August 2020
همانطور که در شکل 1 مشاهده میشود، تغییرات آنتیبادیهای IgG و IgM در تمامی بیماران بین هفتههای سوم و چهارم بیماری به حداکثر خود رسیده و بهخوبی قابل بررسی است. IgM در بیماران از هفته پنجم به حداقل خود رسیده و در هفته هفتم ناپدید میشود. IgG تا 7 هفته یا بیشتر بالا خواهد بود (16).
باید در نظر داشته باشیم که واژه های موج (Wave) و پیک (Peak) دو معنای متفاوت دارند؛ نوسانات افزایشی و طغیان بیماری را پیک میگویند، لیکن موج در زمانی است که بیماری همچنان بهصورت اپیدمی وجود داشته و به مرحله خاموشی و یا به مهار کامل نرسیده است (9 و 10). از آنجا که در تمام گزارشها لفظ “موج” استفاده میگردد، لذا ما نیز افزایش موارد بیماری را در یک بازه زمانی موج نامیده و فزاینده ترین نوسان هر موج را پیک اطلاق مینماییم. زمان رسمی شروع بیماری COVID-19 در ایران 30 بهمن 1398 اعلام گردید. تاکنون چهار موج در ایران گزارش گردیده است. موج اول اواخر فروردین 1399 تا اواخر خرداد 1399، موج دوم از اواخر تیر 1399 تا اواخر مرداد 1399، موج سوم از اوایل مهر 1399 تا اواخر آذر 1399 و موج چهارم از اواسط بهمن 1399 که همچنان ادامه دارد (10 و 9).
نیاز به بررسی موضوع تحقیق
استراتژی خروج از پاندمی (Exit Pandemic Strategy) در فاز اول برمبنای مستقیم شدن منحنی انتقال است که در این راستا باید کلیه جمعیتهای منطقه ای، شهری و … مورد ارزیابی قرار گیرند و همچنین کلید ایجاد ایمنی محافظتی (Protective Immunity) با زدن واکسن و تعقیب و ردیابی ایمنی و ایجاد آنتیبادی در کلیه افراد است (4). تمامی این برنامه ها قرار دادن و تأکید انجام تستهای سرولوژیک را در این الگوریتم برای کلیه جمعیتها قبل و پس از تزریق واکسن ضروری میسازد (7 و 11). بر اساس کلیه شواهد و دلایل ذکرشده، ما نیز بر آن شدیم تا تحقیق حاضر را ارائه دهیم. این پژوهش آنتی بادی IgG و IgM علیه SARS-CoV-2 را طی 9 ماه در طول سه فصل و در طی چهار موج و سه پیک بیماری در مراجعین مشکوک به COVID-19 بیمارستان تخصصی غیاثی، از ساکنین شهرک ولیعصر در جنوب غرب تهران بزرگ، مورد بررسی قرار میدهد. شهرک ولیعصر از شهرکهای پرجمعیت تهران در منطقه 18 بوده که از محله های یافت آباد، نعمت آباد و فلاح تشکیل شده است. این شهرک حدود 141 هکتار وسعت و جمعیتی بالغ بر 31/854 نفر دارد (15). بیمارستان تخصصی غیاثی یکی از قدیمیترین (تأسیس 1331) و هم اکنون از مجهزترین بیمارستانهای این منطقه است.
روش مطالعه
جمع آوری نمونه: در این پژوهش تعداد 1000 نمونه خون مراجعین جهت تعیین آنتـی بادی علیه
SARS-COV-2 که همه از ساکنین شهرک ولیعصر تهران بوده اند و به آزمایشگاه بیمارستان غیاثی واقع در این شهرک مراجعه نموده اند، استفاده گردید. سرم این افراد پس از جداسازی در یخچال نگهداری شده اند و در کمتر از 48 ساعت مورد آزمایش قرار گرفتند.
مواد و روشها: در این بررسی از دو کیت اندازه گیری SARS-CoV-2 IgM و SARS-CoV-2 IgG شرکت ایده آل تشخیص آتیه استفاده شد. این کیتها برای تشخیص وجود آنتـــــیبادیهای اختصاصی IgG ,IgM علیه ویروس SARS-CoV-2 که عامل بیماری COVID-19 است، طراحی شده اند (14).
کیت تشخیصی SARS-CoV-2 IgM بر اساس روش الایزای ساندویچ و نوع Antibody capture طراحی شده است و در آن از آنتی بادی ضد IgM انسان که در چاهکهای پلیت کوت شده اند استفاده گردیده. کونژوگه آنزیمی شامل آنتیژنهای نوکلئوکپسید (N) و اسپایک (S) ویروسSARS-CoV-2 متصل به آنزیم HRP است که در نهایت با تشکیل کمپلکس ایمنی، سپس شستشو، آنتیبادی IgM اختصاصی موجود در نمونه بیمار علیه آنتیژنهای N و S ویروس تشخیص داده میشود.
کیت تشخیصی SARS-CoV-2 IgG این شرکت، بر اساس روش الایزای غیرمستقیم طراحی شده که آنتی ژن (N) ویروس در چاهکها کوت شده است که در صورت وجود IgG، این آنتیبادیها به آنتیژنهای کف چاهک متصل میشوند، در ادامه پس از شستشو با استفاده از IgG Anti Human متصل به آنزیم HRP و تشکیل کمپلکس ایمنی آنتیبادی اختصاصی در نمونه بیمار قابل تشخیص میشود.
برای انجام تستها از دستگاه الیزاریدر Mindray MR-96A استفاده شد. نتایج حاصل از قرائت دستگاه با محاسبه مقدار Cut off حاصل از کنترل منفی ارزیابی گردیده که مقادیر بالاتر از 1/1 مثبت و پایینتر از 0/9 منفی تلقی میگردند، لذا نتیجه منفی نشاندهنده عدم وجود مقادیر قابل تشخیص آنتیبادیهای IgG و IgM علیه SARS-CoV-2 و نتیجه مثبت نشاندهنده وجود این آنتیبادیها قلمداد گردید (14).
حساسیت، دقت و اختصاصیت کیت مورد استفاده: حساسیت کیت SARS-CoV-2 IgG 81/82% و اختصاصیت آن برابر 94/83% و در مورد کیت SARS-CoV-2 IgM مقدار حساسیت برابر 95% و اختصاصیت برابر 99/4% با حدود اطمینان 95 درصد توسط شرکت سازنده اعلام گردیده است (14). لازم به ذکر است که در صورت نیاز به تفسیر نتایج جهت تشخیص یا رد بیماری میباید نتایج منفی کاذب و مثبت کاذب در تستهای سرولوژیک SARS-CoV-2 مد نظر گرفته شود (14 و 1)، به همین دلیل در تحقیق حاضر از تفسیر نتایج جهت رد یا تشخیص بیماری در مراجعین خودداری شده و از این تستها به عنوان آزمایشهای تشخیصی به تنهائی استفاده نگردیده است. یادآوری میگردد که جهت کلیه افراد مورد آزمایش از کیتهای با یک Lot Number استفاده گردید که حساسیت، دقت و اختصاصیت کیت در مورد کلیه تستها یکسان باشد.
نتایج
از آنجا که هدف اصلی تحقیق، بررسی آنتیبادیهای تولیدشده در بیماران در موجهای مختلف است، لذا انجام تستهای آماری نیز بر همین مبنا گذاشته شد.
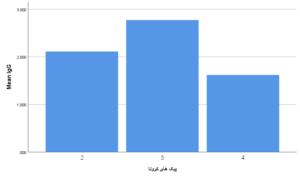
در جدول 1 میتوان میانگین IgG و SARS-COV-2 IgM را به ترتیب برای IgM معادل 0/58 و برای IgG معادل 2/47 مشاهده نمود. جدول 2 نیز میانگین IgG در موجهای دوم و سوم و شروع چهارم را نشان میدهد که بالاترین میزان IgG با ضریب اطمینان 95% نسبت به میانگین در موج سوم برابر با 2/77 است که بهوسیله جدول 3 با انجام تست ANOVA تأئید میشود. همین نتیجه را به صورت نموداری در نمودار 1 نشان دادهایم.
میانگین IgM در موج دوم برابر با 0/77 و بیش از مقدار IgM در موج سوم و شروع چهارم بوده است که با انجام تست ANOVA در جدول 5 تأئید گردیده، در عین حال در نمودار 2 نیز بالاترین میزان IgM در موج دوم نمایش داده شده است. به طور کلی در بازه زمانی پژوهش ماکزیمم میزان IgG برابر 19/1 و ماکزیمم IgM برابر 9/4 است که در جدول شماره 1 قابل رؤیت است.
لازم به ذکر است که شروع موج چهارم از زمستان 99 بوده است و همچنان در بهار 1400 ادامه دارد و تحقیق حاضر شامل بیماران از اول تیرماه تا آخر اسفندماه 1399 بوده است، لذا فقط ابتدای موج چهارم در محاسبات این تحقیق لحاظ شده است.
جدول 1- میانگین کلی IgG و SARS-COV-2 IgM در بیماران مورد مطالعه
| Descriptive Statistics | ||||||
| N | Minimum | Maximum | Sum | Mean | Std. Deviation | |
| IgG | 999 | .005 | 19.100 | 2468.425 | 2.47090 | 4.665901 |
| IgM | 998 | .003 | 9.400 | 585.686 | .58686 | 1.379336 |
| Valid N (listwise) | 998 | |||||
جدول 2: میانگین مقادیر IgG در موجهای دوم، سوم و ابتدای موج چهارم
| Descriptives (IgG) | ||||||||
| N | Mean | Std. Deviation | Std. Error | 95% Confidence Interval for Mean | Minimum | Maximum | ||
| Lower Bound | Upper Bound | |||||||
| 2 | 228 | 2.11360 | 4.432338 | .293539 | 1.53519 | 2.69201 | .010 | 17.430 |
| 3 | 639 | 2.77400 | 4.937111 | .195309 | 2.39047 | 3.15752 | .005 | 19.100 |
| 4 | 132 | 1.62076 | 3.420891 | .297750 | 1.03174 | 2.20978 | .040 | 14.600 |
| Total | 999 | 2.47090 | 4.665901 | .147623 | 2.18121 | 2.76058 | .005 | 19.100 |
جدول 3: اختلاف معنیدار میانگین SARS-COV-2 IgG در موجهای دوم، سوم و ابتدای موج چهارم بر اساس تست ANOVA
| ANOVA (IgG) | |||||
| Sum of Squares | df | Mean Square | F | Sig. | |
| Between Groups | 183.214 | 2 | 91.607 | 4.235 | .015 |
| Within Groups | 21543.875 | 996 | 21.630 | ||
| Total | 21727.089 | 998 | |||
جدول 4: میانگین مقادیر IgM در موجهای دوم، سوم و ابتدای موج چهارم
| Descriptives (IgM) | ||||||||
| N | Mean | Std. Deviation | Std. Error | 95% Confidence Interval for Mean | Minimum | Maximum | ||
| Lower Bound | Upper Bound | |||||||
| 2 | 228 | .77218 | 1.590971 | .105365 | .56457 | .97980 | .007 | 8.600 |
| 3 | 638 | .56089 | 1.323087 | .052382 | .45803 | .66375 | .003 | 9.400 |
| 4 | 132 | .39227 | 1.216660 | .105897 | .18278 | .60175 | .009 | 7.900 |
| Total | 998 | .58686 | 1.379336 | .043662 | .50118 | .67254 | .003 | 9.400 |
جدول 5: اختلاف معنی دار میانگین SARS-COV-2 IgM در موجهای دوم، سوم و ابتدای موج چهارم بر اساس تست ANOVA
| ANOVA (IgM) | |||||
| Sum of Squares | df | Mean Square | F | Sig. | |
| Between Groups | 13.259 | 2 | 6.630 | 3.502 | .031 |
| Within Groups | 1883.600 | 995 | 1.893 | ||
| Total | 1896.859 | 997 | |||
نمودار 1- نمودار مستطیلی میانگین IgG در موجهای مختلف در بازه زمانی تیرماه تا اسفند 1399
نمودار 2- نمودار مستطیلی میانگین IgM در موجهای مختلف در بازه زمانی تیرماه تا اسفند 1399
بحث
مقادیر SARS-COV-2 IgG و SARS-COV-2 IgM در 1000 مراجعهکننده بیمارستان غیاثی مورد بررسی آماری قرار گرفته که در قسمت نتایج ارائه گردیده است. با در نظر گرفتن آنکه زمان درخواست و انجام تستهای سرولوژیک بسیار مهم است و باید از آنها در زمان مناسب استفاده شود، به بحث در مورد نتایج تحقیق حاضر میپردازیم (16). IgG با اختلاف معنیدار و ضریب اطمینان 95% در موج سوم بیشترین میزان خود را نسبت به میانگین نشان داده در صورتی که IgM بیشترین میزان خود را نسبت به میانگین، در موج دوم نشان میدهد. این میتواند بدان معنا باشد که در موج دوم که بازه زمانی اواخر تیرماه 1399 تا اواخر مرداد 1399 بوده است، افراد مشکوک در هنگام بیماری علائم بالینی را به سرعت نشان داده و سریعاً به دستور پزشک و یا شخصاً به بیمارستان مراجعه نمودهاند و با انجام دادن تست و مثبت شدن IgM به بیماری خود واقف گشتند و آن را دنبال نمودند، در صورتی که در موج سوم که بازه زمانی اوایل مهرماه 1399 تا آخر آذرماه 1399 بوده است، بیماری با علائم خفیفتر در جمعیت موردمطالعه بروز نموده و یا افراد، بدون علائم و یا با علائم کمتری بودهاند، لذا دوران ابتدایی بیماری را سپری و سپس جهت اطمینان از وضع خود یا به دستور پزشک اقدام به انجام تست سرولوژیک نمودهاند. به همین دلیل با IgG بالا و IgM پائین در این بازه زمانی روبرو هستیم (15 و 2).
تفسیر دیگری که بر این نتایج قائل شدیم برمبنای رواج آزمایشها در آزمایشگاههای تشخیص پزشکی پس از موج اول بوده است. در موج دوم یعنی تابستان 1399 کیتهای PCR و تشخیص آنتیبادی به روش Elisa به میزان قابلتوجهی وارد بازار شده و رونق کیتهای Elisa داخلی در همین فصل آغاز شد، لذا مقدار بیشتری از افراد مشکوک در مقدمه و شروع بیماری، در آزمایشگاه پذیرش شده و یا توسط پزشکان محترم به آزمایشگاهها فرستاده شدند که این میتواند گویای بالا بودن میانگین IgM در موج دوم به نسبت سایر موجها باشد (2 و 4). اختلاف معنیدار میانگین IgG (2/7) در موج سوم به نسبت موجهای دوم (2/1) و شروع چهارم (1/6) میتواند رویکرد بیماران به انجام تست PCR در مرحله ابتدای بیماری و سپس انجام تستهای آنتیبادی پس از بهبودی و سپری کردن فاز حاد بیماری باشد (5 و 7).
آنچه مسلم است تستهای سرولوژیک تشخیص آنتیبادی SARS-COV-2 کاربرد بسیار بالائی در تعیین استراتژی خروج از پاندمی دارند. کلیه دادهها در تحقیقات مختلف و در جمعیتهای متفاوت میتواند به یاری پژوهشگرانی بشتابد که در تحقیقات اپیدمیولوژیک آینده نیاز به بررسی و مقایسه تولید، میزان و ماندگاری آنتیبادی ایجادشده علیه SARS-COV-2 قبل و بعد از واکسیناسیون را در تحقیقات خود ردیابی میکنند. نتیجه تحقیق ما و مشابه آن میتواند آمار جمعیتهای کوچک را به عنوان الگویی جهت بررسیهای بزرگتر و گسترده تر آینده قرار دهد.
پیشنهادها و توصیه ها
در همه گیریهای با شیوع بالا مانند موقعیت فعلی جهان در ارتباط با COVID-19، به حداکثر رساندن ویژگی آزمایش و به دنبال آن PPV (Positive Predictive Value) یا ارزش پیشگوئی کننده مثبت حائز اهمیت است. در جمعیتی که شیوع بیماری بالاست، آزمایشی با ویژگی و حساسیت بالا دارای PPV بالاتری خواهد بود (12 و 10). این بدان معناست که احتمال یافتن افرادی که آزمایش مثبت واقعی آنتیبادی دارند افزایش می یابد (4،11). از این رو پیشنهاد میگردد که در همه گیری COVID-19 برای به حداکثر رساندن PPV از راهکارهای زیر استفاده نمود:
- همزمانی استفاده از یک Gold Standard مانند RT-PCR همراه با روشهای اندازه گیری آنتی بادی که میباید زمان نمونه برداری در مورد هردو در نظر گرفته شود.
- استفاده از دو روش الایزای متفاوت با آنتیژنهای یکسان یا متفاوت.
- استفاده از دو روش آزمایش اندازه گیری آنتی بادی مختلف مانند الایزا و کمی لومینسانس با آنتیژنهای یکسان یا متفاوت.
- انتخاب آزمایشی با ویژگی بسیار بالا (در حد 99/5%).
تشکر و قدردانی
نویسنده از ریاست محترم بیمارستان غیاثی و مدیریت آزمایشگاه سرکار خانم ماندا جواهری برای به انجام رسیدن این تحقیق تشکر و قدردانی مینماید. همچنین با سپاس و تشکر از کلیه پرسنل کوشای آزمایشگاه غیاثی که با جان و دل در تمام دوران اپیدمی COVID-19 به انجام وظیفه مشغول بوده و هستند.
References:
- Stephanie J Salyer, Justin Maeda, Senga Sembuche et al.
The first and second waves of the COVID-19 pandemic in Africa: A cross sectional study.
Lancet 2021; 397: 1265-75
- Hongyan Hou, Ting Wang, Bo Zhang, Ying Luo, Lie Mao, Feng Wang, shiji Wu and ziyong sun.
Detection of IgM and IgG Antibodies in Patients with Coronavirus Disease 2019.
Clinical and Translation Immunology, 2020, vol.9, e1136.
- Ralph R, Lew J.,Zeng T et al.
219-n Cov (Wuhan virus), A Novel Coronavirus: Human to Human Transmission, Travel Related Cases and Vaccine Readiness
The Journal of Infection in Developing Countries, 2020: 14(01): 3-17.
- Xiao Sy, Wuy, Liu H.
Evolving status of the 2019 Novel Coronavirus Infection: Proposal of Conventional Serologic Assays for Diagnosis and Infection Monitoring.
- Med. Virol 202;92;464-467
- Corine H Geurtsvankessel, Nisreen M.A.Okba, Zsofia Igloi, Susanne Bogers et al.
An Evaluation of COVID-19 serological Assays Inform Future Diagnostics and Exposure Assessment
Nature communications, 2020;11:3436
- Kissler S.M.,Tedijanto C., Goldstein E., Grad Y.H., Lipstich M.
Projecting the Transmission Dynamics of SARS-COV-2 Through the Postpandemic Period.
Science, 2020;368:860-868.
- Long Q.X.,et al.
Antibody Responses to SARS-COV-2 in patients with COVID-19
Nat. Med. 2020;26:845-848.
- Bryant J.E., et al.
Serology for SARS-COV-2: Apprehensions, Opportunities, and the Path Forward.
Sci. Immunol. 202;5,eabc6347.
- Waves and Peaks of COVID-19 in Iran Dr. Soori
Iranian Students News Agency Online
Isna.ir, News code: 99072216578, Oct 2020.
- Hemati
Antibodies Testing, Immunity Passport in COVID-19 Iranian Association of Clinical Laboratory Doctors
Journal of laboratory & Diagnosis, No.47 June 2020.
- Serology Testing for COVID-19 at CDC
National Center for Immunization and Respiratory Diseases (NCIRD), Division of viral Diseases CDC 24/7; Saving Lives, Protecting People; Nov.3,2020.
- Xiaoyong Zhang, Suwen Lu, Hui Li, Yi Wang et al.
Viral and Antibody Kinetics of COVID-19 Patients with Different Disease Severities in Acute and Convalescent phases: A 6-Month Follow up Study Virologica Sinica (2020) 35: 820-829.
- IDEAL TASHKHIS
SARS-COV-2 IgG, IgM, Cat. No:7324-96, 7224-96
Brounchure Rev: 10(2020/08/01)
- Mahale be Mahale-shahrak Valiasr
Neighborhood and Areas in Tehran
Tehran CityGuide(2021)
- Nandini Sethuraman, Sundararaj Stanleyraj Jeremiah, Akihide Ryo
Interpreting Diagnostic Tests for SARS-COV-2 JAMA. Published online May 06/2020. doi: 10:10.1001/Jama.2020.8259
- Jessica, E Metcalf, Jeremy Farrar, Felicity T Cutts, Nicole Basta, Andreal Graham, Justin Lessler, Neil M Ferguson, Donald Burke, Bryan T Grenfell
Use of Serological Survyes to Generate key Insights into the Changing Global Landscape of Infectious Disease. Lancet, 388(2016), PP.728-730.
برای دانلود پی دی اف بر روی لینک زیر کلیک کنید
ورود / ثبت نام