Nanobodies
تعریف، تولید و کاربرد در پزشکی
فهیمه لاوی
دانشجوی دکترای ایمونولوژی
چکیده:
آنتیبادیهای اختصاصی ویژهای در خون شترسانان یافت میشود که فقط از زنجیره سنگین همودایمر تشکیل شدهاند. ویژگی منحصربهفرد این آنتیبادیها نسبت به آنتیبادیهای معمولی عدم وجود زنجیره سبک در ساختمان آنها است. جایگاه متصل شونده به آنتیژن در این آنتیبادیها از یک دومن تنها تشکیل شده که مربوط به دومن متغیر این آنتیبادیها است که به همین علت نانوبادی نامیده میشود. نانوبادیهای اختصاصی به آنتیژن را بهآسانی با زمان ایمنوزاسیون کوتاه در شترسانان با آنتیژن و با استفاده از گنجینه VHH و نمایش فاژ میتوان بدست آورد. خصوصیات بیوشیمیایی سودمند آن شامل حلالیت خوب، پایداری در برابر عوامل دناتورهکننده، پروتئازها و دمای بالا، اختصاصیت به آنتیژن، اندازه کوچک و عدم ایجاد دیمریزاسیون باعث شده است که آنها بهعنوان ابزاری ایدهآل برای تحقیق، تشخیص و درمان بکار روند. در مطالعه حاضر تلاش شده نگاه اجمالی به ویژگیهای نانوبادیها، روشهای طراحی و تولید و کاربرد آنها در تشخیص و درمان بیماریها داشته باشیم.
مقدمه:
آنتیبادیها مولکولهای پروتئینی هستند که در طی پاسخ ایمنی در بدن پستانداران ازجمله انسان و موش توسط لنفوسیتهای B تولید میشوند. از نظر ساختاری آنتیبادهای معمول از چهار زنجیره پلیپپتید تشکیل شدهاند؛ دو زنجیره کوتاهتر را زنجیرههای سبک (L) مینامند که با پیوند دیسولفیدی به دو زنجیره بلندتر سنگین(H) متصل میشوند. هر کدام از زنجیــــــــرههای ایمنوگلوبولین از نواحی ثابت (Constant Region) و متغیر(Variable Region) تشکیل شده است. توانایی شناسایی و اتصال به آنتیژن در نواحی بسیار متغیر زنجیرههای سبک و سنگین (VH & VL) وجود دارد که اصطلاحاً Fab نامیده میشود.
نواحی ثابت زنجیره سنگین (FC) در عملکردهای بیولوژیک آنتیبادیها ازجمله اتصال به گیرندههای روی سلولهای هدف و تثبیت کمپلمان و اپسونیزاسیون نقش دارند که در نهایت به راهاندازی عملکردهای اجرایی بهمنظور حذف آنتیژن منجر میشود. این ناحیه برای کاربردهایی که فقط اتصال به آنتیژن مدنظر است، ضروری نیست.
آنتیبادیهای پلیکلونال و مونوکلونال دارای مصارف تحقیقاتی، تشخیصی و درمانی بسیاری میباشند ولی به علت واکنش ناحیه Fc با رسپتورهای Fc سلولهای بیگانهخوار، دارای اثرات جانبی ناخواسته میباشند، ازاینرو نانوبادیها به علت خصوصیات بیوشیمیایی ویژه ازجمله حلالیت خوب، پایداری در برابر عوامل دناتورهکننده، پروتئازها و دمای بالا، اختصاصیت به آنتیژن، اندازه کوچک و عدم ایجاد دیمریزاسیون بهعنوان ابزاری ایدهآل برای تحقیق، تشخیص و درمان بکار میروند.
نانوبادیها (آنتیبادیهای تک دومن طبیعی)
در اواخر دهه 1980 پروفسور ریموند هامرز و همکارانش آنتیبادیهای IgG اختصاصی را از سرم خون شتر جدا کردند که آنتیبادیهای زنجیره سنگین (antibodies Heavy-chain یا HCAbs) نامگذاری شدند. این آنتیبادیها نسبت به آنتیبادیهای معمولی فاقد زنجیره سبک (زنجیره L) و نخستین دومن ثابت (CH1) زنجیره سنگین (زنجیره H) بودند. آنتیبـــــــادیهای زنجیره سنگین از چینخوردگی دو زنجیره سنگین H به وجود آمدهاند که در ناحیه انتهایی ســــــر N خود دارای یک دومن متغیر اختصاصی هستند که به اصطلاح به آن دومن متغیر زنجیره سنــــــــــــــــــــــگین آنتیبادی (Variable domain heavy chain antibody) یا VHH یا نانوبادی گویند. حیواناتی که این آنتیبادیها را تولید میکنند جزء خانواده شترسانان هستند.
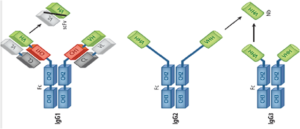
آنتیبادیهای زنجیره سنگین را براساس طول منطقه لولا (hinge region) به دو نوع ایزوتیپ شامل ایزوتیپ لولا کوتاه (short-hinge isotype) و ایزوتیپ لولا بلند (longe-hinge isotype) تقسیم میکنند. (شکل 1)
آنتیبادیهای موجود در سرم شترسانان شامل سه سابایزوتیپ IgG میباشند که IgG1 همانند آنتیبادیهای معمولی میباشد اما IgG2 و IgG3 همان آنتیبادیهای زنجیره سنگین میباشند. وزن مولکولی IgG1 همانند آنتیبادیهای معمولی حدود 150 کیلودالتون و وزن مولکولی IgG2 و IgG3، 90 کیلودالتون میباشد.
از چپ به راست IgG1 یک آنتیبادی معمولی، آنتیبادیهای زنجیره سنگین IgG2 و IgG3شکل 1- انواع ایزوتیپ آنتیبادیهای زنجیره سنگین
مقایسه بین دومنهای VH آنتیبادیهای معمولی و VHH آنتیبادیهای زنجیره سنگین:
1- هر دو دارای توالیهای متغیر CDRها هستند که در بین نواحی بیشتر حفظ شده (FRها) قرار دارند.
2- در VH مناطق حفظ شده هست که از اسیدهای آمینه هیدروفوبیک تشکیل شده و در موقعیتهای 37، 44، 45 و 47 ناحیه FR2 قرار دارند. این اسیدهای آمینه با نواحی هیدروفوبیک زنجیرههای سبک میانکنش میکنند.
3- در VHH، ناحیه FR2 از اسیدهای آمینه هیدروفیلیک (موقعیتهای 37، 44، 45 و 47) تشکیل شده که زنجیرههای سبک قادر به اتصال به آن نیستند.
4- نواحی CDR2 و CDR3 و VHH ازنظر اندازه بزرگتر از VH میباشد.
5- هومولوژی بین VH و VHH در نواحی داربست (FRها) بیش از 90 درصد میباشد.
ساختار VHH
جایگاه اتصال به آنتیژن آنتیبادیهای زنجیره سنگین از دومن تک زنجیره تشکیل شده که بطور مستقیم از طریق منطقه لولا به دومن Fc متصل میگردد. به این دومن متغیر VHH گویند.
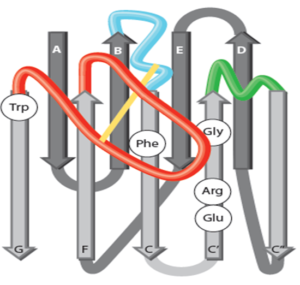
این دومن از 9 صفحه بتا تشکیل شده که همان نواحی حفظشدهای هستند که مناطق داربست(FR) نامیده میشوند. این FRها شامل FR1، FR2، FR3 و FR4 هستند و از 3 لوپ تشکیل شده که این لوپها همان مناطق شاخص مکمل CDR میباشند. این CDRها شامل CDR1، CDR2 و CDR3 هستند. (شکل 2)
شکل 2- ساختار VHH: نواحی رنگی مربوط به شاخص مکمل CDR1,2,3))
پیوندهای دیسولفیدی در VHH
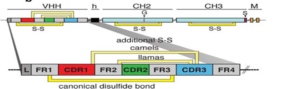
پیوندهای دیسولفیدی عمومی بین FR1 و FR3، پیوند دیسولفیدی اختصاصی در انواع مختلف شترسانان به ترتیب بین CDR3 و انتهای CDR1 و بین CDR3 و ابتدایCDR2 میباشد (شکل 3).
شکل 3- پیوندهای دیسولفیدی در VHH: پیوندهای دیسولفیدی عمومی و اختصاصی
روش تهیه نانوبادیها
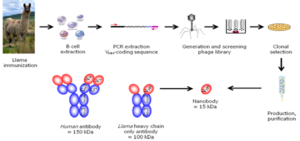
ابتدا خون شتر غیرایمن یا ایمن شده نسبت به یک ایمونوژن را جمعآوری و لنفوسیتهای آن را جدا کرده و سپس mRNA را استخراج کرده و توسط آنزیم ترانسکریپتاز معکوس از روی آن cDNA ساخته میشود. پس از ساخت cDNA، جهت تولید مقدار بیشتر DNA، PCR انجام میشود. سپس نانوبادیها به درون وکتور مناسبی مانند فاژمید کلون میشوند، این وکتورهای حاوی نانو بادیها به درون باکتریهای E.coli TG1 ترانسفورم شده و تولید کتابخانههای نانوبادی (107 VHH) میکنند. با روش Panning میتوان نانوبادی اختصاصی به آنتیژن را جدا کرد. جهت تولید نانو بادیهای محلول از سویههای E.coli و میزبان یوکاریوتی با بازده مثل مخمرساکارومایسس سرویزیه استفاده میگردد، همچنین بهمنظور خالصسازی نانوبادیها از روش کروماتوگرافی میل ترکیبی استفاده میگردد (شکل 4).
شکل 4– روش تولید نانوبادی
کاربرد نانوبادیها در پزشکی
نانوبادیها به خاطر ویژگیهای منحصربهفردی از قبیل تولید آسان و باصرفه، اندازه کوچک، توالی انسانی شده (جایگزینی 12 اسیدآمینه از 14 اسیدآمینه متفاوت بین VH انسانی و VHH شتر)، پایداری و مقاومت به حرارت، حلالیت بالا، چینخوردگی برگشتپذیر، افینیتی اختصاصی و زیاد نسبت به هدف و همچنین شناسایی اپیتوپهایی که توسط آنتیبادیهای معمولی شناسایی نمیشوند برای اهداف کاربردی بسیار ایدهآل هستند.
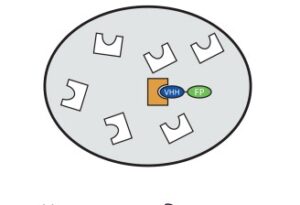
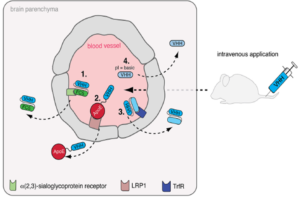
از نانوبادیها میتوان بهعنوان ابزارهایی برای پژوهش، تشخیص و تحقیق استفاده کرد. از نانوبادیهای با میل پیوندی بالا میتوان برای اهداف مهمی مثل خالصسازی پروتئینها، سیستم دارورسانی، بررسی مولکولهای مخابره کننده پیام (signaling) درون سلولی و بیومارکرهای سرطان استفاده کرد (شکل 5 و 6 و 7).
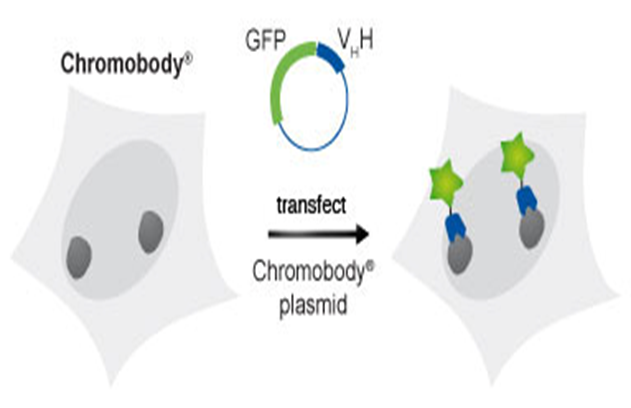
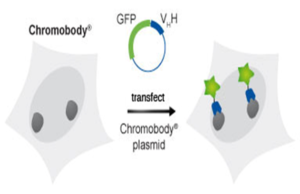
کونژوگه کردن نانوبادی با عناصر رادیواکتیو یا نانوبادیهای متصل شده به GFP، محل تمرکز مولکول را شناسایی میکنند. از این روش در تکنیکهای تصویربرداری با رزولوشن بالا استفاده میگردد، همچنین ادغام ژنتیکی پروتئین فلورسنت به نانوبادیها و بیان درون سلولی، تولید کروموبادی یا فلوبادیهایی میکند که میتوانند آنتیژن در بخشهای مختلف سلولی در سلولهای زنده را ردیابی کنند (شکل 8).
شکل 5- استفاده از VHH درایمنوپرسیپیتاسیون و خالصسازی پروتئین
شکل 6– استفاده از VHH در سیستمهای دارورسانی از طریق عبور از سد مغزی
شکل 7- استفاده از VHH در تصویربرداری داخل سلولی با اتصال به GFP
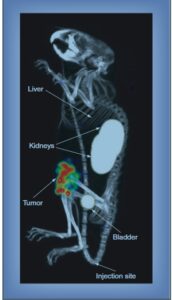
شکل 8– استفاده از VHH در تصویربرداری از مولکولهای سطحی تومور
منابع:
1 de Marco A. Biotechnological applications of recombinant single-domain antibody fragments. Microb Cell Fact. 2011;10
- Hassanzadeh-Ghassabeh G, Devoogdt N, De Pauw P, Vincke C, Muyldermans S. Nanobodies and their potential applications. Nanomedicine. 2013;8(6):1013-26.
- Muyldermans S. Nanobodies: natural single-domain antibodies. Annual review of biochemistry. 2013;82:775-97.
- Helma J, Cardoso MC, Muyldermans S, Leonhardt H. Nanobodies and recombinant binders in cell biology. The Journal of cell biology. 2015;209(5):633-44
- Kijanka M, Dorresteijn B, Oliveira S, van Bergen en Henegouwen PM. Nanobody-based cancer therapy of solid tumors. Nanomedicine. 2015;10(1):161-74.
- Siontorou CG. Nanobodies as novel agents for disease diagnosis and therapy. International journal of nanomedicine. 2013;8:4215
- Williams SC. Small nanobody drugs win big backing from pharma. Nature medicine. 2013;19(11):1355-6.
- Rissiek B, Koch-Nolte F, Magnus T. Nanobodies as modulators of inflammation: potential applications for acute brain injury. Frontiers in cellular neuroscience. 2014;8.
- Chakravarty R, Goel S, Cai W. Nanobody: the “magic bullet” for molecular imaging? Theranostics. 2014;4(4):386
متدهای کونژوگاسیون آنتیبادیها و مصارف درمانی آنتیبادیهای کونژوگه شده
برای دانلود پی دی اف بر روی لینک زیر کلیک کنید
ورود / ثبت نام