Bispecific Antibody
روشهای تولید و کاربرد آنها در درمان و تشخیص بیماری
هانیه غفاری نظری
دانشجوی دکترای ایمونولوژی
چکیده
آنتیبادیها امروزه به فراوانی برای اهداف درمانی و تشخیصی مورد استفاده قرار میگیرند. پیشرفت در تکنولوژی مهندسی آنتیبادیهای نوترکیب منجر به تولید آنتیبادیهای مختلف از نظر اندازه و ساختار، از جمله Bispecific Antibody شده است. Bispecific Antibody قادر به اتصال همزمان دو اپیتوپ مختلف میباشد.
از آنجا که Bispecific Antibodyها دو هدف متفاوت را نشانهگیری میکنند، بنابراین میتوانند بهطور همزمان برای مثال دو رسپتور سطح سلولی یا دو لیگاند را مورد هدف قرار دهند یا با اتصال به آنتیژنهای سطحی دو سلول مختلف باعث تماس بین دو سلول شوند. در حال حاضر Bispecific Antibodies متنوعی بهمنظور فراخوانی و فعالسازی سلولهای ایمنی و اهداف دیگر طراحی شدهاند و در راستای درمان بیماریهایی همچون بیماریهای التهابی و انواع سرطانها در مراحل مختلف کارآزمایی بالینی میباشند.
در این مقاله تلاش شده نگاه اجمالی به روشهای طراحی و تولید Bispecific Antibodies و کاربرد آنها در تشخیص و درمان بیماریها داشته باشیم.
مقدمه
آنتیبادیها پروتئینهای کروی هستند که توسط سلولهای B تولید و ترشح میشوند و در سیستم ایمنی بهمنظور شناسایی و هدفگیری عوامل بیگانه بکار گرفته میشوند.
با ابداع آنتیبادیهای مونوکلونال توسط کوهلر و ملیستن انقلاب بزرگی در درمان بیماریها بهویژه سرطانها رخ داد. امروزه آنتیبادیها بهطور گسترده برای اهداف درمانی و تشخیصی مورد استفاده قرار میگیرند.
با وجود نتایج مثبت آنتیبادیهای مونوکلونال بهویژه در کنترل و درمان بدخیمیهای خونی، استفاده از آنها به دلیل چندعاملی بودن بسیاری از بیماریها از جمله سرطانها، بیماریهای التهابی و بیماریهای آلرژیک با محدودیتهایی روبرو است، ازاینرو راهکارهای زیادی برای بهبود اختصاصیت و اثربخشی آنتیبادی بکار گرفته میشود.
پیشرفت در تکنولوژی مهندسی آنتیبادیهای نوترکیب منجر به تولید آنتیبادیهای مختلف از نظر اندازه، ساختار و کاربرد شده است. یکی از مهمترین این رویکردها، درواقع تکوین و بهکارگیری Bispecific Antibody است.
تعریف Bispecific Antibody
Bispecific Antibodies آنتیبادیهایی هستند که قادر به اتصال همزمان به دو اپیتوپ مختلف که بر روی یک آنتیژن یا دو آنتیژن متفاوت هستند، میباشند. با استفاده از این آنتیبادیها میتوان دو هدف مختلف را بهطور همزمان شناسایی کرد.
سه روش اصلی برای تولید این آنتیبادیها وجود دارد:
- کونژوگاسیون شیمیایی
- الحاق دو ردهی سلول هیبریدومای متفاوت (Hybrid Hydromas)
- رویکردهای ژنتیکی مانند استفاده از تکنولوژی DNA نوترکیب
اکثریت Bispecific Antibodyهایی که در ابتدا طراحی میشدند برای هدایت سلولهای ایمنی عملکردی به سمت سلولهای توموری بودند و ساختارهای متنوعی نیز برای این منظور طراحی شدند. اولین نسل Bispecific Antibodyها غالبـــــــــاً با استفاده از روش Hybrid Hydromas و یا کونژوگاسیون شیمیایی تولید میشدند.
با وجود اثرات بیولوژیک قابلتوجهی که توسط این آنتیبادیها مشاهده شد، در استفادههای بالینی تأثیر قابلتوجه و مداوم نداشتند.
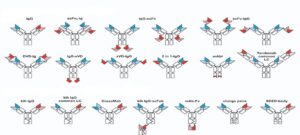
مسائلی که در مورد نسل اول این آنتیبادیها مطرح بود، ابتدا مشکل در تولید حجم بالا و سپس فقدان اثربخشی قطعات موشی موجود در این آنتیبادیها بود، بنابراین روشهایی برای بهبود کیفیت و اثربخشی این آنتیبادیها به کار گرفته شد و موجب به وجود آمدن اشکال متنوعی از این آنتیبادیها گردید و امروزه بیش از پنجاه شکل متفاوت از این آنتیبادیها وجود دارد.
طبقهبندی Bispecific Antibody:
در حال حاضر دو طبقهبندی اصلی برای Bispecific Antibodyها مطرح شده است:
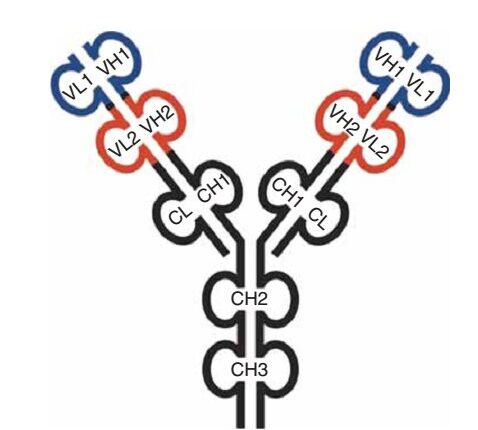
- IgG-like Bispecific Antibody: دارای دومن ثابت ایمونوگلوبولینها میباشند، بنابراین فعالیتهایی که باواسطهی بخش FC رخ میدهد در آنها وجود دارد و همچنین برخی ویژگیهای IgG معمول را دارند اما از لحاظ اندازه و اشکال هندسی با آنها متفاوت هستند (شکل 1).
- Small Bispecific Antibody: آنتیبادیهای نوترکیبی هستند که با تکنیک مهندسی ژنتیک آنتیبادی تولید شدهاند و فاقد دومنهای ثابت میباشند و در درجهی اول بهعنوان عواملی برای فراخوانی سلولهای عملکردی سیستم ایمنی از جمله سلولهای T طراحی شدهاند (شکل 2).
IgG-like Bispecific Antibody پایداری و عملکرد خوبی دارند و بهواسطهی داشتن FC میتوانند باعث القای فرایندهایی مثل سایتوتوکسیسیتی سلولی باواسطهی آنتیبادی (ADCC) و فعال کردن سیستم کمپلمان شوند، همچنین حلالیت و پایداری این آنتیبادیها و نیمهعمر آنها به علت اندازهی بزرگ و همچنین فرایند بازیافت باواسطهی FCRn افزایش مییابد، اما به دلیل اندازهی بزرگ در نفوذ به بافتها دارای محدودیت هستند.
Small Bispecific Antibody به دلیل اندازهی کوچکشان دارای نفوذپذیری بالایی به بافتها هستند، به همین دلیل در درمان تومورهای Solid کارآمد میباشند، اما این آنتیبادیها نیمهعمر کوتاهی دارند و نیاز به کارهای بیشتر در جهت افزایش نیمهعمر سرمی آنها است.
هردوی این آنتیبادیها را میتوان در حجمهای بالا تولید و خالصسازی کرد. در (شکل 1) اشکال متفاوتی از IgG-like Bispecific Antibodyها و در (شکل 2) اشــــکال متفاوتی از Small Bispecific Antibodyها نشان داده شده است.
شکل 1: اشکال متفاوت IgG-like bsAbs
شکل 2: اشکال متفاوت Small bsAbs
طراحی و مهندسی Bispecific Antibody
روشهای طراحی در تولید این آنتیبادیها نقش بسیار مهــمی دارد و تعداد متنوعی Bispecific Antibody با ویژگیهای ساختاری متفاوت ایجاد میکنند. سه ساختار اصلی که در طراحی ساختمانی Bispecific Antibodyها دیده میشود شامل موارد زیر است:
- آنتیبادی کامل که از دو زنجیرهی سنگین مختلف تشکیل شده است (با زنجیرههای سبک متفاوت و یا مشابه)
- آنتیبادی کامل با دومن متغیر اضافه
- قطعات آنتیبادی که فاقد دومین FC هستند مثل diabodies و scFvs
طراحی و مهندسی IgG-like Bispecific Antibody
چهار روش متفاوت برای تولید این دسته از Bispecific Antibodyها وجود دارد:
- Quadroma(hybrid hydromas)
- Knobs into Holes
- CrossMab
- Dual-Variable-Domain Immunoglobulin
Quadroma (hybrid hydromas) .1:
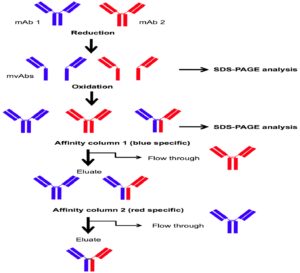
زمانی که در سال 1980 ایدهی تولید Bispecific Antibody مطرح شد اولین راهکار برای تولید آنها Quadroma (hybrid hydromas) بود. تکنولوژی Quadroma شامل ساخت و تولید Bispecific Antibody بهوسیلهی الحاق سوماتیک دو ردهی سلولی هیبریدوما است (سلول هیبریدوما از الحاق سوماتیک یک لنفوسیت B تولیدکنندهی آنتیبادی و یک سلول میلوما حاصل میشود). هر دو سلول هیبریدومای مورد استفاده، یک مونوکلونال آنتیبادی با اختصاصیت متفاوت تولید میکنند و ردهی سلولی Quadromas حاصل از الحاق این دو هیبریدوما طیفی از آنتیبادیها را ترشح میکنـــــــــد که شامل Bispecific Antibody با دو بازوی مجزا نیز میباشد. به علت همراهی تصادفی زنجیرهها در این روش این تکنیک نمیتواند از لحاظ کیفی و کمی Bispecific Antibody موردنیاز برای کاربردهای درمانی یا تشخیصی را فراهم کند زیرا جفت شدن تصادفی زنجیرههای سبک و سنگین ایمونوگلوبولین منجر به تولید کمتر از 1/10 Bispecific Antibody عملکردی میشود، ازاینرو خالصسازی این حجم کم مشکل است. برای غلبه بر این مشکل روش دیگری طراحی شد که در آن از یک کایمریک Quadromas از ردهی سلولی هیبریدومای رت و موش استفاده شد.
کایمریک Quadromas بیانکنندهی آنتیبادیهای کایمریک IgG2b از رت و IgG2a موش است که به سه دلیل از لحاظ تکنیکی بهبود یافته است:
- میزان تولید Bispecific Antibody عملکردی با این روش بیشتر است به علت اینکه همراهی زنجیرههای سبک و سنگین درونگونهای بهصورت حرفهای صورت میگیرد.
- همراهی زنجیرهای سنگین بینگونهای هترولوگ بهصورت مؤثرتری رخ میدهد.
- خالصسازی آنتیبادی به آسانی از طریق افینیتی اختصاصی برای پروتئین A و کروماتوگرافی تعویض یونی انجام میشود.
این روش امکان خالصسازی بهتر و با حجم بالا از Bispecific Antibody را فراهم میکند. اخیراً روش جدیدی به نام Alternative redox بهمنظور بهبود روش قدیمی Quadromas مطرح شده است. در این روش برای تولید سریع Bispecific Antibodyها از عوامل کاهندهی خفیف مثل نمک سدیم 2 مرکاپتو اتانول سولفونیک اسید استفاده میشود. در طول زمان واکنش اکسیداسیون، مخلوطی از آنتیبادیها تولید میشود که شامل آنتیبادیهای مادری و Bispecific Antibodyها هستند. سپس آنتیبادیها بهطور متوالی از دو ستون کروماتوگرافی عبور داده میشوند؛ بدین ترتیب Bispecific Antibodyهایی که با این روش تولید میشوند خلوص بالایی دارند. این آنتیبادیها همچنین ساختار IgG معمول را نیز حفظ کردهاند و با وجود اینکه کایمریک رت و موش میباشند بخش FC در آنها همچنان دارای عملکرد است. به همین دلیل به این آنتیبادیها Trifunctional یا Triomabs گفته میشــود (شکل 3).Bispecific Antibody هایی که با این روش تولید میشوند از لحاظ کاربرد بالینی قدرت بالایی دارند اما مشکل عمدهی آنها ایمونوژنیسیتهی بالا بهواسطهی ماهیت موشی- رتی است. در سال 2009 اولین Bispecific Antibody که در اروپا تأییدیه گرفت، Catumaxomab بود که یک Triomabs Bispecific Antibody است.
شکل 3: مروری بر روش تولی bsAbs با تکنیک Alternative redox
Knobs into Holes .2
پیشرفت در مهندسی آنتیبادیها و تکنولوژی DNA نوترکیب منجر به ایجاد یک راهکار جدید برای تسهیل همراهی زنجیرههای سنــگین در تولید Bispecific Antibodyها به نام Knobs into Holes گردید. این تکنیک بر پایهی ترنسفکشن سلولهای پستانداران با استفاده از ژنهای تغییریافتهی کدکنندهی آنتیبادی انسانی است. از آنجا که در این روش از ژن آنتیبادیهای انسانی استفاده میشود، بنابراین ایمونوژنسیتهی کمی دارد.
اساس این روش جایگزینی یک تک امینواسید در دومن CH3 زنجیرهای سنگین است که هترودایمر شدن زنجیرههای سنگین را ارتقا میدهد. در یکی از زنجیرههای سنگین که بهعنوان Knobs در نظر گرفته میشود یک اسیدامینهی کوچک با یک اسیدامینهی بزرگتر در دومنCH3 جایگزین میشود و در زنجیرهی سنگین مقابل یک آمینواسید بزرگ با یک آمینواسید کوچک جایگزین میشود و یک Hole شکل میگیرد، ایجاد Knob و Hole اجازهی برهمکنش زنجیرههای سبک و سنگین مشابه حالت قفل و کلید را میدهد، علاوه بر این بخش هترودایمر FC نیز از طریق ایجاد پیوند دیسولفیدی در ساختار آنتیبادی ثابت میشود (شکل 4).
میزان همراهی صحیح زنجیرهها با این روش 90% است.
شکل 4: شکل شماتیک از BsAb تولید شده با روش Knobs into Holes
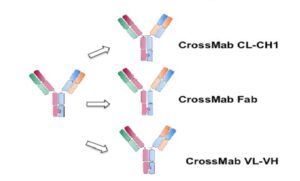
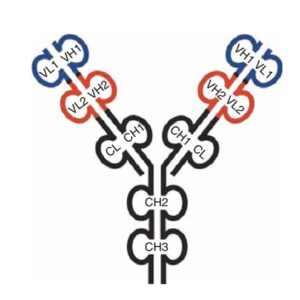
CrossMab .3
زمانی که زنجیرههای سنگین بر اساس روش Knobs into Holes بهدرستی با هم همراه شدند نیاز است زنجیرههای سبک نیز همراهی درستی با یکدیگر داشته باشند که به نظر چالش بزرگی است. روش CrossMab بهعنوان گزینهای است برای اطمینان از همراهی صحیح زنجیرههای سبک در IgG-Like Bispecific Antibody وقتی همراه با تکنیک Knobs into Holes تولید میشوند. در این ساختار یکی از بازوهای آنتیبادی دستنخورده باقی میماند درحالیکه در بازوی زنجیرهی مقابل تغییراتی ایجاد میشود. سه تغییر برای این منظور وجود دارد (شکل 5)، که شامل موارد زیر میباشد:
- تغییر در تمام ناحیهی Fab
- تغییر در ناحیهی متغیر زنجیرهی سبک و سنگین
- تغییر در دومن ثابت زنجیرهی سبک و دومن CH2 در زنجیرهی سنگین
شکل 5: اشکال متفاوت Cross Mab
4. Dual-Variable-Domain Immunoglobulin
روش نوینی برای تولید Bispecific Antibodyها میباشد.
DVDIg Bispecific Antibody از ترکیب دومنهای متغیر دو مونوکلونال آنتیبادی موجود با اختصاصیت متفاوت تولید میشود. دومنهای متغیر دو مونوکلونال آنتیبادی بهصورت پشت سر هم از طریق لینکر الحاق میشود و اجازهی تولید یک dual like IgG اختصاصی داده میشود (شکل 6). DVDIg Bispecific Antibody میل ترکیبی هرکدام از مونوکلونال آنتیبادیها را حفظ میکند و هرکدام از نواحی اتصال به آنتیژن بهطور مستقل عمل کرده و ممانعت فضایی برای یکدیگر ایجاد نمیکنند. این آنتیبادیها قادر به هدفگیری مولکولهای محلول مثل اینترفرونها، اینترلوکینها و کموکاینها علاوه بر مولکولهای سطح سلولی میباشند. با استفاده از این روش میتوان مونوکلونال آنتیبادیها با ماهیتهای متفاوت (انسان، موشی، کایمریک) را نیز با یکدیگر ترکیب کرد. تولید آسان و در حجم بالا و ویژگیهای فارماکوکینتیک مناسب از خصوصیات مطلوب این آنتیبادیها میباشد.
شکل 6: تصویری از DVD-Ig bsAb
طراحی و مهندسی Bispecific Antibodyهای کوچک
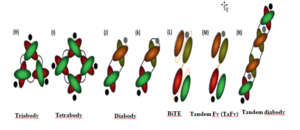
مهندسی ژنتیک آنتیبادیها منجر به تولید قطعات متنوع آنتیبادیها از لحاظ اندازه، طراحی و خصوصیات فارماکوکینتیک شده است که ویژگی ناحیهی اتصال به آنتیژن مربوط به مولکول آنتیبادی کامل را حفظ کردهاند، اما فاقد نواحی ثابت آنتیبادیها میباشند. انواع متفاوتی از Bispecific Antibodyهای کوچک وجود دارد؛ از جمله Triabody،Tetrabody ، diabody، Bispecific Tcell Engager، Tandam Fv و … . دو تا از پرکاربردترین Bispecific Antibodyهای کوچک به اختصار توضیح داده میشود.
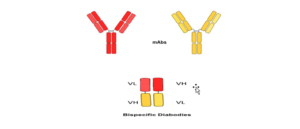
- Diabody: گروهی از Bispecific Antibodyهای کوچک هستند که با تکنولوژی DNA نوترکیب ساخته میشوند و شامل دو دومن متغیر سبک و متغیر سنگین از دو مونوکلونال آنتیبادی متفاوت هستند. در این طراحی هر دومن متغیر سبک بهوسیلهی لینکر پپتیدی کوتاهی به دومن متغیر سنگین از آنتیبادی دیگر متصل میشود (شکل 7). لینکر مورد استفاده باید کوتاه باشد (5 امینواسیدی) و بهگونهای بین دومنهای متغیر سبک و سنگین قرار گیرد که باعث اجبار برای همراهی آنها با دومنهای مکمل آنتیبادی دوم شود. یک Diabody دو ناحیه اتصال برای دو آنتیژن متفاوت دارد و بهراحتی میتوان در باکتریها مثل Ecoli آن را تولید کرد.
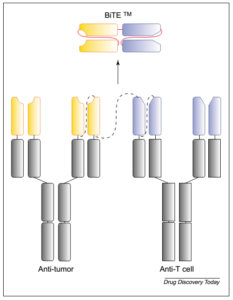
- Bispecific Tcell Engager (BiTE): یکی از مزایای این آنتیبادیها نسبت به دیگر Bispecific Antibodyها توانایی درگیر کردن سلولهای T برای مهار تومور است. BiTEها آنتیبادیهای تکرشتهای هستند که برای فعالیت پلیکلونال و تغییر مسیر سلولهای T سایتوتوکسیک به سمت سلولهای توموری طراحی شدهاند. BiTEها ترکیبی از ScFv دو آنتیبادی مونوکلونال میباشند که بهوسیلهی یک لینکر قابلانعطاف کوتاه به یکدیگر الحاق شدهاند. یکی از بازوها مولکول CD3 (که یک مارکر شناساگر سلولهای T است) و بازوی دیگر آنتیژنهای سلول توموری را شناسایی میکند (شکل 8). BiTE قدرت بالایی برای فعال کردن سلولهای T دارد. برای فعال شدن کامل سلول T باید برهمکنش بین سلول T و آنتیژن سطح سلول هدف باواسطهی BiTE صورت گیرد. اندازهی کوچک BiTE برای برقراری این برهمکنش مناسب میباشد و تضمینکنندهی شکلگیری سیناپس ایمونولوژیک لیتیک بین دو سلول است.
شکل 8: تصویری از یک BiTE
کاربردهای Bispecific Antibody
این Bispecific Antibodyها، هم دارای کاربردهای درمانی و هم دارای کاربردهای تشخیصی میباشند. بیش از بیست Bispecific Antibody مختلف در مرحلهی کارآزمایی بالینی برای بیماریهای مختلف از جمله سرطانها و بیماریهای التهابی میباشند.
- کاربردهای درمانی
مزایای درمانی Bispecific Antibody:
- مسدود کردن یا درگیر کردن همزمان چند ناحیه روی یک یا دو هدف متفاوت که این امر باعث افزایش اختصاصیت و همچنین بهبود جلوگیری از مقاومت به درمان میشود.
- بهبود فعالیتهای عملکردی بر روی سلول هدف از طریق هدفگیری سلولهای اختصاصی ایمنی
- انتقال بهینهی آنتیبادی به بافتهای هدف از طریق هدفگیری پروتئینهای انتقالی
راهکارهای درمانی که بهواسطهی Bispecific Antibody ها اعمال میشود:
- فراخوانی و فعالسازی سلولهای ایمنی
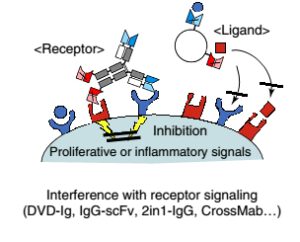
- ممانعت در انتقال سیگنال از طریق اتصال به رسپتورها یا لیگاندهای دخیل در ایجاد سیگنال
- همراهی اجباری کمپلکسهای پروتئینی
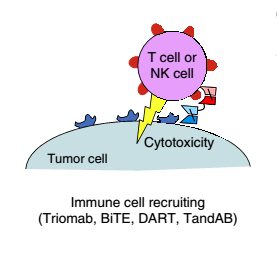
- فراخوانی و فعالسازی سلولهای ایمنی
Bispecific Antibodyهایی مثل Triomab، BITE،DART باعث فراخوانی سلولهای T یا سلولهای NK به ناحیهی توموری میشود. Triomabها میتوانند باعث فراخوانی سلولهای T سایتوتوکسیک به ناحیه و به این ترتیب القای لیز و یا آپپتوز در سلول توموری شوند، از طرفی با هدف قرار دادن سلولهای کمکی مثل ماکروفاژها میتوانند باعث مهار تومور از طریق
شکل 9: فراخوانی و فعالسازی سلولهای ایمنی
فرایندهایی مثل فاگوسیتوز شوند. BITEها میتوانند باعث القای لیز سلول توموری باواسطهی سلولهای T بدون نیاز به مولکولهای MHC و کمک محرک شوند )شکل 9).
مثالهایی در ارتباط با Bispecific Antibody که در درمان مورد استفاده قرارگرفتهاند و یا در مراحل کارآزمایی بالینی هستند در جدول 1 ذکر شده است.
| نام محصول | مولکولهای هدف | ساختار | کاربرد |
| Catumaxomab | CD3-EpCAM
|
Quadroma Ig | از سال 2009 برای درمان بدخیمیهای آسیت استفاده میشود.
در مرحله دو کارآزمایی بالینی برای سرطانهای تخمدان و معده |
| Ertumaxomab | CD3- Her2 | Quadroma Ig | در مرحله دو کارآزمایی بالینی برای سرطانهای پستان متاستاتیک |
| Blinatumomab | CD19-CD3 | BiTE | در سال 2014 برای درمان بیماران لوسمی حاد لنفوئیدی با منشأ سلول B پذیرفته شد.
در مرحله کارآزمایی بالینی برای لنفوم غیرهوچکینی |
2: ممانعت در انتقال سیگنال از طریق اتصال به رسپتورها یا لیگاندهای دخیل در ایجاد سیگنال
Bispecific Antibodyهایی مثل DVDIg با تداخل در رسپتورهای انتقالدهندهی سیگنال یا لیگاندهای مربوط به آنها از انتقال سیگنال جلوگیری کرده و اعمال خود را انجام میدهند. این آنتیبادیها بهطور همزمان دو یا تعداد بیشتری مسیر انتقال سیگنال را در واقع مسدود یا فعال میکنند؛ به این ترتیب مکانیسمهای فرار (این روند در بیماریهای التهابی و سرطانها دیده میشود) را کاهش میدهند و کیفیت درمان را بهبود میبخشند (شکل 10).
شکل 10: ممانعت در انتقال سیگنال از طریق اتصال به رسپتورها یا لیگاندهای دخیل در ایجاد سیگنال
مثالهایی در ارتباط با Bispecific Antibody که از طریق اتصال به رسپتورها یا لیگاندهای دخیل در ایجاد سیگنال اعمال خود را انجام میدهند در جدول 2 ذکر شده است.
| نام محصول | مولکولهای هدف | ساختار | کاربرد |
| MM111 (MerriMack) | Her2-Her3 | Tv-IgGs | مرحله دو کارآزمایی بالینی برای سرطانهای پیشرفته معده و مری |
|
ABT122(Abbvie)
|
IL17-TNF | DVD-Ig | مرحله یک کارآزمایی بالینی برای آرتریت روماتوئید. |
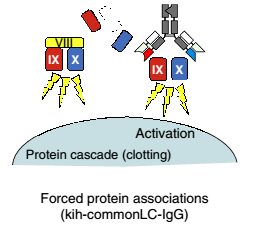
3: همراهی اجباری کمپلکسهای پروتئینی
یکی از کاربردهای درمانی جالب و متفاوت از Bispecific Antibodyها کمک به ایجاد کمپلکسهای پروتئینی توسط این آنتیبادیها میباشد، برای مثــال RG6013 یک Bispecific Antibody Like-IgG است که بهمنظور کنار هم آوردن پروتئینها داخل یک کمپلکس طراحی شده است. این آنتیبادی با یک بازو به فاکتور 9 خونی و با بازوی دیگر به فاکتور 10 خونی موجود در مسیر انعقاد متصل میشود (شکل 11). اتصال این دو فاکتور در افراد نرمال توسط فاکتور 8 صورت میگیرد، در بیماران هموفیلی به دلیل عدم حضور فاکتور 8 این روند مختل میشود. RG6013 با کنار هم قرار دادن اجباری فاکتور 9 و 10 خونی باعث تشکیل این
شکل 11: همراهی اجباری کمپلکسهای پروتئینی
کمپلکس پروتئینی در غیـاب فاکتور 8 خونی و اصلاح روند انعقاد خون میشود. این Bispecific Antibody نیمهعمر سرمی بالایی دارد و در فاز 2 کارآزمایی بالینی در بیماران مبتلا به هموفیلی است و میتواند جایگزین مناسبی بجای مکمل یاری فاکتور 8 در این بیماران باشد.
کاربردهای تشخیصی
علاوه بر کاربردهای درمانی، Bispecific Antibodyها میتوانند کاربردهای تشخیصی نیز داشته باشند و بهعنوان ایمونوپروبهای دو عملکردی در ارزیابیهای تشخیصی به کار گرفته شوند. از مزایای استفاده از Bispecific Antibodyها بهجای مونوکلونال آنتیبادیهای در تشخیص، میتوان به موارد زیر اشاره کرد:
- انعطافپذیری در طراحی و یک مرحلهای شدن انجام مراحل آزمایش
- عدم نیاز به استفاده از آنتیبادی ثانویه و نشاندار کردن آنتیبادی که خود میتواند اثرات مخربی را بر روی آنتیبادی یا آنزیم به دنبال تغییرات شیمیایی ایجاد کند.
استفادهی آسان، سرعت بالا و حساسیت بالای روشهای ایمونـواسی که با استفاده از Bispecific Antibodyها صورت میگیرد باعث تولید Bispecific Antibodyهایی برای تشخیص عفونتهای باکتریال، ویروسی و همچنین تشخیص یکسری بیماریها مثل سرطانها شده است.
- تصویربرداری تشخیص سرطانها
یکی از راهکارهای تشخیصی که توسط Bispecific Antibody اعمال میشود استفاده از آنها بهعنوان سیستمهای انتقالی است که مثالی ازاین گروه تصویربرداری تشخیصی سرطانها میباشد. در این روش Bispecific Antibody برای اتصال به آنتیژن سرطانی و کمپلکسهای پپتید-هاپتن یا radiometal-chelate طراحی میشود. فرایند تصویربرداری دو مرحله میباشد، در مرحلهی اول Bispecific Antibody تزریق شده و به مولکول هدف در سطح سلول توموری متصل میشود. پس از سپری شدن مدت زمان لازم برای پاکسازی آنتیبادیهای اضافی در بدن در مرحلهی دوم هاپتن نشاندار شده با مواد رادیواکتیو اضافه میشود و به بازوی دیگر آنتیبادی متصل شده و تصویربرداری صورت میگیرد. مثالی از این روش Bispecific Antibody TF2 است که به آنتیژن CEA که در اغلب تومورهای Solid از جمله سرطان کلورکتال بیان میشود، متصل شده و از طرف دیگر به یک کمپلکس هاپتن-پپتید که با ترکیبات رادیواکتیو نشاندار شدهاند متصل میگردد و در فاز یک کارآزمایی بالینی برای تصویربرداری در بیماران مبتلا به سرطانهای پیشرفتهی کلورکتال استفاده میشود.
- تشخیص بیماریهای عفونی
کاربرد بعدی در تشخیص بیماریهای عفونی است، از جمله تولید immunoswab برای تشخیص بیماران عفونی با مایکوباکتریوم توبرکلوزیس که امکان تشخیص با استفاده از مایعات مختلف بدن در مدت زمان کوتاه را فراهم میکند (شکل 12). در این immunoswab از یک Bispecific Antibody استفاده شده که با یک بازو به آنتیژن LAM (لیپو آرابینومانان) که در دیواره سلولی مایکوباکتریوم وجود دارد متصل میشود و با بازوی دیگر به مولکول reporter (آنزیم HRPO) متصل میشود.
شکل 12: immunoswab برای تشخیص بیماران عفونی با مایکوباکتریوم توبرکلوزیس
یک تست تشخیصی جدید همچنین برای غربالگری سریع هپاتیت B است که بر مبنای آگلوتیناسیون با استفاده از Bispecific Antibodyابداع شـــــــــــــده است. Bispecific Antibody که بهمنظور غربالگری و تشخیص سریع HBs Ag طراحی شده از یک سمت به HBs Ag و از سوی دیگر به گلبولهای قرمز متصل میشود و در صورت حضور HBs Ag در نمونه، آگلوتیناسیون رخ میدهد (شکل 12). این تست بر روی 712 نمونه انسانی آزمایش شده و دارای اختصاصیت 100% و حساسیت 97/7% بوده است.
شکل 13: تشخیص سریع پروتئین LMP مایکوباکتروم به روش آگلوتیناسیون
منابع:
- Kontermann RE. Dual targeting strategies with bispecific antibodies. mAbs. 2012;4(2):182-97.
- Sarkar S، Tang XL، Das D، Spencer JS، Lowary TL، Suresh MR. A bispecific antibody based assay shows potential for detecting tuberculosis in resource constrained laboratory settings. PloS one. 2012;7(2):e32340.
- Chen Y-P، Qiao Y-Y، Zhao X-H، Chen H-S، Wang Y، Wang Z. Rapid detection of hepatitis B virus surface antigen by an agglutination assay mediated by a bispecific diabody against both human erythrocytes and hepatitis B virus surface antigen. Clinical and Vaccine Immunology. 2007;14(6):720-5.
- Kontermann RE، Brinkmann U. Bispecific antibodies. Drug discovery today. 2015;20(7):838-47.
- Byrne H، Conroy PJ، Whisstock JC، O’Kennedy RJ. A tale of two specificities: bispecific antibodies for therapeutic and diagnostic applications. Trends in biotechnology. 2013;31(11):621-32.
- Tiller KE، Tessier PM. Advances in Antibody Design. Annual review of biomedical engineering. 2015.
- Spasevska I. An outlook on bispecific antibodies: Methods of production and therapeutic benefits. 2014.
Nanobodies تعریف، تولید و کاربرد در پزشکی
متدهای کونژوگاسیون آنتیبادیها و مصارف درمانی آنتیبادیهای کونژوگه شده
برای دانلود پی دی اف بر روی لینک زیر کلیک کنید
ورود / ثبت نام