درباره اهدای خون بیشتر بدانیم
(قسمت سی و نهم)
عوارض انتقال خون- 16

كارشناس ارشد خونشناسی و بانك خون
کارشناس عالی سازمان انتقال خون ایران
safarifardas@ gmail.com
www.shokofanews.blogsky.com
ویروس هپاتیت C
در سال 1974 مطالعه آیندهنگر پیگیری بعد از انتقال خون، شواهد محکمی را ذکر کرد که نشان میداد بیشتر هپاتیتهای وابسته با انتقال خون به ویروس هپاتیت B ارتباطی ندارند. مؤلفان تااندازهای عجولانه نام ویروس هپاتیت C را برای عامل این عفونتها انتخاب کردند. بیماران non B ازنظر اپیدمیولوژی شباهتی به هپاتیت A نداشتند و بعداً نشان داده شد که ازنظر الکترون میکروسکوپی ایمونولوژیکی، هپاتیت A هم نیستند. نامی که عموماً برای این بیماری پذیرفته شد هپاتیت nonA-nonB (NANB) بود. این مسئله نشان داد که بیش از یک عامل میتواند زمینهساز باشد. بعد از 5 سال ناامیدی، اولین کلون مختص به NANB با استفاده از بیان کلون و آنتیبادی انسانی مشخص گردید. ازآنجاییکه توالی این کلون بیگانه بود، نامگذاری کلون ویروس به نام HCV موجه شناخته شد.
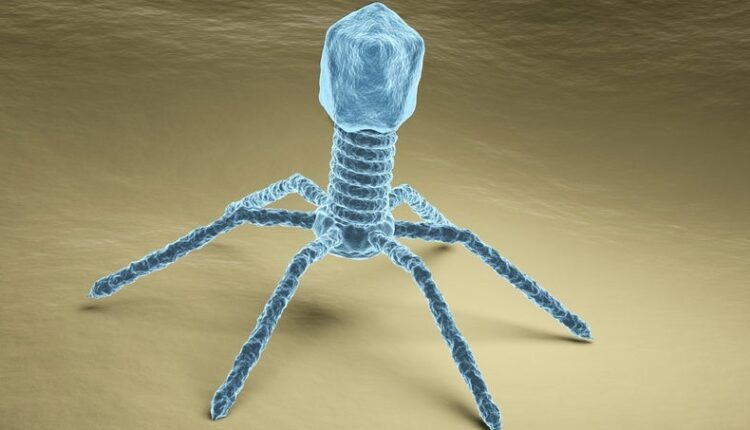
HCV نهایتاً در سال 1989 شناسایی شد. این ویروس دارای 50 تا 80 نانومتر قطر از نوع RNA، پوششدار و تکرشتهای است که ژنوم حدوداً با 9400 نوکلئید دارد و از خانواده فلاوی ویروس میباشد. گرچه وجود عفونت هپاتیت C سالیان سال محرز بوده است، اما این ویروس نهایتاً در سال 1989 شناسایی و مشخص گردید. این ویروس از راههای غیر رودهای و عمدتاً از طریق تزریق مواد مخدر و خون قابل انتقال است. اگرچه هنوز هم تعداد عمدهای از موارد ابتلا مشاهده میشود که مسیرهای غیررودهای در آن به چشم نمیخورد.
در حال حاضر مانند HBV، عفونت هپاتیت C یکی از دو مسیر را طی مینماید: عفونت حاد که هم نسبتاً سریع و هم دورهاش نسبتاً خفیف است و عفونت مزمن که سالیان سال تداوم دارد و موارد بسیاری از آنهم به سیروز و کارسینوهای کبدی میانجامد.
تفاوت اصلی میان هپاتیت B و هپاتیت Cآن است که فقط حدود 20 تا 40 درصد موارد هپاتیت C حاد میباشد و اکثر آنها به عفونت مزمن میانجامد. میزان ناقل بودن از 0/05 تا 0/5درصد در کشورهای با شیوع کم مانند اروپای غربی، آفریقای شمالی و استرالیا متغیر است، این میزان بین 1 تا 5 درصد در بخشهایی از اروپایی جنوبی، آمریکای جنوبی، آسیا و آفریقا متغیراست و در مصر و مناطق خاصی از اروپا و آفریقا به 20 درصد میرسد.
در سال 1974 مطالعه آیندهنگر پیگیری بعد از انتقال خون، شواهد محکمی را ذکر کرد که نشان میداد بیشتر هپاتیتهای وابسته با انتقال خون به ویروس هپاتیت B ارتباطی ندارند. مؤلفان تا اندازهای عجولانه نام ویروس هپاتیت C را برای عامل این گونه عفونتها انتخاب کردند. بیماران مبتلا ازنظر اپیدمیولوژی شباهتی به هپاتیت های A و B نداشتند، بعداً نشان داده شد که ازنظر الکترون میکروسکوپی ایمونولوژیکی، هیچ کدام از آنها هم نیستند. نامی که عموماً برای این بیماری پذیرفته شد هپاتیت nonA-nonB (NANB) بود. این مسئله نشان داد که عوامل ویروسی دیگری هم میتواند زمینهساز هپاتیت باشد. بعد از 5 سال نا امیدی، اولین کلون مختص به NANB با استفاده از بیان کلون و آنتیبادی انسانی مشخص گردید. ازآنجاییکه توالی این کلون بیگانه بود، نامگذاری کلون ویروس به نام HCV موجه شناخته شد.
انتقال HCV
انتقال HCV اساساً از مسیر غیررودهای صورت میگیرد که دربرگیرنده تماس مستقیم با مایعات بدن است. بدین ترتیب شایعترین مسیرهای عفونت عبارتند از:
- تماس با خون آلوده، قرار گرفتن زخم در معرض خون آلوده یا سوزن، سرنگ و چاقوی آلوده برای مثال در محلهای جراحی، تزریق مواد مخدر، خالکوبی، سوراخ کردن گوش و بدن، طب سوزنی یا حجامت
- تزریق خون با فرآوردههای خون آلوده (راه عمده انتقال عفونت در صورت عدم انجام غربالگری)
- پیوند اعضا و بافتها
- انتقال در حین حاملگیها یا در زمان تولد، اما تغذیه از راه شیر مادر بهعنوان منبع انتقال آلودگی شناسایی نشده است. بهنظر میرسد خطر عفونت با میزان RNA در گردش خون حاملگی رابطه مستقیم دارد.
- تماس جنسی و تماس با حیوانات اهلی
گاهی مواردی پیش میآید که در آن مسیر انتقال تعریفشدهای برای عفونت وجود ندارد. در برخی کشورها تا 30 درصد موارد در این مقوله قرار میگیرد، اگرچه در بخشی از آن کاملاً مشخص و محتمل است که یکی از مسیرهای فوقالذکر علت انتقال عفونت هستند، بااینحال مسیر اصلی را نمیتوان بهطور اختصاصی معین کرد.
دوره بالینی عفونت
از نظر بالینی، عفونت حاد HCVمانند عفونت HBV میباشد، اگرچه کمی خفیفتر است. افراد آلوده اغلب در وهله اول با خستگی مواجه هستند و احساس ناخوشی میکنند. برخی عوارض مرتبط با کمپلکسهای ایمنی، آنتیژن– آنتیبادی در گردش خون است. میزان آنزیم کبدی نوساندار (ترانس آمنیاز) که میتوان از آن استفاده کرد تا مشخصه روند فعلی بیماری شناسایی گردد، نشانه عمده عفونت HCV میباشد.
برآورد میشود که در 80 درصد افراد مبتلا به HCV ممکن است عفونت مزمن پیش آید که از میان آنها در 60%، بیماری مزمن به وجود میآید و به مرگومیر ناشی از سیروز یا سرطان کبدی اولیه میانجامد.
ویرمی هپاتیت C که با وجود HCV RNA مشخص میشود. در طول 3-1 هفته بعد از مواجهه رخ میدهد. حدود 90 درصد بیماران سه ماه بعد از عفونت anti-HCV قابل ردیابی هستند. هپاتیت C مزمن در ایالات متحده، سندرم بالینی شایعی است و امروزه شایعترین دلیل پیوند کبد است.
حداقل 70% بیماران افزایش موقتی یا پایدار ALT در پیگیریهای طولانیمدت دارند که با نمونهبرداری از کبد تغییرات التهابی مزمن را نشان میدهد. ویروس با تبدیل مداوم به گونههای متفاوت، پایدار باقی میماند. با ظهور آنتیبادیهای خنثیکننده توسط میزبان یا تغییر ساختاری ویروس، حدود 80% بیماران مبتلا به HCV مزمن بالاخره مبتلا به سیروز میشوند که در 5-1 درصد آنها، حدودا بعد از 20 سال سیروز به سمت کارسینوم سلولی پیشرفت میکند.
هنوز مشخص نشده که چرا 15 درصد آنهایی که به HCV آلوده هستند خودبهخود بهبود مییابند یا چرا بیماران بهطور واضح روندهای بیماری متفاوتی را نشان میدهند.
ارزیابی بالینی
عفونت HCV حاد علائم خفیفتری نسبت به عفونت حاد سایر ویروسهای هپاتیت دارد. در حدود 50 درصد بیماران با عفونتهای HCV حاد، علائم خستگی، بیقراری، کاهش وزن، تهوع، استفراغ و درد شکم دارند که ممکن است بیش از 10 هفته ادامه یابد. بعضی عفونتهای HCV حاد بهطور کامل فاقد علائم هستند. اگرچه هپاتیت فولمینانت کشنده در اثر عفونت با HCV شده است اما بهندرت روی میدهد. در 25 درصد موارد علائم یرقان و ادرار تیره وجود دارد. کبد ممکن است در زمان عفونت HCV حاد، بزرگ و حساس شود.
ارزیابی آزمایشگاهی
افزایش ALT سرم معمول است، اما سطح بالاتر از IU/ml 800 در کمتر از یکسوم بیماران با عفونت HCV حاد دیده میشود. الگوی نوسانی افزایش ملایم ALP معمولترین ناهنجاری بیوشیمیایی در عفونت HCV حاد میباشد، بنابراین تنها با ALT سرم نمیتوان عفونت HCV را تشخیص داد. بیلیروبین مستقیم سرمی معمولاً بالاتر ازmg/dl 10 نمیشود. الگوی مشخصی از یافتههای آزمایشگاهی وجود ندارد که با آن بتوان بهبودی یا عفونت HCV مزمن را پیشبینی کرد. آزمایش قابل دسترس تجارتی که برای آنتیبادی HCV مجوز دارد، EIA میباشد که با استفاده از دو یا چند آنتیژن HCV نوترکیب انجام شود. حساسیت این تست بیش از 97 درصد است اما میزان جواب مثبت کاذب چشمگیری خصوصاً در افراد کمخطر (در اهداکنندههای خون) وجود دارد. میانگین دوره پنجره جهت تشخیص وجود آنتیبادی در سرم با آزمایش EIA نسبتاً طولانی است و EIA معمولاً پس از 70 روز از تماس مثبت میشود. آزمایشهای EIA مثبت باید با آزمایش ایمونوبلات نوترکیب (RIBA) تأئید شود. در RIBA از همان آنتیبادیهای HCV نوترکیب مشابه EIA استفاده میشود ولی نسبت به EIA اختصاصیتر است، زیرا میتواند واکنش آنتیبادی به آنتیژنهای اختصاصی HCV را از واکنش متقاطع کاذب مثبت که در EIA روی میدهد، افتراق دهد.
آزمایش اهداکنندگان با EIA برای هپاتیت C در 1990 به اجرا در آمد. این غربالگری بهطور وسیع سلامت ذخایر خون را بهبود بخشید و بهطور چشمگیری خطر انتقال HCV از راه خون را کاهش داد.
آزمایش RT- PCR برای RNA هپاتیت C بسیار اختصاصی است. این آزمایش براساس اسید نوکلئیک است و زودتر از EIA وRIBA، معمولاً 2-1 هفته پس از آلودگی،HCV را میتوان نشان داد.
RP-PCR مفیدترین روش در تعیین عفونت HCV در شرایط زیر میباشد:
- در طول دوره پنجره قبل از وجود آنتیبادی در سرم
- در نوزادان در حضور anti-HCV مادری که از طریق جفت وارد خون نوزاد شده است.
- در بررسی میزان دوز ویروس HCV بهمنظور ارزیابی مؤثر بودن درمان
بیماران دچار HCV مزمن ممکن است آزمایش RT-PCR آنها بهطور متناوب مثبت یا منفی باشد. در سال 1999 صلیب سرخ آمریکا و دیگر مراکز جمعآوری خون، استفاده از متدهای اسید نوکلئیک را جهت غربال ذخایر خون برای HCV آغاز کردند، روشی که بهطور قطعی انتقال HCV را از طریق خون کاهش داد.
سیتومگالو ویروس (CMV) و سایر هرپسها
سیتومگالو ویروس (CMV)، یکی از هرپسهای انسانی است. همه آنها بهاستثناء ویروس واریسلا، پارازیتهای داخل سلولی انسانی هستند. آنها عفونتهای بدون علامت یا عفونتهای اولیه خفیف ایجاد میکنند و باعث ایجاد عفونتهای نهفته در میزبانشان میشوند. بهطور متناوب میتوانند مجدداً فعال شوند و سایر میزبانهای حساس را آلوده نمایند و در تمام طول عمر باقی بمانند. تا زمانی که سیستم ایمنی میزبان دچار ضعف نشود، تعادل بین ویروس و میزبان برقرار است. با این وجود، سرکوب ایمنی ایجاد شده توسط بیماری یا درمان میتواند تعادل بین ویروس و میزبان را تغییر دهد. درنتیجه عفونت منتشر ویروسی و بهدنبال آن بیماری ایجاد میشود.
توان ایجاد بیماری توسط CMV برای اولین بار در شیرخوارانی که در رحم مادر آلوده شده بودند، شناخته شد. اگرچه عفونتهای CMV پس از تزریق خون اولین بار در سال 1966 توصیف شدند تا سال 1980 مورد توجه نبودند تا اینکه ارتباط بیماری شدید CMV با تزریق خون CMV –Seropositive صراحتاً در شیرخواران نارس مطرح شد.
فراوانی زیاد و پیامدهای شدید عفونت CMV در بیماران دچار نقص ایمنی در بیماران تحت پیوند اعضاء و پیوند مغز استخوان در نیمه و اواخر سالهای 1970 نشان داده شد. برتری نقش اهداکننده عضو در مقابل فرآورده خون در انتقال CMV بهسرعت در موارد پیوند عضو توپر به اثبات رسید.
امکان اینکه خون تزریقشده منشأ CMV در بیماران تحت پیوند مغز استخوان باشد بهتدریج شناخته شد. تأثیر محصولات خون CMV – Seronegative در کاهش خطر عفونت ناشی از تزریق خون در این بیماران بهزودی به اثبات رسید. متعاقباً استفاده از محصولات خون بدون لکوسیت برای کاهش دادن خطر عفونت CMV ناشی از تزریق خون، ابتدا در نوزادان سپس در بیماران تحت پیوند مغز استخوان برقرار شد. پیشرفتهایی در مهار عفونتهای CMV ناشی از تزریق خون بدست آمد ولی یک حد پایینی از خطر مهارنشدنی در بیماران تحت پیوند مغز استخوان باقی ماند. مراقبت مؤثر برای عفونتهای اولیه CMV، با استفاده از آزمونهای آزمایشگاهی حساس مانند آزمون آنتیژن PP65 و دسترسی به عوامل ضدویروسی مؤثر، ازکارافتادگی و مرگومیر برای این گروه از بیماران را کاهش داد، بااینحال هدف نهایی پیشگیری است و با توجه به انواع تحقیقات در حال انجام روی نهفتگی CMV، روشهای مولکولی برای تشخیص CMV و پیشرفت در فنآوری غیرفعالسازی ویروس، یقیناً این هدف بدست خواهد آمد.
خانواده ویروس هرپس انسانی
خانواده ویروس هرپس انسانی Human Herpes Virus (HHV) شامل هشت گونه میباشد که بر اساس شباهت در ساختمان ژنوم، توالی ثابت اسید نوکلئیک، ژنها و خواص بیولوژیکی سه زیر خانواده آلفا هرپسویریده شامل ویروس سیمپلکس و ویروس واریسلا، بتا هرپسویریده شامل سایتومگالو ویروس و ویروس روزئولا و گاما هرپسویریده شامل لنفوکریتپو ویروس و رادینو ویروس میشود. بیشتر اعضاء دارای نامهایی هستند که بهطور معمول به کار برده میشوند مثل سایتومگالو ویروس(CMV)، بهعلاوه نامگذاری دیگری نیز بهصورت HHV طبق راهنمای کمیته بینالمللی طبقهبندی ویروسها طراحی شده است، (مثلاً نام دیگر سیتومگالو ویروس HHV-S میباشد).
خصوصیات مشترک تمام هرپس ویروسها برخورداری از DNA دو رشتهای 120-230Kb نوکلئوکپسید ایکوزا هدرال (که ژنوم را احاطه میکند) و پوشش لیپیدی حاوی گلیکوپروتئین ویروسی است.
ویروس بالغ تقریباً 200 نانومتر قطر دارد (دامنه آن 300-120 نانومتر است) که از سلولهای آلوده آزاد میشود. هرپس ویروسها از نظر خواص بیولوژیکی مانند توانایی رشد لیتیک و نهفتگی با یکدیگر تشابه دارند. در طول رشد لیتیک، بیان ژن ویروس بهصورت فعال بهوقوع میپیوندد و نسل جدید ویروسی به دنبال انهدام سلول میزبان تولید میشود. در مقابل، عفونت نهفته از طریق حفظ ژنوم ویروس در سلول میزبان سالم بدون بیان ژنهای ویروسی فاز لیزکننده و بدون همانندسازی ویروس مشخص میشود. ویروس در مرحله نهفتگی ممکن است فعال شده و وارد فاز لیتیک گردد. هرپس ویروسها در ویژگیهای گونهای، تروپیسم سلولی و اثرات بیماریزایی فرق دارند.
در این مقاله در مورد هرپس ویروسهای انسانی با تأکید بر روی ویروسهای متمایل به گلبولهای سفید (بهطور اولیه CMV) بحث میشود که انتقال آن از طریق انتقال خون یا پیوند با عواقب بالینی چشمگیری مرتبط میباشد.
بهطورکلی اهمیت هرپس ویروس در طب انتقال خون به عوامل زیر نسبت داده میشود:
- شیوع ویروس در لکوسیتهای اهداکنندگان خون سالم
- درصد گیرندههای خون که سرم منفی (سرونگاتیو) میباشند.
در میان میزبانهای دارای سیستمهای ایمنی کارا، CMV مانند بسیاری از هرپس ویروسهای دیگر موجب بروز بیماری میشود. بااینحال در میان افراد دارای سرکوب ایمنی، این ویروسها میتوانند بهطور قابلتوجهی موجب مرگومیر و معلولیت شوند. هرپس ویروسها این قابلیت را دارند که در بافتها بعد از عفونت حاد بهصورت نهان باقی بمانند.
برخلاف برخی هرپس ویروسها مانند هرپس سیمپلکس و ویروس واریسلا که دارای بیان محدود در بافتها است، CMV از بسیاری از اعضاء مختلف، مدفوع و ترشحات و همچنین از فرآوردههای خون ذخیره شده دارای مواد ضد انعقاد و یا تازه، قابل جدا شدن است. با گسترش پیوند عضو و سرکوب ایمنی در درمان بیماران بدخیم، عفونت CMV به مشکلی عظیم بدل شده است و خصوصیات اپیدمیولوژیک آن بهتدریج در حال روشن شدن است.
ویروس هرپس سیمپلکس 1 و2 (HHV1,2)
ویروس هرپس سیمپلکس 1 و 2 گونههای ویروسی مجزایی هستند که توسط ژنومهای خطی نسبتاً بزرگ حدود kb 150 کد میشوند. ویروس هرپس سیمپلکس 1 که بهوسیله تماس با ویروس از مایع تاول دهانی منتشر میشود در سنین اولیه در زندگی کسب میشود و میزان 80 درصد افراد در سن بلوغ از نظر سرمی مثبت میباشند. در مقابل، ویروس هرپس سیمپلکس 2 معمولاً در طی تماس جنسی از مایع تاول در نواحی مقعدی– تناسلی کسب میشود. میزان افرادی که از نظر سرمی مثبت میباشند تا سن بلوغ کم است. در بیشتر مناطق ایالات متحده آمریکا 10 تا 60 درصد بزرگسالان نسبت به ویروس هرپس سیمپلکس 2 سروپوزیتیو هستند.
درحالیکه این دو ویروس بهخوبی مطالعه شدهاند اما هیچ مدرکی مبنی بر انتقال آنها از طریق خون یا پیوند اعضا که از نظر بالینی اهمیت داشته باشد وجود ندارد. این ویروسها بهطور مؤثری سلولهای تکهستهای خون محیطی (PBMCS) را آلوده نمیکنند، در بیماران با بیماری منتشر و ویرمی، ویروس هرپس سیمپلکس مرتبط با پلاکت ممکن است یافت شود، بههرحال این افراد به دلیل وجود علائم بالینی واضح، در هنگام غربالگری اهداکنندگان از اهدای خون معاف میشوند، بهعلاوه بیشتر دریافتکنندگان خون نسبت به ویروسهای هرپس سیمپلکس 1 و2، ایمن هستند.
به دلیل اینکه شواهدی مبنی بر انتقال از را تزریق خون وجود ندارد، فرآوردههای خون استاندارد برای انتقال قابلقبول میباشند.
ویروس واریسلا – زوستر (HHV-3)
ژنوم واریسلا زوستر (VZV) حدود kb125 طول دارد و حامل 70 ژن است که پلیپپتیدهای شناخته شده ویروسی را کد میکنند.
عفونت VZV بهطور اولیه باعث واریسلا (آبله مرغان) میشود. حداکثر شیوع VZV در اوایل کودکی است و 95 درصد جمعیت تا سن 18 سالگی سروپوزیتیو هستند. پس از عفونت، ویروس معمولاً بهطور مادامالعمر بهصورت نهفته باقی میماند اما در افراد مسن یا بیماران دچار ضعف ایمنی،VZV میتواند مجدداً فعال شود و باعث هرپس زوستر (زونا) شود.
واریسلا زوستر از طریق سطوح مخاطی دستگاه تنفسی میزبان وارد میشود، سپس به ندولهای لنفاوی راه مییابد. تکثیر ویروس باعث ویرمی اولیه میشود و در انتهای دوره کمون ویرمی ثانویه روی میدهد و در طی این زمان VZV را میتوان از سلولهای تکهستهای خون محیطی جدا نمود.
تظاهرات مشخصه ویروس در پوست بهصورت راش وزیکولر است، سپس ویروس در گانگلیونهای ریشه خلفی عصب بهصورت نهفته درمیآید. در انتهای دورهی کمون، VZV را میتوان در 0/01 تا 0/001 درصد سلولهای تکهستهای خون محیطی (PBMCS) شناسایی کرد، اما متعاقب 24 تا 72 ساعت بعد ویروس حذف میشود. بههرحال انتقال گذرای VZV از راه تزریق خون از طریق این سلولها مسئله بالینی نیست زیرا بیشتر افرادی که به واریسلای حاد مبتلا میشوند سن کمی دارند و واجد شرایط انتقال خون نیستند. از طرف دیگر بیشتر گیرندههای انتقال خون نیز ایمن هستند.
از آنجایی که هیچ مدرکی مبنی بر انتقال از راه تزریق خون وجود ندارد، فرآوردههای خونی استاندارد برای تزریق خون قابلقبول است.
ویروس ابشتاینبار (HHV-H)
ژنوم ویروس ابشتاینبار (EBV) حدودkb 172 طول دارد. دو واریـــــته بهطور اولیه وجود دارد؛ 1-EBV و 2-EBV که شباهتهای نوکلئوتیدی وسیعی با هم دارند و میتوانند با یکدیگر نوترکیب شده و گرادیان بیولوژیکی از واریانتهای ویروسی را تشکیل دهند.
EBV از طریق تماس نزدیک منتقل میشود و بر اساس تحقیقات سرولوژیک بیشتر جمعیت بزرگسال (بیش از 90 درصد) آلوده هستند. درحالیکه عفونت اولیه EBV بهطور عمده فاقد علائم است.EBV میتواند سبب منونوکلئوزعفونی (IM) حاد شود.EBV بهعنوان عامل اتیولوژیک تعدادی از بدخیمیها شناخته شده است ازجمله اختلال لنفوپرولیفراتیو پس از پیوند (PTLD)، لنفوم بورکیت، کارسینومای نازوفارنژیال و بیماری هوچکین.
درحالیکه EBV میتواند در سلولهای اپیتلیال مخاطی عفونت لیتیک ایجاد نماید، در لنفوسیتهای B غالباً بهصورت نهفته باقیمیماند. 11 ژن ویروسی در طول عفونت نهفته در لنفوسیت B بیان میشوند. مکانیسمهای تنظیمی، سلول B را منهدم کرده و منجر به تکثیر پلیکلونهای لنفوسیت B میشوند که در IM این روند مشاهده میشود. هرچند پاسخ ایمنی سلولی میزبان درنهایت تکثیر لنفوسیتها را کنترل میکند، EBV در یک از 105 تا 106 سلول B افراد با سیستم ایمنی سالم به حالت نهفته پایدار باقی میماند.EBV نهفته بهطور پراکنده درون سلول B مجدداً فعال میشود و باعث آزادسازی ویروسهای تکثیرشده میشود. سیستم لنفوئیدی احتمالاً مخزن واقعی این ویروس میباشد.
چندین سال است که مشخص شده EBV از طریق خون انتقال مییابد. اولین بار منونوکلئوز عفونی پس از انتقال خون به افراد گیرنده سرونگاتیو آشکار شد. این افراد بر اثر تزریق خون افراد سروپوزیتیو از نظر EBV، بیماری مشابه به منونوکلئوز عفونی کلاسیک را نشان دادند. در بیشتر این موارد اهداکنندههای خون در دورهی کمون IM قرار داشتند و میزان ویروس در لنفوسیتهای B آنها زیاد بود. اخیراً از تعیین ژنوتایپ ویروسی بهعنوان سندی جهت اثبات انتقال EBV از اهداکنندههای خون به دریافتکنندههایی که بعدها دچار اختلال لنفوپرولیفراتیو پس از پیوند (PTLD) ناشی از EBV شدند، استفاده شد.EBV همچنین میتواند از طریق پیوند اعضا انتقال یابد. بهطورکلی گیرندههای سرونگاتیو از نظر EBV که دچار نقص ایمنی هستند هنگامیکه عضو پیوندی یا خون سروپوزیتیو دریافت میدارند در معرض بیشترین خطر برای ابتلا به بیماریهای لنفوپرولیفراتیو سریعاً پیشرونده سلول B مرتبط با EBV مثل PTLD میباشند. PTLD میتواند شامل محدودهای از اختلالات هیپرپلازی پلیکلونال لنفوئیدی خوشخیم سلول B تا لنفوم بدخیم غیرهوچکین با درجه بالا باشد.
اگرچه تاکنون مطالعات کنترل شده گزارش نشده است، کاهش لکوسیتهای فرآوردههای سلولدار خون به احتمال زیاد باعث کاهش بروز عفونت EBV منتقله از طریق تزریق خون در افراد سرونگاتیو در معرض خطر از قبیل گیرندههای دچار ضعف ایمنی و سرونگاتیو پیوند کبد یا دیگر افراد دچار ضعف ایمنی میشود. در این حالت، واحدهای خون سرونگاتیو از نظر EBV ممکن است مؤثر باشد، اما بهطور معمول قابل دسترس نمیباشند.
الگوی عفونت سیتومگالوویروس
تمایز میان عفونتهای CMV که از طریق تغییرات سرمی یا جدا کردن ویروس و بیماری CMV شناسایی شده، در تفسیر بسیاری از مطالب علمی در زمینهی عفونت CMV متعاقب تزریق خون حائز اهمیت است. بیماری سیتومگالوویروس بهعنوان یک شاهد آزمایشگاهی به عفونتی اطلاق میشود که عوارض معین خاص این ویروس در فقدان پاتولوژیهای آسیبرسان دیگر یا بیماری زمینه وجود داشته باشد. تظاهر بالینی CMV متعاقب تزریق خون از سندرم منونوکلئوز هتروفیل منفی تا بیماری منتشره گسترده است. لنفودنوپاتی، لنفوسیتوز، تب و فارنژیت به همراه هپاتیت، تشکیلدهنده سندروم شبیه به منونوکلئوز است.
پنومونی، ترومبوسیتوپنی، آنمی همولیتیک، مننگوآنسفالیت و پلینوروپاتی از دیگر یافتههای مرتبط میباشند. افراد دارای ایمنی سرکوبشده دارای طیف گستردهای از عوارض و علائم مرتبط هستند. این علائم و عوارض عبارت است از یافتههایی که ذکر شدند و همچنین رتینیت، کولیت، گاستریت، نفریت، راش، پس زدن پیوند کلیه و آترواسکلروزیس قلب پیوندی.
عفونت اولیه
عفونت اولیه در دریافتکنندگان سرم منفی بهوسیله تزریق خون یا پیوند عضو از اهداکنندگانی که دارای عفونت فعال یا نهفته هستند، اتفاق میافتد. عفونت اولیه همچنین در نتیجه عفونت طبیعی سرایتیافته از طریق جامعه در میان کودکان و نوجوانان بدون آثار و علائم حادث میشود. در عفونت اولیه، ویرمی، ویرواوری (وجود ویروس در ادرار Viruria) و واکنش آنتیبادی اختصاصی IgM و سپس واکنش آنتیبادی اختصاصی IgG رخ میدهد.
Zanghe lini و همکاران با مطالعه عفونت CMV اولیه بدون آثار و علائم در میان نوجوانان به مثبت شدن CMV PCR، گلبولهای سفید خون جدا شده در 75 تا 80 درصد آنها طی 16 هفته پس از عفونت پی بردند. این آمار بعد از 48 هفته به صفر تا 25 در صد کاهش یافت.
بعد از 6 تا 8 هفته، آنتیبادی IgG نسبت به CMV gB و آنتیبادی خنثیکننده مشاهده شد. اوج تکثیر لنفوسیتها نسبت بهCMV (24 هفته بعد از تزریق خون) و نسبت به gB )48 هفته بعد از عفونت) سه الی چهار برابر کمتر از میزان در بزرگسالان سالم دارای نتایج سرم مثبت بود. انتشار ویروس در ادرار حدوداً به 90 تا 100 درصد در تمام نمونهها در 36 هفته اول بعد از تزریق خون بود. بعد از 48 هفته viruria ( وجود ویروس در ادرار) در 40 تا 50 درصد نمونههای ادرار نوجوانان مشاهده شد. علیرغم واکنشهای آنتیبادی نسبتاً شدید و سریع، viruria و ویرومی تا ماهها بعد از تغییرات سرمی از بین نرفتند .
عفونت CMV اولیه ناشی از تزریق خون، موضوع بررسیها و مطالعات بسیاری بوده است. در بسیاری از این مطالعات، میزان تغییرات سرمی بهتنهایی جهت محاسبه میزان خطر عفونت ناشی از واحدهای خون سرم مثبت اهداکنندگان مورد استفاده قرار گرفت. این میزان بروز محاسبهشده بر اساس گروه بیماران و سال مطالعه تغییرات گستردهای پیدا کرده است. میزان بروز عفونت CMV اولیه متعاقب تزریق خون 10 تا 50 درصد گزارش شده است. در مورد بیماران دارای ایمنی سرکوبشده مانند نوزادان کموزن، نشانگر میزان بروز عفونت CMV از 2 تا 32 درصد و همراه با مرگومیر و معلولیت است. نوسان در میزان بروز عفونت به مثبت شدن سرم اهداکننده، تعداد تماس با اهداکننده، مقدار خون تزریق شده و طول عمر خون، نسبت داده شده است.
تعیین خطر واقعی CMV متعاقب تزریق خون در میان دریافتکنندگان پیوند و بهتبع میزان بالای شیوع عفونت در میان اهداکنندگان و دریافتکنندگان پیچیده شده است. در مطالعاتی که در آن افراد سرم منفی دریافتکننده پیوند از اهداکنندگان عضو سرم منفی تحت تزریق فرآوردههای خون CMV سرم منفی یا سرم مثبت قرار گرفتهاند، میزان بروز عفونت CMVو آمار مرگومیر و معلولیت زمانی که اهداکنندگان خون سرم مثبت بودهاند بهطور چشمگیری بالاتر بوده است. میزان بروز عفونت CMVدر میان دریافتکنندگان سرم منفی پیوند مغز استخوان که عضو پیوندی سرم منفی داشتهاند متعاقب تزریق فرآوردههای خون از 25 تا 65 درصد از نظر CMV سرم مثبت شدهاند، درحالیکه متعاقب تزریق فرآوردههای خون سرم منفی این آمار صفر تا 18 درصد بود. در یک مطالعه دیگر در مورد عفونت CMVناشی از تزریق خون در میان افراد سرم منفی دریافتکننده پیوندهای قلب از اهداکنندگان سرم منفی، 1 مورد از 5 مورد که خون غربالگری نشده دریافت کرده بوند به عفونت CMV مبتلا شدند، در مقابل هیچیک از 8 دریافتکننده پس از دریافت خون غربالگری شده به عفونت CMV مبتلا نشدند.
عفونت ثانویه
عفونت ثانویه میتواند بهصورت فعال شدن مجدد یا عفونت همزمان رخ دهد. فعال شدن مجدد ویروس نهفته در دریافتکنندهای که قبلاً CMV سرم مثبت بوده و از خون یا عضو اهداکننده سرم مثبت یا سرم منفی استفاده کرده، رخ میدهد. عفونتهای مجدد فعالشده با افزایش چهار برابر یا بیشتر در تیتر CMV IgG و ریزش ویروس همراه است. واکنش IgM گاهی اوقات آشکارمیشود. ریزش ویروس بدون افزایش واکنش آنتیبادی IgG یا IgM قابل رخ دادن است. عفونت مجدد که عنوان بهتر آن عفونت همزمان است در بیمار سرم مثبت که در معرض گونهای از CMV متفاوت از گونه ایجادکننده عفونت اولیه قرار گرفته رخ میدهد. در این وضعیت واکنش آنتیبادی IgM، ریزش ویروس و واکنش آنتیبادی CMV IgG رخ میدهد.
عوامل زمینهسازی که در اهداکننده و دریافتکننده به عفونت میانجامد
تمام واحدهای سرم مثبت اهداکنندگان قادر به ایجاد عفونت نیستند. عوامل زمینهای اهداکننده و دریافتکننده، برخی دریافتکنندگان را در معرض عفونت CMV متعاقب تزریق خون و برخی از اهداکنندگان را مستعد انتقال این ویروس سلولی مینماید. در مطالعات سرم اپیدمیولوژیک مشخص شد که عفونت CMV متعاقب تزریق خون با تزریق تمامی فرآوردههای سلولی خون مرتبط است. به غیر از فرآوردههای پلاسمایی، آنتیبادی ضد CMVدارای تیتر زیاد بهصورت هایپر ایمونوگلوبولین CMV یا ایمونوگلوبولین وسیعالطیف داخل وریدی (IVIG) سبب محافظت در برابر CMV میشود و بهطور پروفیلاکتیک جهت مراقبت از دریافتکنندگان تزریق با نتایج متغیر مورد استفاده قرار میگیرد. مشخص نیست که آیا پلاکتها به نسبت گلبولهای قرمز راحتتر CMV را انتقال میدهند یا خیر.
کاهش لکوسیتها از طریق شستن خون موجب کاهش CMV شده و دگلیسرینه کردن (گلیسرولزدایی) خطر انتقال CMV را به صفر میرساند، حتی اگر گلبول قرمز از نظر CMV سرم مثبت باشد. فیلترهای کاهشدهنده لکوسیت در این زمینه مؤثرتر میباشند.
خصوصیات سرواپیدمیولوژیک این ویروس به همراه کاهش یا پیشگیری CMV با استفاده از فرآوردههای Leukoreduction (کاهش گلبولهای سفید داده شده) بدین معناست که CMV در گلبولهای سفید تجمع مییابد. Schrier و همکاران، RNA CMV را در سلولهای تکهستهای موجود در گردش خون با استفاده از پروب هیبریداسیون منحصر به پروتئین IE شناسایی کردهاند. این پروبها از این جهت انتخاب شدند که در اوایل عفونت احتمال نسخهبرداری وسیع آنها وجود داشته باشد. علاوه بر این، این گروه از طریق فلوسایتومتری ثابت کردند که 24 درصد سلولهای هیبریدکننده CMV همانا سلولهای CD4مثبت هستند، درحالیکه 0/8درصد آنها را سلولهای CD8 مثبت تشکیل میدهد و این نشان میدهد که لنفوسیتها منبع اصلی CMV میباشند. تکنیک PCR هم در بررسی CMV، هم در بیماران پیوندی و هم اهداکنندگان خون سالم استفاده شده است.
نهفتگی CMV و سیر طبیعی عفونت CMV
CMV یک عامل عفونی بسیار تکامل یافته است. با وجود خاصیت تداوم دفع ویروس پس از عفونت اولیه و قابلیت ایجاد عفونت نهفته همراه با دورههای فعالیت مجدد، CMV توانایی انتشار خود را به حداکثر میرساند. CMV هم از طریق طولی از مادر به کودک متولدشده و یا نوزاد و هم بهطور عرضی از طریق تماس با مایعات بدن، تماس جنسی، پیوند عضو و تزریق خون انتقال مییابد.
مظنون بودن به اینکهCMV میتواند توسط لکوسیتهای موجود در محصولات خون انتقال یابد به مدت طولانی مطرح بوده است. ارتباط انتقال توسط اهداکنندگان آنتیبادی مثبت، قویاً در سال 1980 ثابت شده است، با این وجود هنوز این نکته که آیا همه اهداکنندگان آنتیبادی مثبت میتوانند عفونت را انتقال دهند یا اینکه عفونتزایی محدود به گروهی از اهداکنندگانی است که تجربه عفونت اولیه یا عفونت مجدد فعالشده را دارند، نامعلوم است. شواهد ضمنی به نفع فرضیه قبلی است زیرا میزان بالای عفونت در نوزادان تحت تعویض خون، گیرندگان خون کامل تازه و بیماران تحت تزریق خون و گرانولوسیتها دیده شده است.
سایر متغیرهای وابسته به اهداکننده در انتقالCMV شامل نوع فرآوردههای خون تزریق شده و عمر فرآورده خون است. درحالیکه محصولات خون حاوی سلول مانند خون کامل، گلبولهای قرمز، پلاکتها و گرانولوسیتها در ارتباط با انتقال CMV هستند، مدارکی مبنی بر دخالت پلاسمای تازه منجمد در عفونتهای CMV مرتبط با انتقال خون منتشر نشده است.
میزان بسیار بالای عفونت CMV مرتبط با انتقال خون در مطالعات آیندهنگر انجام شده روی بیماران تحت جراحی قلبی نیز مطرح کننده این نکته است که خون تازه ممکن است نسبت به خون ذخیره شده عفونتزایی بیشتری داشته باشد، گرچه این نکته هرگز توسط مطالعات کنترل به اثبات نرسیده است.
انتقال CMV از طریق تزریق خون تحت تأثیر عوامل مختلفی است؛ بهطور آشکار ویروس عفونتزا، آزاد یا وابسته به سلول و یا سلولهای با آلودگی نهفته در خون اهداکننده وجود داشته باشد. بهطور نظری یک ویروس یا سلول با آلودگی نهفته کافی خواهد بود ولی در حال حاضر مقدار عفونیکننده ویروسی خارج از سلول یا سلولهای با آلودگی نهفته ناشناخته است. اگر سلولهای دارای آلودگی نهفته وسیلهای برای انتقال باشند آنها باید برای فعال شدن ویروس و آزاد شدن ویروس به مدت کافی در گیرنده زنده بمانند.
اگر اهداکنندگانی که اخیراً آلوده شدهاند منشأ عفونت باشند، آنها ممکن است ویرمی در حد کم و یا تعداد بیشتری از سلولهای با آلودگی نهفته نسبت به اهداکنندگان سروپوزتیو که در زمان دورتری آلوده شدهاند داشته باشند. به علت اینکه لکوسیتها بهصورت یکنواخت در فرآوردههای خون توزیع نشدهاند، هم نوع و هم تعداد فرآوردههایی که یک بیمار دریافت میکند، میزان خطر را تحت تأثیر قرار میدهد. عوامل مربوط به گیرنده که در انتقال نقش دارند شامل میزان همخوانیHLA بین اهداکننده و گیرنده، سرکوب ایمنی به علت اقدامات درمانی یا بیماریها و وضعیت سیتوکین در گیرنده است.
بیمارانی که در معرض خطر شدید ازکارافتادگی و مرگ ناشی از CMV مرتبط با انتقال خون شناخته میشوند عبارتند از: نوزادان بهخصوص نوزادان نارس، زنان باردار، بیماران تحت پیوند اعضاء توپر، بیماران تحت پیوند مغز استخوان، بیماران آلوده بهHIV و بیماران مبتلا به بدخیمی
مقدمهای بر عفونتهای ویروسی دستگاه گوارش
اندیکاسیون تزریق خون و فرآوردههای خونی در بیماران مبتلا به سرطان
برای دانلود فایل pdf بر روی لینک زیر کلیک کنید
ورود / ثبت نام