چالشهای آزمایشگاهی در سنجش مارکرهای سرطانی
(قسمت اول)
سارا کهن مظفری کارشناس ارشد ژنتیک پزشکی
دکتر حبیبالله گلافشان
محمد اسماعیل خدمتی کارشناس ارشد بیوشیمی
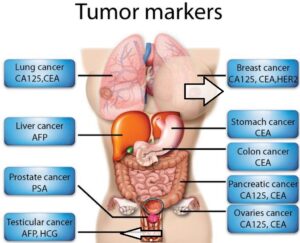
مارکرهای سرطانی مولکولهایی هستند که توسط سلولهای سرطانی و یا دیگر سلولهای بدن در پاسخ به سرطان و گاهی در برخی از موارد خوشخیم تولید میشوند. بیشتر مارکرهای توموری توسط سلولهای نرمال نیز ساخته میشوند، ولی غلظت توموری این مارکرها به بیشتر از چندین برابر سطح نرمال در طی مرحله پیشرفت سلولهای سرطانی میرسد، در حالی که در شرایط غیرسرطانی غلظت این مارکرها پایین است. علاوه بر خون این مارکرها در ادرار، مدفوع و مایعات دیگر بدن بیماران یافت میشوند. تاکنون بیشتر از ۲۰ نوع مارکر توموری برای تشخیص و پیگیری درمان در سرطانها شناخته شدهاند ولی هنوز هیچ تومور مارکر اختصاصی برای یک سرطان مشخص وجود ندارد. از نظر تئوری هر نوع مولکول زیستی میتواند بهعنوان مارکر توموری باشد ولی در عمل بیشترین مارکرهای توموری از جنس پروتئین یا گلیکوپروتئین هستند.
موارد استفاده بالینی از مارکرهای توموری
- غربالگری یک جمعیت سالم یا جمعیت در معرض ابتلای بالا به سرطان
- تشخیص سرطان
- ارزیابی پیشآگهی بیماران
- ارزیابی پاسخهای درمانی در بیماران در حین مداوا
- پیگیری بهبودی بیمار که تحت درمان با جراحی، اشعه و یا شیمیدرمانی قرار گرفته است.
شناسایی مارکرهای سرطانی نهتنها در تشخیص کمککننده است، بلکه در پیگیری درمان نیز کاربرد دارند
غربالگری و تشخیص اولیه سرطان
اولین بار این نشانگرهای توموری در بیماران سرطانی فاقد علائم معرفی شدند، ولی تعداد بسیار کمی از آنها ما را در رسیدن به این هدف یاری کردهاند. در حال حاضر گستردهترین مارکر مورد استفاده در آزمایشگاههای بالینی آنتیژن اختصاصی پروستات (PSA) است.
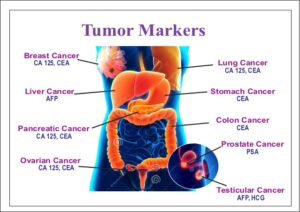
| بیماریهای بدخیم و ارتباط با مارکرهای توموری خاص | |
| مارکر | مورد استفاده در |
| PSA | کارسینومای پروستات |
| CA-125 | کارسینومای تخمدان و لولههای فالوپ |
| AFP | کارسینومای هپاتوسلولار و تومورهای سلولهای زایا |
| CEA | کارسینومای کولورکتال، گوارش، پانکراس، ریه و پستان |
| CA-19-9 | کارسینومای پانکراس و کلانژیوکارسینوما |
| 2Mβ | مالتیپل مایلوما، لنفوما و نئوپلاستهای سلولهای ردهی B |
| hCGβ | کوریوکارسینوما و کارسینوم بیضه |
| Bombesin | سرطان سلول کوچک ریوی |
| CA-15-3 | سرطان پستان |
| CA-72-4 | سرطان معده |
| CA-549 | سرطان پستان |
| CA-M26 | سرطان پستان |
| Calcitonin | کارسینومای مدولاری تیروئید |
| c-erbB oncoprotein | کارسینومای پستان |
| Chromogranin A | فئوکروموسیتوما، نوروبلاستوما |
| CYFRA-21-1 | کارسینومای سلولهای پوششی ریه |
| DHEA | سرطان هیپوفیز- آدرنال |
| Galactosyltransferase | سرطان تخمدان |
| Galactosyltransferase isoenzyme II | سرطان پانکراس |
| Gastrin | تومورهای پانکراس یا دوازدهه، سندرم زولینجر الیسون |
| Her2/neu | کارسینومای پستان |
| Inhibin | تومورهای سلول گرانولوزا |
تشخیص سرطان
مارکرهای توموری استاندارد طلایی تشخیص در سرطان نیستند و هنوز تشخیص تنها با انجام بیوپسی در بیشتر بیماران مشکوک به سرطان انجام میشود. آلفافیتوپروتئین مثالی از این تومورمارکرهاست که در تشخیص سرطان بهخصوص کارسینوم هپاتوسلولار استفاده میشود. اگرچه سطح این مارکر در بیماریهای کبدی نیز افزایش مییابد، ولی هنگامی که به یک حد خاص برسد نشانه کارسینومای هپاتوسلولار است.
برخی از انواع سرطان سرعت رشد و گسترش بیشتری نسبت به بقیه دارند و برخی نیز پاسخ درمانی بهتری از خود نشان میدهند و بنابراین سطح این مارکرهای توموری در تعیین نوع رفتار و پاسخ به درمان این سرطانها کمککننده است؛ برای مثال در سرطان تهاجمی بیضه افزایش سطح hCG و آلفافیتوپروتئین نشاندهنده سرطان پیشرونده با شانس بقای کم است.
پاسخ به درمان نیز میتواند توسط این مارکرهای توموری مورد پیگیری قرار بگیرد، برای مثال در سرطان پستان و معده اگر سطح پروتئین HER2 افزایش داشته باشد، داروهایی مانند هرسپتین میتواند بیشتر کمککننده باشد ولی در صورتی که میزان HER2 نرمال باشد، ممکن است این دارو پاسخ درمان مناسبی را به همراه نداشته باشد، بنابراین بیان میزان HER2قبل از شروع شیمیدرمانی بهصورت روتین اندازهگیری میشود.
برای کمک به تشخیص سرطان یک ارگان میتوان از یک یا ترکیبی از مارکرها برای افزایش حساسیت استفاده کرد
آنتیژن اختصاصی پروستات (PSA)
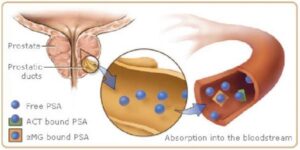
این آنتیژن دارای خاصیت سرین پروتئاز و از خانواده کالیکرین است و یک گلیکوپروتئین تکزنجیرهای ۲۳۷ اسیدآمینهای با چهار زنجیره کربوهیدراتی جانبی است که توسط سلول پوششی پروستات نرمال و نئوپلاستیک بیان میشود. میزان نرمال آن 0 الی 4 نانوگرم در هر میلیلیتر است. تحت شرایط نرمال، آنتیژن اختصاصی پروستات به شکل آنتیژن پیشساز (Pro PSA) توسط سلولهای ترشحی غده پروستات ساخته شده و به داخل مجاری پروستات ترشح میشوند و در آنجا به شکل PSA فعال درمیآید. PSA فعال سپس پروتئولیز شده و فرم غیرفعال PSAرا تولید میکند که قسمتی از آن بهصورت آزاد free PSA وارد جریان خون میشود. PSA فعال میتواند بهصورت مستقیم نیز وارد گردش خون شود که در این حالت به مهارکنندههای پروتئازی مانند آلفا یک آنتیکیموتریپسین و آلفا ۲ ماکروگلوبولین و مهارکنندههای پروتئازی آلفا متصل میشود که همه بهعنوان فرم کمپلکس PSA شناخته میشوند.
پروستات آنتیژن PSA را بهصورت آزاد ترشح میکند و در گردش خون بهصورت کمپلکس و آزاد دیده میشود
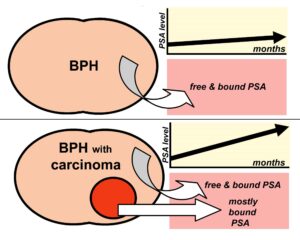
باوجودی که تولید PSA توسط سلولهای سرطانی کمتر از سلولهای نرمال است، ولی به علت تخریب غشای پایه و ساختار مجاری حملونقل مقدار زیادتری از Pro PSA و اشکال مختلف آن به جریان خون نشت پیدا میکند و قسمت زیادی از PSA ترشحی از سلولهای بدخیم از پروتئولیز فرار کرده که نتیجه آن افزایش سطح PSA در خون بیماران مبتلا است.
در مردان با پروستات نرمال، بیشتر free PSAسرمی نمایانگر پروتئین بالغ است که توسط پروتئولیز داخلی غیرفعال شدهاند که این جزء در بیماران مبتلا به سرطان پروستات بهصورت نسبی کاهش مییابد؛ بنابراین درصد آنتیژن اختصاصی بهصورت آزاد یا باندنشده در سرم مردان مبتلا به سرطان پروستات کاهش مییابد و برعکس میزان PSA ترکیبی که متصل به آلفا یک آنتیکیموتریپسین است برخلاف افراد سالم یا افراد مبتلا به هایپرپلازی خوشخیم پروستات افزایش مییابد.
از نسبت میزان free PSA به PSA و از PSA کمپلکس (complex PSA) برای افتراق بین سرطان پروستات و هایپرپلازی خوشخیم پروســــــتات در صورت افزایـــش میزان PSA استفاده میشود. (%fPSA = [fPSA/tPSA] * 100)
آنتیژن PSA در موارد زیر افزایش مییابد:
- هایپرپلازی خوشخیم پروستات (BPH)
- سرطان پروستات
- التهاب پروستات یا عفونت
- ترومای پرینه (میان دوراه)
شایعترین دلیل افزایش سطح PSA، هایپرپلازی خوشخیم پروستات است که در بیشتر مردان بالای ۵۰ سال مشاهده میشود. در سال ۱۹۸۰ تأیید شد که میزان PSAدر سرم باید بهعنوان یک روش غربالگری برای مردان مبتلا به سرطان پروستات استفاده شود، زیرا سطح سرمی این مارکر یک نشانگر حساس برخلاف آزمون مقعدی دیجیتال است. در حال حاضر جدیدترین راهنمای غربالگری، سن 40 سال به بالا را برای بررسی پیشنهاد میدهد.
هرچند اکثر موارد سرطانهای پروستات با بیان PSA همراه است، بین ۲۰ تا ۵۰ درصد مردان در جمعیت کشورهای غربی که برای اولین بار با تشخیص سرطان پروستات شناسایی شدهاند دارای سطح سرمی PSA کمتر از ۴ نانوگرم در هر میلیلیتر بودهاند (سطح بالای این مارکر نیز معادل 4 نانوگرم در هر میلیلیتر در نظر گرفته میشود) که این بیانگر اختصاصیت پایین PSA بهعنوان یک مارکر توموری است. مطالعات بیانگر حساسیت 80 درصدی و اختصاصیت حدود 50 درصدی این تست است.
بهطور کلی بیماران با PSA پایینتر از 4 نانوگرم در هر میلیلیتر بیشتر دارای سرطان محدود به غده پروستات هستند و این بیماران پیشآگهی بهتری را نسبت به افراد مبتلا به سرطان با سطح بالاتر از 4 نانوگرم در هر میلیلیتر از خود نشان میدهند.
التهاب پروستات با یا بدون عفونت فعال یک علت مهم افزایش سطح PSA است که تا سطح بالای ۷۵ نانوگرم نیز در مواردی گزارش شده است. بسیاری از پزشکان ابتدا مردان با افزایش سطح تنها PSA را تحت درمان آنتیبیوتیک قرار داده و بعد از درمان، برای ارزیابی بیشتر سطح PSA را دوباره اندازهگیری میکنند.
%Free PSA سرمی کمتر تحت تأثیر التهاب قرار میگیرد، بهویژه در صورتی که سطح PSA کل سرمی کمتر از ۱۰ نانوگرم در هر میلیلیتر باشـــد، هرچنـــد یک مطالعــــه نشان داده اســــــت که نسبــــــــــت Free PSA /TOTAL PSA توانایی افتراق التهاب مزمن از سرطان پروستات را ندارد، زیرا در هر دو حالت ممکن است درصد Free PSA پایین باشد. سرطان پروستات به علت تخریب غشای پایه با افزایش نفوذپذیری PSAهای نابالغ به جریان خون سبب افزایش سطح سرمی PSA میشود و التهاب نیز با همین رویکرد سبب افزایش سطح سرمی PSA میشود.
هرگونه آسیب به پرینه، ماساژ پروستات و امتحان مقعدی پروستات ممکن است موجب افزایش سطح PSA گردد. هرگونه دستکاری مکانیکی در پروستات توسط سیستوسکوپی، بیوپسی پروستات یا سونوگرافی از طریق مقعد (TURP) میتواند بر روی غلظت سرمی PSA اثرگذار باشد. دوچرخهسواری طولانیمدت و احتباس ادراری نیز میتواند سبب افزایش سطح PSA شود. فعالیت جنسی نیز میتواند تا سطح 0/4 الی 0/5 نانوگرم افزایش PSA را ۴۸ الی ۷۲ ساعت بعد از خروج مایع منی نشان دهد.
گزارش غلظت افزایشیافته PSA به همراه سه فاکتور زیر در تفسیر کمککننده است:
- تراکم PSA (PSA density)
- سرعت PSA (PSA velocity)
- نسبت Free PSA / TOTAL PSA
به نظر میرسد این دستورالعمل برای غربالگری سرطان پروستات وقتی که PSA کل بین 2/5 تا 10 نانوگرم در هر میلیلیتر باشد، بسیار سودمند است. نسبت سطح سرمی PSA به حجم پروستات که با روش سونوگرافی از طریق مقعد (TURS) مورد سنجش قرار میگیرد بیانگر تراکم PSA است که عدد بالاتر از 0.15 ng/ml/cc بیشتر به نفع سرطان پروستات بوده و مقادیر پایینتر پیشنهادکننده هایپرپلازی خوشخیم است، با وجودی که برخی گزارشها بیانگر همپوشی سطح تراکم PSA بین حالت خوشخیم و بدخیمی است.
البته در اندازهگیری تراکم، عواملی از جمله خطاهای اندازهگیری حجم پروستات توسط روش TURS و تغییرات سطح سرمی ۱۵ درصدی در میزان PSAطی اندازهگیریهای مکرر مداخله میکنند. در ضمن به علت هزینه بالای روش TURS عملاً اهداف غربالگری گسترده برای بررسی این فاکتور مشکل بهنظر میرسد.
سرعت تغییر سطح PSAدر طی زمان (velocity) که با افزایش همراه باشد بیشتر به نفع سرطان پروستات است. سرعت 0/6 نانوگرم در هر میلیلیتر در طول یک سال نیاز به بیوپسی بهویژه در افراد با سطح پایینتر PSA دارد.
اندازهگیری سرعت افزایش PSA و مقدار کمپلکس PSA در افتراق سرطان پروستات از بزرگ شدن خوشخیم آن کمککننده است
PSA آزاد و باندشده سرمی:
سرطان پروستات با سطح پایین Free PSA سرمی برخلاف حالت خوشخیم همراه است. برای بهبود حساسیت تشخیص سرطان پروستات وقتی میزان PSA کل کمتر از ۴ نانوگرم در هر میلیلیتر باشد از سنجش درصد آزاد PSA استفاده میشود و همچنین سبب افزایش اختصاصیت وقتی میزان PSA کل در محدوده 4/1 الی 10 نانوگرم در سیسی (محدوده خاکستری) باشد، میگردد.
کاهش درصد PSA آزاد به PSA کل ممکن است همراهی با شکل تهاجمی سرطان پروستات داشته باشد.
PSA کمپلکس:
از نظر تئوری روشهای اندازهگیری PSA-ACT(آنتیژن PSA کمپلکس با آنتیکیموتریپسین) درجه اختصاصیت تقریباً مشابهی با نسبت Free PSA /TOTAL PSA دارد با این تفاوت که تنها نیاز به اندازهگیری یک آنالیت داریم. در یک گزارش برای مردانی که سطح PSA در منطقه خاکستری بین 4 تا 10 نانوگرم در سیسی داشتهاند، سنجش PSA کمپلکس بهتنهایی، قادر به تشخیص یک نفر از 36 نفر فرد مبتلا به سرطان نبوده است. بیشتر این گزارشها مبین این است که cPSA دارای حساسیت مشابهی در برابر اندازهگیری PSA کل و نسبت Free PSA /TOTAL PSA است، ولی اختصاصیت آن بالاتر است.
PSA کمپلکس در حال حاضر برای پیگیری افراد مبتلا به کارسینومای پروستات مورد تأیید قرار گرفته است ولی هنوز بهصورت یک روش عملی روتین بالینی استفاده نمیشود.
درصد[2-] pro PSA
PSA ابتدا بهصورت pro PSA تولید میشود که PSA اولیه توانایی ورود به گردش خون در افراد مبتلا به سرطان پروستات را دارد.
pro PSA [-2] یکی از ایزوفرمهای اختصاصی pro PSA است که بهصورت آزاد و با غلظت بالاتر در افراد مبتلا به سرطان پروستات مشاهده میشود. بر اساس مشاهدات انجامشـــــــــــــــده، استــــــفاده از نسبــــت [2-] pro PSA /Free PSA که بهعنوان%[2-] pro PSA نیز شناخته میشود برای غربالگری سرطان پروستات بسیار موردتوجه قرار گرفته است.
مطالعات انجامشده بر اساس بیوپسی پروستات ۵۶۶ نفر نشان داده است اندازهگیری %[2-] pro PSA بسیار کارآمدتر از اندازهگیری TOTAL PSA و Free PSA% است. در محدودهی حساسیت ۸۰ درصدی، اختصاصیت تست%[2-] pro PSA برابر با ۵۲ درصد بود ولی این میزان برای PSA معادل ۳۰ درصد و برای Free PSA معادل ۲۹ درصد گزارش شده است.
در حال حاضر مجمع اروپایی تشخیص سرطان پروستات استفاده از %[2-] pro PSA را مورد تأیید قرار داده است و FDA در حال ارزیابی این تست است.
موارد مثبت کاذب و نتایج PSA غیرقابل انتظار:
مطالعات انجامشده روی 61604 نفر در اروپا خطای مثبت کاذب 17/8 درصد را نشان داده است؛ هرچند این افراد با جواب مثبت کاذب که توسط تست غربالگری مشخص شدهاند، ممکن است مستعد ابتلا به سرطان پروستات در آینده باشند. با این اوصاف علت اصلی جواب مثبت کاذب PSA در حضور آنتیبادیهای هتروفیل در سرم رخ میدهد که در حقیقت حضور این آنتیبادیها در نمونه نهتنها سبب افزایش کاذب PSA میشود، بلکه بسیاری از نتایج مارکرهای توموری دیگر نیز با افزایش کاذب مواجه میگردد.
در آزمایشگاههای پزشکی قانونی در حملههای جنسی و تجاوز به عنف، بررسی کاندوم لازم است زیرا حضور مایع منی میتواند بهعنوان یک مدرک مهم در تجاوزهای جنسی بهحساب آید. اگرچه مطالعات میکروسکوپی مایع منی و تشخیص اسپرم اهمیت دارد ولی گاهی اوقات به علت تخریب و دیگر عوامل موجود، استفاده از مطالعات مستقیم میکروسکوپی امکانپذیر نیست. در این حالت تستهای شیمیایی مایع منی مانند بررسی حضور PSA نشاندهنده مایع منی است، ولی حضور اسپرمکشهای Nonoxynol-9 که یک دترجنت قوی است، بیشترین عامل جوابهای مثبت کاذب در این بررسیها است.
مقادیر بسیارکم PSA در شیر مادران مشاهده شده است و سطوح قابل اندازهگیری PSA در سرم مادران مبتلا به سرطان پستان و یا کیستهای پستانی قابل شناسایی است. افزایش این مارکر حتی در مردان مبتلا به سرطان سینه که یک نوع سرطان نادر در آنها است، نیز گزارش شده است، علاوه بر این در زنان مبتلا به سرطان پانکراس و التهاب پانکراس نیز مقادیر PSA و Free PSAقابل شناسایی است.
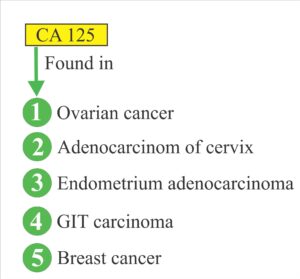
CA-125
CA-125 گلیکوپروتئینی است که با نامهای موسین 16 یا MUC16 نیز شناخته میشود و در انسان توسط ژن MUC16 کد میشود. از آنجا که غلظت آن در خون تعدادی از بیماران مبتلا به برخی سرطانها مانند سرطان تخمدان و برخی شرایط خوشخیم افزایش مییابد، بهعنوان یک مارکر توموری شناخته میشود. سطح سرمی CA125 در نزدیک به 50 درصد از زنان در مراحل اولیه بیماری و در 80 درصد زنان با سرطان پیشرفته تخمدان افزایش نشان میدهد.
مانیتورینگ سطح سرمی این مارکر برای بررسی پاسخ به درمان در زنان مبتلا به سرطان تخمدان و همچنین ارزیابی پیشآگهی بیمار بعد از درمان مفید است. بهطور کلی بالا ماندن سطح CA125 در حین درمان با شانس بقای کم بیمار همراه است و همچنین افزایش سطح آن در دوره بهبودی شاخص مهمی در عود سرطان تخمدان است.
در آوریل 2011 مؤسسه بهداشت انگلستان پیشنهاد کرد که زنان دارای علائم سرطان تخمدان حتماً باید تست CA125 را انجام دهند. هدف این کار کمک کردن به تشخیص بیماری در مراحل اولیه که پاسخ درمانی موفقتری را به همراه دارد، است. زنان با سطح بالاتر این مارکر در خون باید برای انجام اسکن فراصوتی بهمنظور نیاز به تستهای بیشتر، مورد ارزیابی قرار گیرند. اختصاصیت CA125 محدود است و سطح سرمی آن در یک درصد زنان سالم افزایش نشان میدهد و نوسان سطح آن در طول دوره قاعدگی مشاهده میشود. افزایش سطح این مارکر در حالتهای خوشخیم و بدخیم زیر مشاهده میشود:
- اندومتریوز (ENDOMETRIOSIS)
- لیومیومای رحم (UTHERINE LIOMIOMA)
- سیروز با یا بدون آسیت
- بیماریهای التهابی لگن
- سرطانهای اندومتر، پستان، ریه و پانکراس
- التهاب مایع ریوی یا جنب به هر علت
مانیتورینگ سطح سرمی این مارکر در بیماران مبتلا به سرطان لوله فالوپ که بیماری نادری است نیز ارزشمند است. غلظت سرمی پیش از درمان این مارکر در این بیماری ارزش تشخیصی دارد و در پی درمان اولیه یک مارکر حساس برای مانیتورینگ بازگشت و پاسخ به شیمیدرمانی است.
نتایج مثبت کاذب یا منفی کاذب CA125
به همراهی فیبروم تخمدان، افیوژن پلور و آسیت، سندرم میگز (meigs’ syndrom) گفته میشود که ممکن است با افزایش شدید CA-125 همراه باشد و با سرطان بدخیم تخمدان اشتباه گردد، در حالی که سندرم میگز خوشخیم است و با جراحی کاملاً درمان میشود، ازاینرو با افزایش CA-125 بایستی سندرم میگز که علائم بالینی یکسان با تومور تهاجمی تخمدان دارد، تشخیص افتراقی شود.
کاربردهای بالینی مارکر CA-125
افزایش سطح غیرنرمال CA125 و CA19-9 در تومورهای خوشخیم زنان نیز گزارش شده است و پیشنهاد میشود ارزش تشخیصی مارکرهای توموری همراه با اولتراسوند و توموگرافی برای تشخیص سرطان تخمدان مورد ارزیابی قرار گیرند. برخی اوقات قطعه F(ab‘)2 آنتیبادی مونوکلونال OC125 برای سرطان تخمدان تجویز میشود و بهصورت مستقیم به آنتیژن CA125 موجود در سطح سرطانهای تخمدان انسانی متصل میگردد. پاسخ ایمنی با این نوع آنتیبادیها سبب پیدایش آنتیبادی انسانی ضدموشی (HAMA) یا آنتیبادی هتروفیلی میشود که این آنتیبادی میتواند سبب تداخل در اندازهگیری سطح سرمی CA125 شود، هرچند تداخل این آنتیبادی با برداشت ایمونوگلوبینهای سرمی بهخصوص نوع IgG حذف خواهد شد.
نتایج مثبت کاذب با افزودن IgG موشی غیراختصاصی به سرم بیمار تصحیح میشود، در حالی که برای نتایج منفی کاذب امکانپذیر نیست. غلظتهای CA125 قابل اندازهگیری در بیماران بدون سرطان نیز مشاهده میشود.
افزایش سطح این مارکر در بیماران با نارسایی شدید احتقانی قلب (severe congestive heart failure) مشاهده شده است و افزایش سطح آن با شدت بیماری و افزایــــش مارکرهای اختصاصی نارسایی قلب مانند B-type natriuretic peptide (BNP) در ارتباط است.
افزایش سطح CA125 در فاز خونریزی چرخه قاعدگی بانوان ممکن است مشاهده شود. بعد از جراحیهای شکم، بیماری انسدادی مزمن ریوی، توبرکلوز فعال و لوپوس نیز سطح CA125 افزایش مییابد. در طی حاملگی غلظت این مارکر بعد از هفته دهم افزایش مییابد و در دوران بارداری همچنان بالا میماند و در اواخر دوره بارداری غلظت آن تا دو برابر سطح بالای حد نرمال ممکن است افزایش یافته باشد.
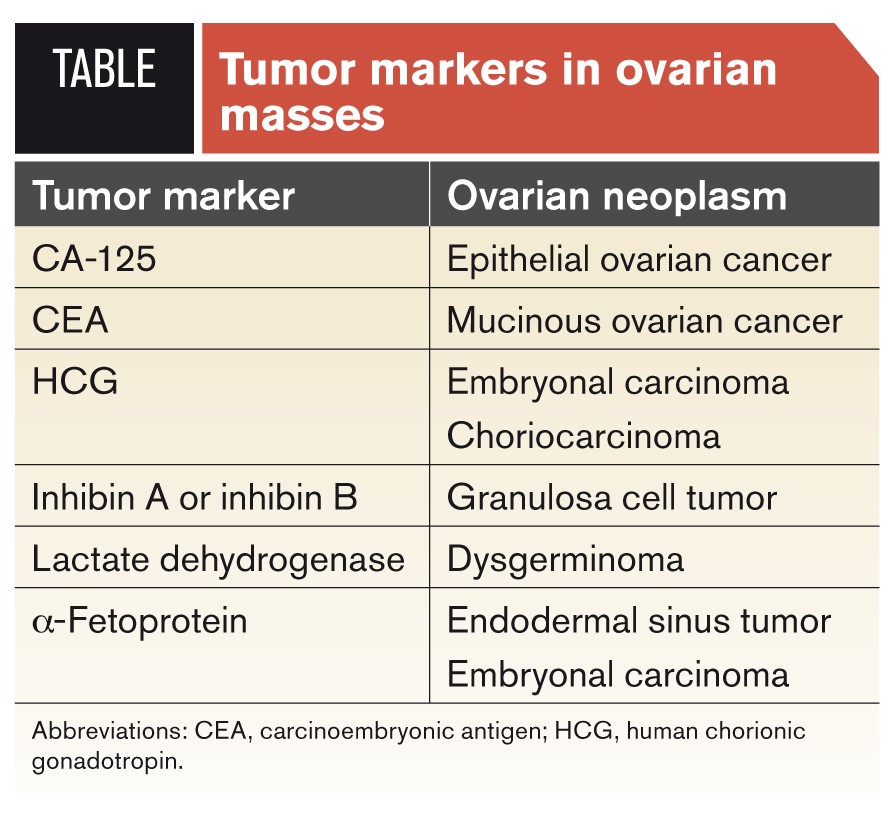
در تومورهای مختلف یک ارگان مارکرهای گوناگونی ممکن است کاربرد داشته باشند. جدول فوق کاربرد مارکرها در فرمهای مختلف سرطان تخمدان را نشان میدهد
آلفا فیتوپروتئین
AFP، پروتئینی است که در انسان توسط ژن AFP کد میشود و بر روی بازوی بلند کروموزوم 4 قرار گرفته است و به نامهای آلفا یک فیتوپروتئین یا آلفا فیتوگلوبولین نیز شناخته میشود. AFP یک پروتئین پلاسمایی اصلی است که توسط کیسه زرده و کبد در طی دوران تکامل جنینی تولید میشود و بهعنوان فرم جنینی آلبومین محسوب میشود. این ماده قابلیت اتصال به مس، نیکل، اسیدهای چرب و بیلیروبین را دارد و به اشکال مونومری، دایمری و ترایمری موجود است. نیمهعمر آن حدود 5 الی 7 روز است. در طی درمان مؤثر سرطان، نرمال شدن غلظت سرمی آن در یک بازهی 25 الی 30 روزه بهعنوان یک خطمشی مناسب بهحساب میآید. میزان آن در سرم افراد مذکر نرمال غیرقابل شناسایی است. ســـــطح بالای نرمال غلظت سرمی آن کمتر از 15-10 μg/L است. بسیاری از بافتها توانایی تولید این پروتئین آنکوفتال را دارا هستند ولی سطح سرمی بالاتر از 10000 μg/L بیشتر در بیماران با تومورهای سلول زایای غیرسمینومایی یا (NCGCTs) و یا کارسینومای هپاتوسلولار مشاهده میشود.
در مردان مبتلا به NCGCTs، سینوسهای اندودرمال تومورهای کیسه زرده و گاهی اوقات کارسینوماهای جنینی عهدهدار تولید AFP هستند. شدت افزایش این مارکر در سرم مانند هورمون βhCG با پیشرفت مرحله بالینی تومور افزایش مییابد.
سمینوماهای خالص باعث افزایش سطح سرمی AFP نمیشوند، اگرچه مطالعات مولکولی نشان میدهد mRNA این مارکر در مقادیر بسیار کم در سمینوماهای خالص و برخی موارد نادر مشاهده شده است و میزان افزایش آن در سرم بین 10/4 الی 16 نانوگرم در هر سیسی ثبت شده است.
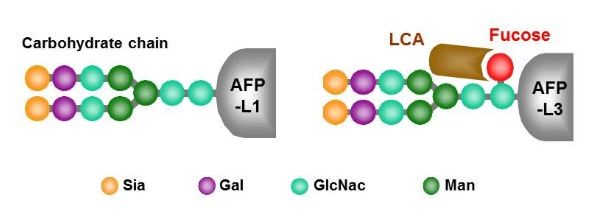
آلفا فیتو پروتئین بهصورت افتراقی در بیماریهای کبد قندی میشود. شکل فوکوزیله (L3) بیشتر در ارتباط با سرطان کبد است که میتوان آن را توسط عصاره گیاهی (لکتین) شناسایی کرد. اندازهگیری سطح L3AFP در تشخیص سرطان کبد بهویژه هنگامی که سطح توتال آن کمتر از 200 نانوگرم در سیسی است کمککننده است
AFP سرمی بیشترین مارکر مورد استفاده شایع تشخیصی در کارسینوماهای هپاتوسلولار است، چون اغلب در بیماران مبتلا به این کارسینوما افزایش مییابد. سطح سرمی آن با علائم بالینی این کارسینوما مانند اندازه، مرحله و پیشآگهی وابستگی چندانی ندارد. افزایش سطح سرمی AFP در هپاتیتهای حاد و مزمن ویروسی نیز دیده میشود و در بیماران مبتلا به سیروز کبدی ناشی از هپاتیت نوع C کمی افزایش نشان میدهد. افزایش شاخص سطح سرمی این مارکر در سیروز کبدی میتواند نمایانگر پیشرفت به سمت کارسینومای هپاتوسلولار باشد. بهصورت کلی افزایش سطح سرمی AFP بالاتر از 500 μg/L(حد بالای نرمال این مارکر در بیشتر آزمایشگاهها 10 الی 20 میکروگرم در هر لیتر است) در بیماران با ریسک خطر بالا برای کارسینومای هپاتوسلولار تشخیصی است.
تمام تومورها این مارکر را ترشح نمیکنند و سطح سرمی این مارکر در حدود 40 درصد از بیماران مبتلا به کارسینوماهای هپاتوسلولار کوچک میتواند نرمال باشد. افزایش سطح AFP بیشتر به نفع کارسینومای هپاتوسلولار به دنبال هپاتیت ویروسی در مقایسه با هپاتیت الکلی است. در مطالعهای بر روی 357 بیمار مبتلا به هپاتیت نوع C و فاقد کارسینومای هپاتوسلولار، 23 درصد آنها AFP بالاتر از 10 میکروگرم در لیتر را نشان دادند. میزان AFP در اکثریت بیماران کارسینومای فیبرولاملار fibrolamellar)) که دستهای از کارسینومای هپاتوسلولار است نیز نرمال است. تخمین زیر بر اساس CUT OFF بیشتر از 20 میکروگرم در لیتر صورت گرفته است:
- حساسیت: 41 تا 65 درصد
- اختصاصیت: 80 تا 94 درصد
جواب مثبت کاذب AFP
جوابهای مثبت کاذب در افزایش سطح سرمی AFP در تومورهای لوله گوارشی و در آسیب کبدی مانند سیروز، هپاتیت و سوءمصرف دارو یا الکل مشاهده میشود. لیز شدن سلولهای توموری حین شروع شیمیدرمانی میتواند سبب افزایش گذرای میزان این مارکر شود. در حاملگی با تومورهای دارای منشأ گنادی (هم سلولهای زایا و هم سلولهای غیرزایا) و طیف وسیعی از بدخیمیها بهخصوص سرطان معده نیز افزایش دیده میشود. افزایش میزان AFP در آسیب کبدی ناشی از مصرف دارو (شیمیدرمانی، داروهای بیهوشی و داروهای ضد صرع)، در عفونتهای ویروسی و سوء مصرف الکل بدون شواهد بالینی حضور تومورهای بدخیم نیز دیده میشود.
آنتیبادیهای هتروفیل نیز در صورت حضور در نمونه سرمی میتوانند سبب افزایش غلظت این مارکر شوند. مقادیر 140 برابر بالاتر از حداکثر میزان نرمال این مارکر در تیروزینمی ارثی توع یک نیز گزارش شده است که در 71 درصد افراد مبتلا این میزان تا دو برابر سطح بالای نرمال دیده شده است. خانمهای حامله مبتلا به لوپوس نیز افزایش غلظت سطح این مارکر را نشان میدهند.
CARCINOEMBRIONIC ANTIGEN
CEA یک گلیکوپروتئین است که دارای نقش چسبندگی سلولی است و بهطور نرمال در طی تکامل جنینی ساخته میشود ولی تولید آن قبل از تولد متوقف میگردد، به همین دلیل بهصورت نرمال در خون افراد بالغ سالم دیده نمیشود ولی افزایش سطح آن در افراد سیگاری شدید مشاهده میشود. CEA از طریق لنگرگاه گلیکوفسفاتیدیل اینوزیتول به سطح غشا میچسبد که فرمهای سیالوفوکوزیلهشدهی آن بهعنوان لیگاندهای عملکردی L-selectin و E-selectin کارسینومای کولون عمل میکند که برای متاستاز سلولهای سرطانی کولون اساسی است.
در شکل فوق ساختار آنتیژنی CEAبهصورت زائدههای گلیکوپروتئینی در سطح سلول مشاهده میشود که نقش مهمی در متاستاز سرطان دارند
در سرم افراد مبتلا به کارسینومای کولورکتال، معده، پانکراس، ریه و سینه این مارکر مشاهده میشود. بیماران مبتلا به کارسینومای مدولاری تیروئید دارای افزایش سطح این مارکر (بیشتر از 2.5 ηg/ml) هستند. تست خونی CEA برای تشخیص سرطان یا بهعنوان تست غربالگری برای تشخیص اولیه سرطان قابلاعتماد نیست. بسیاری از سرطانها میزان زیاد CEA را تولید نمیکنند. افزایش سطح این مارکر باید بعد از جراحی موفقیتآمیز یا 6 هفته بعد از شروع درمان موفقیتآمیز سرطان به سطح نرمال خود بازگردد. از آنجا که این مارکر حساسیت و اختصاصیت زیادی ندارد، بهعنوان تست غربالگری مفیدی برای تشخیص کارسینومای کولورکتال استفاده نمیشود. افزایش سطح CEA در این بیماران باید بعد از جراحی کامل به سطح پایه خود برگردد و در صورت عدم این اتفاق باید به حضور باقیمانده بیماری مشکوک شد.
CEA سرمی و کارسینومای کولورکتال
سطح سرمی مارکر توموری CEA باید بهصورت روتین قبل از عمل به دو دلیل زیر اندازهگیری شود:
- افزایش سطح CEA قبل از عمل که بعد از جراحی به سطح نرمال خود بازنگشته باشد نمایانگر حضور بقایای سلولهای سرطانی و نیازمند ارزیابی بیشتر است.
- میزان قبل از عمل این مارکر دارای ارزش تشخیصی است. میزان بیشتر یا مساوی5.0 ηg/ml پیشآگهی نامطلوبی دارد و وابستگی به مرحله تومور (tumor stage) ندارد.
اندازهگیری سریال CEA میتواند بازگشت بیماری را حتی در میان بیمارانی که میزان CEA نرمال اولیه داشتهاند را تشخیص دهد، اگرچه حساسیت این تست پایین است.
زمانبندی انجام آزمایش CEA
بر اساس راهنمای انجمن انکولوژی بالینی سفارش میشود سطح سرمی CEA بعد از عمل جراحی هر سه ماه برای حداقل سه سال بعد از شروع درمان در بیماران با مرحله 2 و 3 بیماری انجام گیرد، در حالی که برخی از راهنمای اندازهگیری سنجش هر 3 تا 6 ماه به مدت دو سال بعد از جراحی و سپس هر 6 ماه یکبار برای مدت 5 سال سفارش کردهاند.
ارزش تشخیصی CEA در سرطان مجاری صفراوی (Cholangiocarcinoma):
این مارکر بهعنوان یک آنالیت تک اختصاصی و حساس برای سرطان مجاری صفراوی بهکار نمیرود، چون بیماریهای غیرسرطانی از قبیل گاستریت، زخم معده، دایورتیکولیت، بیماریهای کبد، بیماریهای انسداد ریوی، دیابت و التهاب حاد و مزمن میتوانند موجب افزایش سطح آن گردند. یک مطالعه بزرگ بر روی 333 بیمار با کلانژیت اسکلروزان اولیه (PSC) نشان داد که تنها 13 درصد با اندازهگیری سطح CEA مبتلا به کلانژیوکارسینوما با پیگیری حداقل یکساله گردیدهاند. اندازهگیری سطح صفراوی CEA در یک گزارش در بیماران مبتلا به کلانژیوکارسینوما 5 برابر در مقایسه با تنگیهای مجاری صفراوی خوشخیم و اسکلروز بدون بدخیمی بوده است.
مثبت کاذب CEA
آنتیبادیهای هتروفیل موجب مثبت کاذب تست گردیده و موارد غیرنئوپلاسم نیز میتواند افزایش آن را سبب شود. مواردی از قبیل نارسایی کلیه و هپاتیت برقآسا موجب افزایش کاذب آن میگردند. همودیالیز و کمکاری تیروئید ممکن است سطح CEA را بالا برده و این افزایش سطح با طول دوره کمکاری تیروئید نسبت مستقیم دارد. کولیت اولسردار، التهاب پانکراس، سیروز و بیماری انسداد ریوی (COPD)، بیماری کرون و استعمال دخانیات از موارد افزایش سطح هستند.
غربالگری سرطان پروستات با استفاده از تست آنتیژن اختصاصی پروستات (PSA)
برای دانلود پی دی اف برروی لینک زیر کلیک کنید
ورود / ثبت نام