آنتیبادی گمشده:
معایب تست ANCA
دکتر شاهرخ مستور تهرانی
معرفی
یک خانم ۴۴ ساله سفیدپوست با تنگینفس حاد به هنگام بازگشت از تعطیلات از طریق سفر هوایی به بیمارستان مراجعه کرد. وی سابقه سرفه مکرر، خلط خونی، درد قفسه سینه و یا درد ماهیچه ساق پا را منکر شد. او مبتلا به آسم بود و علائم وی با استفاده مکرر از اسپری استنشاقی سالبوتامول، در طول پرواز بهبود یافته بود.
در سابقه پزشکی وی، وجود پولیپهای نازال دیده شد که ۲ سال قبل باعث مداخله جراحی شده بودند.
یک ماه قبل وی برای التهاب «مزمن» گوش میانی تحت درمان با آموکسیسیلین قرار گرفته و در نوبت مراجعه به متخصص گوش، حلق و بینی (ENT) بود، همچنین مفصلهای متاکارپوفالانژیال و قوزک پای وی ورم کرده و حساس شده بود و مشخص شد که فاکتور روماتوئيد وی نیز مثبت است. علائم وی به دنبال یک دوره کوتاه درمان با پردنیزولون بهبود یافته و وی آنقدر احساس بهبودی پیدا کرده بود که به تعطیلات برود.
او منشی یک مؤسسه حقوقی بود، هرگز سیگار نکشیده بود و یک شریک زندگی بلندمدت داشت. او در هر هفته یک بطری شراب مینوشید. او فرزندی نداشت و هرگز باردار نشده بود.
ارزیابی
در معاینه، دمای بدن وی ℃۳۷ و میزان تنفس، ۲۰ تنفس در هر دقیقه بود. ضربان قلب وی ۸۰ بار در دقیقه و فشارخون وی mmHg 125/67 بود. وی برای حفظ اشباع اکسیژن بیش از ۹۵%، به اکسیژن کمکی به میزان L/min ۱۰ نیاز داشت. سمع صداهای قفسه سینه، کراکل دوطرفه و تست نوار ادراری، +۳ برای خون، +۲ برای پروتئین و منفی برای بارداری را نشان داد.
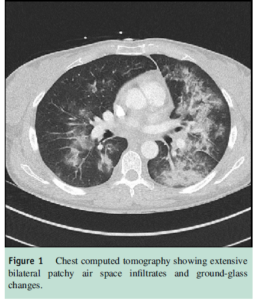
نتایج بررسی اولیه در جدول ۱ نشان داده شده است. توموگرافی کامپیوتری (سیتیاسکن) قفسه سینه، ارتشاح هوای تکهتکه گسترده بهصورت دوطرفه و تغییرات ground glass را آشکار ساخت اما شواهدی از بیماری آمبولیک وجود نداشت (شکل 1).
بر اساس سابقه بالینی بیمار، افزایش پروتئین واکنشگر C، آنمی و ارتشاح آلوئولار منتشر، تشخیص خونریزی ریوی به دلیل یک فرایند خودایمنی یا واسکولیت بهعلاوه یک عفونت در قفسه سینه مطرح شد.
به این بیمار 2 واحد خون تزریق شد و با کو-آموکسیکلاو داخل وریدی و داکسی سایکلین خوراکی تحت درمان قرار گرفت؛ 500 میلیگرم متیل پردنیزولون داخل وریدی طی ۳ روز تزریق شد، سپس با 60 میلیگرم در روز پردنیزولون خوراکی جایگزین شد.
نتایج سرولوژی ویروسی و آزمایشهای ایمونولوژی در روز سوم پذیرش بیمار بهدست آمد (جدول 2). تکرار آزمایشهای سرولوژیک برای هرگونه فرآیند خودایمنی خاص منفی بودند.
اسپیرومتری ریه در روز چهارم، DLCOc (فاکتور انتقالی اصلاحشده) و KCO (ضریب انتقال) را به ترتیب ۱۰۴% و ۸۸% مقدار پیشبینیشده نشان داد.
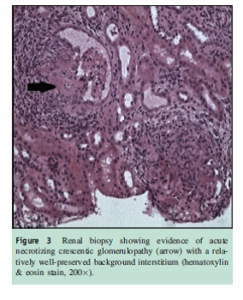
با توجه به پیچیدگی این مورد، بیوپسی ریه در روز دوازدهم انجام شد (شکل 2). بیوپسی، کانونهای تشکیل شده پنومونی را با شواهدی از خونریزی ریوی نشان داد، اما هیچگونه واسکولیت فعال وجود نداشت.
بيمار در طول 2 هفته بهبود يافت و با برنامهای براي كاهش دوز پردنيزولون از بيمارستان مرخص شد. وی، 3 هفته پس از ترخیص به کلینیک روماتولوژی مراجعه نمود و مشخص شد که دچار هماتوپروتئینوری، با کراتینین µmol/L 167 (در هنگام ترخیص این مقدار، برابر µmol/L 80 بود) است.
سنجش (ELISA) برای ایمونوگلوبولین G (IgG)، آنتیبادیهای سیتوپلاسمی ضد نوتروفیل (ANCA) مجدداً منفی بود.
با این حال، در طول این مدت، آزمایشگاه ایمونولوژی، در نتایج ANCA مربوط به یک بیمار دیگر، متوجه نوعی عدم تطابق شده بود. این بیمار دوم، با ANCA مثبت و آنتیبادیهای IgG ضد پروتئیناز ۳ مثبت، از یک بیمارستان دیگر به بخش کلیه در بیمارستان ما منتقل شده بود. با این وجود، اندازهگیری آنتیبادیهای IgG ضد پروتئیناز 3 با متد آزمایشگاه ما منفی بود.
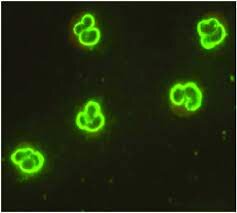
نمونه خون ذخیرهشده از بیمار ما، با روشهای دیگری آنالیز شد. غربالگری ایمونوفلورسانس غیرمستقیم (IIF) با هر دو روش، الگوی رنگآمیزی سیتوپلاسمی را برای ANCA نشان داد. با این حال سطح IgG ضد پروتئیناز ۳ با روش آزمایشگاه ما، کمتر از U/mL ۲ (مقدار مرجع U/mL 0-2) بود اما روش جایگزین U/mL ۴۴ را نشان داد.
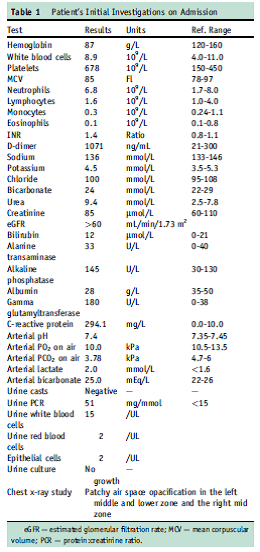
با توجه به نارسایی کلیوی بیمار و سدیمان ادراری فعال، وی تحت بیوپسی کلیوی قرار گرفت (شکل 3) که گلومرولونفریت پاسی ایمیون هلالی (pauci- immune crescentic glomerulonephritis) را در تطابق با واسکولیت نشان داد.
تشخیص
گرانولوماتوز با پلیآنژیت که سابقاً تحت عنوان «گرانولوماتوز وگنر» شناخته میشد، یکی از واسکولیتهای مرتبط با ANCA (AAV) است که بهطور معمول با گرانولومای دستگاه تنفسی فوقانی و تحتانی و گلومرولونفریت پاسیایمیون همراه است. میزان بروز و شیوع گرانولوماتوز با پلیآنژیت در انگلستان به ترتیب 10/2 و 250 مورد در هر یک میلیون نفر در سال تخمین زده میشود و عموماً در بازه سنی 55-35 سالگی مشاهده میشود و نسبت ابتلای زن به مرد 1.2 به یک است.
از دهه ۱۹۸۰، از ANCAها بهعنوان مارکر سرولوژیک برای کمک به تشخیص AAV استفاده میشود. بیشتر آزمایشگاهها در سراسر جهان از IIF برای غربالگری ANCA استفاده میکنند. در این روش سرم بیماران با نوتروفیلها مخلوط میشود. حضور و الگوی هرگونه اتصال با ANCA میتواند با رنگآمیزی فلورسنت آشکار شود. یک الگوی رنگآمیزی سیتوپلاسمی ANCA معمولاً با آنتیبادیهای IgG ضد پروتئیناز 3 (PR3) و یک الگوی پرینوکلئر (p-) میلوپراکسیداز (MOP) همراه است.
اختصاصیت IIF بالا است (۱۰۰- 90%). با این حال، ارزش پیشبینی مثبت آن تنها 73٪ است. به دلیل تفاوت در آمادهسازی اسلایدها و مهارت کارکنان، تنوع قابلتوجهی در نتایج وجود دارد و شرایط التهابی همزمان نیز باعث فراوانی بالای نتایج مثبت کاذب میشود.
در سال 2003، توصيه شد كه غربالگري اوليه IIF براي ANCA باید با یک آزمايش فاز جامد، مانند سنجش (ELISA) تأیید شود، با این حال، اپیتوپهای حائز اهمیت از نظر بالینی در آنتیژنهای هدف یعنی PR3 یا MPO در چاهک میکروتیتر ELISA بهصورت ضعیف در دسترس قرار میگیرند که منجر به ارائه غلظتهای پایین کاذب میشود. در حال حاضر روشهای جدیدتر از یک آنتیبادی استفاده میکنند که برای «لنگر شدن» یا «به دام انداختن» مولکول در محیط پشتیبان، به یک اپیتوپ «غیر عملکردی» متصل میشود. این روش، امکان افزایش اختصاصیت و حساسیت سنجش را فراهم میآورد، با این حال، تنوع در آمادهسازی آنتیژن، تکنیکها و فقدان مواد مرجع بینالمللی به این معنی است که هنوز هم تغییرات قابلتوجهی در نتایج ANCA وجود دارد، بهعلاوه هر بیمار نیز یک آنتیبادی IgG کمی متفاوت برای یک آنتیژن خاص تولید میکند و اپیتوپهای آنتیژن که بیمار به آن پاسخ میدهد نیز ممکن است در طول یک بیماری یا درمان تغییر کند.
پژوهشی که تکنیکهای مختلف ELISA را در گروه کنترل سالم و گروه بیماران مبتلا به گرانولوماتوز با پلیآنژیت، مقایسه کرده است، اختصاصیت بالایی (> 98٪) را برای همه روشها نشان میدهد، اما حساسیت از 72% مربوط به «capture Elisa» تا 96٪ مربوط به «anchor Elisa» متغیر است.
مرجع بینالمللی آمادهسازی برای IgG ضد MPO آماده شده است و برای IgG ضد PR3 در حال حاضر در مرحله ارزیابی نهایی است اما تأثیر کامل معرفی آنها چند سال بهطول میانجامد. سایر اجزای تکنیکهای مبتنی بر ELISA نیز نیاز به هماهنگسازی دارند (مانند تعریف دقیق آنتیژن یا اپیتوپی که مورد استفاده قرار میگیرد).
با این وجود، اختلافات مشاهدهشده در این روشها در روند کمک به تشخیص گرانولوماتوز با پلیآنژیت، بهویژه در بیماران با تظاهرات پیچیده یا غیرمعمول، مشکلساز میشود.
مدیریت بیمار
بر اساس پروتکل واسکولیت انجمن واسکولیت اروپا (EUVAS)، این بیمار، مبتلا به واسکولیت سیستماتیک عمومی تشخیص داده شد و یک دورهی القاء بهبودی از طریق تجویز ریتوکسیماب و پردنیزولون آغاز شد.
دوازده ماه پس از مراجعه اولیه، بیمار هیچ رویداد دیگری از خونریزی ریوی نداشت و کراتینین وی µmol/L 127 بود(فیلتراسیون گلومرولی 40 میلیلیتر در دقیقه/ سطح بدن تخمین زده میشود). دوز پردنیزولون بیمار با مصرف مایکوفنولات مفتیل (2 گرم در روز) برای حفظ بهبودی کاهش یافته است.
این بیمار، خطاهای احتمالی آزمایش ANCA را در تشخیص بیمار مبتلا به گرانولوماتوز با پلیآنژیت برجسته میکند. با وجود پیشرفت در حساسیت و اختصاصیت سنجش ELISA، تنوع در روش) (inter-method بالایی وجود دارد.
اینکه پزشکان از محدودیتهای این آزمایشها آگاه باشند و بدانند که هیچ سنجشی دارای 100٪ اختصاصیت یا حساسیت بالینی نیست، بسیار حائز اهمیت است.
این مورد، لزوم برقراری ارتباط خوب با آزمایشگاه هنگامی که نتایج عجیب بهنظر میرسند یا با تصویر بالینی تناقض دارند را برجسته میسازد و اینکه تشخیص AAV بالینی است و نه آزمایشگاهی. این نکته اخیر توسط معیارهای کالج آمریکایی روماتولوژی که برای شناسایی بیماران مبتلا به گرانولوماتوز با پلیآنژیت برای کارازماییهای بالینی استفاده میشود، منعکس شده است، بهگونهای که این معیارها اصلاً نتایج ANCA را شامل نمیشوند.
ترجمه از:
The Missing Antibody: The Pitfalls of ANCA Testing
The American Journal of Medicine, Vol 130, No 3, March 2017
مزایا و معایب آزمایشهای روماتولوژی
یافتههای آسپیراسیون و بیوپسی سوزنی در ضایعات التهابی و گرانولوماتوز ریه
برای دانلود فایل pdf بر روی لینک زیر کلیک کنید
ورود / ثبت نام