بازنگری در تشخیص تیفوئید
دکتر حمیدرضا هجرانی، دکترای علوم آزمایشگاهی
چکیده
مقدمه. تب تیفوئيد یکی از شایعترین علل بیماریهای حاد تبدار در کشورهای در حال توسعه است؛ بهگونهای که تخمین زده میشود در سال ۲۰۱۷، 10/9 میلیون مورد جدید ابتلا و 116/8هزار مورد مرگ در اثر این بیماری رخ داده است. تستهای تشخیصی تیفوئید که بر بالین بیمار (point of care:POC) انجام میشوند، بهطور گسترده مورد استفاده قرار میگیرند، اما حساسیت و اختصاصیت اندکی دارند و منجر به استفاده بیش از حد از آنتیبیوتیک شده که موجب ظهور و گسترش سویههای مقاوم به چند دارو میشود. با توجه به پیشرفتهای اخیر در نظارت بر تیفوئيد و تشخیص آن، اکنون زمان ایدهآلی برای ارائه پروفایل محصول هدف (target product profile, TPP) است که تولید محصول را هدایت کرده و تضمین میکند که یک تست نسل جدید (next-generation test) پاسخگوی نیاز کاربران در مناطقی با محدودیت منابع باشد که در آنجا تیفوئيد اندمیک است.
روشها. یک مرور روشمند بر نوشتههای تحقیقی با هدف تهیه پیشنویس TPP برای یک تست تشخیصی نسل جدید تیفوئيد با کمترین و بهینهترین مشخصات دلخواه برای 36 پارامتر تست انجام شد. TPP با استفاده از بازخورد جمعآوریشده از نظرسنجی دلفی (Delphi Survey) از صاحبنظران اصلی در پزشکی بالینی، میکروبیولوژی، پزشکی تشخیصی و بهداشت عمومی و جهانی، تصحیح شد.
نتایج. یک تست تشخیصی نسل جدید تیفوئيد باید مدیریت بیمار را از طریق تشخیص و درمان عفونت ناشی از سروتایپهای حاد Salmonella enterica یعنی Typhi یا Paratyphi با حساسیت ≥ ۹۰% و اختصاصیت ≥ 95% بهبود بخشد. این تست در حالت ایدهآل باید در پایینترین سطح از سیستم بهداشت و درمان و در مناطقی بدون وجود منابع قابلاعتماد برق یا آب، مورد استفاده قرار گیرد و نتایج را در کمتر از 15 دقیقه با هزینهای کمتر از ۱ دلار آمریکا ارائه دهد.
نتیجهگیری. این گزارش به تشریح اولین TPP جامع بیماری تب تیفوئيد میپردازد و هدف آن هدایت تولید تست تشخیصی نسل جدید تیفوئید است. یک تست POC دقیق، از طریق تشخیص سریع و درمان بیماری باعث کاهش مرگ و میر تب تیفوئيد میشود و در صورتی که با امکانات تشخیصی سایر علل بیماری حاد تبدار در الگوریتم درمانی همراه باشد، بیشترین تأثیر را در کاهش مقاومت ضدمیکروبی خواهد داشت.
| پرسشهای کلیدی
چه چیزهایی میدانیم؟ تستهای تشخیصی فعلی برای تب تیفوئيد برای استفاده قابل اطمینان بهصورت POC فاقد حساسیت و اختصاصیت کافی هستند که منجر به مصرف بیش از حد آنتیبیوتیک از طریق درمان تجربی شده است. یافتههای جدید، چه میگویند؟ برای برآورده ساختن نیازهای مصرفکنندگان در نواحی اندمیک، صاحبنظران پیشنهاد کردند که یک تست تشخیصی بهبودیافته تیفوئيد باید بتواند علاوه بر S. Typhi، S. Paratyphi را هم تشخیص دهد، حساسیت ≥ ۹۰% و اختصاصیت ≥ 95% و هزینهای در حدود < 3 دلار امریکا داشته باشد. یافتههای جدید بر چه نکاتی تأکید دارند؟ برای اثرگذاری قابلملاحظه بر مصرف بیش از حد آنتیبیوتیکها که میتواند باعث ظهور سویههای مقاوم S. Typhi و دیگر باکتریها شود، یک تست POC بهبودیافته تیفوئيد باید بهعنوان بخشی از یک الگوریتم درمانی و همراه با تستهای تشخیصی دیگر برای مالاریا و سایر عوامل بیماری حاد تبدار، استفاده شود. |
مقدمه
تب تیفوئید (تیفوئيد) یک عفونت باکــــــتریایی روده اســـــت که توسط Salmonella enterica سرووار Typhi (Salmonella Typhi; S. Typhi) ایجاد میشود. این بیماری یکی از شایعترین علل باکتریایی بیماری حاد تبدار در کشورهای در حال توسعه است؛ بهگونهای که تخمین زده میشود در سال ۲۰۱۷، 10/9 میلیون مورد جدید ابتلا و 116/8هزار مورد مرگ در اثر این بیماری رخ داده است. تب پاراتیفوئيد توسط Salmonella enterica سرووار Paratyphi A ,B ,C (S. Paratyphi) ایجاد و منجر به بیماریی میشود که دارای سندرم بالینی یکسان با تب تیفوئيد است، اما اغلب شدت کمتری دارد. تب تیفوئید در آسیای جنوبی و کشورهای جنوب صحرای آفریقا بیشترین شیوع را دارد و عمدتاً کودکان را آلوده میکند. تیفوئید مانند بسیاری از بیماریهای تبدار، بهویژه در مراحل اولیه خود علائم و نشانههای غیراختصاصی دارد. در نظامهای خدمات بهداشتی درمانی معمول در کشورهایی با درآمد متوسط یا کم (LMIC) شک به تب تیفوئيد بهطور معمول وجود دارد و بهصورت تجربی با آنتیبیوتیکها درمان میشود. این استفاده بیش از حد از آنتیبیوتیکها یک فشار انتخابی برای رشد مقاومت ضدمیکروبی (AMR) ایجاد میکند که منجر به ظهور و گسترش سویههای تیفوئیدی میگردد که در برابر همه آنتیبیوتیکهای خط اول درمان مقاوم هستند. همچنین، اختصاصیت پایین تستهای تشخیصی سریعِ (RDTs) فعلی میتواند منجر به تشخیص بیش از حد تب تیفوئيد شود که ممکن است استفاده بیش از حد از آنتیبیوتیکها را به دنبال داشته و درمان مناسب برای بیماریهای زمینهای را به تأخیر اندازد؛ بهعنوان مثال، استفاده از تست Widal حین شیوع بیماری حاد تبدار در نپال منجر به تشخیص نادرست تیفوئيد شد که به تأخیر در درمان مناسب برای عامل اصلی ایجادکننده (یعنی تیفوس) انجامید و در نتیجه دهها نفر کشته شدند. مضرات احتمالی RDTهای فعلی تیفوئيد با این واقعیت که آنها بهطور گستردهای در دسترس و ارزان بوده و بهآسانی استفاده میشوند، نادیده گرفته میشود.
جنبههای مختلفی از بیولوژي S. Typhi، تشخیص با استفاده از روشهای استاندارد آزمایشگاهی را به چالش کشیده است. S. Typhi میتواند از سد مخاطی دستگاه گوارش که سایر باکتریهای روده را محدود میکند، عبور کرده و میتواند با فعالسازی محدود مسیرهای التهابی از پاسخهای معمول ایمنی ذاتی بگریزد. عفونـــــــت باS. Typhi با تهاجم به مخاط ایلئوم انتهایی آغاز میشود و تصور بر این است که ارگانیسم تنها بهطور موقت و قبل از انتشار در سراسر سیستم رتیکولواندوتلیال به سمت مغز استخوان، کبد و طحال، در خون وجود دارد. لود باکتریایی در خون محیطی در هفته اول بیماری به اوج خود میرسد اما همچنان مقدار آن بسیار کم است؛ یعنی بهطور متوسط 1/0- 0/1 واحد تشکیلدهنده کلنی درمیلیلیتر در بیماران علامتدار. تشخیص این غلظت، با استفاده از کشت خون یا PCR دشوار است و در نتیجه حساسیت کمتری برای این تستهای تشخیصی نشان میدهد.
- S. Typhi یکی از اعضای خانواده انتروباکتریاسه است و آنتیبادیهایی که در پاسخ به عفونتهای قبلی با سایر انتروباکتریاسهها تولید شدهاند، به دلیل ثبات قابل توجه آنتیژنهای سطحی، تمایل به واکنش متقاطع با S.
Typhi دارند. این واکنش متقاطع، اختصاصیت سنجشهای تشخیصی مبتنی بر آنتیبادی را کاهش میدهد که اگر این مسئله وجود نداشت، این تستها ساده، سریع و ارزان مناسب میبودند. فارغ از این چالش، خاموش شدن پاسخ ایمنی که به واسطه پلیساکارید کپسولی Vi رخ میدهد، ممکن است مانع دیگری در استفاده از تستهای سرولوژیکی برای تشخیص تیفوئيد باشد.
در مراکز بالینی که از آزمایشگاه میکروبیولوژی بهرهمند میشوند، عفونت تهاجمی تیفوئـــید از طریق جداسازی S. Typhi از کشت خون تأئید میشود، اما این تست نسبتاً گران است و میتواند بیش از 48 ساعت طول بکشد، حساسیت کمی دارد و به زیرساختهای آزمایشگاهی و کارمندان آموزشدیدهای نیاز دارد که معمولاً در کشورهای کمدرآمد که تیفوئيد در آنجا بیشترین شیوع را دارد در دسترس نیستند. کشت مغز استخوان از حساسیت بالایی برای تشخیص S. Typhi برخوردار است، اما به دلیل تکنیکهای تهاجمی موردنیاز برای به دست آوردن آسپیرههای مغز استخوان بهطور معمول مورد استفاده قرار نمیگیرد. تست PCR برای تیفوئيد گران است و در صورت استفاده از نمونه خون محیطی، از حساسیت تشخیصی کمی برخوردار است. سایر آزمایشهای تشخیصی بر بالین بیمار (POC) موجود عبارتند از: تست Widal ،TUBEX ،Typhoidot ، Test-it Typhoid و سنجش تشخیصی تیفوئید- پاراتیفوئيد (TPTest). با این حال، همه این تستها دارای اشکالات قابلتوجهی هستند که استفاده بالینی از آنها را محدود میکند.
آزمایش سرولوژیکی به دلیل پایین بودن تیتر آنتیبادی در مراحل اولیه عفونت، محدودیتهایی دارد و بسته به زمان آزمایش، میتواند برای سنجشهای مبتنی بر IgM، نتایج منفی کاذب ایجاد کند. تست Widal یک تست آگلوتیناسیون کمّی است که آنتیبادیهای ضد آنتیژنهای O-somatic و H-flagellar موجود در Salmonella را شناسایی میکند. در صورتی که یک نمونه سرم در فاز بهبودی دارای تیتر چهار برابر بالاتر از نمونه حاد باشد، این آزمایش مثبت در نظر گرفته میشود؛
اما تست Widal معمولاً بهطور نادرست، فقط با یک نمونه فاز حاد انجام شده و برای تشخیص و درمان مورد استفاده قرار میگیرد. بازبینی کاکرین (Cochrane review)[1] از صحتRDTهای سریع مبتنی بر آنتیبادی تجاری موجود، حساسیت و اختصاصیت تستهای زیر را در حد متوسط نشان داد: رنگسنجی TUBEX که تیتر آنتیبادی anti-O:9 را شناسایی میکند (به ترتیب 78% و 87%)؛ الایزای نقطهای Typhidot که آنتیبادیهای IgG و IgM بر ضد پروتئینهای غشای خارجی S. Typhi را اندازهگیری میکند (8۴% و 79%) و سنجش ایمونوکروماتوگرافیک جریان جانبی Test-it Typhoid که آنتیبادی IgM علیه آنتیژن S. Typhi O را تشخیص میدهد (69% و 90%). TPTest یک آزمایش سرولوژیک جدیدتر است که IgA در گردش را با استفاده از ELISA با حساسیت و اختصاصیت بیش از ۹۵% تشخیص میدهد؛ اما این روش بهصورت تجاری در دسترس نیست، ۴۸-۲۴ ساعت طول میکشد تا نتیجه حاصل شود و نیاز به جداسازی و کشت سلولهای تکهستهای خون محیطی دارد که از نظر فنی چالشبرانگیز بوده و نیاز به تجهیزاتی دارد که بهطور گسترده در مناطقی با محدودیت منابع در دسترس نیست. با توجه به محدود بودن حساسیت تمامی تستهای POC فعلی تیفوئيد، نمیتوان برای هدایت درمان به آنها تکیه کرد.
یک RDT دقیق تیفوئید، در صورت توسعه و اجرای مؤثر میتواند با تشخیص سریعتر، مورتالیتی و موربیدیتی را کاهش دهد. علاوه بر این، میتواند به کاهش استفاده بیش از حد از آنتیبیوتیکهایی که باعث ظهور و گسترش سویههای مقاوم به چند دارو از S. Typhi و سایر باکتریها میشود، کمک کند. در سالهای اخیر، رویکردهای نوینی برای توسعه تستهای تشخیصی تیفوئيد با دقت بهبودیافته در مناطقی با محدودیت منابع، از جمله روشهای سرولوژی، مولکولی، متابولومیک، پروتئومیک و ترانسکریپتومیک شرح داده شده است؛ برای مثال، یک مطالعه جدید نشان داده است که IgA و IgM ضد لیپوپلیساکارید S. Typhi ممکن است یک مارکر خاص از عفونت حاد تیفوئيد و یک هدف نویدبخش برای تولید تست تشخیصی باشد.
با توجه به اینکه نیاز به مدیریت صحیح موارد تبدار مشهودتر است، نیاز به تشخیص ارتقایافته و مناسب تیفوئید برای استفاده در محیطهایی با منابع اندک اهمیت بیشتری مییابد. این گزارش با تکیه بر اقدامات اخیر پیرامون نظارت بهبودیافته بر تیفوئيد و پیشرفتهایی در تشخیص آن، توسعه یک پروفایل محصول هدف (TPP) در تلاش برای تعریف نیازهای تشخیصی برای این پاتوژن مهم را توصیف میکند. TPP با هدف هدایت توسعه محصول و اطمینان از یک راهحل بهینه که پاسخگوی نیازهای کشورهای اندمیک باشد و منجر به پیشرفت ملموس در مدیریت بیمار شود، تهیه شده است. علاوه بر این، TPP قصد دارد به بحث تشخیص بهعنوان یک بخش اساسی در دستور کار جهانی تیفوئيد جان تازهای ببخشد. این گزارش بر روند توسعه TPP با تأکید بر مشخصات کلیدی تست و نکات بحثبرانگیز اشارهشده توسط متخصصان تیفوئید و صاحبنظران باتجربه تمرکز دارد.
روشها
جمعآوری دادهها
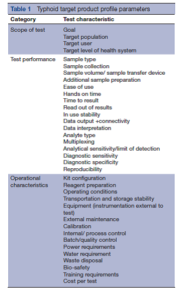
یک بررسی روشمند از مقالات تحقیقی مربوط به Salmonella Typhi با هدف تهیه پیشنویس TPP برای یک تست تشخیصی نسل جدید تیفوئيد با کمترین و بهینهترین مشخصات دلخواه، برای 36 مشخصه تست انجام شد. مشخصههای تست انتخابشده برای TPP بر اساس TPPهای قبلی منتشرشده از سوی بنیاد روشهای نوآورانهی تشخیصی جدید (Foundation for Innovative New Diagnostic)، انتخاب شده و شامل دامنه (scope)، جمعیت هدف، کاربری در نظر گرفتهشده، عملکرد مورد انتظار تست و همچنین پارامترهای عملیاتی و مالی میباشند (جدول ۱).
هر مشخصه تست مطلوب باید یکی از شرایط ذیل را دارا باشد:
حداقل شرایطی که یک آزمایش باید از آن برخوردار باشد تا برای ارائهدهندگان خدمات درمانی که بیماران را در مناطقی با منابع محدود معالجه میکنند مفید باشد، یا یک آستانه بهینه که تست را هم برای ارائهدهندگان مراقبتهای بهداشتی و هم بیماران بسیار مطلوب کند. پایگاه داده Ovid Medline در 21 ژوئن 2018 با استفاده از عنوان موضوع پزشکی (Medical Subject Heading; MeSH) «تب تیفوئيد» و زیرعنوان «تشخیص» بررسی شد. نتایج به مقالاتی با زبان انگلیسی که در 10 سال گذشته منتشر شدهاند، محدود شده است. عناوین و خلاصه مقالات بازیابیشده، برای موارد مرتبط بررسی گردید. مقالات موردنظر کاملاً توسط RGM برای محتوای مرتبط با TPP بازبینی شد. با جستجوی «تیفوئيد» در وبسایتهای کتابخانه کاکرین، WHO و FIND و با بررسی منابع و پژوهشهایی که به مقالههای منتخب در جستجوی اولیه ارجاع داده بودند، اسناد بیشتری شناسایی شدند. بهعنوان بخشی از بررسی مقالات تحقیقی، با صاحبنظران خبره برای نظرسنجی دلفی تماس گرفته شد.
نظرسنجی دلفی
برای مشارکت در تهیه پیشنویس TPP با استفاده از نظرسنجی دلفی، با صاحبنظران تماس گرفته شد. صاحبنظران شامل متخصصان پزشکی بالینی (۱۴=n)، پزشکی آزمایشگاهی (۲=n)، پزشکی تشخیصی (۱۱=n) و سلامت عمومی و جهانی (۶=n) بودند. از یک نظرسنجی آنلاین (فایل ضمیمه آنلاین ۱) استفاده و از پاسخدهندگان خواسته شد تا میزان موافقت خود را با هر یک از مشخصههای TPP با استفاده از مقیاس Likert ارزیابی کنند (۱= شدیداً مخالف، ۲= مخالف، ۳= نه موافق و نه مخالف، ۴= تقریباً موافق، ۵= کاملاً موافق). توافق عمومی به این صورت تعریف شد: بیشتریا مساوی ۷۵% پاسخدهندگان با آن مشخصه TPP تقریباً موافق یا کاملاً موافق باشند. نتایج بهدستآمده از دور اول نظرسنجی (اکتبر ۲۰۱۸) برای تصحیح TPP مورد استفاده قرار گرفت و پیشنویس TPP دوم بین همه شرکتکنندگان اولیه بهعلاوه دو شرکتکننده دیگر که پس از تکمیل دور اول شناسایی شده بودند، توزیع شد.
مشارکت بیماران و عموم
با توجه به حضور صاحبنظران اصلی در تهیه TPP، عموم مردم یا بیماران در این پژوهش شرکت نداشتند.
نتایج
جستجو در Ovid Medline با استفاده از MeSH «تب تیفوئيد»، ۱۰۶۹۸ نتیجه در بر داشت که ۱۵۵۸ مورد حاوی زیرعنوان «تشخیص» بودند. محدود ساختن جستجو به مقالات منتشرشده پس از ۱ ژانویه ۲۰۰۸ به زبان انگلیسی، ۲۹۸ مقاله را در اختیار ما گذاشت که از نظر مرتبط بودن به موضوع مورد بررسی قرار گرفتند. همانطور که در بخش روشها اشاره شد، اسناد دیگری نیز اضافه شد و مقالات منتخب کاملاً بازبینی شدند تا یک پیشنویس TPP با کمترین و بهینهترین معیارهای مشخصههای تست ذکرشده در جدول ۱ تهیه شود.
بازخوردها در مورد پیشنویس TPP در خلال اولین دور نظرسنجی دلفی، از صاحبنظران اصلی بهدست آمد که از 40 صاحبنظرکه با آنها تماس گرفته شده بود، 19 نفر ( ۴۸ %) نظرسنجی را تکمیل کردند. پاسخدهندگان این نظرسنجی گزارش دادهاند که تجربه کار در مناطقی با منابع اندک در آفریقا (۱۴=n)، آمریکا (۲=n)، اروپا (۲=n)، مدیترانه شرقی (۲=n)، آسیای جنوب شرقی (۱۲=n) و منطقه اقیانوس آرام غربی (۲=n) را داشتهاند؛ همچنین برخی از پاسخدهندگان تجربه کار در بیش از یک منطقه را داشتهاند. توافق عمومیِ بیشتر یا مساوی ۷۵% برای ۳۴ معیار TPP از ۳۶ معیار، حاصل شد. معیارهای TPPای که بیشترین بحث را در نظرسنجی دلفی ایجاد کرده بودند، مربوط به دامنه (scope) تست شامل هدف، جمعیت هدف، سطح سیستم مراقبتهای بهداشتی، حساسیت و اختصاصیت تشخیصی و همچنین هزینه تست، میشد. بر اساس بازخورد بهدستآمده از پاسخدهندگان به نظرسنجی، مولتی پلکسینگ «multiplexing» بهعنوان یک مشخصة TPP کنار گذاشته شد و معیارهای TPP حداقل و مطلوبِ باقیمانده مورد بررسی قرار گرفتند. در مورد معیارهایی که به توافق عمومی رسیده بودند، درصورتیکه پاسخدهندگان پرسشنامه پیشنهادهای قانعکنندهای برای بهبود ارائه میدادند، تجدیدنظر صورت میگرفت.
پیشنویس دوم TPP بین 19 نفری که به نظرسنجی اولیه دلفی پاسخ دادند و دو صاحبنظر دیگر که پس از اتمام دور اول شناسایی شدند، توزیع شد. در مجموع 12 نظرسنجی تکمیلشده از 13 صاحبنظر بهدست آمد که دو نفر از آنها که یک نظرسنجی مشترک ارائه کردند و توافق عمومی برای 33 مشخصة TPP از ۳۵ مشخصه (۹۴%) حاصل شد. دو معیار که آستانه توافق عمومی را کسب نکرده بودند، عبارتند از سطح هدف در سیستم بهداشتی درمانی و حساسیت تشخیصی که هر دو 67% موافقت کسب کردند. بازخورد پاسخدهندگان نظرسنجی برای تجدیدنظر در این دو معیار و برای ایجاد تغییرات جزئی در چهار معیار که بیشتر یا مساوی ۷۵% موافقت را کسب کرده بودند، قبل از قرار دادن در نسخه نهایی TPP که در جداول 2 تا 4 ارائه شده است، استفاده شد.
دامنه آزمون
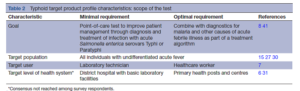
بازخورد نظرسنجی دلفی تأکید کرد که RDT نسل جدید برای تب تیفوئيد، نباید صرفاً روی تشخیص S. Typhi متمرکز باشد. برای کاهش استفاده تجربی از آنتیبیوتیکها که باعث ایجاد فشار انتخابی برای AMR میشوند، یک RDT تیفوئيد باید بهطور ایدهآل با تست تشخیصی مالاریا و سایر علل بیماریهای حاد تبدار بهعنوان بخشی از الگوریتم مدیریت بیمار، همراه شود (جدول 2). با توجه به تظاهرات بالینی مشابه و تغییر اپیدمیولوژی S. Typhi و S. Paratyphi، پاسخدهندگان نظرسنجی توصیه کردند که یک آزمایش نسل جدید تب تیفوئید باید بتواند هم S. Typhi و هم S. Paratyphi را تشخیص دهد.
جمعیت هدف بر اساس دادههای منتشر شده از آفریقا و آسیا مشخص شد. کودکان با سن 2 تا 14 سال بار جهانی تیفوئید را به خود اختصاص دادهاند اما از این نظر که چه کسانی بیشتر آلوده میشوند، تنوع قابلتوجهی در داخل یک منطقه و بین مناطق مختلف وجود دارد. یک مطالعه جدید در پاکستان میزان ابتلای بزرگسالان به تب تیفوئید را بیشتر از کودکان نشان داد. این دادهها، همانگونه که در نظرسنجی دلفی مشخص شد، نیاز به وجود یک RDT تیفوئيد را که بتواند بیماری را در افرادی با همه سنین تشخیص دهد، برجسته میسازد. یک تست POC نسل جدید تیفوئيد باید بتواند بیماری را در تمام افراد با تب افتراق دادهنشده در هر مرحلهای از بیماری، از هنگام بروز تب تا زمانی که تحت مراقبت قرار میگیرند، بهدقت تشخیص دهد.
هنگام طراحی تستهای تشخیصی جدید، سطح سیستم بهداشت و درمانی که تست در آن انجام خواهد شد یک ملاحظه حائز اهمیت است. Ghani و همکاران، پنج سطح مختلف از سیستم مراقبتهای بهداشتی و انواع مختلفی از ابزارهای تشخیصی یا پروگنوستیک مناسب برای هر سطح را مشخص کردهاند. تیفوئيد در مناطق کمدرآمد با منابع بهداشتی درمانی محدود، بیشترین شیوع را دارد و در این موارد تست تیفوئيد بهینه نباید به تجهیزات پیچیده نیاز داشته باشد و باید بتواند بهسادگی توسط پرسنل غیرآزمایشگاهی تفسیر شود.
پاسخدهندگان موافق بودند كه يك تست بهصورت بهینه باید در كمترين سطح يك سیستم بهداشتي قابلاستفاده باشد چرا که در بسياري از موارد پرسنل بهداشت اجتماعي، بيماران را در محيط غيررسمي معاینه میکنند. با این وجود، از آنجا که استاندارد طلایی کنونی یعنی کشت خون، نیاز به تجهیزات آزمایشگاهی دارد، اما حساسیت و اختصاصیت آن کمتر از حد مطلوب است، برخی از پاسخدهندگان احساس کردند در صورتی که یک RDT تیفوئيد بتواند تمام معیارهای TPP را برآورده سازد آنگاه لزوم وجود تجهیزات آزمایشگاهی اولیه و پرسنل آزمایشگاهی آموزشدیده برای انجام آن تست، قابلقبول خواهد بود. براساس بازخورد دور اول نظرسنجی دلفی، حداقل سطح هدف، برای سطح بالاتر سیستمهای بهداشتی تنظیم شد، اما توافق عمومی حاصل نشد، زیرا برخی از پاسخدهندگان بهشدت احساس میکردند که از حداقل ملزومات یک تست این است که بتواند در محیط غیررسمی در پایینترین سطح سیستم بهداشتی استفاده شود.
عملکرد آزمون
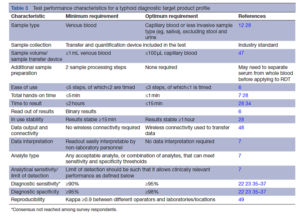
کشت خون معمولاً بهعنوان استاندارد مرجع برای تشخیص حصبه مورد استفاده قرار میگیرد، اما نیاز به تجهیزات پیشرفتهای دارد که در کشورهای کمدرآمد که در آنها تیفوئيد، اندمیک است؛ بهراحتی در دسترس نیست. کشت خون برای تیفوئید، به دلیل اندک بودن لود باکتری در خون محیطی به حداقل به ۱۰-۲ میلیلیتر خون وریدی نیاز دارد و حساسیت اندکی دارد؛ بهگونهای که در یک پژوهش مروری سیستماتیک جدید، حساسیت آن را تنها ۶۱% تخمین زدهاند. استاندارد مرجع ترکیبی (composite reference standard; CRS) که به معنای استفاده ترکیبی از چندین تست با اختصاصیت بالا اما با حساسیت کمتر از حد مطلوب است؛ بهعنوان یک راه احتمالی برای بهبود دقت تشخیصی پیشنهاد شده است. ترکیبات مختلفی از تستهای گوناگون بهعنوان CRS برای تیفوئيد استفاده شدهاند، اما پاسخدهندگان در این فعالیت دلفی توصیه کردند که پذیرش یک ترکیب استانداردشده، پیش از قرار گرفتن آن در TPP، ضروری است.
رایجترین تستهای POC تیفوئيد (Widal، Typhidot، Tubex، Test-It Typhoid، TPTest) نیازمند µL ۵ تا mL۱ خون هستند اما حساسیت و اختصاصیت متوسطی دارند. پاسخدهندگان توافق کردند که یک RDT نسل جدید تیفوئيد باید از نمونه خون مویرگی با حجم ≤ ۱۰۰ میکرولیتر یا یک روش نمونهگیری کمتر تهاجمی بهاستثنای نمونه ادرار و مدفوع، استفاده کند. با این وجود، به دلیل دشواری فعلی در تشخیص دقیق تب تیفوئيد، پاسخدهندگان تصریح کردند که کمتر یا مساوی ۱ میلیلیتر خون وریدی، حداقل مقدار قابلقبول است (جدول ۳). TPP امکان انجام دو مرحله پردازش نمونه را فراهم میکند زیرا ممکن است RDT نیاز به جداسازی سرم از خون کامل داشته باشد. حداکثر مراحل تست میتواند ۵ مرحله باشد که بیش از دو مرحله آن نباید زماندار باشد و کل زمان فرایند دستی (hands-on) باید کمتر از ۵ دقیقه باشد. بر اساس یک TPP مورد توافق تخصصی برای تشخیص بیماری حاد تبدار، عملکرد RDT بهطور ایدهآل دارای ۳ یا ۴ مرحله است که حداکثر یک مرحله آن زماندار است و زمان کل فرایند دستی یک دقیقه یا کمتر است.
با توجه به اینکه یک تست تشخیصی جدید تیفوئيد، بیشترین تأثیر را بر روی تجویز دارو و پیامدهای بالینی خواهد داشت، لازم است نتایج تست در کمتر از چند ساعت آماده شود. توافق عمومی بر این بود که شرایط بهینه باید نتایج را در عرض ۱۵ دقیقه در دسترس قرار دهد تا با میانگین زمان دیگر تستهای تشخیصی POC که عموماً در مناطق کمدرآمد استفاده میشود (مانند RDTهای تشخیصدهنده آنتیژن مالاریا) مطابقت داشته باشد. حداقل شرط لازم برای زمان ارائه نتایج ۲ ساعت تعیین شد، این زمان در مقایسه با زمان بیش از ۴۸ ساعت برای کشت خون، یک پیشرفت قابلملاحظه است و مدت زمان ۲ ساعت، طولانیترین زمانی است که میتوان برای انتظار بیمار سرپایی برای دریافت نتیجه در نظر گرفت؛ بهویژه در مناطق روستایی که بیماران ممکن است برای مراجعه به مراکز درمانی مسافتهای طولانی را طی کنند.
محققان پیشنهاد دادهاند که یک تست تشخیصی ایدهآل برای تیفوئيد، باید بهسادگی بهصورت مثبت/ منفی خوانده شود، مانند تست بارداری خانگی و نتایج نیز باید توسط پرسنل غیرآزمایشگاهی قابل تفسیر باشد؛ بنابراین TPP تیفوئید، نیازمند خوانش دوتایی (binary read-out) نتایج و دادههایی است که یا نیازی به تفسیر نداشته باشند یا بهسادگی تفسیر شوند. هیچگونه آنالیت خاص یا محدودیت در شناسایی، در TPP تیفوئید مشخص نشده است، هرگونه آنالیت یا ترکیبی از آنالیتها در صورتی که تمام شرایط TPP را برآورده سازند، قابلقبول هستند.
بر اساس دادههای حاصل از مدلسازی و نظرات متخصصان، حداقل شرط TPP برای حساسیت تشخیصی، حساسیت ≥ ۹۰% و حساسیت بهینه ≥ 95% است. در نظرسنجی دلفی، توافق عمومی در مورد حساسیت تست بهدست نیامد که نشاندهنده اختلاف اساسی در نظرات تخصصی منتشرشده در رابطه با دقت مطلوب برای RDT تیفوئيد است. با وجود این، پاسخدهندگان به نظرسنجی دلفی بر روی حداقل اختصاصیت ۹۵% و اختصاصیت بهینه ۹۸% به توافق عمومی دست یافتند.
مشخصات عملیاتی
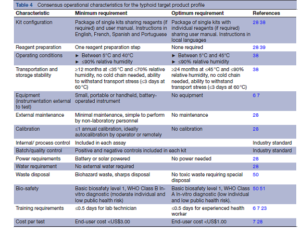
پاسخدهندگان به نظرسنجی بر روی مشخصات عملکردی TPP تیفوئيد، توافق داشتند (جدول ۴). کیتهای تست تشخیصی تیفوئید بر اساس مشخصات TPP برای دیگر تستهای POC در نواحی اندمیک تیفوئيد، در حالت ایدهآل باید شامل تستهای بستهبندیشده بهصورت تکی و معرفهای جداگانه برای هر بسته (در صورت نیاز) و نیز یک بروشور راهنما به زبان محلی باشد. تا یک مرحله آمادهسازی واکنشگرها قابلقبول است تا امکان ترکیب واکنشگرهای پودری فراهم شود. تست نباید به زنجیره سرد نیاز داشته باشد و در دمای بالا و رطوبت زیاد که در بسیاری از مناطق آفریقا و آسیا که تیفوئيد در آنجا شایع است، عمل کند.
در حال حاضر اکثر درمانهای تیفوئيد در مراکز سرپایی از جمله مراکز پزشکی غیررسمی، ارائه میشوند؛ بنابراین یک تست POC نباید به هیچگونه تجهیزات پیچیده یا زیرساختهای آزمایشگاهی رسمی نیاز داشته باشد. یک ابزار کوچک، قابل حمل یا دستی (handheld) که با باتری کار میکند، قابلقبول است اما در حالت ایدهآل نباید به هیچ تجهیزاتی نیاز داشته باشد. برای آنکه کاملاً بدیع و متحولکننده باشد؛ یک POC تیفوئيد باید در مراکزی بدون منبع قابلاطمینان آب یا برق نیز قابل استفاده باشد. اگر به نیروی برق نیاز داشته باشد، باید از طریق ترکیبی از باتریهای قابل شارژ و انرژی خورشیدی، این نیرو تأمین شود.
درمان تجربی و غیرعلمی بیماران مشکوک به تیفوئيد رایج است و عموماً از آنتیبیوتیکهای نسبتاً ارزان استفاده میشود. برای کاهش استفاده بیش از حد از آنتیبیوتیکهای تجربی، هزینه تمامشده یک POC تیفوئيد برای مصرفکننده، کمتر از ۳ دلار امریکا (شرط حداقلی) یا کمتر از ۱ دلار امریکا (شرط بهینه) تعیین شده است که معادل هزینه آنتیبیوتیکهای تجربی در مناطق اندمیک است. بازخورد نظرسنجی دلفی نشان داد که بالاترین هزینه تمامشده مصرفکننده باید معادل ۱ دلار امریکا باشد.
بحث
تستهای تشخیصی تیفوئيد در حال حاضر فاقد حساسیت و اختصاصیت موردنیاز برای تشخیص دقیق در POC هستند که منجر به استفاده بیش از حد از آنتیبیوتیک در قالب درمان تجربی شده است. WHO فهرستی از مشخصههایی تهیه کرده است که یک تست را برای مناطقی با منابع محدود که تیفوئيد در آنجا اندمیک است مناسب میسازد: ASSURED سرواژهای است برای مقرون به صرفه (affordable)، حساس (sensitive)، اختصاصی (specific)، کاربرپسند (user-friendly)، سریع و قوی (rapid and robust)، بینیاز از تجهیزات (equipment-free) و تحویل به افرادی که به آن نیاز دارند (delivered to those in need). TPPها بر اساس این عیارها تدوین میشوند و بهطور روزافزون در جامعه جهانی بهداشت برای هدایت تولید تستهای تشخیصی و آگاه ساختن اهدا کنندگان در مورد اولویتهای بهداشت جهانی، مورد استفاده قرار میگیرند. این TPP، مشخصات مطلوب برای یک RDT بهبودیافته تیفوئيد را در دو سطح «حداقل» و «بهینه» مشخص کرده است و با هدف تسریع تولید یک ابزار تشخیصی بهینه که نیازهای کاربران در نواحی اندمیک را برآورده سازد، طراحی شده است.
مقاومت آنتیبیوتیکی یک تهدید افزاینده در درمان تیفوئيد است؛ بهگونهای که سویههای S. Typhi که به سه آنتیبیوتیک خط اول درمان مقاوم شدهاند در حال حاضر در بخشهایی از آسیا و آفریقا شایع هستند. ظهور کلونیهای مقاوم به چند دارو در ایالت سند پاکستان که مقاومت دیگری به فلوروکینولونها و سفالوسپورینهای نسل سوم نیز کسب کرده است؛ بهعنوان S. Typhi با مقاومت دارویی گسترده (extensively drug resistant) شناخته میشود و این امر باعث شده است که آزیترومایسین و داروهای کارباپنم داخل وریدی گرانقیمت بهعنوان تنها گزینههای درمان آنتیبیوتیکی برای برخی بیماران در نظر گرفته شوند. گزارشهای موردی پراکندهای از S. Typhi مقاوم به آزیترومایسین وجود دارد، اما اگر سویههای بسیار مقاوم در برابر دارو، مقاومت به آزیترومایسین را بهدست آورند، کارباپنمها بهعنوان تنها روش درمانی مؤثر باقی میمانند. برای جلوگیری از شیوع بیشتر S. Typhi مقاوم، انجام تست حساسیت به دارو برای هر بیمار قبل از شروع درمان با آنتیبیوتیک میتواند مفید باشد. تست حساسیت به دارو بهعنوان یکی از الزامات و شروط TPP، مطرح نشده است؛ زیرا به دلیل ماهیت در حال تحول مقاومت تیفوئيد، احتمالاً امکان انجام در تستهای POC بدون کشت خون، وجود نخواهد داشت و میتواند باعث پیچیده شدن تفسیر نتایج تست برای کاربران در مناطقی با سطح پایین بهداشتی شود. با این حال، برخی از پاسخدهندگان نظرسنجی دلفی احساس کردند که یک RDT که قرار است برای همیشه جایگزین کشت خون شود، باید تست حساسیت به دارو را هم شامل بشود. استفاده از یک RDT که تشخیص را با اطلاعات اپیدمیولوژیکی در مورد حساسیت آنتیبیوتیکی سویهها ترکیب کند و در فواصل زمانی مشخص بهروزرسانی شود، میتواند یک راهحل مناسب باشد.
مطالعه Global Burden of Disease 2017 تخمین زده است که S. Paratyphi سالانه 3/4 میلیون نفر را تحت تأثیر قرار میدهد و 19/1 هزار مرگ در پی دارد؛ اما در مقایسه، S. Typhi 10/9 میلیون مورد ابتلا و 116/8 هزار مرگ را در پی دارد. بیشتر بودن موربیدیتی و مورتالیتی S. Typhi، آن را به نگرانی بزرگتری در زمینه بهداشت عمومی تبدیل کرده است اما با توجه به افزایش شیوع S. Paratyphi در برخی نواحی خاص، احتیاط حکم میکند یک تست نسل جدید بتواند علاوه بر S. Typhi، S. Paratyphi را هم تشخیص دهد. بازخورد نظرسنجی دلفی اشاره میکند که عدم توانایی تست در تشخیص S. Paratyphi میتواند اطمینان بالینی به تست POC نسل جدید تیفوئيد را کاهش دهد چرا که S. Typhi و S. Paratyphi میتوانند موجب سندرمهای بالینی غیرقابل افتراق شوند. با توجه به تداوم گسترش تیفوئيد مقاوم به دارو، ممکن است افتراق این دو سویه از یکدیگر پیش از شروع درمان لازم باشد، زیرا آنها ویژگیهای حساسیت آنتیبیوتیکی متفاوتی دارند.
حداقل شرایط تشخیصی برای RDT تیفوئید در این TPP، حساسیت ≥ ۹۰% و اختصاصیت ≥ 9۵%، با آستانه بهینه ≥ 9۵% برای حساسیت و ≥ 9۸% برای اختصاصیت است. در نظرسنجی دلفی، توافق عمومی در مورد اختصاصیت تست حاصل شد اما برای حساسیت توافق بهدست نیامد؛ این امر نشاندهنده تغییرپذیری گسترده در پژوهشهای منتشرشده است که در آنها بازه هدف 90%- 80% برای حساسیت و 98%- 90% برای اختصاصیت پیشنهاد شده است.
حساسیت اندک کشت خون بهعنوان استاندارد مرجع برای تشخیص تیفوئید، ارزیابی دقیق کارایی تستهای تشخیصی جدید را دشوار ساخته است. صحت تشخیصی را میتوان با شناسایی قابلاطمینان عفونتهای دیگر و با استفاده از CRS که نتایج چندین تست را با یکدیگر ترکیب میکند، بهبود بخشید. CRSهایی که برای تشخیص تیفوئید استفاده شدهاند عبارتند از کشت خون و یا یافتههای بالینی؛ کشت خون و یا تست Widal؛ کشت خون و یا PCR؛ کشت خون، تست Widal و یا یافتههای بالینی؛ کشت خون، PCR و یا تست widal. ارزیابی CRSها با فقدان سازگاری بین پژوهشها، محدود است بهگونهای که یک مرور سیستماتیک، ۲۱ مقاله را شناسایی کرده است که استفاده از CRS را بهعنوان روش مرجع برای تشخیص تیفوئید پیشنهاد کردهاند، اما هیچ دو مطالعهای از یک CRS یکسان استفاده نکردهاند. برای اینکه یک CRS تکرارپذیر باشد، پیشنهاد شده است که اجزای تشکیلدهنده هر تست باید استانداردسازی شده باشند، نشانههای بالینی با تعاریف WHO از بیماران مشکوک به تب تیفوئيد مطابقت داشته باشند، سنجشها باید بهصورت تجاری در دسترس بوده و پارامترهای کشت خون باید بهخوبی تعریف شده باشند. قبل از اینکه بتوان CRS را در TPP تیفوئيد قرار داد، لازم است پژوهشهای بیشتری برای شناسایی یک CRS استانداردشده انجام شود.
تب تیفوئيد از طریق مسیر مدفوعی دهانی با مصرف آب و غذای آلوده به S. Typhi موجود در مدفوع انسان منتقل میشود و در مناطقی با کمبود منابع که به آب سالم و مناسب دسترسی ندارند، اندمیک است. اگرچه ارتقاء زیرساختها برای تأمین آب سالم، سیستم تخلیه فاضلاب و امکانات بهداشتی میتواند ابتلا به تیفوئید را کاهش داده یا از بین ببرد، اما این موارد، اقدامات پرهزینه و بلندمدت میباشند. واکسن Typbar- TCV که بهتازگی تأئید شده است میتواند به کاهش بار جهانی تب رودهای ناشی از S. Typhi کمک کند، اما تست تشخیصی بهبودیافته برای تخمین دقیق میزان بروز بیماری و تسهیل گسترش هدفمند واکسن ضروری است. برای اثرگذاری قابلملاحظه بر مصرف بیش از حد آنتیبیوتیکها که میتوانند باعــــث ظهور سویههای مقاوم S. Typhi و دیگر باکتریها شوند، یک تست POC بهبودیافته تیفوئيد باید بهعنوان بخشی از یک الگوریتم درمانی و همراه با تستهای تشخیصی دیگر برای مالاریا و سایر عوامل بیماری حاد تبدار، استفاده شود. استفاده از یک تست تشخیصی اختصاصی برای یک بیماری، بهتنهایی برای یک بیمار تبدار، در صورت مثبت بودن میتواند مفید باشد اما یک تست منفی همانگونه که در مورد مالاریا مشاهده شده است، میتواند به آنتیبیوتیک درمانی تجربی منجر شود. تست حساسیت دارویی برای S. Typhi که در آزمایشگاههای مرجع انجام میشود، میتواند الگوریتمهای درمانی محلی را که بر اساس حساسیت آنتیبیوتیکی محلی هستند، ارتقا دهد.
این پژوهش اولین TPP جامع برای یک تست POC نسل جدید تب تیفوئيد است. محدودیت اصلی این پژوهش، فقدان توافق عمومی بر روی تمامی مشخصههای TPP و نرخ مشارکت نسبتاً پایین در دور دوم نظرسنجی دلفی بود. با توجه به مقدار زمان لازم برای دریافت بازخورد در مورد همه ۳۵ مشخصه TPP، مدت زمان نظرسنجی میتواند مانعی برای تکمیل آن باشد. بحثهای بیشتری بین جامعه تیفوئید لازم است تا سطح هدف بهینه برای سیستم بهداشتی درمانی و حساسیت تشخیصی موردنیاز تعیین شود. با اینکه این TPP اولین گام در راستای نشان دادن نیازهای تشخیصی تیفوئید است، اما برای حفظ و تداوم گفتگوها و پیوستن بانیان بهداشت جهانی، توسعهدهندگان تستها و سیاستگذاران ملی به این بحث ضرورت دارد؛ این بحث مهم که ابزارهای تشخیصی بهبودیافته و نوآوریهای مشابه چگونه باید در راستای ارتقاء دادههای نظارتی و پشتیبانی از تصمیمات مدیریت بیمار، در قالب خدمات بهداشت جهانی، مورد استفاده قرار گیرند.
برگردان از:
Redefining typhoid diagnosis: what would an improved test need to look like?
Mather RG, et al. BMJ Global Health 2019;4:e001831. doi:10.1136/bmjgh-2019-001831
[1] Cochrane Collaboration (بنیاد همکاری کاکرین)
برای دانلود پی دی اف بر روی لینک زیر کلیک کنید
ورود / ثبت نام