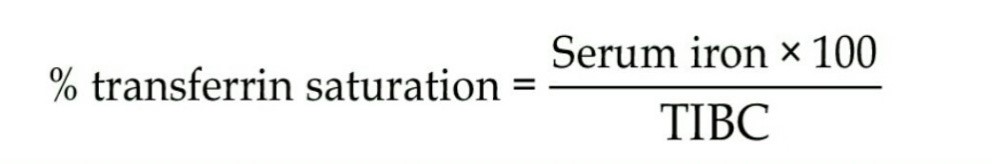تفسير دامنههای مرجع در خونشناسی
(4)
دكتر حبیبالله گلافشان، عضو هيئت علمي دانشگاه علوم پزشكي شيراز
نگين شكرگزار، كارشناس ارشد هماتولوژی و بانک خون دانشگاه علوم پزشكي شيراز
غلظت اریتروپویتین (EPO)
اریتروپویتین گلیکوپروتئینی به وزن 35 کیلودالتون است که بهطور عمده از کلیه و به مقدار بسیار کمتر از کبد ترشح میشود. ژن EPO روی کروموزوم شماره 7 است و در پاسخ به کمخونی و هیپوکسی افزایش بیان مییابد. اندازهگیری EPO با متدهای مختلف متفاوت است و سریال اندازهگیری آن برای یک بیمار بایستی با یک روش صورت گیرد.
غلظت نرمال اریتروپویتین 16- 3 واحد اینترناسیونال در میلیلیتر است (unit/ml). در تمام کمخونیها بهجز آنمی ناشی از نارسایی کلیه، غلظت آن افزایش مییابد و ازاینرو اندازهگیری آن میتواند برای درمان آنمی ناشی از نارسایی کلیه با اریتروپویتین سودمند باشد. افزایش EPO در پرخونیهای ثانویه و سطح نرمال يا كاهش آن در پلیسیتمی ورا مشاهده میشود.
برخی تومورها با ترشح پارانئوپلاستیک EPO باعث افزایش هموگلوبین میگردند؛ ازاینرو سونوگرافی شکم برای هر بیمار بهویژه خانمهای پرخون برای تشخیص بیماریهای کلیه، تخمدان و رحم سفارش میشود. آزمایش جهش Jak2V617F و جهش های اگزون 12 ژن Jak2 در بیش از 95% بیماران مبتلا به پرخونی ورا مثبت است.
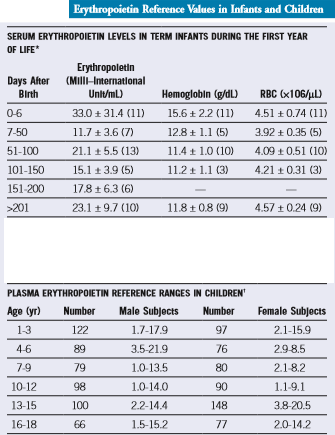
جدول زیر، مقادیر EPO را در سنین مختلف نشان میدهد.
محدوده 95 درصد طبیعی سطح اریتروپویتین از یک سالگی تا 18 سالگی
آهن سرم و ظرفیت ترانسفرین
آهن سرم (Sfe) و ظرفیت ترانسفرین (TIBC) از آزمایشهای روتین برای تشخیص کمبود آهن و اسکرین کردن بیمار از نظر هماکروماتوز میباشد. اشباع ترانسفرین از حاصل SFe×100/TIBC بدست میآید که کمتر از 15% بیانگر فقر آهن است و بیشتر از 55% همراه با فریتین بیشتر از 200 ممکن است بازتابی از هماکروماتوز ارثي باشد و نیاز به آزمایش ژنتیک برای بررسی جهش در ژنهای Hfe (پروتئین هماکروماتوز)، HAMP (هپسیدین)، HJV (هموژوولین)، TFR2 (گیرنده ترانسفرین 2) و 1-FPn (فروپورتین) میباشد. بهجای آزمایش TIBC میتوان مقدار ترانسفرین را اندازه گرفت.
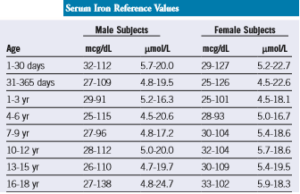
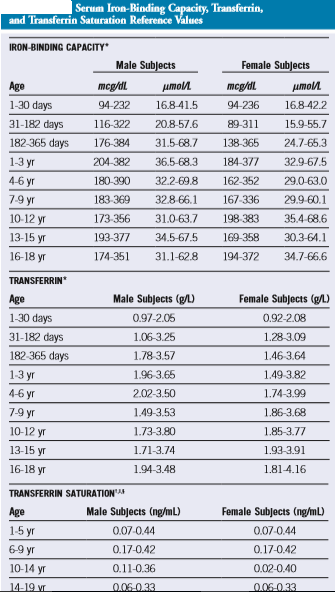
جدول زیر، مقادیر پارامترهای آهن در سنین مختلف را نشان میدهد.
دامنههای 95 درصد طبیعی پروفایلهای آهن سرم، TIBC و اشباع ترانسفرین
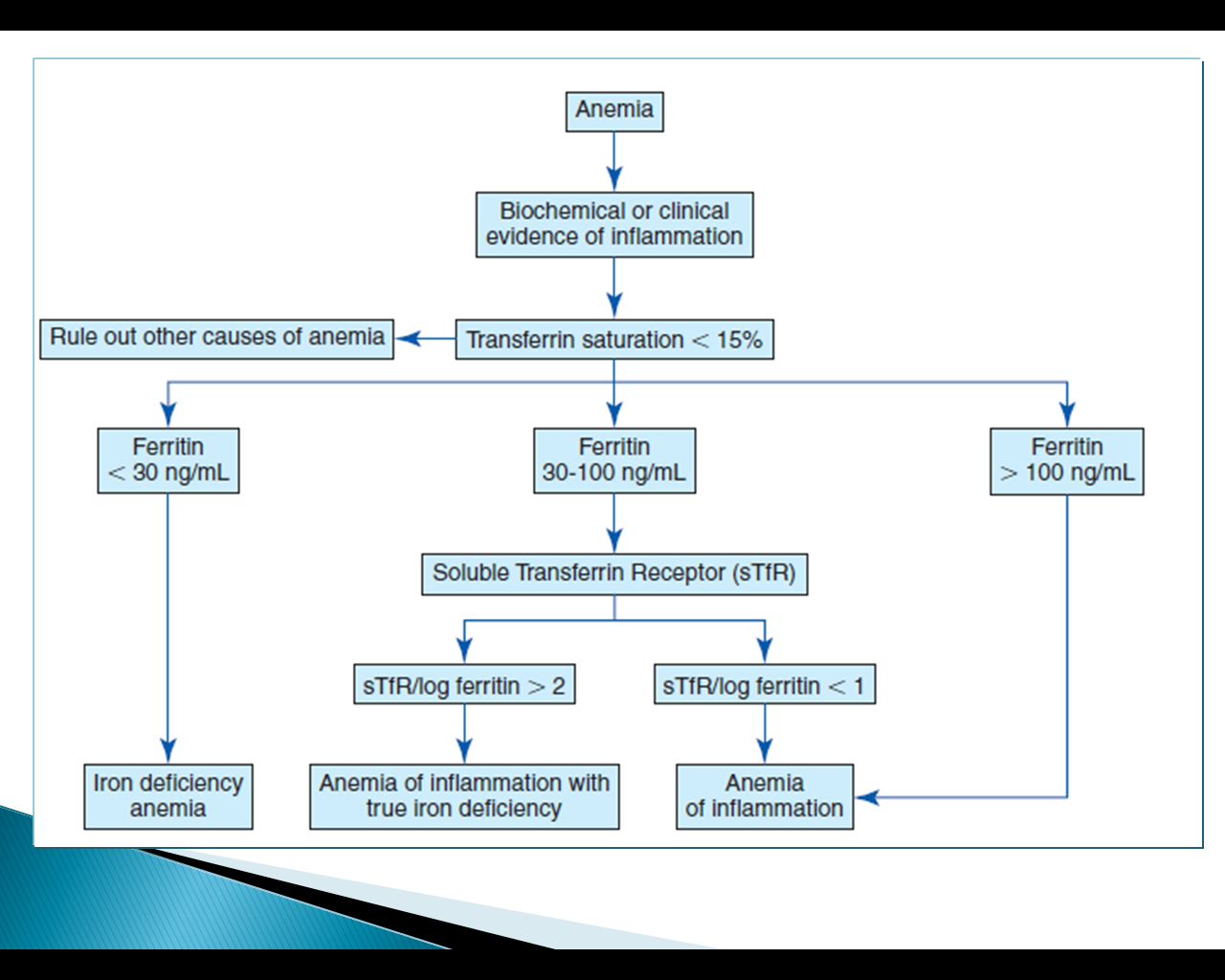
الگوریتم افتراق آنمی فقر آهن از آنمي بیماریهای مزمن با پارامتر فریتین و اندکس گیرنده محلول ترانسفرین به لگاریتم فریتین
برای اندازهگیری فریتین چنانچه بیمار قرص آهن مصرف میکند نیازی به قطع کردن قرص نداشته اما برای اندازهگیری SFe و TIBC نیاز به قطع قرص برای 2 تا 3 روز است. حاملگی و قرصهای ضدبارداری موجب افزایش ترانسفرین و درنتیجه کاهش اشباع ترانسفرین میگردند. ترانسفرین در گروه پروتئینهای فاز حاد منفی است و بیماریهای التهابی با کاهش سنتز ترانسفرین از سوی کبد، مقدار SFe را کاهش و TIBC را نرمال نموده یا کاهش میدهند. افزایش باورنکردنی و بسیار زیاد TIBC در هپاتیت حاد و بعد از تزریق آمپول آهن رخ میدهد.
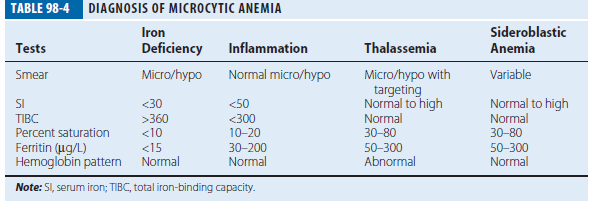
دادههای آزمایشگاهی پارامترهای آهن در چهار آنمی که همگی ممکن است با مرفولوژی میکروسیت و هایپوکروم نمایان شوند
گیرنده محلول ترانسفرین در پلاسما (STFR)
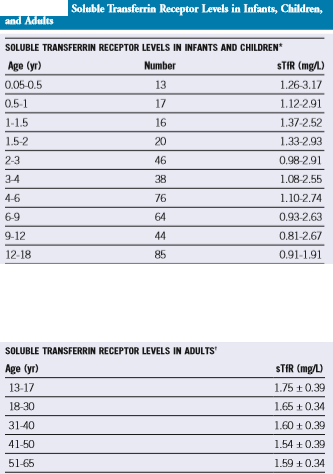
گیرنده محلول ترانسفرین از شکسته شدن گیرندههای ترانسفرین از سطح سلولهای اریتروئیدی مغز استخوان در پلاسما رها میشوند و برخلاف فریتین، اندازهگیری آن تحت اثر التهاب و عفونت قرار نگرفته و برخلاف SFe دارای تغییرات روزانه نمیباشد. سنجش STFR بهوسیله ایمونواسی صورت گرفته و افزایش آن بیانگر آنمی فقر آهن در حضور بیماریهای التهابی است. مقدار STFR ارتباط مستقیمی با جرم اریتروئیدی در مغز استخوان دارد و هایپرپلازی اریتروئیدی و نیاز به آهن موجب افزایش STFR میشود. جدول زیر، مقادیر نرمال STFR در کودکان و بزرگسالان را نشان میدهد.
دامنه طبیعی گیرنده محلول ترانسفرین در سنین مختلف
نمونه برای انجام آزمایش بایستی همولیز و لیپمیک نباشد و بیمار ترانسفیوژن اخیر نداشته باشد. با محاسبه اندکس STF / Log Ferritin میتوان آنمی فقر آهن را از آنمی بیماریهای مزمن تشخیص داد. مقدار بیشتر از 1/8 بیانگر فقر آهن است.
اندازهگیری فریتین
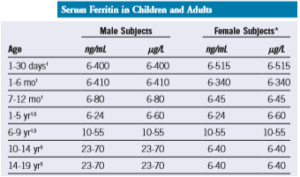
غلظت فریتین بازتابی از آهن ذخیره است و هر میکروگرم آن معادل 8 تا 10 میلیگرم آهن ذخیره است. کاهش کمتر از 12 میکروگرم در لیتر بیانگر تهی شدن ذخایر آهن و افزایش 300- 200 میکروگرمی آن همراه با افزایش بیشتر از 55 درصدی اشباع ترانسفرین از آزمایشهای مهم گرانباری آهن است. افزایش فریتین همراه با آب مروارید نیز مشاهده شده است. در نبود تب و بیماریهای التهابی، اندازهگیری فریتین بازتاب بهتری از سایر تستهای روتین برای شناسایی فقر آهن است. گفتنی است که کمبود آهن در کودکان با اختلالات تمرکز و دقت (Neurocognitive) همراه است. برای اندازهگیری فریتین نیازی به قطع قرص آهن نیست. سطح فریتین در خانمهای منوپاز شبیه به مردان میشود درحالیکه قبل از آن وابسته به سن و جنس است. افزایش شدید فریتین در هپاتیت حاد، بیماریهای بدخیم، سندرم هموفاگوسیتیک و گرانباری آهن مشاهده شده است. جدول زیر، مقادیر نرمال فریتین را در کودکان و بزرگسالان نشان میدهد.
دامنه طبیعی فریتین سرم در بچهها و بزرگسالان
اسکرین هموگلوبین S (Sickledex)
آزمایشی ساده و سریع برای یافتن HbS > 20%
روش آزمایش: افتراق حلالیت خون در محلول بافر فسفاته 2/3 مولار ساپونیندار حاوی سدیم دیتیونات
مقدار طبیعی: منفی
برای دستیابی به پاسخ مثبت، بایستی غلظت هموگلوبین S بیشتر از 30% باشد و بین 20 تا 30 درصد ممکن است جواب مشکوک بدهد. موارد مثبت کاذب در آزمایش حلالیت عبارتند از کرایوگلوبولینمی، پاراپروتئینها، لکوسیتوز شدید و حضور اجسام هاینز.
موارد منفی در حضور افزایش شدید هموگلوبین F، کودکان زیر 6 ماه و ترانسفیوژن اخیر به بیماران مبتلا به کمخونی داسی رخ میدهد. سفارش میشود که از رسوب شسته شده یا از رسوب سانترفیوژ شده نمونه گلبول قرمز برداشته شود و به محلول حلالیت اضافه شود تا موارد مثبت کاذب را کاهش دهد. آزمایش مثبت بایستی با روش الکتروفورز تأیید گردد.
آزمایش حلالیت نمیتواند بین هتروزیگوت و هموزیگوت داسی و سندرمهای داسی شکل (هتروزیگوت داسی و تالاسمی، هتروزیگوت داسی و D و … ) افتراق بگذارد.
آزمایش حلالیت برای تشخیص حضور بیش از 20 درصدی هموگلوبین داسی در بافر فسفاته 2/3 مولار ساپونیندار. کدر شدن لوله آزمایش در مجاورت یک قطره از گلبولهای قرمز بیانگر حضور هموگلوبین داسی میباشد
اسکرین سیستم انعقاد با آزمایشهای PT، PTT و فیبرینوژن
آزمایش PT حساس به فاکتورهای وابسته به ویتامین K (2 و 7 و 9 و 10) میباشد و سه فاکتور 2 و 7 و 10 در مسیر آزمایش PT شرکت دارند و ازاینرو برای کنترل درمان با وارفارین که آنتاگونیست ویتامین K است استفاده میشود.
آزمایش PT بسیار وابسته به کاهش فاکتور 7 بوده و کمترین حساسیت به فاکتور 2 را دارد. آزمایش PT بر مبنای ثانیه با توجه به کنترل و یا بر مبنای نسبت همسو شده بینالمللی (INR) گزارش میگردد. درجه حساسیت معرف PT یا فاکتور بافتی را ISI گویند که بیشترین حساسیت آن ISI=1 میباشد. هرچه ISI به عدد یک نزدیکتر باشد آزمایش PT در كمبود فاكتورهاي انعقادي مسير آزمايش سريع طولانی میشود و ازاینرو برخی بر این عقیدهاند که برای آزمایشهای روتین برای بیماری که جراحی و یا اسکرین دارد از ISI بین 1/4 تا 1/7 استفاده شود ولی برخی ISI زیر 1/4 را ترجیح میدهند ولی در این حالت كه از معرف حساس استفاده میشود آزمايش PT بسیاری از افرادی که فاکتور در حد نرمال دارند بین 14 تا 15 ثانیه گزارش میشود درحالیکه با ISI زیر 2 آزمايش PT در اين افراد 13- 12 ثانيه را نشان میدهد. آزمایش PT تا 24 ساعت با نگهداری نمونه خون در حرارت اتاق قابل اندازهگیری است.
آزمایش PTT یا aPTT مسیر داخلی انعقاد را بررسی میکند و تمام فاکتورها بهجز 7 و 13 در آن نقش دارند. آزمایش PTT به کمبود فاکتورها حساسیت متفاوت دارد و کمترین حساسیت آن به کمبود فاکتور 9 میباشد. نرمال شدن PTT خونریزیهای ملایم بهویژه کمبود فاکتور 9 (هموفیلی B)، فاکتور فون ویلبراند و فاکتور 13 را رد نمیکند. کمبود فاکتور 13 توسط آزمایش PT هم مشخص نمیشود.
طولانی شدن PT و PTT در کمبود ویتامین K، بیماریهای کبد، انعقاد داخل عروقی منتشره و کمبود فاکتورهای مسیر مشترک دیده میشود. نکته مهم تنظیم حجم خون برای آزمایش PT و PTT با توجه به هماتوکریت است که میتوان مقدار سيترات سديم 3/2 درصد را براي آزمايش يك سیسی خون از رابطه زير به دست آورد:
100-HCT / 595 – HCT = سيترات سديم براي يك سیسی خون
فاکتورهای انعقادی در بدو تولد کمتر از بزرگسالان است و ازاینرو طولانی شدن خفیف تا متوسط تستها دیده میشود.
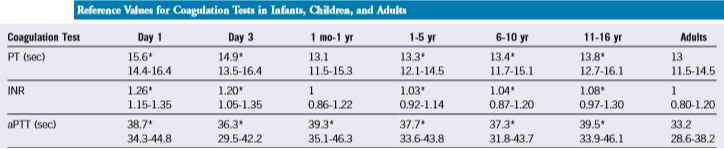
آزمایش PTT نهتنها در کمبود فاکتورها بلکه در هپارین درمانی و حضور بازدارنده لوپوس نیز طولانی میشود. برای آزمایش بازدارنده لوپوس بایستی از کیت PTT حساس به بازدارنده که دارای فسفولیپید کم و با فعالکننده سیلیکا است استفاده کرد. آزمایش PTT بایستی در 4 ساعت انجام شود و چنانچه برای کنترل هپارین درمانی به کار میرود بایستی ظرف یک ساعت انجام شود و یا هرچه سریعتر پلاسما را از گلبول جدا کرد زیرا رها شدن فاکتور 4 پلاکتی موجب خنثی شدن هپارین و کاهش کاذب PTT در بیمار میشود که روی درمان با هپارین است. جدول زیر، محدوده 95% طبیعی آزمایشهای PT و PTT را نشان میدهد.
دامنه طبیعی تستهای انعقادی روتین در کودکان و بزرگسالان
از اندازهگیری فیبرینوژن برای کمبود ارثی و کاهش اکتسابی آن استفاده میشود. اندازهگیری سریال فیبرینوژن در جنین مرده نگهداری شده سودمند بوده و مشاهده افت آن علامت مهمی بر مرگ جنین و شروع انعقاد داخل عروقی منتشره میباشد.
اندازهگیری سطح فاکتورهای انعقادی از تولد تا بزرگسالی
آزمایشهای اسکرین انعقاد راهنمای خوبی برای سفارش آزمایش جهت کمبود اختصاصی فاکتورهای انعقادی است؛ برای مثال طولانی شدن PT بهتنهایی دال بر کمبود فاکتور 7 است و طولانی شدن تنهای PTT امکان کمبود فاکتورهای 8 و 9 و 11 و خونریزی در مبتلایان به آمیلوئیدوز اندازهگیری سطح فاکتور 10 و نرمال شدن PT و PTT با وجود خونریزی اندازهگیری فاکتور 13 را مطرح میکند. گرچه کمبود فاکتور فون ویلبراند ممکن است آزمایش PTT را طولانی کند ولی کاهش خفیف تا متوسط آن با PTT نرمال همراه است.
آزمایش مخلوط 1: 1 پلاسمای نرمال با پلاسمای بیمار و انجام آزمایش PT و PTT روی پلاسمای مخلوط در زمانهای صفر و بعد از یک تا دو ساعت در 37 درجه برای پی بردن به علت طولانی شدن PT و یا PTT بسیار سودمند است. تصحیح PTT در زمان صفر و 37 درجه (برابر کنترل یا حداکثر تا 5 ثانیه بیشتر از کنترل) بیانگر کمبود فاکتور انعقادی و طولانی شدن تست در زمان صفر و 37 درجه (بیشتر از 5 ثانیه از کنترل) بیانگر بازدارنده لوپوس و نرمال شدن در زمان صفر و طولانی شدن در دو ساعت بیانگر آنتیبادی علیه فاکتور انعقادی بهویژه فاکتور 8 میباشد.
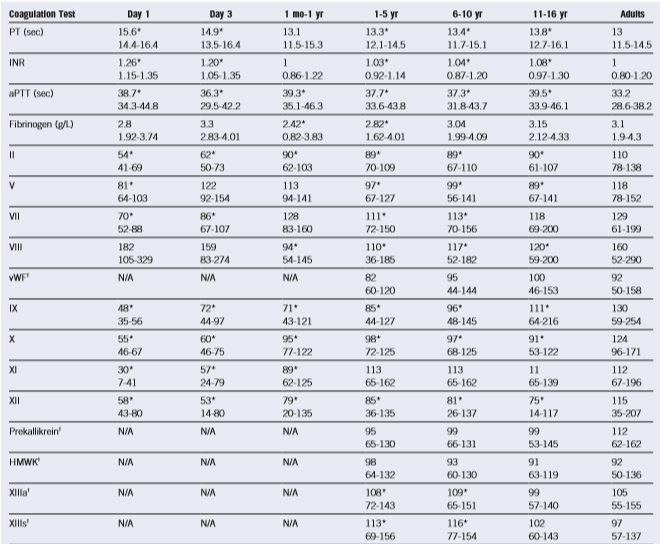
جدول زیر، سطح فاکتورهای انعقادی را از بدو تولد تا بزرگسالی نشان میدهد.
دامنه طبیعی سطح فاکتورهای انعقادی از بدو تولد تا بلوغ
آزمایشهای اسکرین انعقادی طوری طراحی میشوند که کمبود 30 تا 40 درصدی موجب طولانی شدن آزمایش شود. سطح نرمال فاکتورهای انعقادی بین 50 تا 150 درصد است. فیبرینوژن، فاکتور 8 و فون ویلبراند جزء پروتئینهای فاز حاد بوده و در بیماریهای التهابی افزایش دارند. فاکتورهای 5 و 8 جزء فاکتورهای فرار هستند و ازاینرو بایستی سریع تستهای مربوطه را انجام داد. پلاسمای سیتراته برای انجام تست سندرم ضد فسفولیپید بایستی دو بار سانترفیوژ و کاملاً از پلاکت تهی گردد و سپس منجمد شود؛ در غیر این صورت آنتیبادیهای ضد فسفولیپیدی توسط فسفولیپید پلاکتهای آبشده بهسرعت خنثی شده و آزمایش منفی کاذب میشود. کوتاه شدن زمان PTT ممکن است به علت افزایش فاکتور 8 در بیماریهای التهابی باشد. کمبود فاکتورهای 12 و HMWK و پرهکالیکرئین با وجودی که PTT را بسیار طولانی میکنند اما بیمار میل به خونریزی نداشته و جهت اتاق عمل هیچ نیازی به تهیه فرآوردههای پلاسمایی نمیباشد. کمبود چندین فاکتور در بیماری کبد و موارد نادر ارثی از قبیل کمبود همزمان فاکتورهای 5 و 8 و یا کمبود همزمان فاکتورهای 2 و 7 و 9 و 10 مشاهده شده است.
بازدارندهها و تنظیمگرهای سیستم انعقاد خون
پروتئینهای C، S، آنتیترومبین (AT) و بازدارنده مسیر خارجی انعقاد (TFPI) از تنظیمگرهای انعقاد خون هستند که کاهش آنها موجب سرایت لختگی به بدن و ایجاد لختگی در عروق میشود. پروتئینهای C و S وابسته به ویتامین K بوده و توسط کبد سنتز میشوند. پروتئین C فعال در همراهی با فاکتور S، فاکتورهای 5 و 8 فعال را خنثی کرده و از گسترش انعقاد جلوگیری میکنند. آنتیترومبین با پیوند به هپارین، فاکتورهای فعال انعقادی را در بدن که به محل آسیب عروقی محدود نباشد خنثی میکند و بازدارنده مسیر خارجی، خاموشکننده مسیر خارجی انعقاد است.
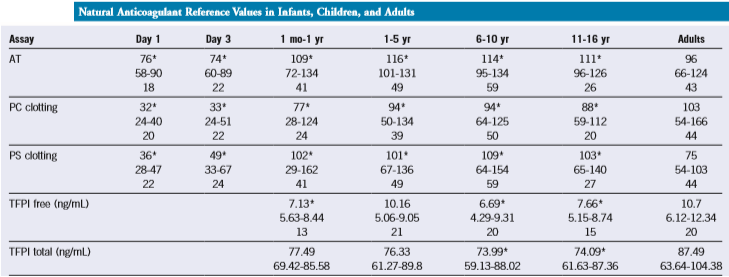
کمبود ارثی و اکتسابی این پروتئینهای تنظیمگر موجب ترومبوز و ترومبوآمبولی میشود. سنجش این پروتئینها بر پایه فعالیت بیولوژیکی با تستهای انعقادی یا روش کروموژنیک و یا سنجش آنتیژنیک بر پایه ایمونواسی صورت میگیرد. جدول زیر، محدوده 95% طبیعی فاکتورهای تنظیمکننده را نشان میدهد.
دامنه طبیعی سطح تنظیمگرهای انعقادی از قبیل آنتیترومبین، پروتئینهای C و S و بازدارنده مسیر خارجی انعقاد
توجه داشته باشید که سطح پروتئینهای فوق در اوایل کودکی کاهش دارد و در مواردی از قبیل حادثه ترومبوز، انعقاد داخل عروقی منتشره و بیماریهای کبدی نیز کاهش دارد. درمان با استروژن، هپارین، آسپارژیناز و سندرم نفروتیک با کاهش سطح آنتیترومبین همراه است. سطح پروتئینهای C و S با درمان وارفارین که آنتاگونیست ویتامین K است کاهش مییابد. سطح پروتئین S به علت پیوند به پروتئین C4BP در فاز التهاب کاهش مییابد. همچنین کاهش سطح پروتئین S در حاملگی، درمان با استروژن، آنمی داسی شکل، عفونت با HIV و سندرم نفروتیک کاهش مییابد. درواقع سطحی که موجب لختگی میشود بهدرستی معلوم نیست ولی کمتر از 70% غالباً غیرطبیعی محسوب میشود. بعد از یک حادثه ترومبوز و بعد از قطع وارفارین نیاز به فاصله زمانی 2 تا 4 هفته برای اندازهگیری دقيق فاکتورهای تنظیمکننده انعقاد است.
پروتئینهای C و S در خنثی کردن فاکتورهای 5 و 8 به حدی اهمیت دارند که چنانچه فاکتور 5 فعال توسط پروتئین C خنثی نشود (فاکتور 5 لیدن) شایعترین علت ترومبوز را شکل میدهد.
آزمایش D-dimer
آزمایش D-dimer بیانگر شکل گرفتن شبکه فیبرینی با اتصالات عرضی توسط ترومبین و فاکتور 13 فعال و هضم این شبکه توسط آنزیم پلاسمین از سیستم آب کننده لخته است و ازاینرو بیانگر فعال شدن ترومبین و پلاسمین است و این به مفهوم لخته در مویرگها مانند DIC (انعقاد داخل عروقی منتشره) و یا شکلگیری لخته در عروق عمقی (DVT) است و ازاینرو آزمایشی اختصاصی برای هر دو مورد یادشده میباشد.
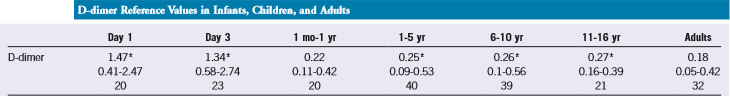
اندازهگیری D-dimer با روشهای ایمونواسی میباشد و مقدار نرمال آن در سنین مختلف در جدول زیر آمده است.
دامنه طبیعی سطح D دایمر در سنین مختلف زندگی
آزمایش FDP به مفهوم اجزای پپتیدی شکسته شده فیبرینوژن است. پلاسمین با تهاجم به فیبرینوژن آن را به اجزای x، y، D و E تجزیه میکند. روشهای ایمونواسی و لاتکس برای اندازهگیری سطح FDP به کار میروند. برای بیماری که ضریب شک برای لختگی زیاد است، مثبت شدن D-dimer تشخیص را قطعیتر میکند.
در انعقاد داخل عروقی منتشره، کمخونی میکروآنژیوپاتیک به علت رسوب فیبرین با حضور گلبولهای شکسته و کاهش پلاکت در گستره محیطی نمایان میشود. شایان توجه است که حضور گلبولهای شکسته مانند کلاهخودی، کراتوسیت، مثلثی و میکرواسفروسیت به همراه گلبولهای نرموسیت و نرموکروم بسیار حائز اهمیت است و بیانگر انعقاد داخل عروقی منتشره یا ترومبوسیتوپنی ترومبوتیک (TTP) میباشد؛ درحالیکه گلبولهای شکسته به همراه مرفولوژی غیرطبیعی مانند الیپتوسیتوز همولیتیک گرچه گزارش آن اهمیت دارد ولی به درجه اهمیت یافته فوق نمیرسد. نکته مهم دیگر اینکه گلبولهای شکسته در آنالیزور بهعنوان پلاکت شمرده میشوند.
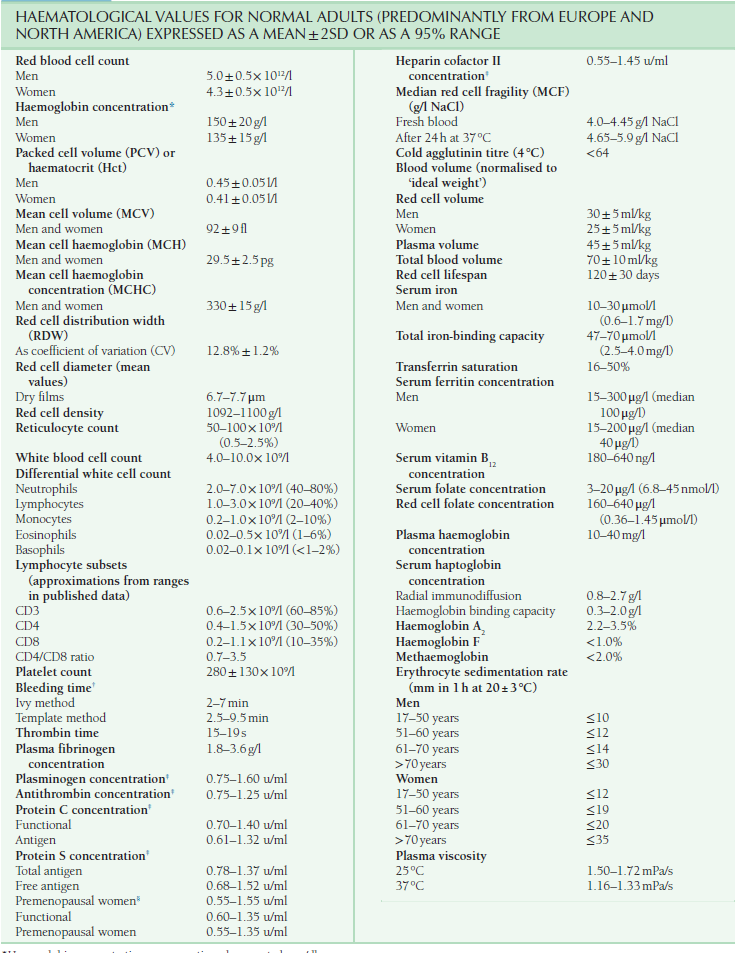
دامنه طبیعی پارامترهای هماتولوژی در یک نگاه
آشنایی با آزمایشهای انعقادی PTT & APTT
رابطۀ RDW با آنمی فقر آهن و كاهش بار اقتصادی منتج از آزمايشات غير ضروری
هموستاز ثانویه و آبشار انعقادی
کنترل کیفی تستهای معمول انعقادی
برای دانلود پی دی اف بر روی لینک زیر کلیک کنید
ورود / ثبت نام