تشخیص ملکولی و طبقهبندی کمبود مادرزادی فیبرینوژن
(بخش سوم)
اکبر درگلاله1، حسن مروتی2
1: گروه هماتولوژی و طب انتقال خون، دانشگاه علوم پزشکی ایران
2: عضو هیئت علمی مرکز تحقیقات واکسن و سرمسازی رازی
تشخیص مولکولی اختلالات مادرزادی فیبرینوژن
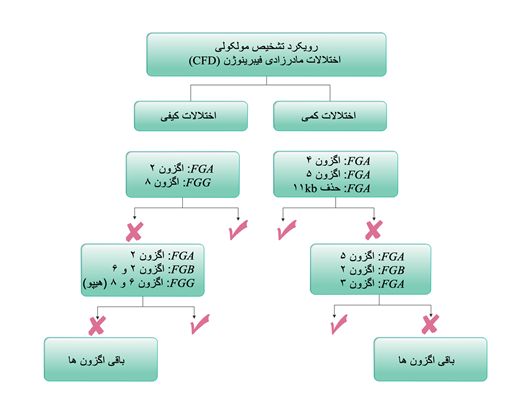
تشخیص مولکولی برای تأیید اختلالات مادرزادی فیبرینوژن، تعیین ارتباط ژنوتیپ با فنوتیپ و تشخیص قبل از تولد[1] اجباری است (138). اختلالات کمّی، در نتیجه موتاسیون در ژنهای FGA,FGB و FGG رخ میدهند که باعث اختلال در یکی از مراحل سنتز پروتئین مثل نسخهبرداری، فولدینگ و یا ترشح پروتئین میشوند (72). در اختلالات کیفی، موتاسیونهای عامل، باعث تغییرات در ساختار پروتئین میشوند (7). تا به امروز بیش از ۲۵۰ موتاسیون عامل گزارش شده است که در پایگاههای آنلاین مختلف (مثل http://site.geht.org/base-fibrinogene/) در دسترس هستند. در اختلالات کمّی فیبرینوژن، بررسی ژنوتیپ با غربالگری موتاسیونها در اگزون ۴ و ۵ از ژن FGA شروع میشود. در مرحله بعد، موتاسیون حذفی 11Kb به عنوان دومین موتاسیون شایع در ژن FGA با روش ساترن بلات بررسی میشود (5). تعیین ژنوتیپ با بررسی اگزون ۲ ازFGA و اگزون ۲ و ۶ از ژنFGB ، بهخصوص در موارد هیپوفیبروژنمی ادامه پیدا میکند )شکل ۷-۶). بعضی از واریانتهای فیبرینوژن که در اگزون ۹-۸ از ژن FGG متمرکز شدهاند، با تجمع کبدی فیبرینوژن موتاسیونیافته همراه هستند (مانند بیماری ذخیرهای فیبرینوژن)؛ بنابراین، در بیماران با سابقه خانوادگی هیپوفیبرینوژنمی و اختلالات کبدی ایدیوپاتیک، بررسی ژنوتیپ با اگزون ۸ و ۹ از ژن FGG آغاز میشود (139). در اختلالات کیفی فیبرینوژن، تشخیص مولکولی با بررسی توالی اگزون ۲ از ژن FGA و اگزون ۸ از ژن FGG آغاز میشود. در واقع ۷۵ درصد موتاسیونهای عامل دیسفیبرینوژنمی، اسیدآمینه آرژنین ۳۵ (Arg 35) در ژن FGA و آرژنین ۳۰۱ (Arg 301) در ژنFGG را درگیر میکنند (موتاسیونهای نقاط داغ) (7). متعاقباً، بررسی توالی اگزون ۵ از FGA، اگزون ۲ از FGB و اگزون ۳ و ۵ از FGG پیشنهاد میشود (140). در مواردی که سابقه خانوادگی ترومبوز وجود دارد، بررسی اگزون ۲ از ژن FGB و اگزون ۵ از ژن FGA پیشنهاد میشود، چرا که بعضی از واریانتهای فیبرینوژن که در این اگزونها متمرکز شدهاند، با افزایش خطر ترومبوز در ارتباط هستند ( 7,141).
|
شکل 6-7 رویکرد مولکولی پیشنهادی برای ژنوتیپ بیماران با اختلالات مادرزادی فیبرینوژن (برگرفته از ۲۲) |
طبقهبندی اختلالات مادرزادی فیبرینوژن
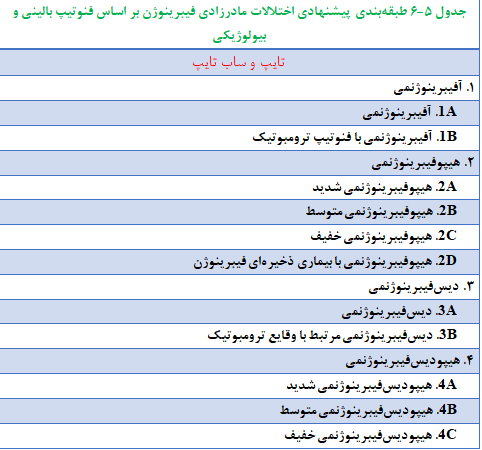
اختلالات مادرزادی فیبرینوژن بر اساس سطح فیبرینوژن به تایپ ۱ (بیماری کمّی) و تایپ ۲ (بیماری کیفی) طبقهبندی میشوند (2). در این روش، ژنوتیپ بیمار در نظر گرفته نمیشود و همچنین روش مناسبی برای شناسایی بیماران با عوارض بالای ناشی از این اختلالات نیست؛ برای مثال بسیار حائز اهمیت است که فنوتیپ بیماران مبتلا به آفیبرینوژنمی (فنوتیپ خونریزیدهنده و یا ترومبوتیک) شناسایی شود (142). بیماران مبتلا به هیپوفیبرینوژنمی با توجه به سطح فیبرینوژن در خطر خونریزی قرار دارند، بنابراین، بهتر است که این اختلال بر اساس سطح فیبرینوژن طبقهبندی شوند (42). همانطور که قبلاً ذکر شد، بعضی از واریانتهای دیسفیبرینوژنمی با افزایش خطر ترومبوز همراه هستند. این دسته از بیماران به منظور دریافت دورهای ترومبوپروفیلاکسی، باید بهطور صحیح شناسایی شوند (122)؛ به همین دلیل، اخیراً انجمن بینالمللی ترومبوز و هموستاز (ISTH)[2]، راهنمایی را برای طبقهبندی اختلالات مادرزادی فیبرینوژن منتشر کرده است. در این راهنما پیشنهاد شده است که فنوتیپ بالینی به فنوتیپ بیولوژیک اضافه شود (جدول ۵-۶)؛ بنابراین، بیماران مبتلا به آفیبرینوژنمی باید بر اساس فنوتیپ خونریزیدهنده و یا ترومبوتیک طبقهبندی شوند. بیماران مبتلا به هیپوفیبرینوژنمی نیز باید بر اساس سطح فعالیت فیبرینوژن طبقهبندی شوند و از مبتلایان به بیماری ذخیرهای فیبرینوژن افتراق داده شوند. دیسفیبرینوژنمی مرتبط با وقایع ترومبوتیک میبایست در بیماران ناقل موتاسیونهای افزایشدهنده خطر ترومبوز یا بیماران با سابقه ترومبوز شدید و یا سابقه خانوادگی ترمبوز وریدی یا شریانی لحاظ شود. این بیماران باید از افرادی که دچار ترومبوز اسپورادیک شدهاند و ارتباط بین فنوتیپ و ژنوتیپ در آنها غیرمحتمل است، افتراق داده شوند (100).
درمان بیماران مبتلا به اختلالات مادرزادی فیبرینوژن
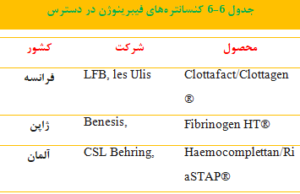
بهطور مرسوم، بیماران مبتلا به اختلالات مادرزادی فیبرینوژن با پلاسمای تازه منجمد (FFP)[3] و/ یا رسوب کرایو درمان میشوند؛ اما استفاده از این فراوردهها به دلیل خطر بیماریهای منتقله از خون محدود شده است. امروزه کنسانترههای فیبرینوژن که از نظر ویروسها غیرفعال شدهاند، درمان انتخابی مناسبی هستند، اگرچه در بسیاری از نقاط جهان همچنان غیرقابل دسترس هستند. کنسانترههای فیبرینوژن مشتق شده از پلاسما با کمترین خطر انتقال بیماریها در دسترس میباشند ( 9,143) (جدول ۶-۶). همچنین، سه کنسانتره دیگر در فازهای مختلف کارآزمایی بالینی هستند (22).
درمان اختلالات کمّی فیبرینوژن
بهطور معمول، بیماران با اختلالات کمی فیبرینوژن بهصورت “تقاضامحور[4]” درمان میشوند، اگرچه رژیم پروفیلاکسی ثانویه[5] بعد از خونریزیهای تهدیدکننده حیات پیشنهاد میشود. در موارد پروفیلاکسی اولیه یا ثانویه، سطح هدف فیبرینوژن باید بیشتر از gr/l 0/5 باشد. به دلیل نیمهعمر طولانی فیبرینوژن، درمان در هر ۷ تا ۱۴ روز کفایت میکند. در موارد خونریزی، سطح هدف فیبرینوژن به شدت و نوع خونریزی بستگی دارد (144). به هنگام جراحی، سطح هدف فیبرینوژن بیشتر از 1 gr/L توصیه میشود و تا پایان بهبودی کامل زخم میبایست بالاتر از gr/l 0/5 نگه داشته شود. در درمان جایگزینی فیبرینوژن، خطر ترومبوز وابسته به فیبرینوژن وجود دارد.
برای تعیین دوز موردنیاز در بیماران با اختلالات مادرزادی فیبرینوژن، فرمول زیر میتواند مورد استفاده قرار گیرد:
عوامل آنتیفیبرینولیتیک مثل ترانکسامیک اسید[6] میتوانند برای خونریزی مخاطی و خونریزی بعد از کشیدن دندان استفاده شوند. این گزینه درمانی میتواند خطر ترومبوز را افزایش دهد، بنابراین، باید در بیمارانی که در معرض خطر بالای ترومبوز هستند، مثل بیماران با سابقه قبلی یا سابقه خانوادگی ترومبوز، با احتیاط مصرف گردد. یک انتخاب درمانی بالقوه برای بیماران مبتلا به آفیبرینوژنمی، پیوند کبد است (145, 144, 24). درمان ترومبوز در اختلالات مادرزادی فیبرینوژن مشکل است و به کنسانتره فیبرینوژن و هم به عوامل ضد ترومبوز نیاز دارد ( 145). ضد انعقادهای مستقیم خوراکی[7] بهخصوص با فعالیت مستقیم آنتیترومبین، سودمند هستند. زنان با اختلالات کمّی فیبرینوژن به دلیل کاهش خطر منوراژی شدید و پارگی خونریزیدهنده کیست فولیکولار تخمدانی[8] ممکن است از مصرف قرصهای ضد بارداری نفع ببرند. در موارد بارداری، زنان مبتلا به آفیبرینوژنمی و هیپوفیبرینوژنمی شدید باید درمانهای جایگزین فیبرینوژن دریافت کنند، چرا که نیاز به فیبرینوژن در طول بارداری افزایش مییابد.
درمان اختلالات کیفی فیبرینوژن
در مدیریت بیماران مبتلا به اختلالات کیفی فیبرینوژن، باید سابقه شخصی و خانوادگی بیمار درباره خونریزی و ژنوتایپ در نظر گرفته شود (42). در موارد خونریزی، توصیههای مشابه اختلالات کمّی فیبرینوژن صادق است (146). دریافت پروفیلاکسی فیبرینوژن جایگزین، قبل از جراحی و فقط در موارد فنوتایپ شدید خونریزی یا در موارد جراحیهای بزرگ ضروری است. در بیشتر مواقع، جایگزینی فیبرینوژن فقط در صورت وجود عوارض نیاز است (145). بیماران با خطر بالای ترومبوز باید مقادیر دقیقی از ترومبوپروفیلاکسیها را دریافت کنند. در موارد ترومبوز، هپارین با وزن مولکولی پایین یا مواد ضد انعقادی مستقیم خوراکی DOAC)[9])، درمانهای انتخابی هستند. مقدار ترومبوز، وابسته به نوع ترومبوز (موضعی، راجعه)، ژنوتایپ (بعضی از موتاسیونها با خطر ترومبوز در ارتباط هستند) و سابقه خانوادگی است (3). بیشتر زنان مبتلا به دیسفیبرینوژنمی به جایگزینی فیبرینوژن حین بارداری نیاز ندارند اما بعد زایمان به دلیل وجود خطر خونریزی باید به دقت پیگیری شوند (70).
[1] Prenatal diagnosis
[2] Internatinal Society of Thrombosis and Hemostasis
[3] Fresh frozen plasma
[4] On-demand
[5] Secondary prophylaxis regimens
[6] Tranexamic acid
[7] Oral direct anticoagulants
[8] Hemorrhagic ovarian cyst rupture
[9] Direct oral anticoagulant
تشخیص آزمایشگاهی اختلالات کمی و کیفی کمبود فاکتور یک انعقادی
برای دریافت فایل پی دی اف بر روی لینک زیر کلیک کنید
ورود / ثبت نام