ضرورت بررسی تغییرات ژن پلیمراز ویروس هپاتیت B قبل از شروع درمان
دکتر مصطفی مهابادی استادیار ویروسشناسی
مقدمه:
ويروس هپاتيت B (Hepatitis B Virus) یکی از عوامل هپاتیت در انسان میباشد. این ویروس علت اصلی سیروز و سرطان کبد در کشور ما میباشد. در ایران بیش از یک و نیم میلیون نفر ناقل این ویروس میباشند. درصدی از آنها ناقل فعالاند و تحت درمان میباشند. درمان قطعی برای هپاتیت B وجود ندارد و هدف از درمان کاهش تعداد DNA ویروس (Viral load) به میزان غیرقابل تشخیص با روشهای مولکولی و به سطح طبیعی رسیدن میزان آنزیمهای کبدی و بهبود هيستولوژيك كبد میباشد. هفت دارو برای درمان عفونت مزمن هپاتیت B تابهحال تائید شده است که شامل اینترفرون آلفا، پگ اینترفرون، لامیوویدین، آدفوویر، انتکاویر، تلبوویدین و تنوفوویر میباشند. هر چند سال یکبار داروی جدید برای درمان هپاتیت B مجوز میگیرد ولی مجدداً نیاز به داروی جدید احساس میشود و علت اصلی آن بروز مقاومت در ویروس و عدم کارآیی دارو میباشد. یکی از علل مهم در بروز مقاومت دارویی عدم تجویز داروی مناسب با توجه به خصوصیات ژنتیکی ویروس میباشد. جهت شروع به درمان بایستی موارد مختلف شامل، داروهای مورد تائید، وضعیت بالینی و فردی بیمار و از همه مهمتر خصوصیات ویروس و موتاسیونهای مرتبط با مقاومت به داروهای مختلف حتماً مدنظر قرار گیرد. در این مطالعه موتاسیونهای رایج مرتبط با داروهای ضدویروسی و اهمیت شناسایی آنها قبل از درمان موردبررسی قرار میگیرند.
روش کار و نتایج:
ويروس HBV يك ويروس Noncytopathic بوده كه طيفي از بیماریهای كبدي را سبب ميشود؛ طيف آن از هپاتيت حاد (با علائم و بدون علائم بالینی) تا هپاتيت مزمن، سيروز و سرطان كبد (HCC) Hepato Cellular Carcinoma ميباشد. سرانجام بيماري، گسترش و شدت عفونت HBV بستگي به فاكتورهاي مختلف ميزبان و ويروس دارد. هپاتيت حاد B عموماً نیاز به درمان ضدویروسی ندارد. درمانهای علامتي براي برطرف كردن تهوع، استفراغ و بیاشتهایی را میتوان انجام داد. ولي در بيماران آلوده به عفونت هپاتيت B مزمن هدف اصلي درمان، نهتنها منجر به ممانعت از انتقال ويروس و كاهش سطح ويروس میگردد، بلكه مانع از گسترش بيماري كبدي، بهبودی علائم باليني و هيستولوژيك كبدي و همچنين جلوگيري از پيشرفت بيماري به سمت سیروز و سرطان كبد ميشود. بیماران هپاتيت B مزمن به دو گروه اصلی HBeAg-مثبت و HBeAg-منفی جهت درمان تقسیم میشوند. امروزه درمان هپاتيت B مزمن در بيماراني صورت میگیرد كه بيماري فعال و تكثير بالای ويروسي دارند و باید درمان قبل از بروز علائم سيروز يا آسيب واضح كبدي شروع شود. هدف از درمان هپاتيت B مزمن کاهش
تعداد HBV-DNA به میزان غیرقابل تشخیص با روشهای مولکولی و به سطح طبیعی رسیدن میزان آنزیمهای کبدی و بهبود هيستولوژيك كبد میباشد. هفت دارو برای درمان عفونت مزمن هپاتیت B تابهحال تائید شده است که شامل اینترفرون آلفا، پگ اینترفرون، لامیوویدین، آدفوویر، انتکاویر، تلبوویدین و تنوفوویر میباشد. این داروها از سال 1990 به ترتیب مجوز تجویز را از FDA کسب کرده و در سبد دارویی جهت درمان هپاتیت B قرار گرفتند.
بعد از شروع به درمان ممکن است پاسخ مناسب به درمان ایجاد شود و فاکتورهای مرتبط با بهبودی فرد مثل نرمال شدن تستهای کبدی و فاکتورهای انعقادی به دست آید و ویروس نیز با روشهای نوین مولکولی به حد غیرقابل تشخیص کاهش یابد در این صورت درمان مناسب میباشد و بایستی ادامه یابد و یا ممکن است پاسخ مناسب به درمان ایجاد نشود و سه حالت زیر ایجاد شود:
عدم پاسخ اولیه به درمان: شکست اولیه درمان (Primary treatment failure): عدم کاهش
1 log IU/ml بعد از 12 هفته از شروع درمان میباشد. در این موارد بایستی بررسی و در صورت لزوم تعویض دارو صورت گیرد.
پاسخ ویرولوژیک نسبی : در مواردی که بعد از 24 یا 48 هفته ویروس به حد غیرقابل تشخیص نرسد در این موارد نیز بایستی بررسی و در صورت لزوم تعویض دارو صورت گیرد.
شکست ویرولوژیک (Viral breakthrough): افزایش 1 log IU/mlHBV-DNA بعد از کاهش اولیه آنکه منجر به شکست کلینیکی (Clinical breakthrough) با افزایش ALT و یا ایجاد مشکل بافتی خواهد شد(1).
سه فاکتور مهم دخیل در شکست در درمان مرتبط با خصوصیات دارو، فاکتورهای سلولی و کارکرد کبد بیمار و از همه مهمتر و اساسیتر فاکتورهای وابسته به ویروس میباشد که بر اثر موتاسیونهای ناحیه پلیمراز ویروس و تغییر در اسیدآمینههای قسمت(Reverse Transcriptase) RT مقاومت دارویی ایجاد میشود و مهمترین علت شکست درمان محسوب میشود. چنانچه خصوصیات ویروس از نظر ژنوم و موتاسیونهای ایجادشده در ژن پلیمراز ویروس بهخوبی قبل از درمان مورد ارزیابی قرار گیرد و ضمن بررسی دقیق داروی مناسب انتخاب شود میتواند تا حدود زیادی از شکست در درمان پیشگیری نماید. چندین عامل مرتبط با بروز مقاومت شناخته شده است. این عوامل شامل جنس مذکر بودن، سن بالا، بالا بودن BMI (BODY-MASS INDEX)، بالا بودن ALT، بالا بودن تعداد ویروس و بالا بودن اسکور بافتی میباشند. در مطالعاتی دیگر ایجاد مقاومت بیشتر در ژنوتیپ A برای لامیوویدین و D برای آدفوویر گزارش شده است.
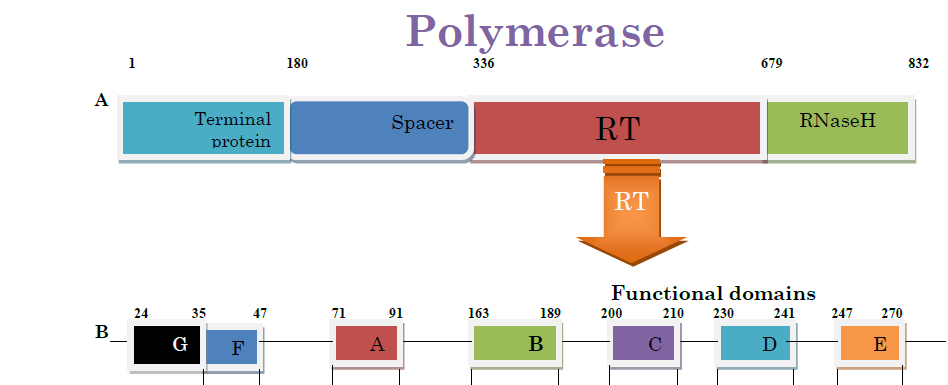
موتاسیونهای مقاومت دارویی پلیمراز ویروس در قسمت RT آن واقع شدهاند. نقش مهم و اساسی و عملکردی پلیمراز ویروس در رونویسی و تکثیر ویروس میباشد. همانطور که در شکل (1) مشاهده میشود پلیمراز دارای بیش از 800 اسید آمینه میباشد که 344 تا از این اسید آمینهها به قسمت RT مربوط میشود و این قسمت نیز شامل هفت دومین و چند اینتردومین میباشد که دومینهای (A,C,D) نقش اتصال به dNTP را دارند و مرکز کاتالیتیک محسوب میشوند. دومین B نقش اتصال به رشته الگو را ایفا مینماید و دومین E نیز به رشته پرایمر اتصال مییابد. اصلیترین موتاسیونهای در سطح اسید آمینه و مرتبط با مقاومت دارویی در این دومینها ایجاد میشوند.
شکل (1) نواحی مختلف پلیمراز و دومینها (A) اینتردومینهای RT(B)
انواع موتاسیونها در سطح اسید امینه در(RT) مرتبط با مقاومت به داروهای مختلف:
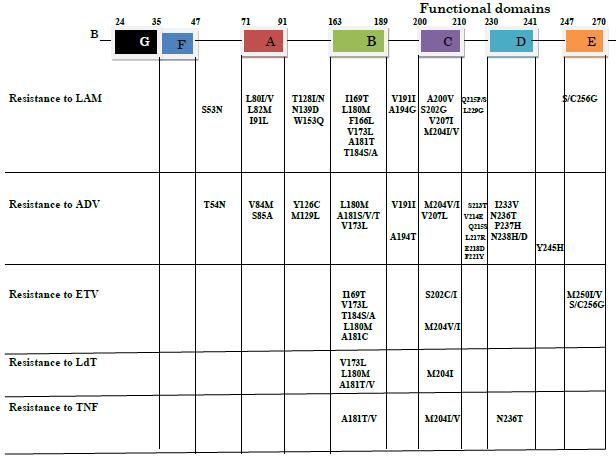
در قسمت RT موتاسیونهای مختلف ایجاد میشود که این موتاسیونها اگر منجر به تغییر در اسید آمینه شوند میتوانند بعد از تائید بهعنوان موتاسیونهای مقاومت دارویی گزارش شوند. در شکل زیر نواحی پلیمراز و موتاسیونهای مقاومت دارویی که تا به حال برای داروهای مختلف Lamivudine(LAM)، Adefovir(ADV) Entecavir(ETV)، Telbivudine(LdT) و Tenofovir(TNF) گزارش شده نشان داده شده است. در شکل موتاسیونهایی که تا به حال بهعنوان موتاسیونهای مقاومت دارویی در مقالات تحقیقی مختلف گزارش شده است با توجه به نوع دارو و محل و نوع اسید آمینه در RT به تفکیک درج شده است.
شکل (2) موتاسیونهایی که تا به حال بهعنوان موتاسیونهای مقاومت دارویی در مقالات تحقیقی مختلف گزارش شده است با توجه به نوع دارو و محل و نوع اسید آمینه در RT.
میزان موتاسیون خود به خودی در ویروس هپاتیت B بالاست. نیمهعمر ویروس در پلاسما سه روز و در هپاتوسیتها 10 تا 100 روز میباشد. با توجه به میزان بالای تکثیر ویروس (بیشتر از 1011) در روز حدود 1010 موتاسیون نقطهای بایستی در ویروس رخ بدهد. با توجه به طول ژنوم ویروس احتمال تغییر کامل ویروس میتواند تصور شود. با توجه به فشارهای داخلی (سیستم ایمنی) و فشارهای خارجی (واکسن) و احتمال موتاسیون بالا در چرخه طبیعی ویروس موتاسیونهای خود به خودی مرتبط با مقاومت به دارو قبل از درمان در درصدی از بیماران وجود دارد.
بحث
از سالها قبل دانشمندان در این فکر بودند که احتمال وجود موتاسیونهای مقاومت دارویی در بیمارانی که هنوز دارویی مصرف نکردهاند وجود دارد. لذا محققان در جمعیتهای مختلف اقدام به بررسی این فرضیه کردند و نتایج متفاوتی نیز به دست آمده است. در این تحقیقات مشخص شده است که موتاسیونهای مقاومت میتواند بدون دریافت دارو نیز در درصدی از بیماران ایجاد شود. در تحقیقات بنده و محققین دیگر در ایران بروز موتاسیونهاهای متعدد مرتبط با مقاومت دارویی با درصدهای قابلتوجه در بیماران مزمن هپاتیت B که هیچ دارویی دریافت نکردهاند را اثبات مینماید. تعداد یازده موتاسیون مختلف مرتبط با مقاومت دارویی مشاهده شد که بیشترین تعداد این موتاسیونها در اینتردومین C-D مشاهده شد و سپس در اینتردومین A-B دیده شده است و مطابق تحقیقات انجام شده محققین دیگر که بر روی ژنوتیپ های B و C انجام شده بیشترین موتاسیون قبل درمان را در اینتردومین A-B نشان میدهد.
موتاسیون M204I/V در بیمارانی که هیچ دارویی دریافت نکرده بودند از 0% تا 23% در کشورهای مختلف گزارش شده است. در ایران نیز مطالعاتی که تا سال 2009 موتاسیونهای گزارش شده صفر درصد بوده است و در مطالعات جدید محققین ایرانی تا 6/6 درصد گزارش شده است.
موتاسیون M204I/V میتواند به چند علت مهم باشد:
به علت بروز سریع این موتاسیون در بعد از درمان و همینطور بروز خودبهخودی در بیمارانی که دارو دریافت نکردهاند این موتاسیون میتواند زنگ خطر شروع بروز تغییر در ژنوم ویروس در بیمار باشد. این موتاسیون مقاومت به داروهای مختلف از جمله لامیویدین، آدفوویر، تلبوویدین، انتکاویر و تنوفوویر را به میزانهای مختلف ایجاد مینماید. این نکته میتواند اهمیت این موتاسیون را در بررسی قبل از درمان و در مراحل درمان بهخوبی متذکر شود. همچنین این موتاسیون میتواند مبنای اولیه بروز مقاومت در نظر گرفته شود.
در انتخاب داروی مناسب استفاده بعضی از موتاسیونها دیگر نیز دارای اهمیت میباشند که بایستی پیش از درمان و در حین درمان بهخوبی مورد شناسایی و ارزیابی قرار گیرند. از جمله این موتاسیونها A181T/V میباشد. این موتاسیون مقاومت به داروهای مختلف از جمله لامیویدین، آدفوویر، تلبوویدین، انتکاویر و تنوفوویر را ایجاد مینماید. همچنین با توجه به اینکه داروی تنوفوویر بهصورت وسیع و معمول در ایران بعد از بروز مقاومت به داروهای دیگر استفاده میشود لازم است این نکته مدنظر قرار گیرد که این موتاسیون مقاومت به تنوفوویر را نیز میتواند ایجاد نمایید و بایستی قبل از شروع درمان بررسی شود. لازم به ذکر است همگامی این موتاسیون با M204I/V میتواند احتمال بروز مقاومت و شکست در درمان را شدت بخشد (35). نکته مهم در رابطه با این موتاسیون این است که بر اساس تحقیقات جدید این موتاسیون ارتباط با سرطان کبد در بیماران هپاتیت مزمن B دارد. وجود این موتاسیون در ژنوم ویروس میتواند به علت همپوشانی با پروتئین سطحی ویروس سبب تولید اسید آمینه خاتمه دهنده شده و در تولید و ترشح آن اختلال ایجاد کرده و با ایجاد استرس داخل سلولی سبب ایجاد سرطان شود. لازم به ذکر است وجود این موتاسیون همزمان با فرم وحشی آن نیز زمینه بروز سرطان را فراهم مینماید. لذا تشخیص آن در حین درمان و قبل از درمان حتماً بایستی مورد بررسی قرار گیرد. نظر به اینکه هر چند سال داروی جدید برای درمان هپاتیت B مجوز میگیرد ولی باز بایستی داروی جدید تولید شود و علت اصلی آن بروز مقاومت نسبت به دارو بعد از چند سال میباشد بهطوریکه استفاده از داروی قبلی غیرممکن میشود. یکی از علل مهم بروز مقاومت عدم بررسیهای اولیه قبل از درمان میباشد. با عنایت به اینکه بررسیهای انجامشده در جهان نشان میدهد بروز موتاسیونهای مرتبط با مقاومت دارویی در بیماران قبل از استفاده از دارو و خودبهخود ایجاد میشود لزوم بررسیهای موتاسیونهای مرتبط با مقاومت دارویی محرز میگردد. در کل میتوان گفت نیاز به بررسی قبل از درمان با توجه به افزایش مقاومت ضروری و لازم به نظر میرسد.
Reference:
- Kay A, Zoulim F. Hepatitis B virus genetic variability and evolution. Virus Res. 2007 Aug;127(2):164-76.
- Takkenberg RB, Weegink CJ, Zaaijer HL, Reesink HW. New developments in antiviral therapy for chronic hepatitis B. Vox Sang. 2010 May;98(4):481-94.
- Carosi G, Rizzetto M, Alberti A, Cariti G, Colombo M, Craxi A, et al. Treatment of chronic hepatitis B: Update of the recommendations from the 2007 Italian Workshop. Dig Liver Dis. 2011 Apr;43(4):259-65.
- Bihl F, Alaei M, Negro F. The new EASL guidelines for the management of chronic hepatitis B infection adapted for Swiss physicians. Swiss Med Wkly. 2010 Mar 20;140(11-12):154-9.
- Rhee SY, Margeridon-Thermet S, Nguyen MH, Liu TF, Kagan RM, Beggel B, et al. Hepatitis B virus reverse transcriptase sequence variant database for sequence analysis and mutation discovery. Antiviral Res. 2010 Dec;88(3):269-75.
- Pastor R, Habersetzer F, Fafi-Kremer S, Doffoel M, Baumert TF, Gut JP, et al. Hepatitis B virus mutations potentially conferring adefovir/tenofovir resistance in treatment-naive patients. World J Gastroenterol. 2009 Feb 14;15(6):753-5.
- Liu BM, Li T, Xu J, Li XG, Dong JP, Yan P, et al. Characterization of potential antiviral resistance mutations in hepatitis B virus reverse transcriptase sequences in treatment-naive Chinese patients. Antiviral Res. 2010 Mar;85(3):512-9.
- Sayan, M., S. C. Akhan, et al. Frequency and Mutation Patterns of Resistance in Patients with Chronic Hepatitis B Infection Treated with Nucleos(t)ide Analogs in Add-On and Switch Strategies. Hepat Mon.2011 11(10): 835-842.
- Schildgen O, Olotu C, Funk A, Zollner B, Helm M, Rockstroh JK, et al. Selection and counterselection of the rtI233V adefovir resistance mutation during antiviral therapy. J ClinMicrobiol. 2010 Feb;48(2):631-4.
- Cuestas ML, Rivero CW, Minassian ML, Castillo AI, Gentile EA, Trinks J, et al. Naturally occurring hepatitis B virus (HBV) variants with primary resistance to antiviral therapy and S-mutants with potential primary resistance to adefovir in Argentina. Antiviral Res. 2010 Jul;87(1):74-7.
بررسی تیتر آنتیبادی ضد ویروس هپاتیت B
انواع تکنیک « واکنش زنجیرهای پلیمراز (PCR)» و انواع آنزیمهای DNA پلیمراز مقاوم به حرارت
مقدمهای بر تکنیک واکنش زنجیرهای پلیمراز و انواع آن
برای دانلود فایل pdf بر روی لینک زیر کلیک کنید
ورود / ثبت نام