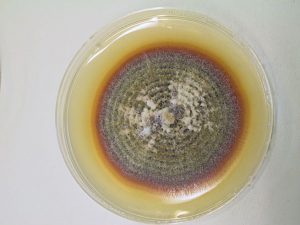
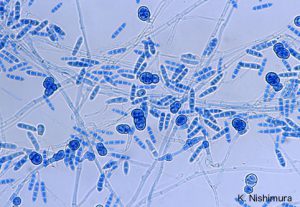
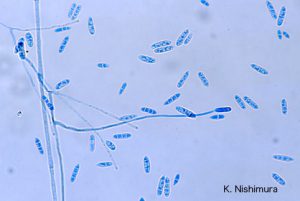
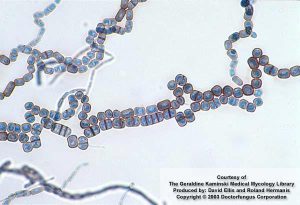
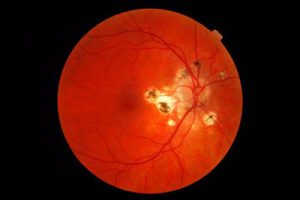
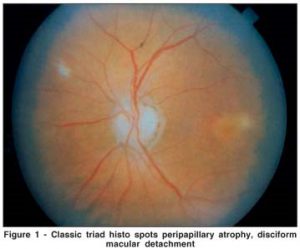
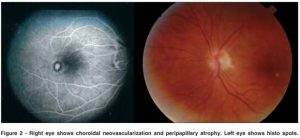
دکتر محمد قهری – آزمایشگاه تشخیص طبی رسالت
مقدمه
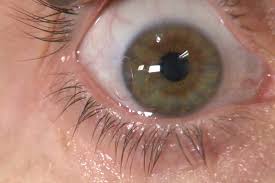
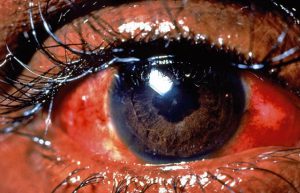
ساختمان منحصر به فرد و بینظیر چشم انسان و برخورد و مواجههی مستقیم آن با محیط، این عضو را آسیبپذیر و حساس در مقابل برخی از عوامل عفونی از جمله قارچها نموده است. دفاعهای میزبان بر علیه این میکروارگانیسمها هنگامیکه از طریق سدهای آناتومیکال رخنه نمایند اغلب برای پیشگیری از کاهش بینائی (و از دست دادن بینائی) ناکافی است. بنابراین شناسائی و درمان بموقع میکروارگانیسمهای درگیر کننده بسیار مهم است. آشنائی و مرور آناتومی چشم و ساختمانهای احاطه کنندهی آن برای مطالعهی عفونتهای اختصاصی قارچها ضروری مینماید. بعنوان مثال عفونتهای قارچی فیلامنتوس چشم معمولا مربوط به تروماهای نفوذکننده توسط اشیاء و وسایلی است که با مواد گیاهی آلوده شده باشند و از طریق قرنیه یا کرهی چشم و یا بوسیلهی گسترش و توسعهی عفونت از سینوسهای پارانازال مجاور چشم به این عضو رسیده باشند.
اندوفتالمیت و کوریورتینیت قارچی معمولا در نتیجهی انتشار فونژمی قبلی (یا فونژمی پایدار) به بافت چشم است. گونههای کاندیدا شایعترین علت اندوفتالمیت اندوژنوس هستند اگرچه عفونت اولیه توسط قارچهای دوشکلی ممکن است سبب عفونت و زخمی شدن کوریورتینا شوند. پوشش لنزهای تماسی با کراتیت ایجاد شده بوسیلهی مخمرها، قارچهای رشتهای و گونههای آکانتامبا مرتبط است.
***
كار اصلي چشم (عضو بینائی) آن است كه نورهايي را كه از خارج دريافت ميكند طوري روي پرده شبكيه متمركز كند كه تصوير دقيقي از شيء مورد نظر روي پرده شبكيه ايجاد شود. شبكيه اين تصاوير را به صورت پيامهاي عصبي به مغز ارسال ميكند و اين پيامها در مغز تفسير ميشوند. بنابراين براي واضح ديدن، قبل از هرچيز لازم است كه نور به طور دقيق روي پرده شبكيه متمركز شود.
ساختمان چشم شبيه يك كره است. در قسمت جلوي اين كره يك پنجره شفاف به نام قرنيه وجود دارد. نور از محيط خارج وارد قرنيه شده پس از عبور از مردمك به عدسي ميرسد. عدسي نور را به صورت دقيق روي شبكيه متمركز ميكند تا تصوير واضحي بر روي شبكيه ايجاد شود. براي آنكه اشياء به صورت دقيق و واضح ديده شوند لازم است مسيري كه نور در چشم طي ميكند شفاف باشد و قرنيه و عدسي نور را درست روي شبكيه متمركز كنند.
***
مروری بر ساختمان تشریحی چشم
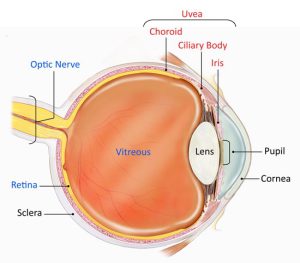
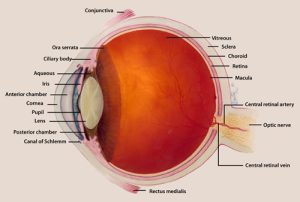
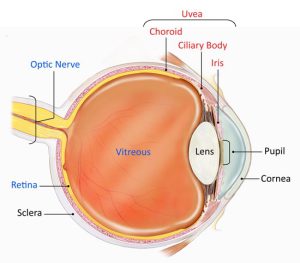
عضو بینائی مرکب از دو قسمت است که شامل کرهی چشم و عصب بینائی میباشد. کرهی چشم در حفرهی استخوانی بنام اربیت قرار گرفته و توسط عضلات و پلکها پوشیده شده و از خارج به داخل حاوی 3 پرده است:
- پردهی خارجی یا فیبروز (fibrous tunic) که خود از دو قسمت تشکیل شده است. یکی در قسمت عقب بنام صلبیه (sclera) و دیگری در جلو بنام قرنیه (cornea). صلبیه پردهی سفید و سختی است در خارج کرهی چشم که حداکثر به ضخامت 1 میلیمتر بوده و عضلات چشم روی آن میچسبند. صلبیه در جلو به پردهی شفاف و بدون عروق بنام قرنیه تبدیل میشود. عمل قرنیه عبارت است از انکسار نور، محافظت، حساسیت (از راه رشتههای عصبی آزاد در اپیتلیوم آن) و ایجاد یک محیط شفاف.
صلبيه
صلبيه بخش سفيد رنگ نسبتاً محكمي است كه دورتا دور كره چشم به جز قرنيه را ميپوشاند و از ساختمانهاي داخل كره چشم محافظت ميكند. اين بخش از چشم اثر مستقيمي در فرايند بينايي ندارد و در واقع مثل يك اسكلت خارجي از كره چشم محافظت ميكند.
قرنيه
قرنيه قسمت شفاف جلوي كره چشم است كه از پشت آن ساختمانهاي داخليتر كره چشم مثل عنبيه و مردمك ديده ميشود. قرنيه چشم را ميتوان به شيشه پنجره تشبيه كرد. همانطور كه اگر شيشه پنجره كثيف باشد اشياء بيرون تار ديده ميشوند، اگر بر روي قرنيه كسي لكه يا كدورتي وجود داشته باشد فرد اشياء را تار ميبيند. به علاوه همانطور كه از پشت يك شيشه موجدار يا مشجر اشياء كج و كوله و ناصاف ديده ميشوند. در صورتي كه سطح قرنيه ناهموار باشد اشياء ناصاف و تار ديده ميشوند.
البته قرنيه انسان يك تفاوت مهم با شيشه پنجره دارد و آن هم اينكه شيشه پنجره يك سطح صاف است در حاليكه قرنيه بخشي از يك كره است. اين ساختمان كروي باعث ميشود كه قرنيه چشم مثل يك ذرهبين عمل كند و نورهايي را كه از محيط خارج وارد كره چشم ميشوند به صورت پرتوهاي همگرا درآورد كه تصوير واضحي روي شبكيه ايجاد كنند.
البته در همه افراد اين امر به صورت دقيق اتفاق نميافتد. مثلاً اگر انحناي قرنيه كسي بيشتر از حد طبيعي باشد تصاوير به جاي آنكه روي پرده شبكيه بيفتد در جلوي پرده شبكيه تشكيل ميشود. چنين فردي نزديك بين (ميوپ) است. همچنين اگر انحناي قرنيه كسي كمتر از حد طبيعي باشد تصاوير به جاي آنكه روي پرده شبكيه بيفتند در پشت آن تشكيل ميشوند.
چنين فردي دوربين (هيپروپ) است. به طوري كه ميبينيم قرنيه افراد نقش مهمي در تعيين دوربيني يا نزديك بيني يا شماره چشم افراد دارد. به همين علت اكثر روشهاي جراحي براي اصلاح ديد و شماره عينك روي اين بخش از چشم انجام ميگيرد. مثلاً در روش هاي ليزر (PRK)، ليزيك(LASIK)، لازك(LASEK) و جراحي با تيغه الماس (RK) مقدار انحناي قرنيه تغيير ميكند و شماره چشم فرد اصلاح ميشود. همچنين استفاده از لنز تماسي (كنتاكت لنز) كمك ميكند كه انحناي قرنيه فرد موقتاً به اندازه مطلوب برسد و ديد فرد اصلاح شود.
- طبقهی میانی یا عروقی (vascular tunic)، پردهی میانی چشم از عقب به جلو شامل مشیمیه (choroid) و جسم مژگانی و عنبیه است. مشیمیه از خارج به داخل شامل 4 طبقه است: طبقهی فوق مشیمی که از سلولهای پیگماندار و رشتههای ارتجاعی ترکیب یافته که بصورت صفحات مایلی به صلبیه چسبیدهاند. طبقهی عروقی که از تعداد زیادی رگ و سلول ستارهای شکل پیگماندار ترکیب یافته است. طبقهی موئینهای که در ساختمان این طبقه شبکهای از موئینهها بکار رفتهاند که اکسیژن و مواد غذائی شبکیه ی مجاور را تامین میکنند.
طبقهی پایهای بروخ، این طبقه خود از دو لایه ترکیب شده، لایه خارجی آن ارتجاعی و لایه داخلی آن خود برای اپیتلیوم شبکیه یک غشاء پایه محسوب میشود.
جسم مژگانی (ciliary body) نوار مخصوص حلقوی شکلی است که مابین مشیمیه و عنبیه قرار گرفته است و تقریبا از 70 رشتهی حلقوی ترکیب یافته و این رشتهها از نظر ساختمانی شبیه مشیمیه هستند و مایع زلالیه (aqueous humor) را از خود تراوش میکنند. در ضخامت طبقهي فوق مشیمی عضلات صافی بنام عضلات مژگانی (ciliary muscle) قرار دارند. عضلات حلقوی (بنام عضله ی مولر) از پاراسمپاتیک عصب ميگيرند و عدسی را گرد ميكنند تا دید نزدیک را تطابق نماید.
عنبیه
عنبیه (iris)، عنبیه قسمتی از پردهی میانی چشم است که به شکل واشر در عقب قرنیه قرار گرفته در طرفین به اجسام مژگانی متصل است و در وسط آن مردمک چشم تشکیل ميشود. عنبیه از جلو به عقب شامل طبقات زیر است:
- آندوتلیوم عنبیه، پوشش نامشخصی است که مقابل قرنیه قرار دارد.
- داربست قدامی که بلافاصله در پشت اندوتلیوم قرار گرفته فاقد عروق و حاوی تعدادی سلول پیگماندار ميباشد.
- داربست خلفی یا اصلی که از بافت فیبروالاستیک اسفنجی شکل به انضمام عروق فراوان و سلولهای پیگماندار ترکیب یافته است.
- سطح خلفی عنبیه توسط شبکیه پوشیده شده است.
- عضلهی تنگ کننده در نزدیکی سرحد مردمک رشتههای عصبی پاراسمپاتیک را دریافت ميكند و در مقابل ازدیاد نور منقبض ميشود.
- عضله ی گشاد کننده در حالیکه رشتههای شعاعی دارد رشتههای عصبی سمپاتیک را دریافت ميكند.
عنبيه بخش رنگي پشت قرنيه است كه رنگ چشم افراد را تعيين ميكند. رنگ اين بخش در چشم افراد مختلف متفاوت است و از آبي و سبز تا عسلي و قهوهاي تغيير ميكند. در وسط عنبيه سوراخي به نام مردمك وجود دارد كه مقدار نور وارد شده به چشم را تنظيم ميكند. كار مردمك مثل پردهاي است كه پشت پنجره آويزان شده و نور ورودي به اتاق را كم و زياد ميكند. همانطور كه وقتي نور خارج شديد و زياد باشد، پرده را ميبنديم تا نور كمتري به اتاق وارد شود، وقتي چشم در محيط پر نور قرار ميگيرد مردمك تنگ ميشود تا مقدار نور كمتري وارد چشم شود. به همين صورت وقتي چشم در محيط كم نور قرار ميگيرد مردمك گشاد ميشود تا نور بيشتري وارد چشم شود.
مشيميه
مشيميه پرده نازك سياه رنگي است كه دور شبكيه را احاطه كرده است. اين پرده تعداد زيادي رگهاي خوني دارد كه مواد غذايي را به بخشهايي از شبكيه ميرساند. به علاوه سلولهاي اين لايه حاوي تعداد زيادي رنگ دانه سياه ملانين است كه رنگ سياهي به اين بخش از چشم ميدهد. وجود رنگ سياه مانع از انعكاس نورهاي اضافي در داخل كره چشم ميشود و به تشكيل تصوير واضحتر كمك ميكند.
- پرده داخلی یا شبکیه (retina). شبکیه پردهای است که در داخل کرهی چشم قرار گرفته و خود شامل دو لایه است:
لایه خارجی که حساس نبوده بنام اپیتلیوم رنگین موسوم است و لایه داخلی که به نور حساس ميباشد شبکیه عصبی یا طبقه ی مغزی نامیده ميشود.
شبكيه يك پرده نازك حساس به نور (شبيه فيلم عكاسي) است كه در عقب كره چشم قرار دارد. پرتوهاي نوري كه به شبكيه برخورد ميكنند به پيامهاي عصبي تبديل ميشوند كه از طريق عصب بينايي به مغز منتقل ميشوند و در مغز تفسير ميشوند.
در شبكيه انسان انواع مختلفي از سلولهاي گيرنده نوري وجود دارد كه ميزان حساسيت آنها به نور متفاوت است. گيرندههاي نوري استوانهاي بيشتر براي ديد در محيطهاي تاريك به كار ميروند. گيرندههاي مخروطي براي تشخيص رنگ و جزئيات ظريف تمايز يافتهاند. ترتيب قرارگيري اين سلولها در شبكيه طوري است كه در ناحيه مركزي شبكيه (ماكولا) تعداد گيرندههاي مخروطي بيشتر است. بنابراين وقتي فردي به صورت مستقيم به شيئي نگاه ميكند تصوير آن شيء مستقيماً روي ماكولا در جايي ميافتد كه تعداد سلولهاي مخروطي بيشتر است و در نتيجه شيء با وضوح بيشتري مشاهده ميشود.
اتاق قدامی و خلفی چشم
- اتاق قدامی از جلو به قرنیه و از عقب به عنبیه و مردمک محدود است. قطر قدامی خلفی آن نزد افراد متغیر و حدود 3/71 میلیمتر است. درون این اتاق مایع زلالیه جریان دارد. این مایع شبیه سرم خون است ولی پروتئین آن بسیار کمتر ميباشد.
- اتاق خلفی از لحاظ تشریحی فضائی است که بین عنبیه و عدسی چشم ميباشد. عمق این اتاق حدود 0/4 تا 0/6 میلیمتر است. اتاق خلفی از جلو به عنبیه، از اطراف به جسم مژگانی و از عقب به رشتههای زین و زجاجیه محدود ميشود. اتاق خلفی چشم توسط مایع زجاجیه (vitreous humor) پر شده است. این مایع حاوی اسید هیالورونیک و پروتئینی بنام ویترین (viterin) است که در مایع زلالیه نفوذ ميكند.
مایع زلالیه (aqueous humor) مایع بیرنگی است که دارای وزن مخصوص حدود 1005 و ضریب انکسار نور 1/135 و pH در حدود 7/2 ميباشد. ترکیب این مایع شبیه به مایع مغزی نخاعی است و تغذیهی عدسی و قرنیه را که فاقد رگ ميباشند تامین ميكند. زلالیه هر یکساعت یکبار تجدید ميشود. اختلال در گردش این مایع باعث تغییر در فشار چشم ميشود. کم شدن ترشح زلالیه باعث تحلیل کرهی چشم (phytisie) و ازدیاد آن موجب افزایش فشار داخل چشم شده و بیماری گلوکوم را تولید ميكند.
اتاق قدامي فضاي كوچكي است كه بين قرنيه و عنبيه قرار دارد. در اين فضا مايعي به نام زلاليه جريان دارد كه به شستشو و تغذيه بافتهاي داخل چشم كمك ميكند. همانطور كه در يك استخر براي پاك ماندن استخر مرتباً مقداري آب خارج ميشود و به جاي آن آب تصفيه شده وارد ميشود، در چشم هم مرتباً مقداري از مايع زلاليه خارج ميشود و مايع زلاليه جديدي كه در چشم توليد شده است جايگزين آن ميشود. اگر به هر دليلي تعادل بين توليد و خروج اين مايع به هم بخورد مقدار مايع زلاليه در چشم افزايش پيدا ميكند و فشار داخل كره چشم از حد طبيعي بيشتر ميشود. (مقدار طبيعي فشار چشم در افراد بالغ بين 10 تا 21 ميليمتر جيوه است). بالا رفتن فشار چشم به پرده شبكيه و عصب بينايي آسيب ميزند و باعث بيماري آب سياه يا گلوكوم ميشود.
عدسی
عدسی یا جلیدیه (crystalline lens)، جلیدیه به شکل عدسی محدبالطرفینی شفاف که در عقب مردمک چشم و در جلو زجاجیه قرار دارد. استقامت عدسی نزد بچهها کم و نزد بالغین بیشتر است و نزد اشخاص مسن خیلی سخت و محکم ميباشد. وزن عدسی 20 سانتیگرم بوده و ساختمان آن به شرح زیر است:
- کپسول، کپسول عدسی غشائی است هموژن و الاستیک که از خارج عدسیها را احاطه کرده است. این کپسول به رباطهای آویزان کنندهی عدسی متصل ميشود و ضخامت آن در سطح قدامی عدسی تقریبا دو برابر سطح خلفی آن ميباشد.
- اپیتلیوم، پوشش عدسی عبارت است از یک ردیف سلول مسطح یا مکعبی که در محیط بتدریج باریکتر و بلندتر میشوند. این پوشش در سطح خلفی وجود ندارد.
- جسم عدسی، از رشتههای منظمی که در وضعیت نصفالنهاری قرار گرفته و بنام رشتههای عدسی موسومند تشکیل شده است. لابلای رشتهها را مادهی سیمانی پر کرده و مقداری از این ماده در مرکز عدسی متراکم گشته بنام هستهی مرکزی عدسی موسوم است. تغذیهی عدسی بطور غیرمستقیم از مایع زلالیه است.
عدسي يك ساختمان شفاف در پشت عنبيه است كه در متمركز كردن دقيق پرتوهاي نور بر روي شبكيه به قرنيه كمك ميكند. ضخامت عدسي چشم در شرايط مختلف تغيير ميكند و بسته به آنكه شيء مورد نظر در چه فاصلهاي از فرد قرار داشته باشد ضخامت عدسي كم و زياد ميشود. بنابراين فرد ميتواند اشياء را در فواصل مختلف (از بي نهايت تا حدود 20 سانتي متري و گاهي نزديكتر) به طور واضح ببيند. هرچه سن افراد بيشتر ميشود قدرت تغيير شكل عدسي كمتر ميشود به طوري كه در حدود سن 40 سالگي قدرت تغيير شكل عدسي آنقدر كم ميشود كه اكثر افراد براي ديدن اشياء نزديك و انجام كارهايي مثل مطالعه و خياطي به عينك كمكي براي ديد نزديك (عينك مطالعه) نياز پيدا ميكنند.
اين همان حالتي است كه به آن پير چشمي گفته ميشود. با گذشت سن علاوه بر آنكه قدرت تغيير شكل عدسي كم ميشود ميزان شفافيت عدسي هم كم ميشود. گاهي كدورت عدسي آنقدر زياد مي شود كه مثل پرده اي ديد فرد را تار مي كند. اين كدورت عدسي را اصطلاحاً آب مرواريد يا كاتاراكت ميگويند
ملتحمه
ملتحمه، عبارت از یک بافت همبند است که در سطح توسط اپیتلیوم پوشیده شده است. این اپیتلیوم در حاشیهی پلکها از نوع مطبق سنگفرشی است. ملتحمهی پلکی اپیتلیوم منشوری مطبق با سلول گابلت دارد.
ملتحمه يك لايه شفاف محافظ است كه سطح داخلي پلكها و روي سفيدي كره چشم را ميپوشاند. در ملتحمه رگهاي خوني و گلبولهاي سفيد به مقدار زيادي وجود دارد. اين رگها و سلولهاي دفاعي تا حد زيادي از ورود ميكروبها و عوامل بيماريزا به قسمتهاي عمقي چشم جلوگيري ميكند. به علاوه ترشحات ملتحمه سطح چشم را نرم و مرطوب نگه ميدارد و در حقيقت سطح چشم را روغنكاري ميكند كه اين امر باعث آسانتر شدن حركات چشم در جهات مختلف ميشود.
پلکها
پلکها (eyelids)، پلکها عبارت از 2 چین پوستی هستند که چشم را از نور زیاد و آلودگی محافظت مینمایند. هر پلک بوسیلهی پوست نازکی پوشیده شده است که در سطح خلفی به یک غشاء مخاطی و شفافی بنام ملتحمه (conjunctive) تبدیل شده است. در ضخامت پلک غدد چربی میبوم و غدد عرق کوچکی وجود دارد ولی هیپودرم پلک رشتهی ارتجاعی زیاد داشته فاقد بافت چربی است و به سستی به عضلات مدور پلک چسبیده است. در حاشیهی پلکها مژهها (eyelashes) در امتداد 2 تا 3 خط غیرمستقیم قرار دارند. مژهها دارای عضلهی راست کنندهی مو نیستند ولی غدد چربی وسیعی دارند و غدد عرق بزرگ و مارپیچی مژه بنام غدد مژهای مول معروف هستند.
وقتي جسم نوك تيزي به چشم ما نزديك ميشود ما بياختيار پلكها را ميبنديم. پلكها در حقيقت ساختمانهاي تمايز يافتهاي از جنس پوست و عضلات زير پوستي هستند كه وظيفه محافظت از چشمها را بر عهده دارند. مژهها مثل يك صافي از ورود گرد و غبار و ذرات مختلف به داخل چشم جلوگيري ميكنند. خود پلكها دو وظيفه مهم دارند: اول آنكه مثل يك ديوار دفاعي جلوي قسمت عمدهاي از كره چشم را ميگيرند و از كره چشم محافظت ميكنند، دوم آنكه پلكها هر 5 تا 10 ثانيه يك بار باز و بسته ميشوند كه اين امر به شسته شدن ميكروبها و ذرات خارجي از سطح چشم كمك ميكند و در حقيقت سطح چشم را جارو ميكند. به علاوه باز و بسته شدن پلكها به توزيع يكنواخت اشك بر روي كره چشم كمك ميكند.
غدهی اشکی
غدهی اشکی (lacrimal gland)، غدهای است از نوع غدد آسینی سروزی شبیه به غدهی پاروتید که ترشحات آن کرهی چشم را شستشو داده و مرطوب نگاه میدارد. اشک محتوی آب، املاح، و فاکتورهای باکتریسید از قبیل لیزوزوم میباشد.
عصب بينايي
عصب بينايي كه رابط كره چشم و مغز ميباشد از عقب كره چشم خارج ميشود و از طريق سوراخي در استخوان پروانهاي جمجمه به مغز ميرسد. اين عصب پيامهاي بينايي را به مغز ارسال ميكند و اين پيامها در مغز تفسير ميشوند.
عضلات چشم
براي آنكه ما بتوانيم اشياء را در جهات مختلف ببينيم لازم است بتوانيم چشم را در جهات مختلف بالا، پايين، چپ و راست بچرخانيم. حركات كره چشم در هر چشم به وسيله 6 عضله كوچك كه به اطراف كره چشم ميچسبند كنترل ميشود. بيماري اين عضلات و يا عدم هماهنگي آنها ميتواند به انحراف چشم يا لوچي منجر شود.
عفونتهای قارچی چشم
عفونتهای قارچی چشم گروهی از مشکلات کلینیکی مختلف را هم برای افتالمولوژیست و هم برای متخصص بیماریهای عفونی پدید ميآورد. بسیاری از افتالمولوژیستها با علل قارچی و درمانهای اختصاصی مربوط به اینگونه مشکلات آشنا نیستند، در صورتیکه نسبت به عفونتهای باکتریال چشم که مشکلات کلینیکی شایعتری هستند و نیز درمانهای آنها آشناتر میباشند.
عفونتهای قارچی چشم همچنین چالشی را برای متخصصین عفونی مطرح ميكنند. آنها با عوامل قارچی در جاهای دیگر غیر از چشم آشناتر بوده اما در مورد بیماریهای قارچی چشم کمتر آشنائی داشته و علاوه براین قابلیت دسترسی محدود به مواد ضدقارچی چشمی برای استفاده موضعی یا داخل چشمی (اینترااوکولار) و فقدان مطالعات کنترل شده در درمان موارد غیرشایع نیز انتخابهای درمانی را بازهم محدودتر میسازد.
علیرغم وقوع ناشایع بیماری قارچی چشمی، تهدید به کور شدن ناشی از اوضاعی مثل کراتیت قارچی یا اندوفتالمیت وضعیت را پیچیدهتر ميكند. درگیریهای پیچیدهی چشمی اغلب بعنوان بخشی از میکوز منتشره دیده میشود بنابراین افتالمولوژیست نقش مهمی در ادارهی این بیماران دارد. میکوزهای سینوسی- چشمی نیز بصورت بالقوه وضعیتهای تهدید کنندهای هستند که میتوانند همراه با یافتههای چشمی وجود داشته باشند. شناخت سریع و فوری این بیماریها توسط پزشک عمومی یا متخصص عفونی میتواند منجر به مداخلهی هرچه سریعتر توسط چشم پزشک شود و بدنبال آن برای پایش وضعیت پیشرفت بیماری یا پاسخ درمانی آزمایشهای چشمی پشت سرهمی انجام شود.
عوامل قارچی
هر گونهی قارچی که در عفونت سیستمیک درگیر شده باشد میتواند اندوفتالمیت ایجاد کند. گونههای کاندیدا شایعترین قارچهائی هستند که در اندوفتالمیت درگیر میشوند. علل نادرتر اندوفتالمیت قارچی شامل بلاستومایسس، کوکسیدیوئیدس و فوزاریوم میباشد.
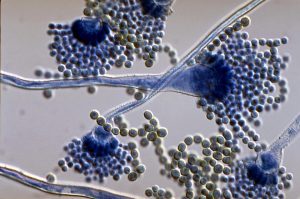
کاندیدا. شایع ترین گونهای که با آن مواجه میشویم کاندیدا آلبیکانس است، اما گونههای دیگری از قبیل کاندیدا پاراپسیلوزیس، کاندیدا کروزی و کاندیدا تروپیکالیس نیز مسئول میباشند.
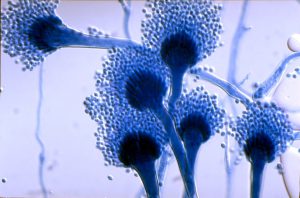
آسپرجیلوس. اندوفتالمیت اندوژنوس مربوط به آسپرجیلوس اغلب در نتیجهی آسپرجیلوزیس پیشروندهی منتشره دیده میشود. این ارگانیسم در بیماران ایمیونوکامپرومایزد از یک کانون ریوی از طریق خون به چشم گسترش میيابد.
اپیدمیولوژی. اندوفتالمیت میتواند بعلت آلودگی میکروبی اگزوژن و اندوژن بافتهای داخل چشمی ایجاد شود. اندوفتالمیت اگزوژنوس معمولا با جراحت به چشم رابطه دارد اگرچه میتواند در نتیجهی آلودگی داخل چشم توسط ابزار و وسایل، مایعات، و مواد خارجی در حین عمل جراحی چشم ایجاد شود. از طرف دیگر اندوفتالمیت اندوژنوس اصولا در نتیجهی انتشار خونی ایجاد ميشود اما همچنین میتواند در نتیجهی توسعهی مستقیم پروسهی عفونی مثل کراتیت ایجاد شود. در اینجا کراتیت به سمت داخل چشم گسترش میيابد.
انسیدانس اندوفتالمیت اگزوژنوس بدنبال ترومای نفوذ کننده به چشم تقریبا 5 درصد است و بیش از 10 درصد این موارد توسط قارچها ایجاد ميشوند. در مقابل انسیدانس اندوفتالمیت اگزوژنوس بدنبال جراحی داخل چشمی بینهایت اندک و معادل حدود 0/05 درصد تا 2/ 0 درصد ميباشد و تقریبا 5 درصد اینها علت قارچی دارند. این اختلاف قابل توجه بین انسیدانس اندوفتالمیت متعاقب جراحی یا ضربه بدلیل افزایش مواجههی چشم ضربه دیده (traumatized) به مواد خارجی آلوده شده با باکتریها و قارچها ميباشد.
در اندوفتالمیت اندوژنوس بیش از 50 درصد موارد با عامل قارچی روبرو هستیم. این درصد بالای اندوفتالمیت اندوژنوس با علت قارچی منعکس کنندهی وضعیت ایمنی مختل شدهی میزبان با بیماری سیستمیک قارچی است. فاکتورهای خطرساز برای توسعهی اندوفتالمیت اندوژنوس قارچی همان ریسک فاکتورهای مربوط به عفونتهای تهاجمی قارچی ميباشد و معمولا بیماری سیستمیک مقدم بر بیماری چشمی است.
سرکوب ایمنی مربوط به پیوند ارگان، استعمال داروهای تزریقی وریدی، بدخیمیها و آلودگی با HIV شایعترین و معمولترین فاکتورهای خطر ميباشند. باید بخاطر آورد که شبکیه چشم بیشترین حجم خون را نسبت به هر واحد از بافتهای بدن دریافت میکند و منبع عروقی اصلی شبکیه از کوروئید ميباشد.
اندوفتالمیت اندوژنوس قارچی از طریق گسترش هماتوژنوس به چشم از ارگانهای عفونی شده که معمولا ریهها است صورت ميگيرد. اندوفتالمیت اندوژنوس قارچی ممکن است در افرادی که بیماری منتشرهی قارچی دارند شناخته نشود. این بیماران اغلب در بیان شکایات بینائی خود دچار مشکل هستند. علاوه بر این آبنرمالیتیهای افتالمیک ممکن است در بیماران وخیمالحال چشمپوشی شود. بعنوان مثال در یک گزارش اتوپسی مربوط به گیرندگان پیوند کبد ارتوتوپیک 1 (orthotopic) در 7 مورد شواهدی از اندوفتالمیت آسپرجیلوسی یافت شد که تنها در یکی از این 7 مورد قبل از اتوپسی تشخیص اندوفتالمیت داده شده بوده است.
کاندیدا
در یک مطالعهی پروسپکتیو مربوط به 118 بیمار مبتلا به کاندیدمی در همهی آنها یافتههای چشمی ثبت شده بود. 1- بیماران با توپهای کرکدار یا پف کرده داخل زجاجیه یا گسترش داخل زجاجیهای قابل مشاهده ارتشاح کوریورتینال بعنوان اندوفتالمیت طبقه بندی شدهاند. 2- آن دسته از بیماران با لزیونهای کوریورتینال غیرمرتبط با آبسههای ویترئوس یا گسترش ویترئوس تحت عنوان کوریورتینیت کاندیدائی طبقهبندی شدند زیرا این لزیونها بطریق هیستوپاتولوژیک کاندیدا را نشان داده است. 3- بیماران با خونریزی داخل شبکیهای، انفارکتهای لایهای فیبرهای عصبی و خونریزی با مرکز سفید رنگ (Roth spots) بدون ارتشاح کوریورتینال بعنوان ضایعات غیراختصاصی طبقه بندی شدند زیرا این قبیل لزیونها ممکن است بعلل دیگری غیر از عفونت نیز ایجاد شده باشند.
بعنوان مثال انفارکتهای لایهای فیبرهای عصبی میتواند یا تظاهری از پرفوزیون ضعیف چشمی باشد – همانطور که در یک گروه از بیماران بدحال مثل بیماران مبتلا به کاندیدمی قابل انتظار است یا تظاهراتی از تجمع گرانولوسیتی در رتینوپاتی نوع Purtscher باشد.
کاندیدیازیس چشمی
پاورقی:
- پیوند یک ارگان بداخل موقعیت نرمال آناتومیکی خودش
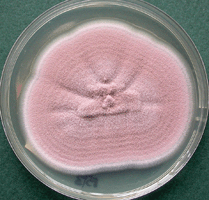
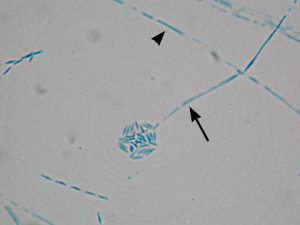
Candida albicans on culture plate growing on filter paper from vitrectomy specimen
رتینیت و اندوفتالمیت قارچی
آناتومی
مرور مختصری بر آناتومی چشمی برای درک گرفتاری بافتهای چشمی در عفونتهای مربوطه مفید است که این مهم در شمارهی قبل انجام گرفت. برای پرهیز از برخی اشتباهات احتمالی ترمینولوژی چشمی مرور میگردد. بخش خارجی چشم شامل قرنیه و اسکلرا (سفیدهی چشم یا صلبیه) که یک دیوارهی خارجی کلاژندار متراکم است و شامل چهار پنجم قسمت خلفی کرهی چشم میباشد. قسمت میانی و عروقی چشم شامل مجرای uveal (لایهای شامل عروق خونی و رنگدانه) است که از عنبیه، جسم مژگانی و کوروئید (غشاء چشمی دارای عروق خونی) تشکیل گردیده است. جسم مژگانی یک تنابه یا خلط آبدار تولید میکند که اتاقک قدامی (فضای بین سطح داخلی قرنیه و عنبیه) را پر میکند. کوروئید قسمت خارجی شبکیه را تغذیه میکند.
ساختمانهای داخلی چشم شامل عدسیها، زجاجیه و شبکیه میباشد. شبکیه از اپیتلیوم پیگمانتهی شبکیهای و شبکیهی عصبی حسی تشکیل شده است. زجاجیه یک ساختمان ژل مانند شفاف (نورگذران) است که حجم زیادی از چشم را اشغال میکند. زجاجیه بوسیلهی داربست لطیفی از فیبرهای کلاژن به قسمت قدامی محیطی شبکیه و اطراف عصب بینائی متصل شده است. شبکیهی عصبی حسی شامل رسپتورهای نوری، میلهها و مخروطها و سلولهای گانگلیون است. بیش از یک میلیون آکسون سلولهای گانگلیون وارد دیسک بینائی میشوند و عصب بینائی را تشکیل میدهند. التهاب داخلی چشم عموماً با یووئیت (uveitis) مشخص میشود هرچند که لایهی uveal با اکثریت عفونتهای داخل چشمی درگیر میشود، پروسهی التهابی ممکن است ساختمانهای دیگر چشم را نیز درگیر کند.
عفونت چشمی را میتوان با توجه به ساختمانهای آناتومیک درگیر شده توصیف نمود؛ بعنوان مثال یک پروسهی عفونی اولیهی شبکیه با گرفتاری ثانوی کوروئید رتینوکوروئیدیت (retinochoroiditis) نام دارد. واژهی “اندوفتالمیت” نوعاً برای توصیف پروسهی عفونی “پان افتالمیک” بکار میرود؛ بعنوان مثال در بیماری با عفونت سیستمیک کاندیدا با انتشار خونی به کوروئید و تغییرات ثانوی التهابی در شبکیهی مجاور “کوریورتینیت اندوژنوس کاندیدائی” توصیف ارجحی میباشد. اگر کوریورتینیت به سمت زجاجیه توسعه یابد در آنصورت “اندوفتالمیت اندوژنوس کاندیدائی” توصیف بهتری خواهد بود.
جدول 1- اجزاء دفاعی موجود در اشک چشم و عملکرد آنها
| اجزاء اشک چشم | عملکرد |
| لاکتوفرین | پروتئینی که توسط غدد اشکی ساخته میشود و اثر مستقیم باکتریوستاتیکی روی باکتریها دارد. |
| لایزوزیم | پروتئینی که دیواره سلولی را هدف قرار داده و موجب باکتریولیز در باکتریهای گرم مثبت میشود. |
| بتا-لایزین | با هدف قراردادن غشاء سلولی موجب سیتولیز باکتریهای مقاوم به لایزوزیم میگردد. |
| سرولوپلاسمین | در طول دورهی التهاب آسیب به بافت چشمی را تنظیم (regulate) میکند. |
| کمپلمان | موجب پیش بردن روند لیز باکتری، کموتاکسی و فاگوسیتوز میشود. |
| ایمنوگلوبولینها | اشک حاوی ایمنوگلوبولینهای G, M, E, A میباشد. IgA از چسبندگی باکتریها جلوگیری میکند، فلور نرمال چشم را تعدیل مینماید، باکتریها را آگلوتینه کرده و میتواند سموم را خنثی نماید. |
اپیدمیولوژی عفونتهای قارچی چشم
شایسته است که افتالمولوژیستها و اپتومتریستها بطور خاص و کلینیسینها بطور عام نسبت به پاتوژنز عفونتهای قارچی چشم اطلاع و دانش خوبی داشته باشند. عفونتهای قارچی چشم معمول است و بعنوان مثال کاندیدا آلبیکنس شایعترین علت اندوفتالمیت اندوژنوس است. قارچهای رشتهای مانند فوزاریوم سولانی و آسپرجیلوس فلاوس ممکن است تا یک سوم تمامی موارد کراتیت عفونی تروماتیک را شامل شوند. علاوه بر این بیماران مبتلا به ایدز ممکن است با بسیاری از انواع عفونتهای قارچی چشم و ساختمانهای مجاور آن درگیر شوند. در بیماری قارچی چشم پاتوژنز عفونت با اپیدمیولوژی مرتبط است، بنابراین در بحث اپیدمیولوژی عفونتهای قارچی چشم ابتدا ارزش آن را دارد که به چند اصل پاتوژنیک در مورد بیماری قارچی چشم توجه شود:
- به نظر میرسد که فونژمی استقرار یافته (حتی با قارچهای ساپروفیتیک) باعث اندوفتالمیت میشود.
- در زمان عفونت اولیه با برخی از قارچهای پاتوژنیک دو شکلی مانند هیستوپلاسما کپسولاتوم و کوکسیدیوئیدس ایمیتیس، یک فونژمی شناخته نشده پدید میآید و اغلب موجب اندوفتالمیت میشود.
3- سینوسهای اطراف بینی بدلیل ارتباط مستقیم با هوای محیط، دربردارندهی اسپورهای قارچهای ساپروفیتیک هستند که ممکن است سبب فرسایش و سائیده شدن دیوارههای استخوان سینوسها شوند و در وضعیتها و موقعیتهای معینی (مثلاً در یک بیمار نوتروپنیک) به چشم تهاجم نمایند.
4- تروما و ضربه، هم از طریق مواد گیاهی و یا از طریق اعمال جراحی ممکن است قارچهای ساپروفیتیک به قرنیه و یا بافتهای مجاور معرفی شده باعث ایجاد بیماری مهاجم شوند.
تظاهر بالینی اندوفتالمیت
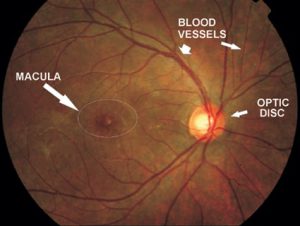
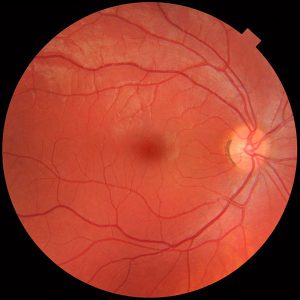
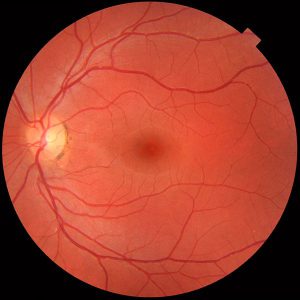
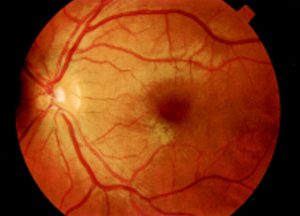
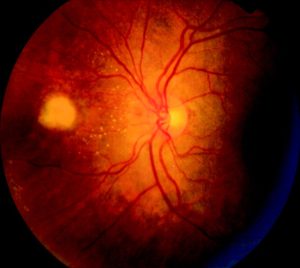
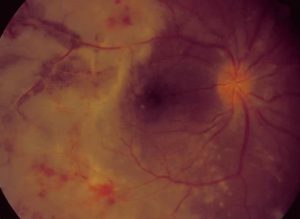
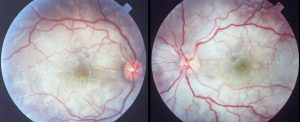
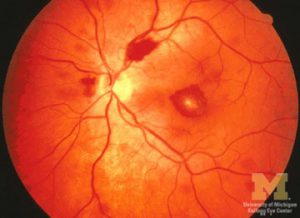
منظره طبیعی شبکیه
Fundus photograph of normal right eye
Fundus photograph of normal left eye
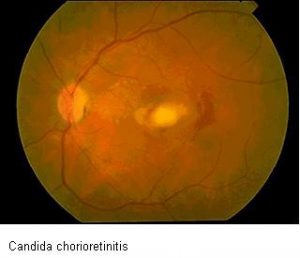
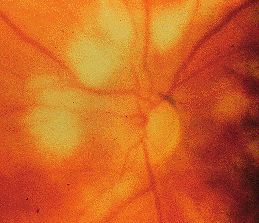
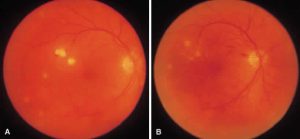
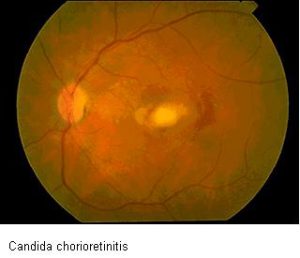
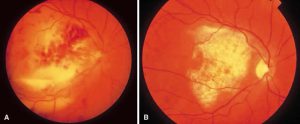
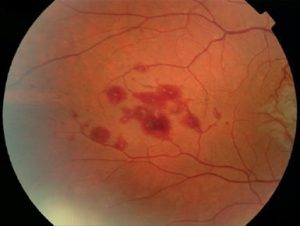
کوریورتینیت
اندوفتالمیت کاندیدائی
اپیدمیولوژی اندوفتالمیت اندوژنوس منعکس کنندهی زیستگاه طبیعی قارچهای درگیر کننده و وضعیت بهداشتی و عادات بیماران میباشد. اندوفتالمیت اندوژنوس کاندیدا بدنبال پیشرفتها و موفقیتهای طب مدرن که بیماران صعبالعلاج را (توسط آنتی بیوتیکهای وسیعالطیف، کاتترهای ورید مرکزی، تغذیهی غیر دهانی و تزریقی، جراحی شکم و شیمی درمانی سیتوتوکسیک) زنده نگه میدارد، پدید میآید. اندوفتالمیت کاندیدائی اولین بار در سال 1958 بصورت کلینیکی شناخته شد.
گونههای کاندیدا و آسپرجیلوس همچنین در استفاده کنندگان از داروهای تزریقی داخل رگی سبب اندوفتالمیت میشوند. تقریباً هر نوع وسیله یا دستگاه مصنوعی داخل رگی ممکن است بوسیلهی قارچهای فرصت طلب پخش شده از طریق خون آلوده شوند و از طریق چنین عفونتهائی فونژمی پدید آید که ممکن است به اندوفتالمیت اندوژنوس بیانجامد.
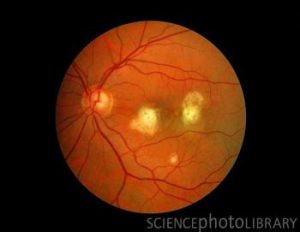
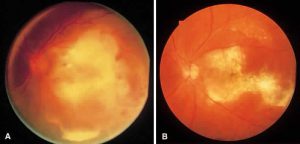
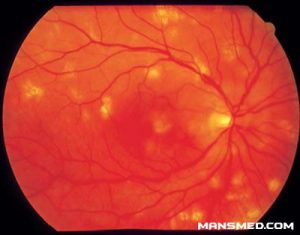
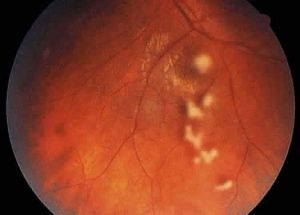
لزیونهای کوریورتینال متعدد ناشی از کاندیدا
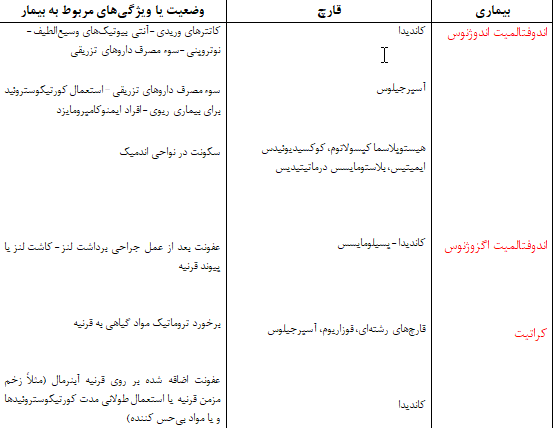
جدول 2- بیماری قارچی چشم در بیماران مبتلا به ایدز
| محل ضایعه یا نوع ضایعه | عامل قارچی |
| ندولهای پلکی
کنژکتیویت، کلونیزاسیون ملتحمه قرنیه اتاق قدامی، لبه و مرز کوروئیدیت (التهاب مشیمیه) رتینیت اندوفتالمیت اندوژنوس نوروپاتی اپتیک بیماری سینو- اربیتال |
کریپتوکوکوس
پنموسیستیس، کاندیدا کاندیدا کریپتوکوکوس، هیستوپلاسما کریپتوکوکوس، پنموسیستیس، هیستوپلاسما، کاندیدا، آسپرجیلوس کریپتوکوکوس، هیستوپلاسما آسپرجیلوس، فوزاریوم، بایپولاریس زیگومیستها، هیستوپلاسما، کریپتوکوکوس آسپرجیلوس |
اندوفتالمیت اندوژنوس بعنوان بخشی از بیماری منتشره در قارچهای دو شکلی نظیر هیستوپلاسما کپسولاتوم، بلاستوسیستیس درماتیتیدیس و کوکسیدیوئیدس ایمیتیس ناشایع است. افراد مبتلا به این دسته از میکوزها در نواحی اندیمیسیتهی این قارچها ساکن بوده و یا به آن مناطق مسافرت کردهاند. این مناطق عبارتند از درههای رودخانهی اوهایو و میسیسیپی برای هیستوپلاسما کپسولاتوم، قسمتهای جنوبی کالیفرنیا، آریزونا، نیومکزیکو، تکزاس غربی و بخشهائی از مکزیک و آرژانتین برای کوکسیدیوئیدس ایمیتیس و ایالات جنوب شرقی و قسمتهای میانی– شمالی ایالات متحده (از اوهایو تا کوههای راکی) برای بلاستومایسس درماتیتیدیس.
هیستوپلاسما کپسولاتوم قادر است که در فضولات پرندگان و خفاش رشد و نمو کند، بنابراین مواجهه با قارچ میتواند از طریق حرفه و شغل افراد اتفاق افتد، بعنوان مثال هنگام تخریب ساختمانهای قدیمی که پرندگان در آنها ساکن شدهاند و یا سرگرمیها یا مشاغلی مانند کشف و مطالعهی غارها، اردو زدن و چادر زدن و در موقعیتهای نظامی محل استقرار لشكرها و …
اندوفتالمیت اگزوژنوس در نتیجهی تروما به کرهی چشم یا در بیماران با سابقهی قبلی کراتیت پدید میآید، همچنین ممکن است بصورت عارضهی بعد از عمل جراحی برداشت عدسی و یا کاشت و جای دادن لنز مصنوعی و یا عارضهی پیوند قرنیه ایجاد شود. اکثریت قابل توجهی از عفونتهای چشمی بعد از عمل جراحی مربوط به استافیلوکوک کوآگولاز منفی هستند، هرچند که طغیانهائی از اندوفتالمیت اگزوژنوس قارچی بصورت تصادفی اتفاق میافتند. اینها مربوط به آلودگی لنزها هنگام عمل جراحی و یا آلودگی مایعات شستشو دهنده قبل و یا بعد از جراحی است. در این رابطه احتمال آلودگی با گونههای مختلف کاندیدا وجود دارد و شانس استقرار عفونت در نتیجهی کاربرد کورتیکوستروئیدها و عوامل آنتی باکتریال موضعی افزایش مییابد.
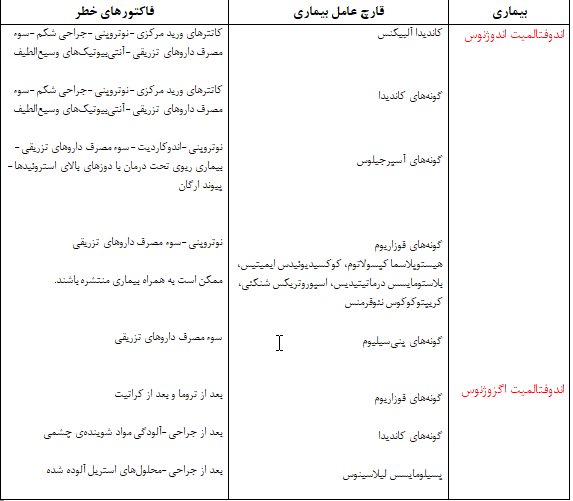
جدول 3- ویژگیهای اپیدمیولوژیک عفونتهای قارچی
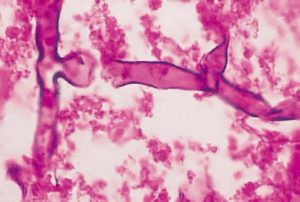
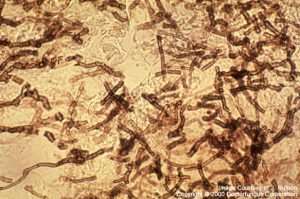
Typical broad hyphae of Aspergillus fumigatus on Giemsa stain
جدول 4- فاکتورهای خطر برای اندوفتالمیت اندوژنوس و اگزوژنوس
عفونتهای منتقله از راه خون: اندوفتالمیت اندوژنوس
اندوفتالمیت اندوژنوس ناشایع است، اگرچه بیشتر اوقات قارچها ایجاد کنندهی بیماری هستند تا باکتریهای گرم مثبت یا گرم منفی. واژهی اندوفتالمیت اندوژنوس دلالت دارد بر اینکه پخش و انتشار میکروارگانیسم به چشم از طریق خون اتفاق افتاده است، بنابراین عفونت در چشم در نتیجهی پراکندگی یا گسترش متاستاتیک عفونت از یک محل دور بعنوان مثال از دریچههای قلبی عفونی شده یا مجاری ادراری واقع شده است. در این حالت چشم محل تشکیل میکروآبسههای متعدد میشود.
این مکانیسم عفونت متمایز از اندوفتالمیت اگزوژنوس است که از معرفی مستقیم میکروارگانیسمها به چشم در جریان ضربه یا جراحی ناشی میشود. علاوه بر این اندوفتالمیت اندوژنوس در بیماران ایمنوکامپرومایزد (بعنوان مثال در بیماران دریافت کنندهی شیمی درمانی یا تغذیه غیر دهانی یا افرادی که سوء مصرف داروهای تزریقی دارند) بیشتر از نوع اگزوژنوس تشخیص داده میشود.
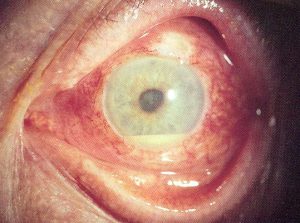
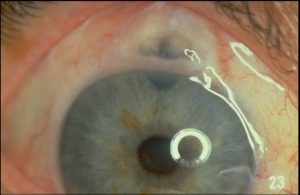
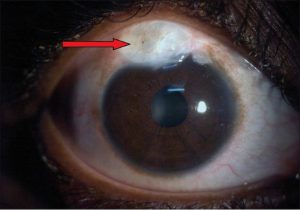
اندوفتالمیت از نظر بالینی با حضور یک یا چند ضایعهی کرم مایل به سفید با حدود مشخص در کوروئید و شبکیه و اغلب همراه با ارتشاح سلولهای التهابی در زجاجیه تشخیص داده میشود. این لزیونها را بوسیلهی افتالموسکوپ بعد از گشاد کردن مردمکها میتوان نشان داد. اغلب در اتاق قدامی التهاب وجود دارد که بوسیله ی انباشتگی چرک (hypopyon) آشکار میشود.
بیماران از درد چشم شکایت دارند و ممکن است تاری دید یا نقطههائی در میدان بینائی خود داشته باشند. در بیماران مبتلا به اندوفتالمیت اندوژنوس قبل از اینکه علائم و نشانههای چشمی آشکار شوند ممکن است کشت خون مثبت داشته باشند. در غیاب کشت خون مثبت و یا در عدم حضور سندرم کلینیکی مشخص، برای جداسازی و تعیین میکروارگانیسم عامل، آسپیراسیون زجاجیه یا بیوپسی ممکن است ضرورت یابد.
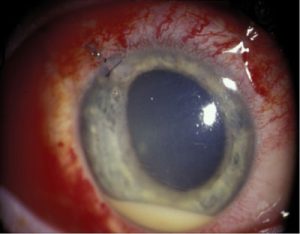
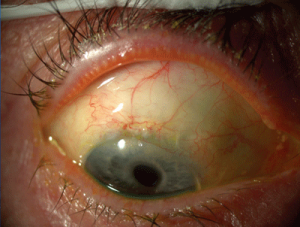
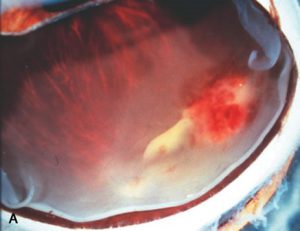
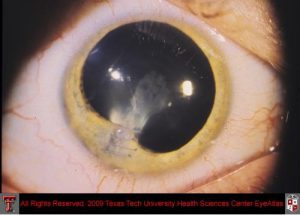
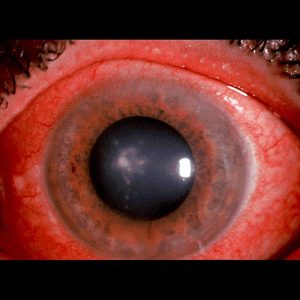
هایپوپیون (به تجمع چرک در اتاق قدامی توجه کنید)
توضیحی دربارهی هایپوپیون:
هایپوپیون اکسودای لکوسیتی است که در اتاق قدامی چشم دیده میشود و معمولاً با قرمزی ملتحمه و اپیاسکلرای زیرین آن همراه است. هایپوپیون نشانهی التهاب uvea قدامی و عنبیه است. اکسودای جمع شده بعلت نیروی جاذبه به سمت پائین نشست میکند. هایپوپیون در زخم قرنیه بویژه با اتیولوژی قارچهائی نظیر گونههای آسپرجیلوس و فوزاریوم و بعلاوه در بیماریهای دیگری مانند بهجت، اندوفتالمیت، panuveitis و panophthalmitis دیده میشود. هایپوپیون بعنوان چرک استریل نیز شناخته شده است زیرا نه بعلت تهاجم واقعی پاتوژنها بلکه بعلت رها سازی توکسینها هم اتفاق میافتد. هایپوپیون تنها چرکی در بدن است که به درمان اختصاصی نیاز ندارد و درمان عامل زمینهای موجب بهبود آن میشود.
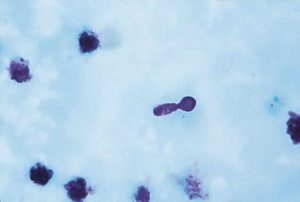
Candida albicans on Giemsa stain showing budding
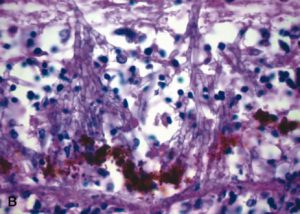
علت اینکه چرا چشم یک ارگان هدف نهائی شایع در فونژمی است چندان معلوم نیست؛ اگرچه در اندوفتالمیت ناشی از کاندیدا آلبیکنس مدل خرگوشی به ازای هر گرم از بافت چشم نسبت به کلیههای همان حیوان عناصر قارچی بیشتری یافت میشود. این نکته از این جهت حائز اهمیت است که عقیده بر این است کاندیدا آلبیکنس تروپیسم قابل توجهی به کلیهها و اندوتلیوم دارد و حضور تعداد زیادی ارگانیسم در چشم بخوبی نشانگر وجود تمایل و گرایش خاصی به چشم میباشد. لزیونهای کاندیدائی در خرگوش با آنچه که در انسان دیده میشود همانند است و نشان دهندهی کوریورتینیت کانونی (فوکال) با مخلوطی از واکنشهای گرانولوماتوزی و چرکی میباشد. عفونت احتمالاً در کوروئید شروع میشود و به سمت جلو بطرف لایههای شبکیهای توسعه میيابد.
این مسئله ممکن است تابع قوانین مکانیکی باشد به اینصورت که لایههای خارجیتر شبکیه- یعنی آنهائی که ابتدا عفونی شدهاند- خون را از یک سیستم با جریان بالاتری دریافت میکنند (150 میليمتر در ثانیه) در حالیکه لایههای داخلیتر خون را از یک سیستم با جریان کمتری (25 میلیمتر در ثانیه) دریافت میکنند. باید خاطرنشان ساخت که درناژ از لایههای شبکیهای تماماً از طریق سیستم وریدی انجام میشود و داخل کرهی چشم سیستم لنفاوی وجود ندارد. شایعترین عامل اندوژنوس اندوفتالمیت قارچی کاندیدا آلبیکنس است.
اندوفتالمیت اندوژنوس قارچی بر طبق تعریف بدنبال فونژمی پدید میآید. از آنجا که کاندیدا آلبیکنس چهارمین عامل شایع کشتهای خون مثبت بیمارستانی در ایالات متحده است و تعداد آنها از تعداد کشتهای مثبت هریک از باکتریهای گرم منفی به تنهائی فراتر است، تخمین زده میشود که در آمریکای شمالی حدود 120000 بیمار بطور سالانه به کاندیدیازیس منتشره (کاندیدمی) دچار هستند و تخمین معمولی انسیدانس اندوفتالمیت کاندیدائی در بیماران مبتلا به کاندیدمی حدود 30% است و بنابراین بیماری بطور متوسط شایعی است.
اگر تعریف کوریورتینیت بسیار دقیق باشد (یعنی اگر لزیونهای غیر اختصاصی مثل نقاط پنبهای پشمی شکل و خونریزیهای شبکیهای حذف شود) انسیدانس بسیار کمتر است و به حدود 3/9 درصد میرسد. پاتوژنز کاندیدمی ناشناخته باقی مانده است اما احتمالاً چند فاکتوری است. اشکال کلینیکی مشخصی از بیماران دچار کاندیدمی وجود دارد،
در هر بیمار ممــــــــکن است علامت یکسان یا متفاوتی نسبت به یکدیگر یافت شود. این علامات شامل استفاده از آنتیبیوتیکهای وسیعالطیف که میکروفلور نرمال را حذف میکند، حضور کاتترهای ورید مرکزی، تغذیهی غیر دهانی، عمل جراحی شکمی و یا نوتروپنی است. یکی یا همهی این فاکتورها کافی است که بیمار را در خطر بروز کاندیدمی قرار داده و در نتیجه شانس را برای ایجاد اندوفتالمیت ایجاد نماید.
در مدل خرگوشی نوتروپنی که یک فاکتور خطر برای کاندیدمی است انسیدانس اندوفتالمیت کاندیدائی را کاهش میدهد. این نکته مطرح کنندهی این است که تنها تعداد مطلق و خالص میکروارگانیسمهای عفونی کننده تعیین کننده نیست بلکه پاسخ نیرومند میزبان نقش مهمی در برطرف کردن لزیونهای کوریورتینال بازی میکند. در جریان آغاز روش تغذیهی غیر دهانی در دههی 1970 افزایش قابل توجهی در تعداد بیماران مبتلا به اندوفتالمیت کاندیدائی وجود داشت که احتمالاً به استفادههای طولانی مدت از کاتترهای ورید مرکزی مربوط بوده است. موارد وقوع اندوفتالمیت کاندیدائی متعاقب سقط جنین القاء شده، بعد از زایمان، بدنبال درمان مگاکولون توکسیک و بعنوان پیامد سوء مصرف داروهای تزریق وریدی، گزارش شده است.
استفاده از مواد مخدر تزریقی توسط معتادان اغلب منجر به سندرم مشخصی میشود که شامل لزیونهای پوسچولار پوستی، اندوفتالمیت و استئومیلیت است، این سندرم زمانی در اروپا شایع بوده است. از تمام این لزیونها کاندیدا آلبیکنس را میتوان جدا کرد. میکروارگانیسمها در این سندرم ممکن است از طریق سطح پوست خود فرد معتاد نفوذ کرده باشند. اندوفتالمیت کاندیدائی همچنین بعد از جایگذاری یک دستگاه خارجی بطریق داخل وریدی مانند جایگذاری باطری قلبی، یا بدنبال تزریقات مکرر داخل عضلهای داروها– مثل استروئیدهای آنابولیک- ممکن است اتفاق افتد. گونههای دیگر کاندیدا غیر از کاندیدا آلبیکنس قادر به ایجاد اندوفتالمیت اندوژنوس هستند و بر حسب توانائی خودشان موجب کاندیدمی میشوند.
اگرچه گونههای کاندیدا شایعترین عوامل اندوفتالمیت قارچی هستند اما قارچهای دیگر نیز گاهگاهی موجب آن میشوند. دومین علت شایع اندوفتالمیتهای قارچی گونههای آسپرجیلوس میباشند. البته گونههای آسپرجیلوس نسبت به گونههای کاندیدا کمتر موجب اندوفتالمیت میگردند. یک مثال خوب در این مورد مدل خرگوشی اندوفتالمیت اندوژنوس است که در آن تلقیح مقادیر بیشتری از آسپرجیلوس نسبت به کاندیدا لازم است تا بیماری را ایجاد کند.
بسیاری از گونههای آسپرجیلوس را بعنوان عوامل اندوفتالمیت گزارش کردهاند اما آسپرجیلوس فلاوس شایعتر از بقیه و بعد از آن به ترتیب آسپرجیلوس فومیگاتوس، آسپرجیلوس نیجر، آسپرجیلوس ترئوس، آسپرجیلوس گلوکوس و آسپرجیلوس نیدولانس قرار میگیرند. اندوفتالمیت اندوژنوس آسپرجیلوسی ممکن است در بیماران نوتروپنیک یا در بیمارانی که دوزهای فارماکولوژیک کورتیکوستروئیدها را دریافت میکنند (اغلب برای بیماری مزمن ریه) واقع شود. وقوع اندوفتالمیت آسپرجیلوسی بدنبال periodontitis شدید گزارش شده است گرچه ورود گونههای آسپرجیلوس بداخل جریان خون از طریق دهان مطمئناً شایع و معمول نیست. معتادان به داروهای داخل وریدی بویژه برای آسپرجیلوزیس منتشره در معرض خطر هستند.
اندوفتالمیت آسپرجیلوسی در معتادانی که مخلوطی از کوکائین، پنتازوسین (pentazocine) و تریپلنامین (tripelennamine) وریدی مصرف میکنندگزارش شده است. بیمارانی که از دوزهای بالای کورتیکوستروئیدها برای کنترل بیماری ریوی خود استفاده میکنند ممکن است کشتهای خون منفی داشته باشند اما همزمان دارای شواهد و مدارکی از اندوفتالمیت اندوژنوس آسپرجیلوسی شدید هستند، بنابراین اندوفتالمیت تنها تظاهر بیماری منتشره است و باید بوسیلهی آسپیراسیون از زجاجیه ثابت شود. اندوفتالمیت آسپرجیلوسی همچنین در گیرندگان پیوند عضو جامد- که در آنها ارگان دهنده احتمالاً منبع و منشأ قارچ بوده- نیز دیده میشود. نمونههای پاتولوژیک آسپرجیلوزیس تهاجمی معمولاً تهاجم عروقی (angioinvasion) توسط هایفیها را نشان میدهد و بنابراین گونههای آسپرجیلوس تمایل و گرایش به بافتهای عروقی (واسکولار) دارند.
اندوفتالمیت آسپرجیلوسی
ارتشاح کوریورتینینال آسپرجیلوسی
ارتشاح کوریورتینینال آسپرجیلوسی با پسودوهاپوپیون
ظهور پاتوژنهای جنس فوزاریوم بعنوان عوامل اندوفتالمیت در میزبان نوتروپنیک در افرادی که سوء مصرف داروهای تزریق وریدی دارند و در بیماران مبتلا به ایدز دیده شده است.
گونههای پنیسیلیوم نیز در نتیجهی سوء مصرف داروهای تزریقی موجب اندوفتالمیت اندوژنوس میشوند. همانطور که در ارتباط با کاندیدا آلبیکنس ذکر گردید اندوفتالمیت اندوژنوس ممکن است از طریق پخش و انتشار قارچ در جریان خون از طریق یک کاتتر یا اندوکاردیت ایجاد شود.
سودوآلشریا بویدیای از یک آلوگرافت porcine عفونی شدهی دریچهی آئورت و حتی در یک بیمار فاقد فاکتور خطر برای بروز این بیماری، اندوفتالمیت ایجاد کرده است. چهار قارچ دیمورفیک هیستوپلاسما کپسولاتوم، بلاستومایسس درماتیتیدیس، اسپوروتریکس شنکئی و کوکسیدیوئیدس ایمیتیس و همچنین قارچ فرصت طلب کریپتوکوکوس نئوفرمنس میتوانند بعنوان بخشی از بیماری منتشره اندوفتالمیت اندوژنوس ایجاد کنند. در نواحی اندمیسیتهی هیستوپلاسما کپسولاتوم در آمریکای شمالی، درههای رودخانهی “اوهایو” و “میسیسیپی” یک سندرم خوب توصیف شدهای مرتبط با هیستوپلاسما کپسولاتوم وجود دارد.
این حالــت که تحــت عنــوان POH شنـــــــــــــاخته میشود (مخفف عبارت Presumed Ocular Histoplasmosis) در افراد با ایمنی شایسته واقع شده و بوسیلهی حضور اسکارهای کوریورتینال آتروفیک دیسکی شکل متعدد بدون التهاب زجاجیـــــــه و مایع زلالیه (aqueous humor) شناخته میشود.
گفته میشود که POH هر سال 2000 مورد جدید را در نواحی اندمیسیته تحت تأثیر قرار میدهد و برخی از این موارد ممکن است به کاهش بینائی و کوری منجر شوند. ضایعات معمولاً خاموش شده (burned out) هستند اما همهی آنها ساکن و ایستا نیستند و برخی حالت واکنشی و انفعالی دارند. بنظر میرسد که لزیونها از انتشار هماتوژنوس قارچ بدنبال عفونت اولیه ایجاد شده باشند. عفونت اولیه با استنشاق میکروکونیدیها بداخل ریه ایجاد شده و به تمام بدن از جمله به چشم گسترش مييابد و البته بوسیلهی پاسخ ایمنی یک میزبان با ایمنی شایسته بموقع کنترل میشود.
هیستوپلاسما کپسولاتوم در اسکارهای POH قابل آشکار سازی نیست اگرچه شواهد اپیدمیولوژیکی محکمی وجود دارد که عمدتاً از طریق مطالعات روی تستهای پوستی بدست آمده که اسکارها را به هیستوپلاسموزیس مرتبط میسازد.
یک مدل پریماتی (primate) پاتولوژی یکسانی را با آنچه در انسان یافت میشود نشان داده است. لزیونهای مشابهی با آنچه که در POH وجود دارد در اروپا دیده شده یعنی جائی که در آن هیستوپلاسموزیس نادر است و بنابراین احتمال دارد که لزیونهای کوریورتینال متشابه، نتیجهی نهائی مربوط به عوامل عفونی مختلفی باشند.
اندوفتالمیت فعال در بیماران با هیستوپلاسموزیس منتشره ثانوی به ایدز و یا ثانوی به ایمنوسوپرسیون واقع میشود و با حضور سلولهای مخمری فراوان در بافت کوروئیدال و اندوتلیوم مرتبط است. در برخی موارد اندوفتالمیت همراه است با سلولهای مخمری در زوایای ساختمانی اتاق قدامی مثل iris، ماهیچهی سیلیاری و کانال schlemm.
دو مورد هیستوپلاسموزیس منتشره با نشان دادن سطح افزایش یافتهی آنتیژن هیستوپلاسما کپسولاتوم در خون و ادرار و نیز افزایش سطح آنتیبادیهای فیکس کنندهی کمپلمان، در دو برادر با ایمنی شایسته تشخیص داده شده است. بیماری آنها با کوروئیدیت (choroiditis) مرتبط بوده که به نظر میرسد که به سمت لزیونهای تیپیک POH پیشرفت کرده است، بنابراین ارتباط یا پیوند بین هیستوپلاسموزیس فعال و POH ممکن است توسط اینها و موارد مشابه ساخته شده باشند.
بلاستومایکوزیس منتشره در سگها شایع و اغلب همراه با اندوفتالمیت است. بعنوان مثال 78 چشم در 74 سگ مبتلا به بیماری منتشره، اندوفتالمیت داشتهاند. در مدل سگی بلاستومایکوزیس چشم همیشه کوریوکاپیلریها گرفتار هستند و ارگانیسم در کوروئید به تعداد فراوان وجود دارد و بیماری اغلب به سمت پانافتالمیت (panophthalmitis) پیشرفت میکند. در بلاستومایکوزیس منتشره در انسان با حضور لزیونهای کوریورتینال اندوفتالمیت تائید میشود.
در اندوفتالمیت اندوژنوس مربوط به کوکسیدیوئیدومایکوزیس لزیونهائی در سراسر چشم دیده میشود. در افراد ساکن در نواحی اندمیسیته با تست مثبت به کوکسیدیوئیدین- اسکار شدن کوریورتینال شایع است. لزیون های کوریورتینال احتمالاً در زمان عفونت اولیه اتفاق میافتد و معمولاً بلحاظ کلینیکی خاموش و بدون علامت هستند.
از طرف دیگر کوریورتینیت فعال در بیماران با بیماری منتشره شرح داده شده است. بیماری اتاق قدامی كه در بیماران مبتلا به بیماری منتشره نشان داده شده است شامل آماس عنبیه (iritis) و تودههای التهابی بزرگ در اتاق قدامی است. قابل توجه است که کوکسیدیوئیدومایکوزیس منتشره در سگها اغلب از اتاق خلفی شروع میشود و بعد از گسترش آن اتاق قدامی را گرفتار میسازد. همانطور که گفته شد عقیده بر این است که توسعه و گسترش اندوفتالمیت همانند اندوفتالمیت با علت کاندیدا و بلاستومایسس درماتیتیدیس میباشد.
مننژیت ایجاد شده بوسیلهی کریپتوکوکوس نئوفرمنس غالباً علائم بینائی را موجب میشود. این علائم معمولاً مربوط به تورم مغز و فشار روی عصب بینائی یا صرفاً بعلت ادم عصب بینائی است. هرچند که کریپتوکوکوزیس ممکن است با اندوفتالمیت مرتبط باشد و تظاهراتش را با کوریورتینیت و یا با از هم گسیختگی شبکیهای (retinal tears) و التهاب مفرط زجاجیه (vitritis) نشان بدهد.
پنموسیستیس کارینی یک عامل نادر کوریورتینیت در بیماران مبتلا به ایدز است.
رتینیت ناشی از پنموسیستیس کارینی
عوامل اوکولومایکوزیس
تا حدود چهار دهه قبل نمونههای اوکولومایکوزیس آنقدر کمیاب بودند که موارد دیده شده بصورت “گزارش مورد” مطرح میگردید. هرچند که امروزه نیز در مقایسه با علل باکتریال نسبتاً کمتر شایع هستند، اما موارد گزارش عفونتهای قارچی چشم در حال افزایش است و ضمائم چشم مانند پلکها، ملتحمه، سیستم اشکی، حدقه و سایر قسمتهای کرهی چشم (قرنیه، صلبیه، شبکیه، مشیمیه، شبکیه، زجاجیه و عصب بینائی) را گرفتار میکنند. اگرچه سهم قابل توجهی از این افزایش موارد نتیجهی افزایش آگاهی کلینیکی و بهبود و ارتقاء تکنیکهای تشخیصی است اما استفادهی وسیع از آنتی بیوتیکهای وسیعالطیف، کورتیکوستروئیدها، و کاتتریزاسیون تهاجمی طولانی مدت و نیز ظهور و پیدایش اختلالات نقص ایمنی، اختلالات یاتروژنیک (پزشکزاد) و یا آنهائی که با عفونت پدید میآیند همگی در افزایش میزان وقوع اکولومایکوزیس سهیم میباشند.
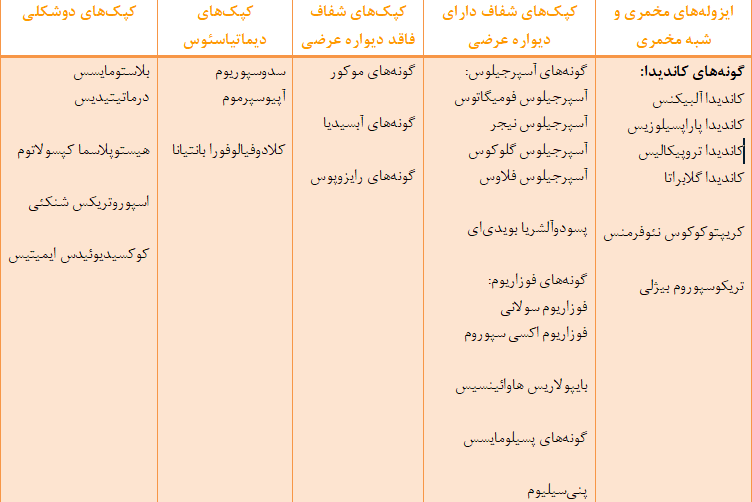
بیش از 150 گونه قارچی که در 56 جنس قرار میگیرند بعنوان عوامل اوکولومایکوزیس گزارش شدهاند. قارچهای عامل اوکولومایکوزیس را در 4 طبقه بررسی مینمایند:
- هیفومیستهای شفاف که شامل گروهی از قارچهای دارای تیغه ی میانی و فاقد ملانین در دیوارهی سلولی در بافت یا در کشت میباشند.
- هیفومیستهای فئوئید شامل قارچهای میسلیال دارای تیغهی میانی با حضور ملانین در دیوارهی سلولی در کشت و معمولاً در بافت
- مخمرها
- زیگومیستها که دارای هایفی بدون تیغهی میانی و واجد اسپورانژیا و زیگوسپور میباشند.
قارچ میتواند یک ساختمان منفرد چشمی مانند قرنیه را مبتلا سازد (مثلاً گونههای فوزاریوم و یا اینکه بطور همزمان چندین ساختمان چشم مانند اربیت، عصب بینائی و کوروئید را درگیر کند (مثلاً گونههای رایزوپوس)، همچنین یک گونهی خاص ممکن است ساختمانهای متعدد چشمی را در افراد مختلف مبتلا کند مثلاً در یک بیمار عفونت قرنیه و در دیگری اندوفتالمیت ایجاد نماید.
مایکوبیوتای چشم نرمال
گزارشهای متعددی وجود دارند که نشان میدهند که طیف وسیعی از قارچها از قسمتهای خارجی چشم در حالات “سلامت و بیماری” جدا شده است. منظور از “بیماری” در اینجا صرفاً “عفونت” نیست بلکه شامل حالات مختلف از قبیل “استفاده از کورتیکوستروئید موضعی”، “سندرومهای چشم خشک”، یا “سایر اختلالات غیرعفونی چشم” نیز میباشند. در اکثر این موارد قارچها از یک مرتبه کشت بدست آمدهاند. اصطلاح “فلور قارچی” برای نشان دادن چنین ایزولههائی بکار میرود. اما این اصطلاح در اینجا با آنچه که در سایر جاها بکار رفته است متفاوت میباشد.
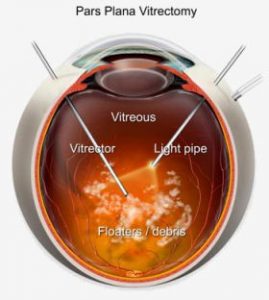
شکل شماره 1- ویترکتومی پارس – پلانا
تمام گروههای سنی و هر دو جنس در این گزارشها شامل بودهاند و فصول مختلف و مناطق مختلف جغرافیائی نیز در برگرفته شده است. شیوع کشتهای مثبت از 2/9 درصد تا 37/1 درصد در بین گروههای مختلف تحت مطالعه که شامل 43 تا 1347 فرد بوده متغیر بوده است. کپکهای فرصت طلب مثل گونههای آسپرجیلوس، پنیسیلیوم و مخمرهای گونههای کاندیدا و ردوترولا بصورت شایعی از چشمهای سالم در تمام این گزارشها جدا شدهاند. قارچها بصورت شایعتری از قسمتهای خارجی چشم افراد مسنتر کشت شدهاند و پلکها بیشتر از ملتحمه کشتهای مثبت داشتهاند.
در یک مطالعه استفاده از کورتیکوستروئیدهای موضعی چشمی موجب افزایش کشــــــــــــتهای مثبت قارچی شده است (Mitsui and Hanabusa, 1955) در حالیکه در مطالعات دیگران استفاده از کورتیکوستروئیدهای چشمی موضعی اثر قابل توجهی در افزایش میزان جداسازی قارچها از ملتحمه نداشته است.
مخمرها علیالخصوص گونههای کاندیدا از بخشهای خارجی چشم نرمال بیماران بستری نسبت به افراد غیربستری بسیار بیشتر جدا شدهاند. بسیاری از قارچهای جدا شده از قسمتهای خارجی چشم افراد سالم همانهائی هستند که از موارد اوکولومایکوزیس جدا میشوند؛ بویژه عفونتهای قارچی قرنیه (کراتومایکوزیس). ممکن است اینطور درنظر گرفته شود که قارچهائی که موجب ایجاد برخی از عفونتها میشوند بعنوان بخشی از فلور میکروبیال نرمال چشمی هستند، اکثر موارد اوکولومایکوزیس اگزوژنوس با تروما مرتبط هستند و بوسیلهی قارچهای فرصت طلب پاتوژن ایجاد میشوند.
از آنجا که احتمال وجود میکوبیوتای چشم نرمال کم است بنابراین عفونت بستگی دارد به حضورگذرای قارچ در زمان تروما یا تلقیح اسپورها از طریق وسیله یا ابزار. هنگامی که یک گونهی قارچی بیش از یکبار از قسمت خارجی چشم فردی جدا شود به معنی آن است که مواجههی مستمر با آن قارچ از طریق محیط یا از راه استفاده از وسایل چشمی آلوده شده صورت گرفته است.
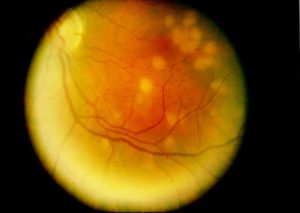
شکل شماره 2- کوروئیدیت چند کانونی
اندوفتالمیت قارچی
اندوفتالمیت قارچی و کوریورتینیت قارچی هر دو عفونتهای مایکوتیک داخل چشمی (intraocular) هستند. اختلاف عمدهی بین آنها حضور عفونت قارچی فعال جسم زجاجیه در اندوفتالمیت قارچی است. زجاجیه یک ژل بیرنگ، فاقد سلول و نورگذر است که چهار پنجم قسمت خلفی چشم (بین شبکیه و عدسی) را پر میکند و دارای ترکیب آبدار و قوام ژل مانند است. زجاجیه قوام ژل مانند خود را از طرز قرارگرفتن فیبریلهای کلاژن طویل، نازک و بدون انشعاب دارد که در یک شبکه از زنجیرهای بسیار هیدراتهی گلیکوزامینوگلیکان و پلیمرهای خطی از واحدهای دیساکاریدی بصورت سوسپانسیون درآمده است.
عفونت کانونی کوروئیدال ناشی از قارچها میتواند از طریق غشاء Bruch’s رخنه نموده و به شبکیه تهاجم نماید و اگر چک نشده باقی بماند به سمت زجاجیه توسعه یابد. قارچ سپس میتواند به راحتی زجاجیه را بعنوان سوبسترا برای رشد خود مصرف نماید.
شایعترین فرم اندوفتالمیت قارچی نوع اندوژنوس است و تقریباً همیشه از توسعه یا بسط عفونت کوروئیدال فوکال یا رتینال بداخل زجاجیه نتیجه میشود. گونههای کاندیدا عوامل اصلی کوریورتینیت قارچی و همچنین شایعترین علت اندوفتالمیت اندوژنوس هستند (Holland,1989). کاندیدا آلبیکنس شایعترین عامل اما کاندیدا گلابراتا، کاندیدا گیلرموندی، کاندیدا کروزی، کاندیدا پاراپسیلوزیس، کاندیدا تروپیکالیس و سایر گونههای غیرآلبیکنسی بعنوان عوامل ایجاد کنندهی کاندیدیازیس داخل چشمی گزارش شدهاند. لزیونهای مربوط به کوریورتینیت کاندیدائی پیشرفت میکنند تا جائیکه زجاجیه بصورت تودهی کروی، پرمانند و سفید با واکنش سلول التهابی قابل ملاحظه درمیآید. بیمار اگر متوجه باشد به لکهها یا نقطههای شناور و اشیائی که در میدان بینائی وی قرار میگیرند توجه میکند.
یک فوکوس فووئوماکولار (foveomacular) منتج به از دست دادن دید مرکزی میشود. همانطور که تودهها به هم آمیخته میشوند یک آبسهی زجاجیهای چرکدار تشکیل میشود که کل میدان بینائی را معیوب مینماید. برعکس اندوفتالمیت باکتریال حاد، درد یک شکایت متغیر در بیمار است. بدون مداخلهی درمانی آبسهی داخل زجاجیهای توسعه یافته بطوریکه قسمت قدامی چشم را گرفتار میسازد. فاصلهی زمانی از انتشار اولیه از زجاجیه تا تشکیل آبسه متغیر است و به مقدار زیادی بستگی به وضعیت ایمنی میزبان، تعداد سلولهای قارچی و دسترسی به زجاجیه و فاکتورهای ویرولانس کاندیدا دارد.
اگرچه کوریورتینیت کاندیدائی داخل چشمی اندوژنوس یا اندوفتالمیت تقریباً همیشه پیامد کاندیدیازیس منتشره است، اما شیوع گرفتاری چشمی در بیماران مبتلا به کاندیدمی کمتر بررسی شده است. همانطور که قبلاً ذکر گردید بزرگترین مطالعهی آیندهنگر که تا بحال گزارش شده است (Donahue et al, 1994) به کوریورتینیت در بیماران دارای کاندیدمی به میزان کمتر از 10% اشاره دارد و مطرح میکند که اندوفتالمیت حقیقی از عواقب غیرشایع است. معهذا همانطور که کاندیدیازیس منتشره یک وقوع بالقوه مرگبار است که ممکن است تظاهرات زودرس چشمی داشته باشد، آزمایشات چشمی غیرمستقیم بصورت سریال در اطفال و بالغین که مبتلا یا در معرض خطر کاندیدمی هستند به روشنی نشان داده شده است.
گونه های آسپرجیلوس روی هم رفته دومین عامل شایع اندوفتالمیت قارچی اندوژنوس هستند. عفونت چشمی در افرادی که درمان ایمونوسوپرسیو بدنبال پیوند عضو یا پیوند مغز استخوان میگیرند و یا در افرادی که از داروهای ضد سرطان استفاده میکنند عموماً بعنوان عارضهی آسپرجیلوزیس منتشره اتفاق میافتد. در یک مطالعه روی آسپرجیلوزیس منتشره، چشم دومین محل شایع عفونت بوده، در حالیکه در کاندیدیازیس منتشره چشم پنجمین ارگان بسیار شایع درگیری بوده است.
آسپرجیلوزیس چشمی اندوژنوس همچنین متعاقب استفادهی داخل وریدی داروئی و بدون نشانههای کلینیکی از درگیری ارگانهای دیگر ممکن است اتفاق افتد. در یک مطالعه ی مروری از 40 مورد اندوفتالمیت آسپرجیلوسی 13 مورد (5/32 درصد) به سوء مصرف داروهای داخل وریدی نسبت داده شده است. اندوفتالمیت آسپرجیلوسی اندوژنوس به نظر میرسد که یک عارضهی ناشایع آسپرجیلوزیس تهاجمی در بیماران مبتلا به ایدز باشد مگر اینکه تاریخچهای از سوء مصرف همزمان داروهای تزریق وریدی در کار بوده باشد. عفونت اندوژنوس همچنین در التهاب پریودونتیوم (periodontitis)- یعنی بافتهای احاطه کننده و پشتیبان دندانها- و در افراد دارای سیستم ایمنی شایسته بدون سابقه سوءمصرف داروئی و بدون سابقهی بدخیمی یا جراحی گزارش شده است.
آسپرجیلوس فومیگاتوس (شکل 12 و 13) شایعترین گونهای است که از کشت جدا میشود و 26 مورد از 47 مورد اندوفتالمیت اندوژنیک را که توسط Hunt و Glasgow در سال 1996 مطالعه شده شامل میشده است. آسپرجیلوس فلاوس (شکلهای شماره 14 و 15 و 16 و 17) عامل شایع بعدی و بدنبال آن آسپرجیلوس ترئوس، آسپرجیلوس نیجر و آسپرجیلوس نیدولانس قرار میگیرند.
در میزبانهائی که پوست بسیار روشن دارند قرمزی چشم، حساسیت به نور، درد و کاهش بینائی از شکایتهای غالب بیمار هستند. التهاب عنبیه و جسم مژگانی (iridocyclitis) با یک هایپوپیون متغیر در معاینهی بیومیکروسکوپیک دیده میشود. زجاجیه کدر و ابری است و ممکن است حتی عمل بینائی فوندوس را بقدر کافی مسدود نماید. تودههای پف کردهی توپ مانند و سفید ممکن است در زجاجیهی خلفی دیده شوند. غلاف عروقی، خونریزیهای شبکیهای و اگسوداهای واقع شده در جلوی شبکیه (preretinal) و زیر شبکیهای (subretinal) از یافتههای شایع هستند. اگسوداهای جلوی شبکیه ممکن است شکل قایق مانندی بخود بگیرند و اینها را بعنوان سودوهایپوپیون ارجاع دادهاند.
اغلب اوقات عفونت در قطب خلفی چشم شروع میشود و در صورت چک نشدن میتواند در جهت قدامی توسعه یافته و اجسام مژگانی، عنبیه (Iris) و عدسیها را درگیر نماید. نکروز شبکیهای وسیــــــــــــع است و جداشدگی احتمالی (eventual detachment) و بهم ریختگی یا بینظمی (disorganization) و از دست دادن بینائی نتیجه میشود. هر دو چشم ممکن است بطور همزمان دچار عفونت شوند.
در آزمایش هیستوپاتولوژی، زجاجیه، شبکیه و کوروئید انفیلتراسیون سلولهای التهابی حاد و مزمن را در کنار هایفی تیغهدار دیکوتوموس و منشعب نشان میدهند. شکل شماره 18 رتینیت هموراژیک نکروز دهنده و کوروئیدیت در بیمار مبتلا به آسپرجیلوزیس منتشره را نشان میدهد. در شکل شماره 19 هایفیهای منشعب و دیکوتوموس آسپرجیلوس مشاهده میشوند که شبکیه و کوروئید را درگیر کرده است. اگرچه عفونت کاندیدائی بطور غالب در کوروئید شروع میشود، اندوفتالمیت آسپرجیلوسی بطور غالب شبکیه و زجاجیه را درگیر میکند. یک تمایل برای تهاجم عروق خونی بوسیلهی انفیلتراسیون هایفال دیوارهی عروقی و لومن در شبکهی عروقی رتینال (شبکیهای) و کوروئیدال ثابت میشود. ترومبوز و انفارکتوس بافتی از عارضههای باقیماندهی این حوادث هستند. فرآیند تکاملی رویدادهای کلینیکی در اندوفتالمیت اندوژنوس بعلت آسپرجیلوسها بسیار سریعتر و دراماتیکتر از حوادث مشابه ناشی از کاندیدیازیس چشمی هستند.
اگرچه همانند کاندیدیازیس اوکولار معاینه ی مکرر افتالمولوژیکال میتواند به تشخیص زودتر عفونت منتشره بالقوه مرگآور در افراد در معرض خطر کمک کند. کپکهای شایعی مانند گونههای آسپرجیلوس تقریباً در همه جا حضور دارند (ubiquitous) و معمولاً محیط بیمارستان را آلوده میکنند. افرادی که در معرض خطر بوده و تحت درمان در بیمارستان هستند از طریق استنشاقی کنیدیهای آسپرجیلوس را گرفته و متعاقبا امکان گرفتار شدن به عفونت ریوی را دارند و این یک پیش درآمد برای اسپرجیلوزیس چشمی میتواند باشد. آلودگی مواد یا داروهای مخدر تزریقی (paraphernalia) با کنیدیهای آسپرجیلوس و مصرف آنها میتواند به افتالمیت اندوژنوس منجر شود.
گونههای فوزاریوم از عوامل شایع کراتوهیالوهایفومایکوز ولی از علل نادر اندوفتالمیت اندوژنوس هستند. عفونتهای داخل چشمی فوزاریال همانند اندوفتالمیت اسپرجیلوسی هم در افراد دارای ایمنی شایسته و هم در میزبانان دارای اختلال در سیستم ایمنی گزارش شده است. اندوفتالمیت فوزاریال اندوژنوس همچنین با سوءمصرف داروهای تزریق وریدی ارتباط دارد. اکثر گونههای عامل در فوزاریوز اکولار “فوزاریوم سولانی” بوده است (شکل های شماره 9 و 10 و 11) ولی یک مورد بعلت فوزاریوم دیمروم (F. dimerum) نیز جدا شده است. تظاهرات کلینیکی عفونت داخل چشمی فوزاریال بسرعت پیدا و نمایان میشود و تقلیدکنندهی آسپرجیلوزیس اکولار اندوژنیک است.
یافتههای هیستوپاتولوژیکال نیز شبیه به هم هستند. عناصر قارچی در زجاجیه، شبکیه و کوروئید همراه با تمایل به تهاجم و انسداد کانالهای عروقی داخل چشمی دیده میشود که به انفارکتوس بافتی و هموراژ و نکروز منتج میشود. عفونت داخل چشمی اندوژنیک دوطرفه که توسط بایپولاریس هاوائینسیس (Bipolaris hawaiiensis) ایجاد شده در یک فرد مبتلا به ایدز گزارش شده است. از نظر کلینیکی وضعیت بصورت یک کوروئیدیت رتینال چند فاکتوری شدید بدون هیچگونه گرفتاری وسیع زجاجیه ظاهر میشود. بلاستومایسس درماتیتیدیس، کریپتوکوکوس نئوفرمنس، کوکسیدیوئیدس ایمیتیس، هیستوپلاسما کپسولاتوم واریتهی کپسولاتوم، و اسپوروتریکس شنکئی نیز از قارچهائی هستند که بعنوان عوامل ایجاد کنندهی رتینیت اولیه و یا بصورت بسیار شایعتر بعنوان عوامل کوریورتینیت گزارش شدهاند. نوعاً اینگونه عفونتهای داخل چشمی اندوژنوس در بیماران ایمنوساپرس واقع میشوند. اگر اجازه داده شود که لزیونهای کوریورتینال رشد و پیشرفت کنند عفونت میتواند شبکیه را از هم باز کرده (break) و به زجاجیه تهاجم نماید.
اگر از طریق زجاجیهی کدر امکان مشاهده یک منظره از قطعهی خلفی چشم باشد تودههای پفآلود سفید زجاجیه ممکن است دیده شود که واسکولیت رتینال، خونریزی رتینال و انفیلتراهای داخل شبکیه و زیر شبکیه را پوشانده است. برای بنا کردن تشخیص (agent-specific) در غیاب کشت مثبت، بیوپسی از زجاجیه ضروری خواهد بود. علیرغم وجود گزارشهائی که در مورد پیامدهای موفقیت آمیز استفادهی صرف از داروهای ضدقارچی سیستمیک برای درمان اندوفتالمیت قارچی اندوژنوس بحث میکنند مداخلهی جراحی عموماً موقعی مطرح میشود که یک آبسهی میسلیال در زجاجیه شکل گرفته باشد. ویترکتومی پارس پلانا (شکل شماره 1) علاوه بر اینکه حفرهی ویتروس را از عناصر قارچی و سلولهای التهابی تخلیه میکند (debulking) نمونهی مناسبی (زجاجیه) را برای آزمایـــش گسترش مستقیم میکروسکپی و کشت فراهم مینماید. اغلب تزریق آمفوتریسین بی بداخل زجاجیه (intravitreal) همراه با ویترکتومی سیر عفونت را متوقف میکند و به ترمیم و اعادهی بینائی بیمار کمک میکند.
اگر درمان مداوم (ongoing therapy) کاربرد داشته باشد ثابت شده است که فلوکونازول داروی ایمنی است و در عفونتهای ناشی از اکثر گونههای کاندیدا، کوکسیدیوئیدس ایمیتیس و کریپتوکوکوس نئوفرمنس مؤثر است. ایتراکونازول که دارای اندازهی ملکولی بزرگتری نسبت به فلوکونازول است در صورت استفاده از طریق دهان سطح داروئی پائینتری را در زجاجیه بدست میآورد اما به هر حال اگر مصرف آن بلافاصله بعد از ویترکتومی شروع شود هنوز تأثیر درمانی میتواند داشته باشد.
اندوفتالمیت قارچی اگزوژنوس در نتیجهی ورود عناصر قارچی به زجاجیه از طریق خارج پدید میآید. این اتفاق بصورت بیشتر شایع بعنوان عفونت بعد از عمل جراحی داخل چشمی و بصورت کمتر شایع بعد از ترومای نفوذ کننده به داخل چشم دیده میشود. عفونت اگزوژنوس بعد از پرفوراسیون زخم قرنیهی قارچی یا عفونت مایکوتیک یک تاول یا وزیکول روی چشم (شکل شماره 3 و 4 و 5) حتی کمتر شایع است.
شکل شماره 3- حباب تا تاول فیلتر کننده (filtering bleb)
شکل شماره 4- حباب تا تاول فیلتر کننده (filtering bleb) منتشر شده (دیفیوز)
شکل شماره 5- حباب تا تاول فیلتر کننده (filtering bleb) کیستی شده
در 2 سری گزارش شده از اندوفتالمیت قارچی بعد از جراحی کاتاراکت مشخص گردید که محلولهای شستشو به همان عاملی که عفونت را ایجاد کرده آلوده بوده است. پسیلومایسس لیلاسینوس (Paecilomyces lilacinus) (شکلهای شماره 6 و 7 و 8) عامل عفونت بعد از عمل در یک سری سیزدهتائی از بیمارانی بوده که مورد عمل جراحی کاتاراکت قرار گرفته بودند و در آنها لنز داخل چشمی کاشته شده بود. یک محلول بیکربنات سدیم که برای شستشوی لنزهای چشمی استفاده شده است بلافاصله بعد از کاشت (implantation) لنزها نشان داده شده که پناهگاه پسیلومایسس لیلاسینوس بصورت آلوده کننده بوده است.
شروع علائم و یافتهها در این بیماران از 2 تا 15 هفته بعد از عمل جراحی متفاوت بوده است. درد یک شکایت نسبتاً کمتر و کاهش بینائی یک شکایت بسیار شایع بوده است. التهاب عنبیه، هایپوپیون متغیر و تودههای پف کردهی سفید در اتاق قدامی و بر روی سطح IOL و نیز در زجاجیه مشاهده شد.
شکل شماره 6- کلنی پسیلومایسس لیلاسینوس
شکل شماره 7- کلنی پسیلومایسس لیلاسینوس
شکل شماره 8- منظره میکروسکپی پسیلومایسس لیلاسینوس
شکل شماره 9- منظره کلنی فوزاریوم سولانی (محیط سابورودکستروز آگار)
شکل شماره 10- منظره پشت کلنی فوزاریوم سولانی (محیط چاپکسدوکس آگار)
شکل شماره 11- منظره میکروسکپی فوزاریوم سولانی
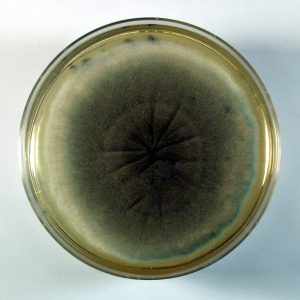
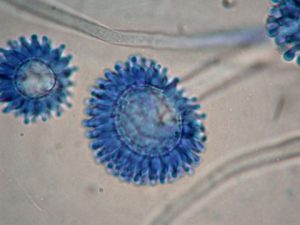
شکل شماره 13 – سرهای زایشی آسپرجیلوس فومیگاتوس
شکل شماره 14- کلنی آسپرجیلوس فلاوس
شکل شماره 15- کلنی آسپرجیلوس فلاوس
شکل شماره 16 – سرهای زایشی آسپرجیلوس فلاوس
شکل شماره 17- سرهای زایشی آسپرجیلوس فلاوس
شکل شماره 18 – کوریورتینیت آسپرجیلوسی
شکل شماره 19- کوریورتینیت آسپرجیلوسی
عفونتهای قارچی منتقله از راه خون بداخل چشم اگرچه ناشایع اما از علل مهم بیماریهای التهابی چشم میباشند. انسیدانس این دسته از بیماریها طی سالیان اخیر بدلائلی رو به افزایش نهاده است؛ از جملهی این دلائل افزایش تعداد بیماران ایمنوسوپرس است که از داروهای ضد سرطانی تهاجمی و یا رژیمهای درمانی دیگر استفاده میکنند، همچنین بیمارانی که پیوند عضو میگیرند و یا آنهائی که از آنتیبیوتیکهای قوی و جدیدتر و مؤثرتر استفاده میکنند که موجب کاهش فلور میکربی نرمال در سطوح بدن میشود. بیماران مبتلا به ایدز و یا افرادی که سابقهی سوء مصرف داروهای تزریق وریدی دارند همگی در افزایش ریسک اندوفتالمیتهای قارچی اندوژنوس سهیم میباشند.
رتینیت (التهاب شبکیه)
8 بیمار از 13 بیمار تحت عمل خارج کردن کره چشم قرار گرفتند، 2 نفر بینائی خود را بطور كامل از دست دادند و فقط یکی از 13 نفر با یک عفونت مشکوک بینائیاش در حد 6/18 حفظ شد. در آزمایش هیستولوژیکی از 5 چشم قارچها در برش قرنیه، اتاق قدامی، عنبیه و زجاجیه نشان داده شد. هیچ عنصر قارچی در کوروئید یا در شبکیه مشاهده نشد، اگرچه هر دو این ساختمانها با سلولهای التهابی حاد و مزمن انفیلتره شده بودند. پسیلومایســس لیــلاسیــنوس همــچنین موجب اندوفتالمیت اگزوژنوس بدنبال کراتــــــــــــــوپلاستی (a tectonic penetrating keratoplasty)و نیز بعد از عمل جراحی کاتاراکت بدون هیچگونه شواهدی از آلودگی مایعات شستشو دهنده شده است.
دومین سری مربوط به 15 مورد پشت سرهم اندوفتالمیت مربوط به کاندیدا پاراپسیلوزیس بعد از عمل جراحی کاتاراکت بوده است. تمام این بیماران توسط یک جراح که از محلول شستشوی داخل چشمی آلوده به کاندیدا پاراپسیلوزیس استفاده کرده بوده منتقل شده است. 13 مورد دیگر اندوفتالمیت اگزوژنوس ایجاد شده توسط این مخمر از جنوب شرقی ایالات متحده در نتیجهی استفاده از یک محلول شستشوی داخل چشمی آلوده گزارش شده است. همانند طغیان مربوط به پسیلومایسس لیلاسینوس مدت زمان بعد از عمل جراحی تا شروع علائم به تأخیر افتاده و از چند روز تا چند هفته ذکر شده است. از نظر کلینیکی التهاب عنبیه و “snowballs” در زجاجیه مشاهده شد. اداره و کنترل موارد مربوط به کاندیدا پاراپسیلوزیس بیشتر حملهای (aggressive) است و شامل ترکیبی از ویترکتومی و استفاده از آمفوتریسینB داخل چشمی و آمفوتریسینB داخل وریدی و نیز استفاده از 5-فلوروسیتوزین خوراکی میباشد.
‘‘snowballs”
برخلاف شیوع پسیلومایسس تنها یکی از 28 بیمار با اندوفتالمیت، بعد از عمل بوسیله ابتلا به کاندیدا پاراپسیلوزیس بینائی خود را بطور کامل از دست داد، در حالیکه بسیاری از بیماران در چشم مبتلا، بینائی در حد نزدیک به نرمال را بدست آوردند.
گونههای آکرومونیوم (سفالوسپوریوم) قارچهای محیطی خاکزی هستند که اغلب اوقات موجب مایستوما میشوند تا اینکه مسبب اندوفتالمیت باشند. در سال 1988Pflug felder et al ,، سه مورد وقوع در یک مرور روی 19 مورد اندوفتالمیت قارچی اگزوژنوس را گزارش کردند، 2 مورد مربوط به جراحی کاتاراکت و یک مورد در نتیجهی توسعهی مستقیم کراتیت ناشی از آکرومونیوم کورولوم (A. curvulum) بوده است.
گونههای آکرومونیوم علت نادر اندوفتالمیت بعد از تروما هستند اما این موارد در بیمارانی که در یک اتاق عمل مشترک جراحی کاتاراکت داشتهاند، دیده شدهاست. به تازگی 4 مورد اندوفتالمیت ناشی از آکرومونیوم کیلینزه (A. kiliense) که تماماً عمل کاتاراکت داشتهاند در همان اتاق عمل گزارش شده است. در این سری آکرومونیوم کلینزه با ایزولههای بدست آمده از بیماران عفونی شده که از آب آلوده شده در یک دستگاه رطوبت ساز که یک مجرای تهویه هوا به اتاق عمل را تغذیه میکرده بطور فنوتیپیکال یکسان بوده است.
منظره میکروسکپی آکرومونیوم
منظره میکروسکپی آکرومونیوم
مطالعات مربوط به آزمایشهای تعیین حساسیت ضد قارچی نشان داده است که گونههای آکرومونیوم نسبت به آمفوتریسین B مقاومت نسبی دارند و یک دوز داخل چشمی به میزان 5 میکروگرم برای درمان 4 مورد اندوفتالمیت ناشی از آکرومونیوم کلینزه ناکافی بوده است. شروع علائم به تأخیر افتاده و یافتههای کلینیکی مشابه با آنهائی بود که برای اندوفتالمیت ناشی از پسیلومایسس لیلاسینوس توصیف شده بود. یک طیف متنوع از مخمرها و کپکهای دیگر بعنوان عوامل مربوط به موارد انفرادی اندوفتالمیت قارچی گزارش شدهاند.
بسیاری از آنها همان ارگانیسمهائی هستند که بعنوان عوامل کراتومایکوزیس، کوریورتینیت و اندوفتالمیت اندوژنیک شناخته شدهاند. آلترناریا، آسپرجیلوس، کلادوسپوریوم، cylindrocarpon، اگزوفیالا، فوزاریوم، هیستوپلاسما، Lasiodiplodia، نوروسپورا، اوادندرون (Ovadendron)، پسودوآلشریا، سیتالیدیوم، اسپوروتریکس و گونههای تورولوپسیس را بعنوان مثال میتوان نام برد.
penetration ocular injury
بعضی از قارچها بعنوان عوامــــل اندوفتالمیت پس از جراحی یا جراحت چشمی نفوذ کننده (penetration ocular injury) گزارش شدهاند. علائم ظاهری و یافتههای کلینیکی بسته به عامل ایجاد کنندهی عفونت تا حدودی متغیر هستند. بطور کلی اگرچه عفونتهای قارچی بعد از عمل نسبت به عفونتهای باکتریال بعد از عمل یا حتی نسبت به عفونتهای قارچی اندوژنیک تمایل به تکامل بسیار آهستهتری دارند؛ بسیار محتمل است که مادهی تلقیحی که در جراحی به زجاجیه دسترسی پیدا میکند در مقایسه با انتشار اندوژنیک از لزیونهای کوریورتینال چند کانونی در حد مینیمال باشد.
از زمان جراحی نخستین تا آغاز علائم عموماً هفتهها تا ماهها زمان لازم است در صورتی که در اندوفتالمیت باکتریائی این فاصله در حد چندین روز است. در یک مورد عفونت ناشی از آلترناریا آلترناتا التهاب مزمن وجود داشت و از طریق کشت محتویات داخل چشمی تشخیص داده شد و متعاقب آن التهاب کنترل شد. هیستوپاتولوژی هایفیهای فئوئید را در کیسهی کپسول عدسی نشان داد. التهاب پایدار و کشت مثبت از زجاجیه، برداشت کیسهی کپسولی و لنز داخل چشمی را تصدیق میکند.
در اغلب موارد عفونت قارچها بدواً داخل زجاجیه هستند. زجاجیه کدر است و تودههای سفید پفآلود علائم کلینیکی هستند که بشدت مطرح کنندهی عفونت مایکوتیک میباشند. ویترکتومی پارس پلانا با تزریق داخل زجاجیه (intravitreal) آمفوتریسین B از اقدامات درمانی معمول هستند. درمان ضد قارچی سیستمیک بستگی به ارزیابی کلینیکال افتالمولوژیست از بیمار در وضعیت بعد از ویترکتومی دارد. وضعیت نهائی بینائی مشروط و موکول به اندازه و حد عفونت در زمان تشخیص است. بطور کلی عفونتهای هایفومایستیک بدتر از عفونتهای ایجاد شده توسط قارچهای مخمری هستند. اگر اسکلرا بوسیلهی یک کپک مورد حمله قرار بگیرد پیشآگهی وضعیت بینائی ضعیف است و کره چشم را اغلب خارج میکنند .(enucleated)
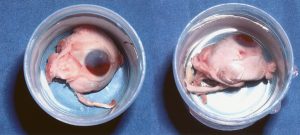
Enucleated eyes
عفونت متاستاتیک ممکن است فقط کوروئید و شبکیه را درگیرکند (کوریورتینیت لوکالیزه قارچی)، یا اینکه ممکن است به سمت زجاجیه یا مایعات اتاق قدامی پیشروی کند (اندوفتالمیت قارچی) و یا اینکه تمام بافتهای چشم را درگیر نماید (پانافتالمیت قارچی). همانطور که گفته شد قارچهای متعددی بعنوان عوامل ایجاد کنندهی عفونت داخل چشمی اندوژنوس گزارش شدهاند، اما گونههای کاندیدا بسیار بیشتر گزارش میشوند. کاندیدا آلبیکنس شایعترین بوده و بعد از آن آسپرجیلوسها قرار میگیرند.
التهاب حاد عنبیه
در جدول زیر قارچهای جدا شده از اندوفتالمیت قارچی اندوژنوس بصورت طبقه بندی شده لیست شدهاند:
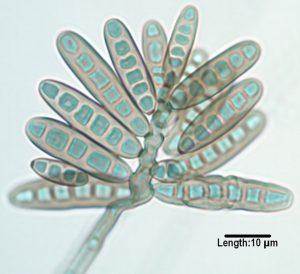
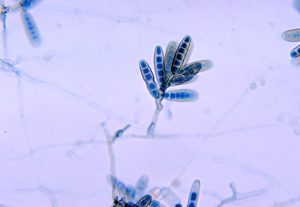
کلنی بایپولاریس هاوائینسیس
دستگاه زایشی بایپولاریس هاوائینسیس
دستگاه زایشی بایپولاریس هاوائینسیس
Cylindrocarpon destructans colony
Cylindrocarpon destructans
Cylindrocarpon candidulum
Cylindrocarpon lichenicola
Cylindrocarpon lichenicola
Scytalidium dimidiatum
Scytalidium dimidiatum
حالات التهابی و نئوپلاستیک چشمی بیشماری وجود دارد که شباهتهائی به اندوفتالمیت قارچی اندوژنوس دارند. در برخی موارد تشخیص افتراقی آنها از یکدیگر آسان ولی در برخی دیگر مشکل است. در اکثر این موارد یک شرح حال دقیق با جزئیات، معاینهی دقیق و بررسیهای مناسب آزمایشگاهی میتوانند به تشخیص صحیح کمک نمایند.
در جدول زیر لیست بیماریهائی که در تشخیص افتراقی با اندوفتالمیت قارچی اندوژنوس مطرح هستند دیده میشود:
| Endogenous bacterial endophthalmitis | Harada disease |
| Toxoplasmosis | Posterior scleritis |
| Sarcoidosis | Occlusive diseases of the choriocapillaris associated with systemic disease (e.g., DIC, TTP) |
| Tuberculosis | Steroid-induced severe central serous retinopathy |
| Pars planitis | Uveal effusion syndrome |
| Ocular lymphoma | Sympathetic ophthalmia |
| Retinoblastoma | Polyarteritis |
| Toxocara canis | APMPPE |
| Syphilis | Serpiginous choroiditis |
| Lyme disease | |
| Behcet’s disease | |
| Lens-induced uveitis | |
| Amyloidosis |
جداشدگی سروز چندکانونی دوطرفه در بیماری هارادا، هایپرمی دیسک در چشم راست (تصویر سمت چپ) بخوبی آشکار است.
درمان اندوفتالمیت قارچی اندوژنوس با توسعه ی داروهای ضد قارچی جدید در مسیر بهتر شدن پیش میرود. روش اختصاصی مداوای این بیماری هنوز بحث برانگیز است و بستگی به نوع قارچ، درجه و شدت گرفتار شدن چشم، حضور عفونت سیستمیک و وضعیت کلی سلامت بیمار دارد. سه مدل اصلی درمانی وجود دارد: استعمال سیستمیک یک داروی ضد قارچی، استفادهی داخل زجاجیهای داروی ضد قارچی و ویترکتومی پارس پلانا.
* * *
شرح اصطلاحات بکار رفته در این متن:
Iritis: التهاب حفره جلوئی چشم. از علائم آن درد، حساسیت به نور، قرمزی و کاهش بینائی است.
Pars planitis: التهاب زجاجیه و قسمت جلوئی شبکیه. اکثر بیماران از فلوتر Floaters و تاری دید شکایت دارند. درد، قرمزی و حساسیت به نور کمتر شایع هستند. التهاب عنبیه (ایریت) هم ممکن است وجود داشته باشد.
Floaters: لکههائی در پشت چشم. رسوباتی در مایع زجاجیه که معلق بوده و احیاناً از تجمع پروتئینها ناشی میشوند. این پدیده نشاندهندهی تغییرات دژنراتیو خوشخیم است.
Behcet’s disease: التهاب شدید تمام یا قسمتی از uvea، واسکولیت شبکیه، آتروفی اپتیک، و لزیونهای آفت مانند در دهان و ژنیتال، اغلب همراه با نشانهها و علائم دیگری که مطرح کنندهی واسکولیت منتشر است.
Uvea: مجموعهی عنبیه، جسم مژگانی و کوروئید (مشیمیه).
APMPPE: مخفف (Acute Posterior Multifocal Placoid Pigment Epitheliopathy) است و عبارت از التهاب تمام یا قسمتی از uvea که متعلق است به گروه هتروژنوس سندرومهای لکهی سفید که در آنها لزیونهائی به رنگ روشن در ماکولاي داخل شبکیه چشم شروع به تشکیل میکنند. با گذشت زمان لزیونها موجب کاهش بینائی میشوند که ممکن است از فرم متوسط تا شدید باشند اما بدون درد هستند و یک اختلال التهابی حاد اما خود محدود شونده میباشند.
Harada disease: این بیماری یک اختلال چند سیستمی است که بوسیلهی panuveitis گرانولوماتوز با جدائی لایههای داخلی شبکیه از اپیتلیوم پیگمانته اگزوداتــیو (exudative retinal detachment) مشخص میشود که اغلب با تظاهرات نورولوژیک و پوستی همراه است.
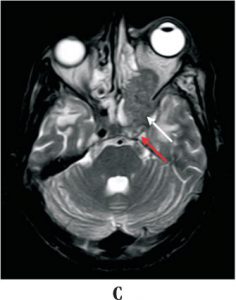
تصویر توموگرافی کامپیوتری از آسپرجیلوزیس سینوس کاورنوس و اربیت
اندوفتالمیت اگزوژنوس
اندوفتالمیت اگزوژنوس همانطور که از نامش پیداست بوسیلهی معرفی میکروارگانیسمها به چشم از طریق تروما یا جراحی ایجاد میشود. همچنین میتواند نتیجهی نهائی التهاب صلبیه یا کراتیت باشد. زایگومایکوزیس بافتهای نرم مجاور محاطی و نورورتینیت کریپتوکوکال نیز میتواند به این نوع اندوفتالمیت بیانجامد. بیماران مبتلا به اندوفتالمیت اگزوژنوس بندرت دارای نقص سیستم ایمنی هستند. برداشت کاتاراکت که بدنبال آن جایگذاری لنزهای پروستتیک انجام میگیرد و پیوند قرنیه از روشهای جراحی هستند که اغلب با اندوفتالمیت اگزوژنوس پس از جراحی در ارتباط میباشند.
در یک گزارش 19 بیمار از یک بیمارستان با اندوفتالمیت اگزوژنوس شرح داده شده است و بین علل اندوفتالمیت پس از عمل جراحی، اندوفتالمیت بدنبال تروما و اندوفتالمیت بدنبال کراتیت توزیع تقریباً متعادلی وجود داشته است. اندوفتالمیت اگزوژنوس ممکن یک دورهی کمون (مرحلهی پنهانی) معادل چندین هفته یا چندین ماه تا قبل از اینکه علائم بالینی خود را آشکار کند، داشته باشد. حتی بعد از آن، عفونت اغلب محدود و منحصر به اتاقک قدامی، papillary space یا ویتره قدامی است.
در یک سری 84% از بیماران قبل از تشخیص، کورتیکوستروئیدهای موضعی دریافت کرده بودند و این مسئله ممکن است با کاهش ایمنی موضعی میزبان موجب تقویت بیماری شده باشد. شایعترین علت اندوفتالمیت اگزوژنوس پس از عمل جراحی باکتریهای گرم مثبت هستند که شامل استافیلوکوک کوآگولاز منفی، دیفتروئیدها و پروپیونیباکتریوم آکنه میباشند. علل قارچی اندوفتالمیت اگزوژنوس نظیر مخمرها (بویژه گونههای کاندیدا؛ شامل کاندیدا گلابراتا و کاندیدا فاماتا) فقط در گروه پس از عمل جراحی یافت شدند، درحالیکه گونههای فوزاریوم تنها در گروههای “اندوفتالمیت بدنبال تروما” و “اندوفتالمیت بدنبال کراتیت” مشاهده شدند.
سایر گونههای کاندیدا، بدنبال عمل جراحی عدسی موجب اندوفتالمیت اگزوژنوس شدهاند. یک وضعیت اپیدمیک اندوفتالمیت مربوط به کاندیدا پاراپسیلوزیس پس از جراحی متعاقب قرار دادن لنزهای اتاقک قدامی و خلفی گزارش شده است. 15 بیمار در طول یک دورهی زمانی 3 ماهه جراحی چشم داشتهاند. در زمان جراحی همهی چشمها با محلولی (واحد) مورد شستشو قرار گرفتند که با کاندیدا پاراپسیلوزیس آلوده بوده است.
پسیلومایسس لیلاسینوس یک قارچ کپکی ساپروفیت خاک حاضر در همه جا است که در مواردی از کراتیت و اندوفتالمیت پس از تروما جدا شده است. یک طغیان بزرگ اندوفتالمیت اگزوژنوس مربوط به پسیلومایسس لیلاسینوس بدنبال کاشت داخل چشمی عدسی دیده شده است، لنزها بوسیلهی یک محلول بیکربنات که برای خنثی کردن مایع استریل هیدروکسید سدیم که به لنزها اضافه شده بود مورد استفاده قرار گرفته است و پسیلومایسس لیلاسینوس از محلول بیکربنات در کشت جدا شد.
قارچهائی مانند گونههای آسپرجیلوس و آکرومونیوم کیلینز بدنبال جراحی عدسی موجب عفونت شدهاند. این عفونت ها مانند عفونتهای مربوط به پسیلومایسس لیلاسینوس بعد از عمل جراحی، ممکن است در نتیجهی آلودگی محلولهای شستشو دهنده در حین عمل و یا پس از عمل جراحی به قارچها واقع شده باشند. پاتوژنهای قارچی در اندوفتالمیت پس از ضربه یک گروه بزرگ هستند و مشابه عوامل مسبب کراتیت قارچی میباشند. گزارشهای اخیر شامل فوزاریوم مونیلیفرم، اگزوفیالا جینسلمی، پسودوآلشریا بویدیای، آسپرجیلوس نیجر، سیتالیدیوم دیمیدیاتوم، گونههای هلمینتوسپوریوم، اسپوروتریکـس شنکئی، پنیسیلیوم کرایزوژنوم و Lasiodiplodia theobromae میباشد.
کراتیتهای قارچی
مقدمه
معمولاً بعلت قارچهای رشتهای و متعاقب اثرات ضربهای مواد گیاهی به قرنیه ایجاد میشوند. در نواحی گرمسیری در مردان کشاورز شایعتر است. جنسهای قارچی که در نواحی گرمسیری موجب کراتیت میشوند بسیار متنوع هستند و برخی از آنها نظیر Lasiodiplodia theobromae در نواحی معتدله رشد نمیکنند. در نواحی معتدل نیز ضربه به چشم عامل کراتیت قارچی است، اما شایعترین قارچهای مسبب عبارت از فوزاریوم، آلترناریا و آسپرجیلوس میباشند. کراتیتهای ناشی از مخمرهائی مثل گونههای کاندیدا تقریباً همیشه در چشمهائی که آبنرمال هستند اتفاق میافتند، مثلاً در بیمارانی که چشم خشک دارند و یا در افرادی که زخمهای مزمن قرنیه دارند یا آنهائی که دارای اسکار قرنیه هستند.
کراتیت قارچی
آناتومی
قرنیه یک ساختمان آناتومیکی نازک و شفاف و نورگذر میباشد که شامل یک پنجم قدامی چشم است و به لحاظ ساختمانی به سه قسمت تقسیم شده است:
1- یک اپیتلیوم سطـحی از سلولهای اسکواموس مطبق غیرکراتینیزه که بر روی یـک غشاء پایهای (basal lamina) واقع شده که به غشاء Bowman’s موسوم است.
2- یک لایهی استرومال از فیبریلهای کلاژن، فیبروبلاستها (کراتوسیتها)، موکوپروتئینها و گلیکوپروتئینها که 90% ضخامت قرنیه را در بر میگیرد.
3- یک اندوتلیوم مشتق شده از نورواکتودرم که در جهت اتاقک قدامی قرار گرفته و بر روی یک غشاء پایه به اسم غشاء Descemet’s واقع است. پروسههای التهابی که قرنیه را درگیر میکند تحت عنوان “کراتیت” شناخته شده است. همانند پوست، اپیتلیوم دفاع اولیه و ابتدائی بر علیه پروسههای تهاجمی به قرنیه است و یک نقص در اپیتلیوم اغلب اولین حادثهای است که اجازه میدهد عفونت استقرار یابد. پاسخ التهابی منجر به انفیلتراسیون سلولار با تخریب کلاژن قرنیه، نازک شدن استروما و در موارد شدید سوراخ شدن قرنیه با نشت مایع زلالیه و خطر گسترش و توسعهی داخل چشمی (اندوفتالمیت) میشود.
قارچ شناسی
فراوانی کلینیکی بیماری و عامل مسبب کراتیت قارچی بوسیلهی نواحی جغرافیائی جمعیت مورد مطالعه تحت تأثیر قرار میگیرد. عفونت قارچی قرنیه بصورت شایعتر در نواحی با آب و هوای گرمتر اتفاق میافتد؛ بعنوان مثال در جنوب فلوریدا 35% موارد کراتیت مربوط به قارچها هستند و شایعترین ایزولهی کلینیکی فوزاریوم است. در مقابل در نیویورک 1% از موارد کراتیت علت قارچی داشتهاند و کاندیدا شایعترین ایزولهی کلینیکی است و به دنبال آن فوزاریوم و آسپرجیلوس قرار میگیرند.
قارچهای دیماتیاسئوس از قارچهای شایع ساپروفیت خاک و گیاه هستند که بر اساس پیگمان سیاه آنها در یک گروه مطالعه میشوند و این پیگمان سیاه رنگ در رنگ آمیزیهای بافتی قابل مشاهده است. اعضاء قارچهای دیماتیاسئوس که در کراتیت درگیر هستند شامل گونههای کوروولاریا در نواحی گرمتر است. قارچهای دیماتیاسئوس ممکن است 10 تا 15 درصد تمام موارد کراتیت قارچی را به خود اختصاص دهند. کپکهای فاقد پیگمان (هیالوهایفومایکوزیس) نیز موجب کراتیت میشوند و اینها شامل گونههای فوزاریوم، پنیسیلیوم مارنفئی، گونههای سدوسپوریوم، پسیلومایسس لیلاسینوس و گونههای آکرومونیوم میباشند.
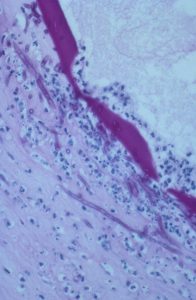
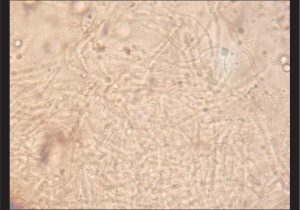
هایفیهای قارچی در نمونهی بیوپسی از قرنیه
اپیدمیولوژی
قارچها به احتمال بیشتر هنگامی که چشم در مواجههی مادهی آلی قرار میگیرد موجب کراتیت میشوند. قارچها باید بعنوان یکی از علل کراتیت در کشاورزان و افراد دیگری که در فضای خارج از اماکن بویژه در نواحی گرمسیری کار میکنند و جراحتهای چشمی دارند، در نظر گرفته شوند. باغبانان و کارگرانی که در طراحی و محوطه سازی مناظر محیطی با استفاده از قیچی یا ماشینهای چمنزنی کار میکنند و جراحتهای چشمی مستمر دارند نیز در معرض خطر هستند. مخمرها بویژه کاندیدا اغلب موجب عفونت قرنیه در بیماران مبتلا به نقص سیستم ایمنی میشوند. برش قرنیه (کراتوتومی) انکساری (Refractive Keratotomy) با کراتیت مرتبط است و 5% اینگونه موارد یک عامل قارچی داشتهاند.
همانطور که اقبال عمومی از این روشها افزایش مییابد یک افزایش متناسب در کراتیت قارچی نیز در این جمعیت بیمارانی که از جهات دیگر سلامت هستند دیده میشود. بیمارانی که از لنز تماسی استفاده میکنند و بیمارانی که قرنیه مخروطی (Keratoconus) دارند و نیاز به استفاده از لنزهای تماسی دارند نیز در معرض خطر ابتلا به کراتیت قارچی میباشند، هرچند که این بیماران نوعاً جوان و سلامت هستند، هایپوکسی و اثر سایندهی سطحی مربوط به لنزهای تماسی میتواند به اپیتلیوم قرنیه صدمه زده و بنابراین خطر کراتیت را افزایش دهد. سرانجام، هنگامی که بیماران مبتلا به کراتیت نسبت به آنتیبیوتیکهای موضعی پاسخ نمیدهند، شاخص سوءظن به قارچها بعنوان عامل عفونی مسبب افزایش مییابد.
پاتوژنز
پاتوژنز کراتیت قارچی عبارت از یک تهاجم فرصت طلب چشم آسیب دیده یا چشم تروماتیک توسط مادهی آلی است. واکنش التهابی و تخریب بافتی در کراتیت قارچی بوسیلهی اجزاء سلولی آنتیژنیک، مایکوتوکسینها و پروتئازها که به تهاجم استرومال عمقیتر کمک میکنند، ایجاد میشود. پیشرفت کراتیت بسیار متغیر است و از یک زخم بدون درد (indolent) و آرام قرنیه در یک پوشندهی لنز تماسی تا یک عفونت بسرعت مهاجم در نتیجهی یک ترومای شدید و برخورد با مادهی آلی فرق میکند. قارچها میتوانند به استرومای قرنیه نفوذ کنند و به غشاء Descemet’s آسیب زده و وارد اتاق قدامی شوند. تهاجم به داخل چشم (Intraocular) با کاهش بینائی خفیفترین پیامد و عاقبت کراتیت قارچی است.
تظاهرات کلینیکی
علائم کراتیت شامل درد چشم، قرمزی، کاهش بینائی، فتوفوبی، اشکریزش و ترشح از چشم است. در معاینه چشم (Gross Examination) به نظر میرسد که به چشم تزریق شده است و قرنیه ممکن است کدورت قابل توجهی داشته باشد و از دست دادن جلا و درخشش و یا یک ناحیه از کدر شدگی (Opacification) را نشان میدهد. یک ترشح چرکی مخاطی ممکن است وجود داشته باشد، پلکها ممکن است اریتماتوس و ادماتوز باشند و بلفاروسپاسم واکنشی (اسپاسم عضلهی مدور پلکهای چشم) ممکن است وجود داشته باشد. آزمایش چشمی با استفاده از Slit Lamp biomicroscopy اولسراسیونهای بیضوی کوچک را با یک ناحیهی وسیع از انفیلترای استرومال و ادم نشان میدهد. این یافتهی بیومیکروسکوپیک میتواند مشابه کراتیتی باشد که بوسیلهی کوکسیهای گرم مثبت ایجاد میشود. در کراتیت قارچی پیشرفته قرنیه سفید میشود (مشابه کراتیت باکتریال) و پرفوراسیون قرنیه از طریق نکروز و اولسراسیون ممکن است حاصل شود.
اندوفتالمیت میتواند عاقبت پرفوراسیون و تهاجم داخل چشمی باشد. نشانههای اولیهی کراتیت که با Slit Lamp biomicroscopy دیده میشود شامل انفیلترای گرانولار ظریف تا خشن در استرومای قدامی، انشعاب پر (کرک) مانند (feathery) قارچها به داخل استرومای قرنیه و سلولهای التهابی و پروتئینها در مایع زلالیه است. اگرچه این نشانههای اولیه در کراتیتهای قارچی علائمی عمومی است، شناسائی این اشکال بوسیلهی افتالمولوژیست باید شاخص شک و تردید به یک علت قارچی را افزایش دهد.
علائم دیررستر شامل یک حلقهی ایمنی (Immune Ring) است که میتواند بصورت مرکزی (فوکال) در استرومای قرنیه در اطراف ناحیهی عفونت یا لزیونهای اقماری و یا اطراف یک پلاک اندوتلیال شکل بگیرد. اشکال بیومیکروسکوپیک بخوبی با یافتههای هیستولوژیک همبستگی نشان میدهد؛ هایفیهای قارچهای رشتهای تمایل دارند که در سطح لایهی استرومال ارگانیزه شوند و سلولهای التهابی بطرف ارگانیسم مهاجرت نمایند.
تشخیص
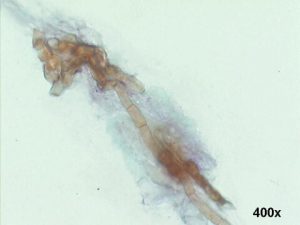
تشخیص باید با کشتهای تراشههای قرنیه دنبال شود. بیوپسی معمولاً در بیمارانی که در آنها درمان ضد باکتریال تجربی موفقیت آمیز نبوده و تشخیص میکروبیولوژیک بنا نشده است در نظر گرفته میشود. برای تشخیص قارچهای غیر از آسپرجیلــــــوس کمک مایکولوژیست مجرب ضروری است. قارچها بوسیلهی رنگ آمیزیهای استاندارد بافتی به آسانی قابل رؤیت هستند رنگ آمیزی Fontana-Masson برای آشکارسازی قارچهای دیماتیاسئوس مفید است، زیرا این رنگ ملانین را در دیوارهی این قارچها آشکار میسازد. اکثر قارچها در کشت در طول 2 تا 7 روز قابل مشاهده خواهند بود اما برای شناسائی قطعی آنها ممکن است به چند هفته زمان نیاز داشته باشیم.
منظره هایفیهای فراوان قارچ کپکی در نمونه تراشیده شده از قرنیه
تصاوير بالا هایفی قهوهای رنگ مربوط به قارچهای دیماتیاسئوس را در تراشهی قرنیه نشان میدهد
درمان
برای اکثر کراتیتهای قارچی اولیه سوسپانسیون 5% ناتامایسین که بصورت موضعی (Topical) تجویز میشود یک داروی انتخابی است. ناتامایسین بصورت موضعی بمدت یک هفته و بصورت هر یکساعت یکبار تجویز میشود و سپس به مدت 12 هفته در طول بیداری روزانه هر یکساعت یکبار مصرف میشود. آمفوتریسین B سیستمیک چندان مؤثر نیست زیرا نفوذ ناکافی و ناقص به قرنیه دارد. در کراتیتهای قارچی شدید از قطرهی آمفوتریسین B پانزده صدم درصد (0/15%) بعنوان تک درمانی یا در ترکیب با ناتامایسین یا فلوسیتوزین (محلول 1%در آب) نیز استفاده شده است.
گزارشهائی وجود دارد که نشان میدهد که قطرهی آمفوتریسین B بر علیه قارچهای دیماتیاسئوس تأثیر قابل ملاحظهای ندارد، هرچند که میکونازول و کتوکونازول موضعی بصورت موفقیت آمیزی بر علیه این دسته از قارچها استفاده شده است. برای موارد شدید یا مواردی که به درمان ضد قارچی موضعی پاسخ نمیدهند درمان خوراکی با کتوکونازول (400mg/d) با موفقیت همراه بوده است.
ایتراکونازول (400mg/d) نیز بجز قارچهای دیماتیاسئوس بر علیه قارچهای مختلف دیگر با موفقیت استفاده شده است. اگر تهدیدی برای سوراخ شدن چشم و یا ریسک اندوفتالمیت وجود داشته باشد، تزریق زیر ملتحمهی میکونازول یا فلوسیتوزین خوراکی توصیه شده است. بعد از شناسائی ارگانیسم مهاجم و بوسیلهی پاسخ کلینیکی نسبت به داروی مصرفی، میتوان درمان را اصلاح کرد و در اینجا میتوان از یک متخصص بیماریهای عفونی در انتخاب درمان مطلوب ضد قارچی کمک گرفت.
درمانهای کمک کننده میتواند شامل استفاده از میدریاتیکها و cycloplegics (عواملی که باعث فلج عضلات مژگانی یا بعبارت دیگر فلج تطابقی میشود) باشد که در کاهش اسپاسم مژگانی (ciliary) و در پیشگیری از به هم چسبیدن عنبیه به قرنیه یا عدسی (iris synechia) مفید هستند. (در نتیجهی التهاب داخل چشمی، عنبیه اغلب چسبیده به قرنیه یا عدسی میباشد).
استفاده از کورتیکوستروئیدهای موضعی بحث برانگیز است و برخی از منابع معتبر با استفاده از آنها مخالفت میکنند. در صورت تجویز، کورتیکوستروئیدها باید تنها بعد از 7 تا 10 روز بعد از شروع درمان ضد قارچی با بهبود کلینیکی خالی از ابهام و آزمایش و معاینه به فواصل نزدیک مورد استفاده قرار گیرند. اگر واکنش التهابی یا عفونت منجر به نکروز قرنیه با پرفوراسیون فعلی یا قریبالوقوع گردد، کراتوپلاستی (پیوند قرنیه) ممکن است ضرورت یابد. تقریباً 95% گرافتها معمولاً در عرض 4 هفته رد میشوند، معهذا تکرار پیوند قرنیه میتواند چندین ماه بعد از بهبود کلینیکی عفونت با موفقیت انجام شود.
عود عفونت در قرنیهی پیوند شده یک نگرانی مهم است. در یک مطالعه، 27% چشمهای مبتلا به کراتیت قارچی نیاز به پیوند قرنیه داشتند و 18% چشمهای پیوند شده عفونت عود کننده و تکرار شونده را نشان دادند.
بیماری سینوسی- چشمی (Sino-Orbital Disease)
آناتومی
سپتوم اربیتال یک سد آناتومیکی مهم در پلکها است که از انتشار عفونت از پلکها بداخل بافتهای چشمی جلوگیری میکند. سپتوم یک لایهی فیبروزی نازک است که از پریوست (بافت همبند تخصص یافتهای که تمام استخوانها را پوشانده و پتانسیل تشکیل و تبدیل شدن به استخوان را دارد) در طول لبههای چشمی فوقانی و تحتانی برمیخیزد. سپتوم در پلک با عضلات رکراکتور (عضلهای که موجب کشیدگی میشود) جوش میخورد: با evator apoeneurosis در پلک فوقانی و capsulopalpebral fascia در پلک تحتانی.
طبق تعریف بافتهای قسمت قدامی سپتوم بخشی از پلک هستند و بافتهای خلف سپتوم در فضای چشمی قرار میگیرند. پروسههای عفونی در فضای اربیتال میتواند بسرعت منتشر شود تا اعصاب جمجمهای و ماهیچهها را درگیر کند. اغلب مشکلات عفونی اربیتال بوسیله گسترش مجاورتی از سینوسها برمیخیزند. برخلاف عفونتهای پلکهای چشم که بطور غالب بوسیلهی باکتریهای گرم مثبت حاصل میشوند، عفونتهای اربیتال اغلب بوسیلهی قارچها یا مخلوطی از باکتریها ایجاد میگردند.
اپیدمیولوژی و قارچ شناسی
عفونت های تهاجمی اربیتال عمدتاً توسط قارچهای زایگومایکوز و آسپرجیلوس ایجاد میشوند. این قارچها از طریق هوا با استنشاق کنیدیها بداخل مجاری تنفسی انتقال پیدا میکنند. قارچهای فوق بیماری مهلک سینو- اربیتال مهاجم را در افراد مبتلا به نقص سیستم ایمنی و ناتوان شده ایجاد مینمایند. آسپرجیلوس میتواند موجب عفونتهائی در افراد دارای ایمنی شایسته بشود كه برخی از آنها ممکن است مهلک و کشنده باشند. آسپرجیلوزیس شایعترین عفونت قارچی سینوس در بیماران با سیستم ایمنی شایسته است. دو فرم از این بیماری شناخته شده است: یک توپ قارچی که در یک سینوس مسدود شده توسعه مییابد یا یک گرانولومای فیبروز شده که در اطراف هایفی ایجاد میشود.
پروسهی گرانولوماتوز میتواند به اروزیون استخوانی یا لیز استخوان (resorption) و گرفتاری مجاورتی اربیت و ساختمانهای داخل جمجمهای منجر شود. این بیماری در افراد با ایمنی شایسته بصورت کند و آهسته ایجاد میشود در صورتیکه در افراد دارای سیستم ایمنی آسیب دیده بصورت تهاجمی بروز میکند.
زایگومایکوزیس نامی است که به عفونتهای مختلف ایجاد شده توسط قارچهای راستهی موکورالها که در ردهی زایگومیستها هستند اطلاق ميشود. واژهی فیکومایکوزیس یک واژهی منسوخ شده است، زیگومیستها قارچهای کپکی هستند که در محیط رشد میکنند و در بافتهای زنده نیز به فرم هایفال رشد مینمایند.
گونههای رایزوپوس و رایزوموکور شایعترین قارچهای ایجاد کنندهی زایگومایکوز هستند. گونههای دیگر در راستهی موکورالها که بعنوان پاتوژنهای قارچی نادر در میزبانان ایمنوسوپرس مشاهده میشوند شامل آبسیدیا، موکور، کانینگهاملا، ساکسنهآ (sakscnaea) و Apophysomyces هستند؛ اگرچه اغلب آنها را بعنوان آلوده کنندههای آزمایشگاهی در نظر میگیرند. عفونتهای حاصله از قارچهای زایگومایکوز معمولاً در بیماران دیابتیک- بویژه در آنهائی که کتواسیدوزیس دارند – و نیز در گیرندگان پیوند و بیماران مبتلا به لوکمی و سایر بدخیمیها (بویژه آندسته که نوتروپنیک هستند) اتفاق میافتد.
درمان با آنتیباکتریالهای با طیف اثر وسیع نیز یک ریسک فاکتور مهم است. بطور مشابه عفونتهای مربوط به آسپرجیلوس اغلب در میزبانان ایمنوسوپرس بخصوص در بیماران نوتروپنیک اتفاق میافتد. در یک مطالعه 92% بیماران با آسپرجیلوزیس تهاجمی که در آنها اربیت درگیر شده بود یک فرم از بدخیمی را داشتهاند. 50% از عفونتهای اربیتال در افراد HIV مثبت بوسیلهی آسپرجیلوس ایجاد میشود. آسپرجیلوس فلاوس شایعترین گونه در این موارد است.
تظاهرات کلینیکی
بیماری در افراد با ایمنی شایسته به آهستگی پیشرفت میکند و علائم اغلب مبهم و گنگ و یا خفیف و جزئی هستند. حالت سنگینی در صورت و ترشح بینی اغلب از شکایتهای بیمار است. با گرفتاری اربیتال، جابجائی کرهی چشم و بیرون زدگی تخم چشم (proptosis) دیده میشود، اما معمولاً شواهدی از صدمه به عصب بینائی یا درگیری عصب جمجمهای دیده نمیشود. در بیماران دارای نقص سیستم ایمنی بیماری تهاجمی سینو– اربیتال قارچی نوعاً با درد صورت، سردرد، یا علائم دیگر مربوط به سینوزیت فولمینانت نشان داده میشود. با پیشرفت بیماری و گرفتاری اربیت، تحرک چشمی کاهش یافته منجر به دیپلوپی، پروپتوزیس و از دست دادن بینائی میشود.
با درگیری orbital apex و تخریب اعصاب جمجمهای 2، 3، 4، 5 یا 6 و یا همهی آنها، بیمار افتالموپلژی اکسترنال نسبی یا کامل، آنستزی قسمت فوقانی صورت و کوری در اثر تهاجم و ترومبوز شریان شبکیهای را نشان میدهد. درگیری عصب هفتم جمجمهای و دیگر شاخههای عصب پنجم نشان دهندهی بیماری وسعت یافته به خارج از فضای اربیتالی است.
تمایل این دسته از ارگانیسمها به عروق خونی منجر به ترومبوز شریانی، نکروز و انفارکتوس میشود. اگرچه نکروز بافتی یک اسکار سیاه از ترومبوز ایجاد میکند و بعنوان یک شکل کلاسیک در نظر گرفته میشود، فقدان آن نباید ما را از تشخیص دور سازد، تنها در 19% موارد يك بررسی، این یافته مشاهده شده است، بنابراین باید در تمام بیماران آزمایش و معاینهی بینی انجام شود و وجود نکروز بشدت مطرح کنندهی علامت کلینیکی زایگومایکوزها میباشد.
تشخیص
تصویربرداری رادیوگرافیک از اربیت و سینوس پارانازال برای ارزیابی اولیه و پایش پیشرفت بیماری و پاسخ به درمان در این بیماران بسیار ارزشمند است، بعلاوه مطالعه و بررسی جزئیات رادیولوژیک برای طرح ریزی عمل جراحی لازم و ضروری است. هر دو روشهای توموگرافی کامپیوتری (CT) و تصویربرداری رزونانس مغناطیسی (MRI) در مشخص کردن وسعت این پروسههای عفونی نقش مهمی دارند. MRI وضوح آناتومیکی بافت نرم اربیت را فراهم میکند و از این لحاظ نسبت به CT ارجحیت دارد، CT نیز تصاویر ارجحی از استخوان را فراهم میکند و لذا هر دوي این تصویربرداریها برای ارزیابی هرگونه پروسهی تهاجمی سینوس ضروری هستند.
علاوه بر این CT اغلب وضوح عالیتری از تودهی قارچی در داخل سینوس را نشان میدهد. تصاویر با وضوح بالای محوری (axial) و تاجی یا کورونال (coronal) هر دو، بوسیلهی CT یا MRI و یا هر دو آنها باید فراهم شود.
تصاویر کورونال رزونانس مغناطیسی را میتوان بدون دادن وضعیت (position) ویژهای به سر بدست آورد که این مسئله در مورد بیمارانی که همکاری خوبی ندارند یک مزیت است. در مقابل، تصاویر کورونال روش توموگرافی کامپیوتری نیاز به خم کردن (flexion) گردن دارد که همیشه میسر نیست بخصوص در بیمارانی که تیرگی شعور دارند. CT و MRI اغلب اطلاعات تکمیلی را فراهم میکنند و بنابراین بسیاری از بیمـاران بوسیلهی هر دو تکنیک مــورد بررسی قرار میگیرند. تشـــخیص بافــتی مــیتواند بوسیلهی رنگ آمیزیهای استاندارد صورت پذیرد اما یک مایکولوژیست مجرب میتواند به تفسیر آن کمک نماید، بویژه اگر ارگانیسم در محیط کشت رشد نکند.
درمان
درمان عفونت سینو –اربیتال ناشی از قارچها ترکیبی از دبریدمان جراحی و داروی ضد قارچی است. شناسائی سریع و شروع فوری درمان، کارهای اساسی برای توقف و پیشرفت عفونت و پیشگیری از مرگ میباشند. خارج کردن چشم (orbital exenteration) زمانی در حضور گرفتاریهای اربیتال ضروری در نظر گرفته میشد اما امروزه میتوان از انتخاب آن اجتناب ورزید. درمان ضد قارچی یک اقدام کمک کننده (یاور) برای جراحی است و جهت رسیدن به پیامد موفق اقدامی اساسی است. در گذشته پیشآگهی ضعیف بوده است و مرگ و میر بالائی نزدیک به 90% داشته است. در حال حاضر مرگ و میر بعلت تشخیص زودتر و طرحهای درمانی سریعتر و تهاجمیتر به میزان 15 تا 35 درصد کاهش یافته است.
آمفوتریسین B همچنان بعنوان داروی اصلی برای زایگومایکوز مهاجم باقی مانده است. دوز ابتدائی در یک بیمار با وضعیت بحرانی 1 تا یک و نیم میلیگرم به ازای هر کیلوگرم وزن در روز است. معمولاً برای چند روز نخست یک دوز آزمایشی 1 میلیگرم بکار گرفته میشود و بعد از چند روز از یک دوز نگاهدارندهی پائینتر برابر 1- 0/8 میلیگرم به ازای هر کیلوگرم وزن در روز که دوز استاندارد است استفاده میشود.
هنگامی که بوسیلهی ارزیابی کلینیکی و رادیوگرافیک پاسخ داکومنته شد به منظور به حداقل رساندن سمیت دارو، دوز دارو را میتوان بصورت یک روز درمیان ادامه داد. دوز توتال دارو دو و نیم الی 3 گرم در طول 3 ماه میباشد. فرمهای لیپوزومال آمفوتریسین B بهتر تحمل میشوند. با توجه به اینکه مقاومت نسبت به آمفوتریسین B اتفاق میافتد آزمایش تعیین حساسیت in vitro توصیه میشود.
در گزارشهای نه چندان معتبری از کاربرد موفقیتآمیز ایتراکونازول و فلوکونازول در درمان زایگومایکوز رینوسربرال ذکر شده است. در چندین گزارش نامعتبر نیز از کاربرد اکسیژن هایپربار (hyperbaric) و در گزارشهای دیگری از اینترفرون گاما بعنوان درمان کمکی پشتیبانی شده است. درمان عفونت آسپرجیلوسی سینو –اربیتال مشابه با اندوفتالمیت آسپرجیلوسی است که قبلاً شرح داده شده است.
التهاب کیسهی اشکی و مجرای اشکی (Dacrocystitis and Canaliculitis)
آناتومی
سیستم خروج اشک از منافذ سرسوزنی شکل و نقاط خروج اشک (puncta) در قسمتهای میانی پلکهای فوقانی و تحتانی تشکیل شده است. این نقاط در واقع منافذ پروکسیمال مجاری اشکی هستند و یک مجرای ظریف و باریک نزدیک تاندون میانی گوشهی چشم (canthal tendon) قرار میگیرد، در اکثر افراد مجاری فوقانی و تحتانی به هم پیوسته و قبل از ورود به کیسهی اشکی (lacrimal sac) به یک مجرای مشترک کوتاه تبدیل میشــــود.
اشک از کیسه به سمت پائین بطرف مجرای بینی اشکی (nasolacrimal duct) روانه شده و به بینی در بخش سوراخ تحتانی (inferior meatus) تخلیه میشود. انقباض و انبساط مداوم و همیشگی obicularis oculi در جریان پلک زدن معمولی علت تغییرات داخل لومن است که اشک را از چشم به سمت بینی حرکت ميدهد. انسداد آناتومیکی در سیستم خروج اشکی معمولاً در مجرای بینی اشکی بدلیل توقف جریان اشک (tear stasis) فاکتور مستعد کنندهای برای عفونت کیسهی اشکی است.
اپیدمیولوژی
زنان بسیار بیشتر از مردان تحت تأثیر قرار میگیرند و علت آن احتمالاً این است که به لحاظ آناتومیکی مجاری بینی اشکی باریکتری دارند. دهه پنجم یا ششم زندگی شایعترین سن بروز این علائم است. ترومای midfacial تازه یا قدیمی بخصوص شکستگی nasoethmoid بیمار را به انسداد مجرای بینی اشکی و التهاب کیسهی اشکی مساعد میسازد. فاکتورهای خطر دیگر شامل تشکیل سنگ مجاری اشکی و بیماری سینوس نازال یا پارانازال میباشند. آلرژی یا وضعیت التهابی مزمن مخاط بینی مانع خروج اشک از مجرا شده و توقف (استاز) آن را بدتر میکند و در نتیجه ریسک التهاب کیسهی اشکی را افزایش میدهد. علیرغم فراوانی انسداد مجرای بینی اشکی در اطفال، التهاب کیسه اشکی در این گروه بندرت دیده میشود.
قارچ شناسی
هرچند که اکثر موارد التهاب کیسهی اشکی منشأ باکتریال دارند، موارد قارچی در التهاب کیسه اشکی اکتسابی و مادرزادی گزارش شدهاند. کاندیدا آلبیکنس و آسپرجیلوس نیجر غالبترین قارچهای جدا شده هستند.
تظاهرات بالینی
داکریوسیستیت نوعاً با اریتم، سفت شدگی و احساس فشار در زاویهی پلکی میانی نشان داده میشود. بدلیل برگشت مادهی عفونی شده از کیسهی اشکی به cul-de-sac اکولار، چشم ممکن است قرمز و پلکها ادماتوز باشند. سلولیت ناحیه اطراف چشم (پری اربیتال) و وسط صورت (midface) بویژه با پاره شدن یک کیسهی اشکی متورم و باد کرده اتفاق میافتد. در پوستی که اربیت میانی تحتانی را پوشانیده است معمولاً فیستول تشکیل میشود. غالباً درد شدید وجود دارد و ممکن است به ناحیهی گلابلار لوکالیزه شود (ناحیهای بر روی استخوان پیشانی که در بالای نازیون و بین ابروها واقع شده است).
داکریوسیستیت در بیمارانی که بصورت اورژانس درد حاد در قسمت تحتانی پیشانی دارند باید درنظر گرفته شود، اگرچه این عفونت اکثر اوقات کند و آهسته و درد ملایم است. کانالیکولیت با التهاب یک طرفی ملتحمه، ترشحات مخاطی- چرکی، جمع شدن (تنگی) منافذ و التهاب کانونی بر روی کانالیکولهای گرفتار شده مشخص میشود. سنگ کانالیکولار و دیورتیکول معمولاً یافت میشود.
درمان
درمان برای داکریوسیستیت حاد میتواند محافظه کارانه باشد، درمان آنتی میکروبیال خوراکی یا جراحی با درناژ کیسهی اشکی برای برداشتن فشار کیسهی اشکی متورم شده و کاهش درد انجام میگیرد. در التهاب کیسهی اشکی مزمن یا تکرار شونده dacryocystorhinostomy که به معنای باز کردن راهی بین کیسهی اشکی و حفرهی بینی است (برای بایپس مجرای مسدود شده) بکار برده میشود.
یک بررسی نتیجهی بهتری را با ترکیبی از درمان جراحی و طبی و 80% نسبت بهبودی در مقایسه با درمان طبی به تنهايی (نسبت بهبودی 10%) نشان داده است. اطفال نوعاً با probing مجرای اشکی و برخی اوقات به همراه انتوباسیون سیلیکون درمان میشوند درمان اولیهی داکریوسیستیت استفاده از داروهای آنتیمیکروبیال خوراکی است.
به استثنای بیماران ناتوان یا اطفال در سایر گروهها بندرت نیاز به بستری در بیمارستانها وجود دارد. در بیماران با التهاب کیسهی اشکی تکرار شونده یا در آنهائی که به درمان خوراکی پاسخ نمیدهند درناژ جراحی کیسهی عفونی شده در ترکیب با داکریوسیستورینوستومی کاربرد دارد و بعد از این عمل اگر عفونت برگشت کرد ممکن است انجام dacryocystectomy (برش و برداشت کیسهی اشکی) موجه و مجاز باشد زیرا بعنوان یک آشیانه و مرکز فساد، عفونت میتواند در کیسه یا باقیماندهي مجرا و یا هردوي آنها باقی بماند.
کانالیکولیت نوعاً با پنیسیلین خوراکی درمان میشود زیرا اکتینومایسس شایعترین پاتوژن در این رابطه است. در صورتیکه نتیجهی کشت، از تشخیص عامل قارچی حمایت کند درمان ضد قارچی خوراکی کاربرد خواهد داشت. موارد Recalcitrant ممکن است نیاز به کورتاژ و دبریدمان کانالیکولهای عفونی داشته باشد. اکسیزیون جراحی کانالیکولها اغلب تنها راه درمان در موارد مزمن است.
منابع مورد استفاده:
- Stephen A. Klotz., and others. “Fungal and Parasitic Infections of the Eye”. Clin Microbiol Rew. 2000 13(4): 662-85.
- Elias J Anaissie. “Clinical Mycology”. CHURCHILL LIVINGSTONE . 2009
سندرم هیستوپلاسموز چشمی
اپیدمیولوژی
“سندرم هیستوپلاسموز چشمی فرضی” یک بیماری چشمی است که بصورت غالب در افراد سفید پوست و در سنین متوسط عمر در نواحی اندمیک عفونت هیستوپلاسموزیس دیده میشود. در نواحی شمال مرکزی (Midwest) و قسمتی از شرق ایالات متحده 59 درصد مردم تست پوستی مثبت برای هیستوپلاسما دارند اما تنها 4/4 درصد از افرادی که تست پوستی مثبت دارند دارای لزیونهای مشخص در ته چشم (فوندوس) که شرح داده میشود، هستند. دو آنتیژن HLA یعنی HLA-B7 و HLA-DRW2 در ارتباط با سندرم هیستوپلاسموز چشمی فرضی شناخته شده است.
یافتههای چشمی تیپیکالی که در زیر شرح داده میشود، اغلب اوقات در بیمارانی که در نواحی اندمیک هیستوپلاسموزیس در ایالات متحده زندگی میکنند و یا به نواحی مربوطه مسافرت میکنند، دیده شده است. البته این یافتهها در سایر نقاط دنیا بدون وجود بیماری هیستوپلاسموز نیز دیده شدهاند، بنابراین یافتههای چشمی در “سندرم هیستوپلاسموز چشمی فرضی” ممکن است منحصراً توسط هیستوپلاسما کپسولاتوم ایجاد نشده باشد و نتیجهی یک پروسهی پاتولوژیک مشترک با تصویر افتالمیک یکسان و مشابهی باشند. هیچگونه شواهد و مدارکی دال بر هیستوپلاسموز سیستمیک در بیماران دچار “سندرم هیستوپلاسموز چشمی فرضی” وجود ندارد.
این مسئله با موارد شناخته شدهی گرفتاری مشیمیه ((Uveal با هیستوپلاسموز منتشره در تقابل است. اندوفتالمیت هیستوپلاسمائی بیماری نادری است و یافتههای ته چشم را آن گونه که نوعاً در “سندرم هیستوپلاسموز چشمی فرضی” دیده میشود، نشان نمیدهد. 6 مورد شرح داده شده است که در آنها اشکال کلینیکی “سندرم هیستوپلاسموز چشمی فرضی” وجود داشته است و در آنها هیستوپلاسما کپسولاتوم یا آنتیژنهای آن بوسیلهی تکنیک هیستوپاتولوژی نشان داده شده است.
ساختمانهای داخل چشمی – مشیمیه (uvea)
تظاهرات بالینی
اکثر بیماران دچار “سندرم هیستوپلاسموز چشمی فرضی” بدون علامت هستند و تغییرات ته چشم در آزمایش روتین چشم مشاهده میشود. گسترش یک غشاء نئوواسکولار (neovascular) در ماکولا میتواند موجب کاهش تیزبینی دید مرکزی یا metamorphopsia (نوعی اختلال بینائی که در آن تصاویر مورد دید کج و معوج دیده میشوند) یا هردو حالت شود.
straight lines in central vision are distorted (metamorphopsia); peripheral vision is unaffected.
اکثر بیمارانی که در آنها غشاءها یا پردههای نئوواسکولار ایجاد میشود قبلاً بعنوان “سندرم هیستوپلاسموز چشمی فرضی” تشخیص داده شدهاند. علائم و نشانههای تیپیک ته چشم در “سندرم هیستوپلاسموز چشمی فرضی” شامل آتروفی اطراف پاپیلای بینائی (peripapillary)، لزیونهای چند کانونی کوروئیدال با هایپوپیگمانتاسیون مرکزی و هایپرپیگمانتاسیون محیطی، و یک عدسی شفاف و روشن است. آتروفی اطراف پاپیلای بینائی بصورت از دست دادن کوروئید و رتین (شبکیه) اطراف دیسک اپتیک دیده میشود.
ضایعات کوروئیدال که معمولاً حدود واضح (sharp) دارند بعنوان ‘histo spots’ ارجاع داده میشود و صفت بارز و مشخصه این سندرم است. وضوح و شفافیت عدسی در “سندرم هیستوپلاسموز چشمی فرضی” نشانگر این است که پروسه در این سندرم بداخل عدسی توسعه نمییابد، همچنین یک یافتهی مهم برای افتالمولوژیست برای افتراق این سندرم از دیگر بیماریهای کوریورتینال که یافتههای ته چشمی مشابهی دارند میباشد. ‘histo spots’ بصورت دو طرفه در 62 درصد این دســـــــته از بیماران یافت میشود.
‘histo spots’ نزدیک ماکولا ریسک برای توسعهی غشاءهای نئوواسکولار کوروئیدال و از دست دادن دید مرکزی را افزایش میدهد. غشاءهای نئوواسکولار کوروئیدال در آن نواحي که بافت تحت تأثیر قرار گرفته گسترش مییابد. از طریق این پردهها ممکن است پروتئینهای سرمی و مایع به داخل بافت زیرشبکیهای (subretinal) نشت کنند و نیز میتواند موجب خونریزی شود. خونریزی اغلب منجر به از دست دادن دائمی عملکرد شبکیهی مجاور میشود.
‘histo spots’ نزدیک ماکولا
تشخیص
تشخیص بوسیلهی یافتههای کلاسیک افتالمولوژیک که در بالا شرح داده شد صورت میگیرد. کشت معمولاً هیستوپلاسما را نشان نمیدهد. هنگامی که “سندرم هیستوپلاسموز چشمی فرضی” در یک بیمار شناخته شد، مسئلهی مهم توسعهی غشاء نئوواسکولار ماکولار در آینده است. انسیدانس این غشاءها بخوبی معلوم نشده و علت آن طبیعت بدون علامت سندرم در اکثر بیماران است. از آنجا که غشاءهای نئوواسکولار در ماکولا از ‘histo spots’ در آن ناحیه منشأ میگیرند، بیمارانی که در معرض خطر هستند باید از نزدیک پایش شوند.
پایش در منزل برای تغییرات در ماکولا بوسیلهی یک Amsler grid (یک نوع کاغذ میلیمتری صفحه شطرنجی با یک نقطه مرکزی است) یا دیاگرام مشابه صورت میگیرد. از بیمار خواسته میشود که دید خودش را روی نقطهی مرکزی فیکس کند و اگر بیمار یک نقص بینائی در طرح صفحه شطرنج نشان دهد یا خطوط را کج و معوج و یا تیره و تار ببیند توصیه میشود که هر چه سریعتر برای رد کردن اینکه اخیراً غشاء نئوواسکولار ایجاد نشده است، مورد آزمایش قرار گیرد. اگرچه غشاءهای نئوواسکولار معمولاً به کمک تکنیکهای افتالموسکوپ غیرمستقیم برای افتالمولوژیست قابل مشاهده است، اما بوسیلهی آنژیوگرافی فلئورسین بهتر مشخص میشوند. فلئورسین بطریق داخل رگی تجویز شده و تصاویر سریال را میتوان در واسکولاچور (سیستم عروقی) ته چشم توسط روشهای فتوگرافیک مخصوص بدست آورد.
نشت از عروق آبنرمال شامل غشاءهای نئوواسکولار به آسانی نشان داده میشود. علاوه بر این محل آناتومیک غشاء نئوواسکولار مشخص شده، در صورتی که اندیکاسیونی وجود داشته باشد از آنژیوگرام فلئورسین برای فتوکوآگولاسیون دقیق لیزری استفاده میشود. هنگامی که بیمار بعنوان “سندرم هیستوپلاسموز چشمی فرضی” شناخته شد فتوگرافهای رنگی از ته چشم بعنوان سند و داکومنت پایه به منظور انجام مقایسه در آینده تهیه میشود.
Amsler grid: (کاغذ میلیمتری صفحه شطرنجی با یک نقطه مرکزی)
درمان
درمان محدود است به برداشت از طریق برش (ablation) غشاءهای نئوواسکولار کوروئیدال که بوسیلهی فتوکوآگولاسیون لیزری انجام میشود. درمان فتودینامیک برای برداشت از طریق برش غشاء نئوواسکولار کوروئیدال در دیگر بیماریهای ماکولار مورد استفاده قرار گرفته است و ممکن است در “سندرم هیستوپلاسموز چشمی فرضی” سودمند باشد. درمان ضد قارچی یا استفاده از کورتیکوستروئید چه بصورت جداگانه و یا در ترکیب با هم هیچگونه فوائد ثابت شدهای نداشته است.
عوارض چشمی ایجاد شده توسط کریپتوکوکوس در بیماران ایدزی
اپیدمیولوژی و مایکولوژی
کریپتوکوکوزیس یک عفونت مهم فرصت طلب در بیماران HIV است، اگرچه انسیدانس آن با ظهور و پیدایش عوامل ضد ویروس مهارکنندهی پروتئاز سقوط کرده است. کریپتوکوکوس نئوفرمنس واریتهی گتی در بسیاری از نواحی گرمسیری موجب مننژیت کریپتوکوکال میگردد. اگرچه کریپتوکوکوس نئوفرمنس واریتهی نئوفرمنس در سراسر جهان استرین غالب است اما عفونت معمولاً بعنوان مننژیت با تغییراتی در وضعیت ذهنی، فلج عصب جمجمهای، کری و از دست دادن بینائی ظاهر میشود. از دست دادن بینائی فاجعه بارترین عارضه است زیرا اغلب غیر قابل بازگشت میباشد. اندوفتالمیت کریپتوکوکال بدون شواهدی از مننژیت کریپتوکوکال داکومنته شده است.
در پاپوآ (papua) گونهي جدید کریپتوکوکوس نئوفرمنس واریتهی گتی مسبب 95% موارد مننژیت کریپتوکوکال میشود. از دست دادن بینائی مسئلهی شایعی بوده و معمولاً در بیماران با ایمنی شایسته واقع میشود. در مقابل، در موارد گزارش شدهی مننژیت مربوط به کریپتوکوکوس نئوفرمنس واریتهی نئوفرمنس از دست دادن بینائی نادر است و معمولاً در بیماران دارای اختلال در سیستم ایمنی اتفاق میافتد. آیا واریتهی گتی دارای قدرت ویرولانس بیشتری است و یا اینکه تأخیری که احتمالاً در تشخیص آن بین بیماران ساکن این نواحی تروپیکال وجود دارد موجب شیوع بیشتر این عارضه است، بخوبی روشن نیست. Kestelyn و همکاران دریافتند که 76% بیماران با بیماری سیستمیک کریپتوکوکال یافتههای چشمی را داشتهاند.
***
ادامه مبحث مربوط به اپیدمیولوژی کاندیدا
بصورت مشابهی ‘Roth spots’ بعنوان یافتههای غیر اختصاصی در نظر گرفته شدهاند. اگرچه کاندیـــدا از ‘Roth spots’ جدا شده است، اما علل متعدد دیگری (بعنوان مثال پرفشاری خون، دیابت ملیتوس، آنمی، بیماریهای کلاژن واسکولار و حالات لنفوپرولیفراتیو) مشمول هستند.
Roth spots
Roth spots
از بین 118 بیمار مبتلا به کاندیدمی تنها یک مورد معیارهای کلاسیک برای اندوفتالمیت کاندیدائی را در برداشت که در این مورد گرفتاری زجاجیهای داکومنته نشد. هرچند که برای کوریورتینیت کاندیدائی در 9/3 درصد (11 بیمار از 118 بیمار) موارد مدارکی وجود داشت، در 20 درصد (24 بیمار از 118 مورد) لزیونهای ته چشم وجود داشت که جزء یافتههای غیر اختصاصی طبقه بندی شدند. 3 مطالعه پروسپکتیو قبلی از شیوع اندوفتالمیت به میزان 28%، 29% و 45% در بیماران بستری شده در بیمارستان كه مبتلا به کاندیدمی هستند حکایت دارد. یک مطالعه پروسپکتیو دیگر شیوع 10% از اندوفتالمیت کاندیدائی را در بیمارانی که تغذیه بیش از حد (hyperalimentation) دارند گزارش کرده است.
دلائل این اختلاف در شیوع اندوفتالمیت بین مطالعه Donahue و آنچه که توسط محققین قبلی انجام شده احتمالاً مربوط است به معیارهای سخت گیرانه برای تشخیص کاندیدیازیس داخل چشمی (intraocular) و این حقیقت که عوامل ضد قارچی بلافاصله برای مداوای کاندیدمی در مطالعه Donahue تجویز شده بوده است؛ بعنوان مثال در یک مطالعه “لزیونهای شبکیهای نرم و بادکردهی تیپیک” در 29% از بیماران مبتلا به کاندیدمی گزارش شده و هیچ اشارهای به مقدار یا حد گسترش داخل زجاجیهای (intravitreal) نشده و نیز از اینکه آیا هر یک از چشمها لزیونهای غیر اختصاصی داشته باشند یا خیر نامی برده نشده است.
Brooks بیماران با کاندیدمی را که در آنها ‘Roth spots’ وجود داشت مورد ملاحظه قرار داد تا بررسي كند كه آیا اندوفتالمیت داشتهاند یا خیر. حداقل 2 نفر از 9 بیمار در مطالعـــــهی Brooks با اندوفتالمیت، ‘Roth spots’ بعنوان تنها ضایعهی موجود در فوندوس را داشتهاند. در مطالعه ی دیگری بر روی 48 بیمار مبتلا به کاندیدمی، یک انسیدانس 44% اندوفتالمیت بعنوان یک یافتهی فرعی گزارش شد. در این مطالعه معیارهای تشخیصی تعیین (not specified) نشده بود، هیچیک از محققین مربوطه افتالمولوژیست نبوده و نقش افتالمولوژیستها در معاینه و آزمایش بیماران گزارش نشده است.
آسپرجیلوس
اندوفتالمیت آسپرجیلوسی معمولاً در بیماران مبتلا به آسپرجیلوزیس تهاجمی که ایمنی آنها سرکوب شده است اتفاق میافتد. این حالت در بیمارانی که سوء مصرف داروهای تزریق وریدی داشته و نیز در بیمارانی که داروهای کورتیکوستروئیدی دریافت میکنند دیده شده است و بندرت بعنوان یک عارضهی بعد از عمل جراحی چشم دیده میشود. همچنین یک طغیان بیمارستانی، اندوفتالمیت آسپرجیلوسی را به عملیات ساختمان سازی بیمارستانی مرتبط دانستهاند.
تظاهرات بالینی
شایع ترین علائم چشمی قرمزی، درد و کاهش دید یا تاری دید در چشم گرفتار شده میباشد. آزمایش چشم نوعاً احتقان و پرخونی (hyperemia) سطح چشمی و اتساع عروقی را نشان میدهد و آزمایش ته چشم (فوندوس) توسط افتالموسکوپ ارتشاح کوریورتینال را آشکار میسازد. این نواحی انفیلتره شده بصورت لزیونهای رنگ پریده یا کرمی رنگ در فوندوس چشم ظاهر میشوند. نواحی انفیلتره زمینهی قرمزی کوروئید و همچنین سطح عروقی شبکیه را تیره میکنند. بدلیل اینکه این نواحی ارتشاحی جزئیات ساختمانهای عروقی را تیره میکنند بوسیلهی شبکیهی غیر گرفتار اطراف با قرمزی طبیعی و معماری خاص خود بارزتر و مشخصتر خود را نشان میدهند.
آزمایش بیومیکروسکوپیک چشم ممکن است گلبولهای سفید و نیز روشنائی خیره کنندهی نامنظم در اتاق قدامی و همینطور سلولهای زجاجیه و ناصافی و تیرگی آن را آشکارا نشان دهد. روشنائی نامنظم و وجود گلبولهای سفید در آب نشانگر التهاب چشمی است. بطور مشابهی مهآلود بودن زجاجیه نشان دهندهی از دست دادن شفافیت و وضوح مربوط به پروتئین و دبریهای سلولی است. حضور تیرگی و وجود گلبولهای سفید در زجاجیه نشانگر التهاب یا عفونت در کوروئید یا شبکیه است.
تشخیص
تشخیص قطعی و نهائی (definitive) اندوفتالمیت عفونی بوسیلهی کشت مایعات زلالیه و زجاجیه میسر میشود. نمونهها در محیطهای مناسب کشت شده و رنگ آمیزی گرم نیز بعمل میآید. مایعات زلالیه را در بالین بیمار و یا در اتاق معاینه با استفاده از یک بیحس کنندهی موضعی و با کمک سوزن نمره 30 که از طریق کنارههای قرنیه بداخل اتاق قدامی عبور میدهند میتوان بدست آورد. در مقابل یک نمونهی مایع زجاجیه تنها هنگام انجام ویترکتومی میتواند تهیه شود که به اتاق عمل جراحی مجهز به میکروسکوپ و دستگاههای افتالمیک نیاز دارد. همچنین به تسکین (sedation) وریدی یا بیهوشی عمومی نیاز است.
ویترکتومی میتواند برای تشخیص مورد استفاده قرار گیرد، نمونههای زجاجیه برای رنگ آمیزی گرم و کشت مورد آزمایش قرار میگیرد و نیز میتواند اثر درمانی برای بیمار داشته باشد؛ به این طریق که بار میکروبی چشم را کاهش میدهد. علاوه بر این داروهای آنتیبیوتیک را میتوان بداخل حفرهی ویتروس به آهستــــــــــــگی وارد کرد (instilled). برای انتخاب عامل مناسب ضدمیکروبی از رنگ آمیزی گرم یا رنگ آمیزیهای قارچی میتوان کمک گرفت. در مورد علائم و نشانههای چشمی باید بیدرنگ نظر یک افتالموژیست را جویا شد. اگر آزمایش افتالمیک مطرح کنندهی اندوفتالمیت باشد ویترکتومی تشخیصی با کشت از مایع زجاجیه میتواند تشخیص را تأئید نماید.
درمان
تمام اشکال اندوفتالمیت پتانسیل تهدید بینائی را دارند، معهذا درمان فوری و مناسب شانس بازیابی بینائی را بهبود میبخشد.
کاندیدا
استفادهی موفقیت آمیز از تزریق آمفوتریسین B اولین بار در یک مورد اندوفتالمیت کاندیدائی در سال 1960 گزارش شد، هرچند که اثربخشی آن محدود بود كه علت آن نفوذ پذیری نسبتاً ضعیف این دارو به داخل زجاجیه است. یک دوز تزریقی کلی 750 الی 1000 میلیگرم برای حداکثر اثربخشی آن توصیه شده است. استعمال داخل زجاجیهای آمفوتریسین B (0.005mg/0.1ml) با یا بدون ویترکتومی پارس پلانا بصورت موفقیت آمیزی برای اندوفتالمیت کاندیدائی که بوسیلهی التهاب ویتره پیچیدهتر شده بکار رفته است. از دوز کلی 5 تا 10 میلیگرم بعنوان یک روش تک درمانی (monotherapy) یا همراه با آمفوتریسین B سیستمیک استفاده شده است، اگرچه استفادهی موفقیت آمیز از فلوسیتوزین بعنوان یگانه عامل در گزارشهای قدیمی وجود دارد.
اهمیت حضور غیرمنتظرهی کاندیداهای مقاوم به فلوسیتوزین منجر به استفاده از آن بعنوان بخشی از درمان ترکیبی با آمفوتریسین B شده است. برتری فلوکونازول به آمفوتریسین B برای اندوفتالمیت کاندیدائی هرگز ارزیابی نشده است، اما با توجه به سمیت آمفوتریسین B اکنون فلوکونازول بصورت تک درمانی برای اندوفتالمیت کاندیدائی حتی در حضور التهاب شدید زجاجیه پذیرفته شده است. Akler و همکاران از دوز پائین فلوکونازول در حدود 200 میلیگرم در روز بمدت 2 ماه استفاده کردهاند، اما دوزهای بالاتر (800 میلیگرم در روز) بصورت تزریق داخل وریدی برای شروع درمان توصیه میشود. دوزهای پائینتر یعنی 200 الی 400 میلیگرم در روز فلوکونازول خوراکی ممکن است بعنوان درمان کاهندهی تدریجی (stepdown) بدنبال آمفوتریسین B مورد استفاده قرار گیرد.
طول مدت مطلوب درمان معین نیست اما 2 تا الی 4 ماه بوده است. موارد اندوفتالمیت کاندیدائی اندوژنوس بصورت موفقیت آمیزی با ویترکتومی پارس پلانا و فلوکونازول درمان شده است و طول مدت درمان تنها 3 هفته بوده است. ممکن است در صورت داشتن عدسی برداشتن آن در فرآیند درمانی لازم باشد. در دو مورد شکست درمانی با فلوکونازول در اندوفتالمیت کاندیدائی وجود داشته که در آنها معالجه با آمفوتریسین B داخل زجاجیهای بدنبال استفادهی طولانی مدت از فلوکونازول خوراکی میسر شده است. در مدلهای حیوانی کتوکونازول و ایتراکونازول نفوذ داخل چشمی ضعیفتری نسبت به فلوکونازول از خود نشان دادهاند.
گزارشهای خوبی از موفقیت درمانی با کتوکونازول وجود دارد. سودمندی ایتراکونازول در اندوفتالمیت آزمایش نشده است. برخی مدارک تجربی مطرح کنندهی این مسئله هستند که ممکن است استفادهی همزمان کورتیکوستروئیدها با عوامل ضد قارچی بصورت داخل زجاجیهای سودمند باشد. اگرچه کورتیکوستروئیدها میتوانند التهاب چشمی را به حداقل برسانند ولي ممکن است زمینه را برای پیشرفت عفونت نیز مساعد نمایند، بنابراین تا زمانی که مطالعات مقایسهای سودمندی آن را نشان دهد نمیتوان استفادهی روتین از کورتیکوستروئیدها را توصیه کرد.
آسپرجیلوس
پیشآگهی اندوفتالمیت آسپرجیلوسی ضعیف است، با مروری در تاریخچه، تنها 10 بیمار با این عفونت بینائی خود را مجدداً بدست آوردهاند. همهی این 10 بیمار دارای سیستم ایمنی شایسته بوده و 5 نفر از آنها داروی تزریقی استفاده کرده بودند. در 9 بیمار از این تعداد ویترکتومی انجام شد و 8 نفر از آنها بصورت توأم با ویترکتومی، آمفوتریسین B داخل زجاجیهای نیز دریافت کرده بودند. دوز استفاده شده اغلب پنج هزارم میلیگرم و در یک گزارش 5 تا 10 میلیگرم بوده است.
استفادهی روزانهی زیر ملتحمهای از داروی آمفوتریسین B (به میزان 1 تا 2 میلیگرم) میتواند متعاقباً ادامه یابد. مصرف سیستمیک آمفوتریسین B بدلیل نفوذ ضعیف آن بداخل چشم چندان توصیه نمیشود، اگرچه در یک مورد یک بیمار با آمفوتریسین B داخل وریدی به تنهائی درمان شده است. کاربرد فلوسیتوزین خوراکی و فلوکونازول خوراکی همراه با درمان موضعی در گزارشهای قدیمی موفقیت آمیز بوده است و یک بیمار نیز با ترکیبی از آمفوتریسین B سیستمیک، ریفامپین و فلوسیتوزین معالجه شده است.
منابع مورد استفاده:
- Stephen A. Klotz., and others. “Fungal and Parasitic Infections of the Eye”. Clin Microbiol Rew. 2000 13(4): 662-85.
- Elias J Anaissie. “Clinical Mycology”. CHURCHILL LIVINGSTONE . 2009
https://medlabnews.ir/%d8%b9%d9%81%d9%88%d9%86%d8%aa%e2%80%8c%d9%87%d8%a7%db%8c-
%d9%88%db%8c%d8%b1%d9%88%d8%b3%db%8c-%da%86%d8%b4%d9%85/
https://www.healthline.com/health/eye-parasites
برای دانلود پی دی اف بر روی لینک زیر کلیک کنید
ورود / ثبت نام