سندرم روده تحریکپذیر
Irritable Bowel Syndrome


شاهین اسعدی (دانشجوی ژنتیک مولکولی)، مهسا جمالی (دانشجوی کارشناسی ارشد ژنتیک)، دکتر علی نظیرزاده (متخصص ژنتیک)، مینا نیکنیا (دانشجوی کارشناسی ارشد ژنتیک)، مریم صافی (دانشجوی کارشناسی ارشد ژنتیک)، رؤیا آزادخواه (دانشجوی کارشناسی ارشد ژنتیک)
نگارنده مسئول: شاهین اسعدی (Molecular Geneticist)
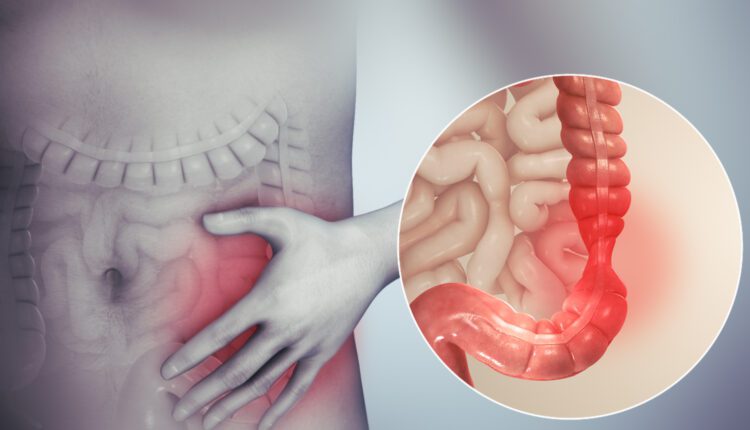
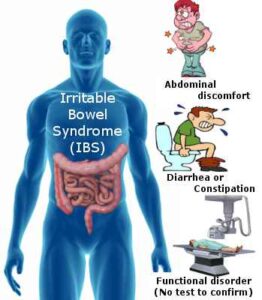
سندرم روده تحریکپذیر یکی از بیماریهای شایع گوارشی است که بخش قابلتوجهی از جامعه را درگیر میکند. این بیماری که با درد مزمن شکمی و تغییرات در اجابت مزاج همراه است، در زنان شایعتر از مردان بوده و ماهیتی مزمن دارد.
در این بیماری گرچه از نظر ارگانیک یافته خاصی وجود ندارد، اما دردهای مزمن شکمی، اسهال، یبوست یا نفخ، کیفیت زندگی در این بیماران را تحتتأثیر قرار میدهد؛ بهگونهای که غیبت از کار و کاهش کیفیت اجتماعی از عوارض مهم آن هستند.
در 90-80% این بیماران، مشکل روحی- روانی زمینهای از قبیل اضطراب، افسردگی، وسواس و … وجود دارد. جالبتوجه اینکه بسیاری از بیماران مبتلا، مراجعه پزشکی ندارند.
برخی علائم غیررودهای از قبیل سردرد، کمردرد، اختلال قاعدگی، سرگیجه، تهوع، خستگی، اختلال عملکرد جنسی و سوزش سر دل نیز در این بیماری وجود دارند که میتوانند بهموازات علائم رودهای، وجود داشته باشند.
علت این بیماری نامشخص است، ولی عواملی همچون استرس، حوادث دوران کودکی، عفونت قبلی رودهای و تغییرات نوروترانسمیتری مغز در این بیماران مطرح شده است.
تشخیص سندرم روده تحریکپذیر بایستی با احتیاط انجام شود و قبل از آن، بررسیهای اولیه در مورد وجود بیماریهای ارگانیک دستگاه گوارش انجام شود.
درمان سندرم روده تحریکپذیر مشکل است و درمانهای غیردارویی و دارویی متعددی برای آن پیشنهاد شده است، اما درمان بر پایه شکایت غالب و نیز پاسخ به درمان بیمار، میتواند متفاوت باشد.
سندرم روده تحریکپذیر (Irritable Bowel Syndrome) که اختصاراً IBS گفته میشود با درد مزمن شکمی و تغییرات در اجابت مزاج در غیاب هرگونه علت ارگانیک مشخص میشود. این بیماری از شایعترین بیماریهای گوارشی است که تشخیص داده میشود. شیوع IBS در آمریکای شمالی تقریباً 15-10% تخمین زده شده است. یک بررسی جمعیتی در اروپا رقم 11/5 % را نشان داده است که تقریباً مشابه شیوع IBS در آمریکاست. گرچه شیوع IBS در کشورهای مختلف، بسیار متفاوت گزارش شده است.
IBS هر دو جنس را درگیر میکند و میتواند در جوانی یا پیری بروز کند. در بیماران جوانتر و زنان، تشخیص IBS بیشتر صورت میگیرد. یک بررسی سیستماتیک، نسبت زنان به مردان مبتلا در آمریکای شمالی را دو به یک گزارش کرده است.
تنها 15% بیماران مبتلا به IBS مراجعه پزشکی دارند، از طرف دیگر ۲۵ تا 50% مراجعات به مطبهای گوارشی را بیماران IBS تشکیل میدهند. همچنین بیماران IBS تعداد قابلتوجهی از بیماران مراجعهکننده به مراکز مراقبتی اولیه را تشکیل میدهند. جالبتوجه اینکه IBS شایعترین علت غیبت از کار بعد از سرماخوردگی محسوب میشود. تخمین زیان سالیانه این بیماری در آمریکا ۳۰ میلیارد دلار است.
تظاهرات بالینی
بیماران مبتلا به IBS با طیف وسیعی از علائم گوارشی و غیرگوارشی مراجعه میکنند، هرچند مجموعه علائم درد مزمن شکمی و تغییرات اجابت مزاج شایعترین شکایات در این بیماران میباشد.
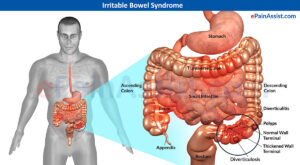
– درد مزمن شکمی: درد شکمی در بیماران IBS معمولاً بهصورت کولیکی با شدتهای مختلف و تشدید در زمانهای مختلف بروز میکند. درد شکمی معمولاً در قسمت تحتانی شکم و عمدتاً در سمت چپ احساس میشود، گرچه محل درد و مشخصات آن میتواند بسیار متغیر باشد.
شدت درد شکمی میتواند از یک درد خفیف تا یک درد شکمی ناتوانکننده متفاوت باشد.
فاکتورهای مختلفی از جمله استرسهای هیجانی و غذا خوردن میتوانند سبب تشدید درد شکمی شوند، درحالیکه اجابت مزاج سبب تخفیف درد شکمی میشود.
علیرغم متغیر بودن درد شکمی در بیماران مبتلا به IBS، برخی نمودهای بالینی درد شکمی با IBS همخوانی ندارند که در این مواقع بررسی سریع در مورد علل ارگانیک درد شکمی لازم است. این علائم عبارتند از: درد شکمی همراه با بیاشتهایی، سوءتغذیه و کاهش وزن. این مجموعه علائم در بیماران IBS بسیار نادر است، مگر اینکه یک بیماری یا اختلال روحی-روانی جدی وجود داشته باشد. درد شکمیای که حالت پیشرونده داشته باشد، بیمار را از خواب بیدار کند یا مانع به خواب رفتن بیمار شود از مشخصاتIBS نیست.
– تغییرات اجابت مزاج: بیماران مبتلا به IBS از تغییرات اجابت مزاج شاکی هستند ولی این تغییرات اجابت مزاج میتوانند در طیفی وسیعتری قرار گیرند، بنابراین بایستی شرححال دقیق در مورد حجم مدفوع، تعداد دفعات اجابت مزاج در روز و قوام مدفوع اخذ شود. در حالت نرمال، تعداد دفعات اجابت مزاج، متغیر است، بهعنوان مثال در یک مطالعه، 99% افراد سالم ۳ بار اجابت مزاج در روز تا ۳ بار اجابت مزاج در هفته را گزارش کردهاند. بیماران مبتلا به IBS از اسهال، یبوست، اسهال یا یبوست متناوب، حالت نرمال و اسهال متناوب و حالت نرمال و یبوست متناوب شاکی هستند.
– اسهال: اسهال معمولاً با دفع مدفوع شل با حجم کم تا متوسط مشخص میشود. اسهال معمولاً در ساعتهای بیداری روی میدهد و اغلب در صبحها یا بعد از غذا خوردن است. اغلب حملات اسهال با درد کولیکی قسمت تحتانی شکم شروع شده، میتواند حالت فوریتی و بیاختیاری داشته و با احساس دفع ناکامل پس از اجابت مزاج همراه باشد. تقریباً نیمی از بیماران مبتلا به IBS از وجود موکوس (بلغم: مایعی لزج و سفید رنگ است که حالتی سرد و مرطوب دارد) در مدفوع شاکی هستند.
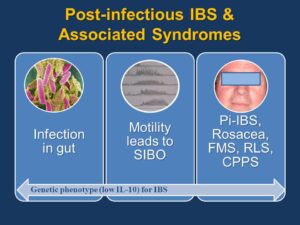
مدفوع با حجم زیاد، مدفوع خونی، اسهال شبانه و اسهال چرب در IBS وجود ندارند. وجود حالتهای ذکرشده، ضایعه ارگانیک را مطرح میکند. بخشی از بیماران، شروع علائم IBS را بعد از یک اسهال ویرال یا باکتریال حاد گزارش میکنند که به این حالت، IBSبعد از عفونت (Post Infectious IBS) گفته میشود.
– یبوست: یبوست ممکن است از چند روز تا چند ماه طول کشیده باشد و حالت تبدیل به نرمال یا تبدیل به اسهال را در پی داشته باشد. مدفوع اغلب خشک بوده و شکل گلولهای دارد. بیماران همچنین ممکن است درحالیکه رکتوم خالی است از احساس ناکافی بودن دفع مدفوع، شاکی باشند. یبوست در این بیماران میتواند سبب معطلی در توالت، زور زدن در هنگام دفع و استفاده نامناسب از ملینها و تنقیهها شود.
– سایر شکایات گوارشی: علائم گوارشی فوقانی از جمله ریفلاکس اسید از معده به مری، دیسفاژی، زودسیری، سوءهاضمه متناوب، تهوع و درد سینه غیرقلبی در بیماران مبتلا به IBS شایع هستند. بیماران مبتلا به IBS همچنین بهطور شایعی از نفخ، آروغ و دفع گاز رنج میبرند.
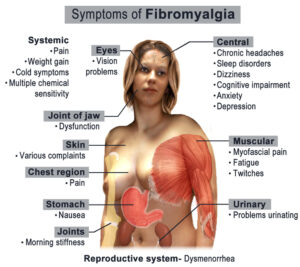
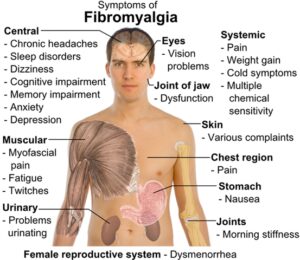
– شکایات غیر گوارشی: بیماران مبتلا به IBS، اغلب از علائم غیرگوارشی هم شاکی هستند. این موارد عبارتند از: اختلال عملکرد جنسی، قاعدگی دردناک، مقاربت دردناک و تکرر ادرار. همچنین بیماران مبتلا به IBS شانس بیشتری برای ابتلا به فشارخون، بیماریهای حساسیتی ریه و سندرمهای روماتولوژیک از جمله فیبرومیالژیا دارند.
معیارهای تشخیصی
در غیاب هرگونه مارکر بیولوژیک برای تشخیص IBS، تلاشهای زیادی برای استاندارد کردن معیارهای تشخیصی IBS براساس شکایات بالینی انجام شده است. این تلاش اولین بار در سال ۱۹۷۰ توسط Manning انجام شد. این شکایات شامل رفع درد شکمی بعد از اجابت مزاج، مدفوع شل و مکرر با شروع درد شکمی، دفع موکوس و احساس دفع ناکافی بودند. گزارش بعدی بر اساس استفاده از این شکایات در ۳۶۱ بیمار سرپایی بود که نهایتاً ۸۱ نفر از آنها IBS و ۱۰۱ نفر از آنها مبتلا به بیماری ارگانیک دستگاه گوارش بودند. ۱۴۵ نفر نیز در گروه کنترل قرار گرفتند. از نتایج مهم این مطالعه، بررسی حساسیت و اختصاصی بودن کرایتریاهای تشخیصی Manning برای افتراق IBS از افراد نرمال بود که به ترتیب 42% و 85% بدست آمد.
براساس مطالعه فوق، قابلیت پیشبینی کرایتریاهای تشخیصی Manning در سنهای بالا و نیز در مردان، کم بود و مطالعات بعدی نیز این مطالب را تأیید کردند. هرچند مطالعات متناقضی هم در این مورد منتشر شد. در مطالعه دیگری، کراتیریاهای تشخیصی Manning در مورد تشخیص IBS بر اساس جنسیت در هردو زیرگروه مرد و زن، کاربردی نداشت.
تلاش دیگری که برای استاندارد کردن معیارهای تشخیصی IBS انجام شد در سال ۱۹۹۲ بود که به نام معیارهای تشخیصی Rome معروف شد و سپس در سال ۱۹۹۹ و بعد از آن در سال ۲۰۰۵، مورد تجدیدنظر قرار گرفت. در معیارهای تشخیصی Rome ، IBS بهعنوان یک بیماری عملکردی یا اختلال رودهای مطرح گردید که با درد شکمی همراه با اختلالات دفع مشخص میشد. شکایات حمایتکننده (که البته جزو معیارهای تشخیصی Rome III نیستند) عبارتند از:
دفعات غیرطبیعی اجابت مزاج (کمتر از ۳ بار در هفته یا بیشتر از ۳ بار در روز)، شکل غیرطبیعی مدفوع (آبکی، تودهای، خشک یا شل)، زور زدن در هنگام دفع، احساس فوریت در دفع، احساس دفع ناکافی، دفع موکوس و وجود نفخ.
چهار زیرگروه IBS مشخص شده است:
اول، IBS یبوستی (مدفوع سفت یا تودهای در بیشتر از 25% موارد و مدفوع اسهالی در کمتر از 25% موارد).
دوم، IBS اسهالی (مدفوع اسهالی در بیشتر از 25% موارد و مدفوع خشک یا تودهای در کمتر از 25% موارد).
سوم، IBS مختلط (مدفوع خشک یا تودهای در بیشتر از 25% موارد و مدفوع اسهالی در بیشتر از 25% موارد).
چهارم، حالت غیرطبقهبندیشده که هیچکدام از موارد سهگانه فوق را در برنمیگیرد.
یکی از معایب معیارهای تشخیصی Rome، تأکید بیشازحد بر روی درد شکمی است، درحالیکه بر روی احساس دفع بعد از غذا خوردن، درد شکمی بعد از غذا خوردن یا اسهال بعد از غذا خوردن تأکید چندانی ندارد، به همین دلیل برخی محققین همچنان از معیارهای تشخیصی Manning یا استفاده از هر دو سیستم Manning و Rome استفاده میکنند. از معیارهای تشخیصی دیگر میتوان معیارهای تشخیصی Kruis را نام برد که البته استفاده از آن مرسوم نیست.
برخی مطالعات به ارزیابی دقت معیارهای تشخیصی Rome و Manning پرداختهاند. گرچه در این مطالعات، حساسیت و اختصاصی بودن این معیارهای تشخیصی بالا بوده است اما نتایج، متغیر بودهاند و همین موضوع احتمالاً سبب تغییراتی در این معیارها در آینده خواهد شد. علاوه بر این، ارزش پیشبینیکننده این معیارها بسته به میزان شیوع IBS و بیماریهای ارگانیک در جامعه موردمطالعه، متفاوت بوده است.
Rome-III معیارهای تشخیصی
درد یا ناراحتی شکمی عودکننده، حداقل سه بار در ماه، در سه ماه گذشته همراه با دو یا بیشتر از معیارهای زیر:
۱- بهبود درد شکمی با اجابت مزاج
۲- شروع درد شکمی با تغییر در دفعات اجابت مزاج
۳- شروع درد شکمی با تغییر در قوام مدفوع
– این معیارها بایستی حداقل در سه ماه اخیر تکمیل شده باشند و شکایات، حداقل از شش ماه قبل شروع شده باشند.
برخورد تشخیصی
برخی پزشکان بر روی موضوع رد کردن علل ارگانیک ایجادکننده شکایات تأکید بسیاری دارند، اما اکثر پزشکان به جهت پرهیز از اقدامات تشخیصی اضافی و هزینههای غیرضروری، دقت به علائم کلاسیک بیماری را برای تشخیص IBS کافی میدانند. اقدامات تشخیصی برای بررسی مسائل ارگانیک هنگامی ضرورت دارد که علائم هشداردهنده و یا یافتههای بالینی و آزمایشگاهی غیرطبیعی مانند آنمی و اختلالات الکترولیتی وجود داشته باشند.
اولین قدم تشخیصی در IBS، بررسی دقیق شکایات بیمار است. یکسری پرسشنامهها نیز در این مورد وجود دارند. یک شرححال دقیق، نقش غذا یا داروها را در ایجاد یا تشدید شکایات آشکار میسازد. لاکتوز، سوربیتول یا آنتیاسیدهای حاوی منیزیم میتوانند ایجاد اسهال کنند، درحالیکه مصرف داروهای آنتیکولینرژیک یا کلسیم بلوکرمی توانند ایجاد یبوست نمایند.
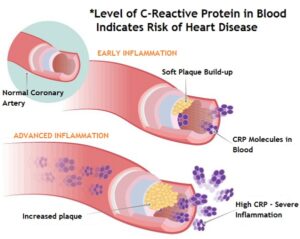
– اقدامات تشخیصی اولیه: انجام برخی تستهای تشخیصی برای بررسی شکایات بیماران IBS توصیه شده است، البته استفاده روتین از تستهای تشخیصی تخصصی در بیمارانی که علائم هشداردهنده ندارند توصیه نشده است. علیرغم این موضوع، برخی تستهای تشخیصی اولیه کاربرد دارند. در بیمارانی که براساس معیارهای تشخیصی Rome -III، IBS دارند، تستهای آزمایشگاهی محدودی جهت رد کردن علل ارگانیک ضرورت دارد. تستهای آزمایشگاهی روتین مانند شمارش سلولهای خونی (CBC) در بیماران IBS طبیعی است. تست CRP (C-Reactive Protein) نرمال، ردکننده بیماریهای التهابی است. در بیمارانی که از اسهال رنج میبرند، بررسی مدفوع از نظر وجود پارازیت الزامی است. در صورت شک به اسهال اسموتیک، ترشحی یا سوء جذبی، بررسیهای لازم در این مورد ضروری میباشد. با توجه به اینکه وزن مدفوع بیشتر از سیصد گرم در روز یا افزایش چربی مدفوع در بیماران IBS غیرمحتمل است، جمعآوری مدفوع ۲۴ ساعته، برخی اوقات کمککننده میباشد.
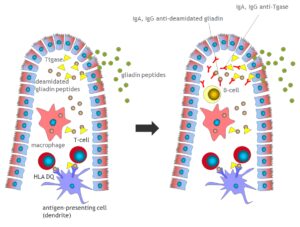
همچنین بررسی بیمار از نظر بیماری سلیاک (بررسی آنتیبادی IgA بر ضد ترانـــسگلوتامیناز بافتی( IgA-Anti tTG) توصیه میشود. سیگموئیدوسکوپی بهصورت روتین توصیه نمیشود و مقرونبهصرفه نیست، گرچه میتواند اضطراب وجود بیماری ارگانیک روده بزرگ را در بیمار مرتفع کند. گاهی اوقات نیز برای افتراق IBS از بیماریهای التهابی روده بزرگ، سیگموئیدوسکوپی الزامی میشود. انجمن گوارش آمریکا، انجام کولونوسکوپی را فقط برای بیماران بالای ۵۰ سال که علائم IBS دارند توصیه میکند که البته این توصیه در مورد بیماریابی سرطان کولون در تمامی افراد بالای ۵۰ سال است که شامل بیماران IBS هم میشود. بیوپسی کولون برای بیمارانی توصیه میشود که اسهال مقاوم و مداوم دارند تا کولیت لنفوستیک و کولیت کلاژنوز در آنها رد شود.
این بررسیهای تشخیصی محدود در 95% بیماران IBS، وجود مشکل ارگانیک را رد میکند. کمتر از 5% بیمارانی که به غلط تشخیص IBS داده میشوند در حقیقت بیماری ارگانیک دستگاه گوارش دارند، بنابراین در صورت نرمال بودن تستهای تشخیصی، شروع درمان علامتی در بیماران IBS توصیه میشود. البته بیماران باید ۳ تا ۶ هفته پس از شروع درمان از نظر پاسخ به درمان، بررسی مجدد شوند. ادامه شکایات بیمار علیرغم شروع درمان، نشاندهنده غلط بودن تشخیص نیست، هرچند بررسی تشخیصی وسیعتر در بیمارانی که شکایتهایشان پیشرفت مینماید الزامی است.
علاوه بر آن، به دلیل ارتباط مستقیم بین سوءاستفاده جنسی و فیزیکی و شکایات گوارشی در برخی بیماران مبتلا به IBS، بایستی در مورد این گونه سوءاستفادهها در گذشته، بسیار محتاط و ظریف از بیمار سؤال نمود. همچنین بایستی به مشکلات روانی که سبب تشدید بیماری فرد شده است (بهعنوان مثال مرگ نزدیکان یا …) توجه کافی داشت.
– سایر بررسیهای تشخیصی: درصورتیکه بیمار به درمانهای مرسوم IBS جواب ندهد انجام یکسری بررسیهای تشخیصی تکمیلی قابلقبول میباشد. ارزیابیهای تشخیصی تکمیلی، بستگی به شکایت غالب در این گروه از بیماران دارد. بیماران IBS که از یبوست مزمن رنج میبرند بررسی تشخیص یبوست مزمن را میطلبند و بیماران IBS با غلبه اسهال، نیاز به بررسیهای تشخیصی اسهال مزمن دارند.
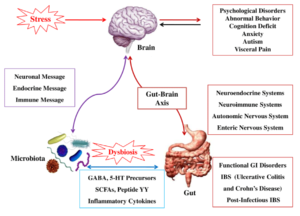
پاتوفیزیولوژی سندرم روده تحریکپذیر
پاتوفیزیولوژی IBS نامشخص است. فاکتورهای ارثی و غیرمحیطی میتوانند نقش ایفا کنند. برخی مطالعات، حرکات غیرطبیعی دستگاه گوارش، تحریکپذیری احشایی، اختلال عملکرد روانی و استرسهای هیجانی را در ایجاد IBS دخیل دانستهاند، اما علیرغم مطالعات وسیعی که در مورد علت ایجاد IBS انجام شده است، کماکان، نتایج متفاوت بوده و هیچ اختلال فیزیولوژیک یا روانی خاصی برای ایجاد IBS شناخته نشده است.
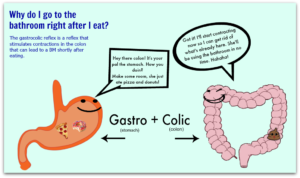
– حرکات دستگاه گوارش: شکایات موجود در IBS بهطور سنتی بر روی حرکات روده بزرگ (کولون) متمرکز شده است، اما در این میان یافتههای دیگری نیز بدست آمده است. در یک مطالعه، میزان انقباضات کولون، سه انقباض در دقیقه در کولون غیرتحریکشده در بیماران IBS بوده، درحالیکه در گروه کنترل، شش انقباض در دقیقه بوده است. مطالعات دیگری حاکی از افزایش انقباضات پایه روده بزرگ در بیماران IBS بوده است، اما این یافتهها در بیماران اضطرابی- روانی بدون علائم IBS نیز وجود داشته است. “پاسخ گاسترو کولونیک” (Gastro –Colonic Response) نسبت به مصرف غذا در بیماران IBS، تحریکپذیری طولانیتری در ناحیه رکتوسیگموئید نسبت به گروه کنترل داشته است. بررسی دیگری نشان داده است که استرس، خشم، تزریق وریدی کلهسیستوکینین و پرفیوژن کولون با د- اکسیکولیک اسید سبب افزایش فعالیت حرکتی کولون در بیماران IBS شده است، اما این نتایج در گروه کنترل نیز بدست آمده است. بدلیل ناهمگونی مطالعات و نیز نتایج بدست آمده، تابهحال هیچ الگوی خاصی از حرکات رودهای بهعنوان مشخصه IBS بدست نیامده است.
بهمثابه بررسیهای کولونی، نتایج در بررسیهای روده باریک نیز ناهمگون بوده است. کاهش دامنه و زمان کمپلکسهای حرکتی مهاجر (Migrating Motor Complex = MMC) و افزایش فرکانس انقباضات خوشهای در حالت ناشتا در روده باریک بیماران IBS دیده شده است. البته این یافتهها در بیماران بدون شکایات IBS نیز دیده شده است.
– افزایش حساسیت احشایی آوران: حسپذیری در دستگاه گوارش، از تحریک گیرندههای شیمیایی و مکانیکی مختلفی در دیواره روده ناشی میشود. این گیرندهها، سیگنالهای حرکتی گوارشی را از طریق راههای آوران به شاخ خلفی نخاع و نهایتاً به مغز ارسال میدارند. برخی مطالعات بر افزایش حساسیت احشایی انتخابی در برخی نورونهای سیستم گوارش بهعنوان یک مارکر بیولوژیک IBS تمرکز نمودهاند.
یافتههای قابل اهمیت: افزایش حساسیت پذیری کولون ناشی از فاکتورهای روانی، ایجاد درد و فوریت در دفع پس از اتساع بالون در رکتوم و افزایش فعالیت کورتکس مغز پس از اتساع رکتوم. بیماران IBS که از نفخ و گاز در رودهها شاکی هستند درواقع حجم گاز معادل افراد نرمال دارند.
مطالعات اخیر نشان داده است اختلال عملکرد رودهها در دفع گاز، با میزان کم چربی موجود در رودهها ارتباط دارد و به همین علت، بیماران مبتلا به IBS نسبت به مکانیسمهای تعدیلکننده ناشی از لیپیدها حساس هستند.
دریک سوم بیماران مبتلا به IBS (بخصوص بیماران با غلبه یبوست)، افزایش اندازه کمربند شکمی همراه با نفخ وجود دارد که به میزان حجم گاز موجود در رودههای آنها ارتباطی ندارد. علاوه بر این، برخی بیماران IBS تحمل کمتری در مقابل اتساع رکتوم توسط بالون دارند. گرچه افزایش حساسیت احتمالی بهنظر میرسد اختصاصی سیستم آوران احشایی باشد، اما برخی بیماران IBS، آستانه درد سوماتیک بالایی نیز دارند. تحریک مکرر سیگموئید سبب افزایش درد احشایی (Visceral Hyperalgesi) در رکتوم بیماران IBS میشود که در گروه کنترل اینگونه نیست. این یافتهها منجر به این نظریه شده است که انقباضات سیگموئید که در حالت عادی توسط استرس و غذا خوردن تشدید میشوند ممکن است در بیماران IBS سبب افزایش درد احشایی گذرا شود. افزایش درد احشایی در بیماران IBS محدود به کولون نمیشود و در سایر قسمتهای دستگاه گوارش نیز دیده میشود.
افزایش درد احشایی فقط در گروهی از بیماران IBS دیده میشود، بهعنوان مثال در یک بررسی انجامشده، بیماران IBS که مراجعه پزشکی نداشتهاند، افزایش درد احشایی را نشان نمیدهند. این یافتهها، ارتباط فاکتورهای روانی یا رفتار مزمن عدم مراجعه پزشکی را با میزان حساسیت اعصاب آوران احشایی نشان میدهد.
افزایش درد احشایی، مارکر بیولوژیک برای IBS نیست. افزایش درد احشایی همچنین در بیمارانی که فاقد شکایات گوارشی هستند ولی دچار سندرمهای دردناک هستند، دیده میشود. از جمله این موارد میتوان درد قفسه سینه ناشی از مری، درد قفسه سینه با شریان کرونر نرمال و فیبرومیالژیا را نام برد.
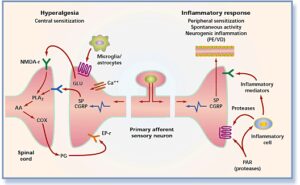
این موضوع که افزایش درد احشایی توسط سیستم عصبی دستگاه گوارش القاء میشود یا توسط سیستم عصبی مرکزی یا مجموعهای از هر دو سیستم، هنوز نامشخص است. در یک گزارش دیده شده است که اتساع رکتوم در افراد نرمال، سبب افزایش جریان خون ناحیه سینگولای کورتکس میشود، درحالیکه در بیماران IBS سبب افزایش خون ناحیه پرهفرونتال میگردد. مطالعات بعدی با MRI نشان دادند که پس از اتساع رکتوم، جریان خون مغزی در MRI بیماران IBS، توزیع نرمال داشته اما شدت جریان خون بیشتر بوده است. مجموعاً این یافتهها نشان میدهد که سیگنالهای آوران احشایی به سیستم عصبی مرکزی نقش مهمی دارند. مدیاتورهای مغزی که مطرح شدهاند عبارتند از: سروتونین، پپتید مرتبط با کالسیتونین، ماده P، برادیکینین، تاکیکینینها و نوروتروفینها. یک مطالعه انجامشده به نقش ان- متیل- دی- آسپارات (NMDA) در نورونهای شاخ خلفی نخاع میپردازد که سیگنالهای ارسالی از دستگاه گوارش را دریافت میکنند.
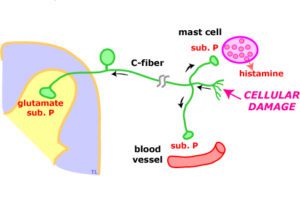
نکته: ماده P یک پپتید 11 اسیدآمینهای است. این ماده در نورونهای ویژهای در مغز بهویژه نورونهای حسی و در نورونهای شبکهای در دیواره دستگاه گوارش وجود دارد. دیواره دستگاه گوارش به میزان خیلی زیادی با نورونهایی عصبدهی میشوند که این نورونها یک شبکه عصبی را تشکیل میدهند.
شبکه داخلی دستگاه گوارش، فعالیتهای حرکتی و ترشحی دستگاه گوارش را کنترل میکند. در نورونهای رودهای، نوروپپتیدهایی مانند ماده P که در مغز و نخاع وجود دارد، دیده شده است.
ماده P در انتقال درد نقش داشته و اثر قوی روی عضلات صاف دارد.
ماده P احتمالاً نوروترنسمیتر سیناپسهای بین نورونهای حسی اولیه (جسم سلولی این نورونها در ریشه پشتی نخاع قرار دارد) با نورونهای واسطهای نخاعی در شاخ خلفی ستون نخاعی میباشد.
بنابراین این ماده مثالی از پپتیدهایی است که بهعنوان ترنسمیتر اصلی در سیناپسها عمل میکنند.
انکفالینها رهایش این ماده را در این سیناپسها کاهش میدهند و بنابراین مسیر احساس درد را در اولین سیناپس مهار میکنند. این ماده احتمالاً یکی از مهمترین عوامل در ایجاد پاسخهای التهابی است.
علاوه بر این، فرض شده است که فاکتورهای روانی، علت تمام یا بخشی از افزایش حساسیت به درد در بیماران IBS میباشند.
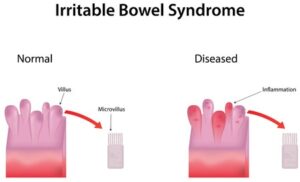
– التهاب میکروسکوپیک: بررسیهای دقیق ایمنوهیستولوژیک نشاندهنده فعال شدن سیستم ایمنی در گروهی از بیماران مبتلا به IBS است (بخصوص در بیماران IBSبا اسهال غالب). یافتههای مشابهی در بیمارانIBS بعد از عفونت (Post Infectious IBS) دیده شده است. در یک مطالعه انجام شده در ۱۰ بیمار مبتلا به IBS، افزایش انفیلتراسیون لنفوسیتها در شبکه میانتریک ژژونوم ۹ تن از آنها و دژنرسانس نورونی در ۶ تن از آنها دیده شده است. البته این یافتهها با توجه به اینکه بر روی تعداد کمی از بیماران IBS انجام شده، قابل تعمیم نیست. سایر مطالعات به فعال شدن ماستسلها در کولون برخی بیماران اشاره دارد.
– IBS بعد از عفونت: ایجاد IBS بعد از عفونتهای رودهای را Post Infectious IBS میگویند که در برخی بیماران دیده میشود. برخی مطالعات کنترلشده نشان دادهاند که 30-10% بیماران IBS پس از عفونتهای حاد باکتریال دچار IBS شدهاند. بررسی سیستماتیک بر روی مطالعات نشان میدهد که بروز IBS پس از عفونت، 10% است، درحالیکه در گروه کنترل 1% میباشد. بررسی سیستماتیک دیگری به نقش فاکتورهایی از قبیل سن پایین، تب طولانی، اضطراب و افسردگی در بروز IBS پس از عفونت پرداخته است.
در مورد ایجاد IBS پس از عفونت چندین تئوری فرض شده است؛ اولین تئوری در ارتباط با شدت گاستروانتریت اولیه است که هرچه شدت بیماری اولیه بیشتر باشد احتمال ایجاد IBS بیشتر است که این موضوع میتواند در ارتباط با شدت تهاجم ارگانیسمها به مخاط باشد. در عفونتهای شدید، گسیختگی اعصاب زیر مخاطی میتواند منجر به تحریکپذیری روده شود. تئوری دوم دلالت بر سوءجذب ایدیوپاتیک اسیدهای صفراوی دارد که ممکن است به کلستیرامین پاسخ دهد. تئوری سوم به افزایش سلولهای انترواندوکرین، لنفوسیتهای T و افزایش نفوذپذیری رودهای متعاقب گاستروانتریت کمپیلوباکتر میپردازد. در گزارش دیگری، این یافتهها بیش از یکسال ادامه یافته بود.
مطالعه دیگری نشان داد که کاهش سلولهای آنترواندوکرین و افسردگی، فاکتورهای پیشگوییکننده در ایجاد IBS پس از عفونت هستند. اسهال ایجادشده در بیمارانی که برای درمان گاستروانتریت، آنتیبیوتیک دریافت کرده بودند با تغییر فلور کولون همراه بوده است. برخی از این بیماران در حقیقت، بیماریهای مخفی التهابی روده داشتهاند یا پس از عفونت ویروسی، بیماری التهابی روده پیدا کرده بودند. از طرف دیگر کاهش دیساکاریدازهای رودهای متعاقب عفونت رودهای دیده شده است. نهایتاً اینکه بنظر میرسد در بررسیهای اپیدمیولوژیک در مورد IBS متعاقب گاستروانتریت، بروز IBS بیشازحد تخمین زده شده باشد، علاوه بر این فقط برخی مطالعات بروز IBS بعد از عفونت را گزارش کردهاند و همه مطالعات بر این یافته تأکید ننمودهاند.
– اختلال عملکرد روانی: برخی بیماران IBS که به مراکز فوق تخصصی، ارجاع میشوند از اضطراب، افسردگی، ترس مرضی (Phobia) و جسمیسازی (Somatization) رنج میبرند. این گروه از بیماران، بهندرت علائم کامل بیماری روانی موردنظر را دارند، علاوه بر این، آن گروه از بیماران IBS که مراجعه پزشکی ندارند، از نظر وجود مشکلات روانی، قابل افتراق از افراد سالم نیستند. البته باید در نظر داشت که مشکلات روانی، عمدتاً سبب تشدید علائم IBS میشوند تا ایجاد آن. بیماران دچار IBS احتمال بیشتری دارند که در گذشته دچار سوءاستفاده فیزیکی یا جسمی شده باشند و یا الگوی رفتاری یادگیری شدهای از دوران کودکی داشته باشند. در یک مطالعه دیده شده است که بیماران دچار IBS نسبت به افراد سالم، روانپریشی (Neuroticism) بیشتری را نشان میدهند. روانپریشی با سوءاستفاده فیزیکی یا جنسی در کودکی و بزرگسالی ارتباط دارد. محققین این تئوری را پیشنهاد کردهاند که همان روندی که سبب روانپریشی میشود سبب ایجاد IBS هم میشود.
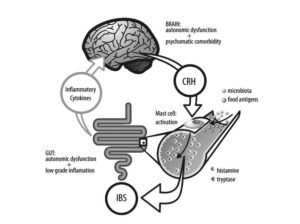
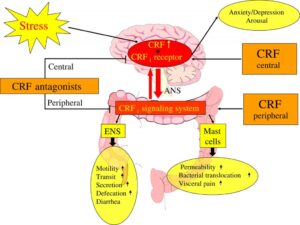
فرضیات دال بر نقش استرس و روانپریشی در IBS براساس نقش فاکتور آزادکننده کورتیکوتروپین (Corticotropin Releasing Factor=CRF) استوار شده است. CRF پیپتیدی است که از هسته پاراونتریکولر ترشح میشود و نقش آن در پاسخ به استرس به اثبات رسیده است. یافتههای اخیر بر این موضوع دلالت دارند که افزایش فعالیت CRF مغزی و گیرندههای CRF سبب اضطراب و افسردگی میشود. تزریق داخل وریدی CRF سبب افزایش درد شکمی و تحریکپذیری کولون در بیماران IBS میشود. همین یافته در مدلهای حیوانی نیز دیده شده است. از طرف دیگر دیده شده است درد شکمی و تحریکپذیری کولون با تجویز مهارکنندههای گیرندههای CRF برطرف میشود.
ارتباط بین رفتار یادگیری شده و ژنتیک در IBS در حال بررسی است. یک مطالعه نشان داده است که همشیبی (Concordance) IBS در دوقلوهای یکسان بیشتر از دوقلوهای غیریکسان است و اگر یکی از والدین، مبتلا به IBS باشد احتمال گرفتاری فرزندان بیشتر میشود.
– سایر مکانیسمهای احتمالی: برخی فاکتورها در تقلید یا تشدید علائم IBS مورد بررسی قرار گرفتهاند ولی هیچکدام از آنها بهعنوان عامل اساسی، تأیید نشدهاند. این فاکتورها عبارتند از: سوء جذب کربوهیدرات (مانند عدمتحمل لاکتوز یا فروکتوز)، سوء جذب اسیدهای صفراوی، پاسخ نوروهومورال یا نوروایمون، افزایش سطح اسیدهای چرب با زنجیره کوتاه در مدفوع، رشد بیشازحد باکتری در روده و افزایش غلظت سرین پروتئاز در روده.
درمان
– اصول کلی: IBS یک بیماری مزمن با نتیجه درمانی نامشخص است، بنابراین اساس درمان، تخفیف علامتی بیماری است. یک پرسش مهم در این میان، چگونگی کمک به بیمار است. فاکتورهای تشدیدکننده اخیر از قبیل داروها و غذا باید مدنظر باشند. همچنین باید به فاکتورهای استرسزا، موارد پنهانکاری یا بیماریهای روانپزشکی همراه دقت داشت.
– ارتباطات درمانی: اصل مهم درمان، نوع ارتباط پزشک– بیمار است. پزشک بایستی از قضاوت زودهنگام و انتظارات غیرواقعی دوری نموده و بیمار را در روند درمانی شریک نماید. بیمارانی که ارتباط مثبت با پزشک خود دارند نیاز کمتری به مراجعه در آینده خواهند داشت.
– آموزش بیمار: آموزش بیمار در مورد مکانیسم ایجاد بیماری و نحوه دخالتش در روند درمان، کمک شایانی به درمان مینماید. بیمار بایستی از ماهیت مزمن و درعینحال خوشخیم بیماری خودآگاه گردیده و به او اطمینان داده شود که به خاطر بیماری، زندگیاش در خطر نیست و عمر طبیعی خواهد داشت. براساس مطالعه انجام شده در مایو کلینیک، در طی پیگیری ۲۹ ساله ۱۱۲ بیمار مبتلا به IBS، فقط ۱۰ نفر بیماری ارگانیک دستگاه گوارش پیدا نمودند و بقای بیماران IBS مشابه بقای افراد سالم بود.
– اصلاح رژیم غذایی: شرححال دقیق میتواند غذاهای تشدیدکننده بیماری و نیز غذاهای ایجادکننده گاز در رودهها را شناسایی کند. در ابتدا بایستی بهطور آزمایشی، شیر از رژیم غذایی بیماران حذف شود. برخی بیماران که تشخیص IBS روی آنها گذاشته میشود در حقیقت کمبود لاکتاز و عدم تحمل به شیر دارند. چنین علائمی همچنین ممکن است در مصرف فروکتوز موجود در نوشابهها وجود داشته باشد که آنها را نسبت به مصرف فروکتوز حساس میکند. غذاهای گاززا (حبوبات، پیاز، کرفس، هویج، کشمش، موز، زردآلو، جوانهها، آرد گندم، چوبشور و نان بیگل) بایستی محدود شوند زیرا وجود گاز در رودهها سبب افزایش درد احشایی میشود. سودمندی حذف سایر غذاها ثابت نشده است زیرا احتمال دارد مسئله آلرژی غذایی یا عدمتحمل غذایی خاص مطرح باشد. شناسایی غذای آلرژیزا با بررسی سطح ایمنوگلوبولینها مطرح شده است اما به مطالعات بیشتری در مورد تأثیربخشی این روش نیاز میباشد. عموماً توصیه میشود بیماران IBS فیبر بیشتری چه بهصورت غذایی و چه بهصورت بستهبندی دارویی استفاده نمایند، گرچه برخی صاحبنظران بر این موضوع توافق ندارند و حداکثر ۱۲ گرم در روز فیبر (مانند سبوس گندم) را توصیه مینمایند.
مکانیسمهای احتمالی که در مورد اثر فیبر مطرح شدهاند عبارتند از: جذب آب مدفوع، ایجاد حالت لغزندگی مدفوع، افزایش حجم مدفوع و باند شدن به اسیدهای صفراوی، اما علیرغم مصرف گسترده فیبر برای تسکین شکایت بیماران IBS، یک مطالعه سیستماتیک که دربرگیرنده سیزده مطالعه میباشد نشان داده است که مصرف فیبر، ارزشمندی بیشتری نسبت به دارونما ندارد. از طرف دیگر، اثربخشی فیبر در آن گروه از بیماران IBS که از درد شکم و یبوست رنج میبرند را برخی مطالعات ثابت کردهاند. ترکیبات فیبر سنتتیک مانند پلیکربوفیل و متیل سلولز، حلالیت بیشتری نسبت به فیبرهای طبیعی مانند پسیلیوم دارند.
این موضوع که فیبرهای سنتتیک سبب نفخ کمتری در مقایسه با فیبرهای طبیعی میشوند بهصورت کامل مشخص نشده است. از طرف دیگر برخی بیماران بدلیل سوءهضم کولونی فیبر، دچار تشدید نفخ میشوند. بدلیل بیخطر بودن مصرف فیبر، یک دوره درمان با فیبر در تمام بیماران IBS بخصوص آنهایی که یبوست دارند، توصیه میشود. مقدار مصرف فیبر بایستی براساس پاسخ بیمار تنظیم شود. شروع فیبر به میزان نصف یا یک قاشق مرباخوری در روز، روش معقولانهای به نظر میرسد.
– درمانهای روانی- اجتماعی: درمانهای رفتاری، سبب افزایش توانایی بیمار در مقابله با استرس میشود هرچند اثر آنها تاکنون نامشخص مانده است.
هیپنوتیزم، بیوفیدبک و رواندرمانی، سبب کاهش اضطراب، تغییرات رفتاری مثبت، افزایش مسئولیتپذیری بیمار و افزایش درگیر شدن بیمار در روند درمانی خود و نتیجتاً کاهش درد در وی میشود.
یک بررسی سیستماتیک که شامل بیست و پنج مطالعه کنترلشده میباشد، نشان داده است که مداخلات رواندرمانی، ارجحیت بیشتری نسبت به درمانهای رایج دارد. مطالعه دیگری که به بررسی اثرات درمانی روشهایی مانند شناختدرمانی، رواندرمانی دینامیک و هیپنوتراپی پرداخته است نیز اثرات مفیدتر این روشها را نسبت به درمانهای مرسوم نشان داده است.
– درمان دارویی: درمان دارویی در IBS فقط یک درمان کمکی محسوب میشود. علاوه بر این انتخاب دارو برای هر بیمار بستگی به شکایت اصلی وی دارد، بنابراین بیمار مبتلا به IBS با اسهال غالب، درمان متفاوتی با بیمار مبتلا به IBS با یبوست غالب دارد.
توصیه ما بر اینست که از درمان طولانیمدت دارویی در بیماران IBS پرهیز شود زیرا این بیماری برای تمامی عمر وجود داشته و تأثیر درمانهای طولانیمدت، ثابت نشده است. مشکل اصلی در مورد تأثیربخشی درمان دارویی به مسائلی همچون ناهمگون بودن بیماران IBS، عدم وجود مارکر تشخیصی برای بیماری و پاسخ بسیاری از بیماران به دارونما برمیگردد.
– داروهای آنتیاسپاسمودیک: داروهای ضداسپاسم به میزان وسیعی در درمان IBS بکار میروند. برخی آنتیاسپاسمودیکها مانند هیوسین، سیمتروپیوم، پیناوریوم و روغن نعناع ممکن است اثرات درمانی کوتاهمدت داشته باشند، اما مصرف طولانیمدت آنها، تأثیر مثبتی نشان نداده است.
آنتیاسپاسمودیکها یا مستقیماً عضلات صاف رودهای را هدف قرار میدهند (مانند مبورین و پیناورین) یا با مکانیسم آنتیکولیزژیک یا آنتیموسکارینیک عمل مینمایند (مانند دیسیکلومین و هیوسین). مهار انتخابی عضلات صاف سیستم گوارش سبب کاهش فعالیت حرکتی کولون شده که این حالت میتواند در بیماران با شکایت درد شکمی بعد از غذا خوردن، گاز، نفخ و احساس فوریت دفع، کمککننده باشد.
یک متاآنالیز که شامل ۳۲ بررسی کنترلشده در مورد اثرات داروهای شلکننده عضلات صاف دستگاه گوارش بوده، نشان داده است که اثرات این داروها بسیار مؤثرتر از دارونما بوده است، اما یک متاآنالیز دیگر، اثرات ضعیفی از تأثیر این داروها را در دفع درد شکمی و سایر علائم نشان داده است. یک بررسی سیستماتیک دیگر، فقط اثرات این داروها را در کوتاهمدت به اثبات رسانده است. تجویز این داروها بایستی براساس نیاز بیمار و یا پیشگیری از اثر یک استرسور در ایجاد حمله باشد. دوز تیپیک این داروها در مورد دیسیکلومین ۲۰ میلیگرم چهار بار در روز از راه خوراکی یا در صورت نیاز و در مورد هیوسین 0/25 تا 0/125 میلیگرم بهصورت خوراکی یا زیرزبانی سه تا چهار بار در روز است. در مورد هیوسین آهسته رهش این دوز 0/75تا 0/375 میلیگرم بهصورت خوراکی هر دوازده ساعت است.
داروهای ضدافسردگی: داروهای ضدافسردگی میتوانند علاوه بر اثرات خود بر روی خلق با اثر تسکینی در IBS مؤثر باشند و بدین لحاظ در دردهای نوروپاتیک هم مؤثر هستند. مکانیسم احتمالی در مورد اثرات ضددرد ضدافسردگیهای سهحلقهای (TCAs) و احتمالاً مهارکنندههای انتخابی، بازجذب سروتونین (SSRIs)، تسهیل در آزادسازی اندورفینهای اندوژن، و مهار بازجذب نوراپینفرین است که منجر به تشدید عملکرد مهاری نورونهای پایینرونده و همچنین بلوک سروتونین میشود. داروهای ضدافسردگی سهحلقهای همچنین از طریق اثرات آنتیکولینرژیک سبب کاهش سرعت ترانزیت روده میشوند که این اثر میتواند سبب تسکین علائم در بیماران IBS با غلبه اسهال شود. یک متاآنالیز که شامل ۱۲ مطالعه کنترلشده در مورد مقایسه اثرات داروهای ضدافسردگی و دارونما بوده است، نشان میدهد که داروهای ضدافسردگی سهحلقهای سبب بهبود علائم در بیماران IBS شدهاند. مطالعه سیستماتیک بعدی نشان داد که داروهای ضدافسردگی سهحلقهای و داروهای مهارکننده انتخابی بازجذب سروتونین، اثرات بهبودی بیشتری (نسبت به دارونما) در بیماران IBS ایجاد کردهاند و سبب کاهش درد شکمی گردیدهاند. مطالعه کنترلشده بعدی نشان داد که آمیتریپتیلین نسبت به سایر داروهای این گروه اثرات درمانی بهتری در رفع علائم بیماران بزرگسال مبتلا به IBS داشته است.
بهبودی دردهای نوروپاتیک با ضدافسردگیهای سهحلقهای در دوزی کمتر از آن مقدار که برای درمان افسردگی به کار میرود، روی میدهد، بنابراین اگر داروی ضدافسردگی جهت درمان IBS استفاده شود باید با دوز پایین شروع گردیده و سپس دوز آن بر اساس پاسخدهی و یا تحمل بیمار، تنظیم گردد. با توجه به اینکه اثر ضدافسردگیها با تأخیر حدود چهارهفتهای شروع میشود، بنابراین در مورد افزایش دوز یا اطلاق عدم پاسخ به درمان، باید مدتی صبر نمود. نمونههایی از داروهای ضدافسردگی که در IBS کاربرد دارند عبارتند از: آمیتریپتیلین، ایمیپرامین، نورتریپتیلین و دزیپرامین (با دوز ۱۰ تا ۲۵ میلیگرم موقع خواب). دوز اولیه باید براساس پاسخ و تحمل بیمار تنظیم شود.
تجویز ضدافسردگیهای سهحلقهای در بیماران IBS مبتلا به یبوست بایستی با احتیاط باشد. پاروکسیتین و فلوکسیتین (۲۰ میلیگرم خوراکی روزانه)، سرترالین (۱۰۰ میلی گرم خوراکی روزانه) یا دیگر ضدافسردگیها در صورت وجود افسردگی همزمان مصرف میشوند. درحالیکه همه این داروهای بهصورت کلینیکی مصرف میشوند، تجربیات منتشرشده اندکی در مورد ضدافسردگیهایی مانند مهارکنندههای انتخابی بازجذب سروتونین (SSRIs) یا مهارکنندههای بازجذب سروتونین- اپینفرین (SNIRs) در دست است. نتایج چندین مطالعه در مورد این داروها بهخصوص مهارکنندههای انتخابی بازجذب سروتونین (SSRIs) متفاوت بوده است.
– داروهای ضد اسهال: در بیماران IBS با غلبه اسهال، گرچه مدفوع، اسهالی و متناوب میباشد ولی حجم کلی روزانه آن نرمال است. یک مرور سیستماتیک که شامل سه مطالعه کنترلشده میباشد تأثیر لوپرامید در درمان این بیماران را بررسی کرده است. همه این مطالعات کوتاهمدت بوده، تعداد اندکی بیمار را دربرگرفته و معیارهای استاندارد برای مشخص کردن بیماران را نداشتهاند. در مجموع تمام مطالعات نشان دادهاند که لوپرامید برای رفع اسهال در این بیماران مفید بوده اما برای سایر شکایات و نیز درد شکمی آنها مؤثر نبوده است. تجویز لوپرامید به روش (PRN) در صورت نیاز مؤثرتر بوده است و برای بیمارانی که اسهال بعد از غذا خوردن پیدا میکنند بهصورت مصرف قبل از غذا نیز، اثربخش بوده است.
از لوپرامید در بیماران IBS با غلبه یبوست نباید استفاده کرد و همچنین تجویز آن در بیمارانی که IBS متناوب اسهالی- یبوستی دارند بایستی با احتیاط باشد.
– بنزودیازپینها: داروهای ضداضطراب، مصرف محدودی در بیماران مبتلا به IBS دارند زیرا این داروها سبب وابستگی، تداخل دارویی و در صورت قطع، علائم ترک میشوند، علاوه بر این، بنزودیازپینها با تحریک گاماآمینوبوتیریک اسید (GABA) آستانه درد را پایین آورده و سبب کاهش سروتونین مغزی میشوند، بنابراین مصرف کوتاهمدت آنها (کمتر از دو هفته) برای مرحله حاد اضطراب که سبب ایجاد علائم در بیماران مبتلا به IBSشده است، مفید است.
– آنتاگونیستهای گیرنده ۳-هیدروکسی تریپتامین (سروتونین): آنتاگونیستهای گیرنده ۳-هیدروکسی تریپتامین مانند آلوسترون، سیلانسترون، اندانسترون و گرانیسترون سبب تعدیل فعالیت سیستم آوران احشایی از دستگاه گوارش شده و ممکن است سبب رفع درد شکمی شوند. یک متاآنالیز که شامل چهارده مطالعه کنترلشده تصادفی در مورد آلوسترون و سیلانسترون بوده است تأثیربخشی این داروها در بهبود کلی شکایات بیماران IBS و رفع درد شکمی آنها را ثابت کرده است.
آلوسترون از طریق اثر بر سیستم عصبی آوران احشایی و با تأثیر بر موتیلیتی و ترشح دستگاه گوارش، کاربرد مؤثری در بیماران IBS دارد. در مطالعات کلینیکی، این دارو عمدتاً در زنان مبتلا به IBS با غلبه اسهال مؤثر بوده است.
با توجه به عوارض جانبی آلوسترون از قبیل کولیت ایسکمیک و عوارض مرتبط با ایجاد یبوست، سازمان دارو و غذای آمریکا (FDA) این دارو را از داروخانهها جمعآوری کرده است. با توجه به نیاز برخی بیماران به این دارو، FDA مدتی بعد این دارو را با شرایط تجویز کنترلشدهای وارد داروخانهها نمود.
– آگونیستهای گیرنده ۴- هیدروکسی تریپتامین (سروتونین): آگونیستهای گیرنده ۴- هیدروکسی تریپتامین سبب تحریک آزادسازی نوروترانسمیترها و افزایش موتیلیتی کولون میشوند و بهمین دلیل در بیماران IBS با غلبه یبوست کاربرد دارند. داروی اول این گروه (تاگاسرود یا زلنورم) در ابتدا برای درمان بیماران IBS تأیید شد اما در مارس ۲۰۰۷ بدلیل ایجاد عوارض قلبی- عروقی از داروخانهها جمعآوری شد. این دارو سپس با شرایط تجویز کنترلشدهای مجدداً وارد بازار گردید.
– لوبیپروستون: لوبیپروستون دارویی است که بهطور موضعی بر روی کانالهای کلر تأثیر گذاشته و سبب افزایش ترشحات رودهای غنی از کلر میشود. این دارو، ابتدا برای درمان یبوست مزمن ایدیوپاتیک توسط FDA تأیید شد، اما بعداً برای استفاده در زنان بالای ۱۸ سال مبتلا به IBS با غلبه یبوست نیز تأیید گردید.
تأیید این دارو براساس دو مطالعه چندمرکزی بود که بر روی ۱۱۵۴ بیمار مبتلا به IBS با غلبه یبوست (که 92% آنها زن بودند) انجام گرفت. این بیماران تحت درمان با لوبیپروستون (۸ میکروگرم دو بار در روز) و دارونما برای ۱۲ هفته قرار گرفتند. بیمارانی که لوبیپروستون دریافت کرده بودند بهطور معناداری پاسخدهی بهتری داشتند (18% در مقابل 10% در گروه دارونما). عوارض جانبی شدید دارو مشابه با دارونما بود. شایعترین عارضه جانبی دارو، تهوع بود (8% در مقابل 4% در گروه دارونما). پیگیری ۵۲۲ تن از این بیماران نشان داد که بهبودی آنها تا ۵۲ هفته ادامه داشته است. دوز تأییدشده برای درمان IBS (۸ میکروگرم دو بار در روز) دوز پایینتری نسبت به دوز مصرفی در یبوست مزمن ایدیوپاتیک میباشد.
در مورد مقایسه اثر لوبیپروستون با سایر داروها، هیچ بررسی مقایسهای صورت نگرفته و بیضرری طولانیمدت آن ثابت نشده است، علاوه بر این با توجه به پاسخ بیماران به دارونما در برخی مطالعات و نیز طرح این موضوع که لوبیپروستون آیا واقعاً با اثر ترشحی سبب بهبود بیماران IBS میشود یا خیر، سبب این پیشنهاد شده است که لوبیپروستون فقط برای بیمارانی تجویز شود که به سایر درمانها پاسخ نداده باشند.
– آگونیستهای گوانیلات سیکلاز: لیناکلوتید یک آگونیست گوانیلات سیکلاز است که سبب افزایش ترشح رودهای و افزایش حرکات رودهای میشود. در فاز سه مطالعهای که ۴۲۰ بیمار IBS با غلبه یبوست در آن شرکت دارند، بهبودی در دفعات اجابت مزاج و شکایات کلی بیماران دیده شده است.
– آنتیبیوتیکها: گزارشهای پراکندهای در مورد اثربخشی آنتیبیوتیکها در برخی بیماران IBS منتشر شده است. آنتیبیوتیکها عمدتاً بر روی بیمارانی مؤثر بودهاند که دچار نفخ بودهاند اما بر روی سایر شکایات بیماران مانند درد شکمی و تغییرات اجابت مزاج مؤثر نبودهاند. مکانیسمهایی که سبب این تأثیر میشوند ناشناختهاند اما تصور میشود اثر عمده آنها در مهار باکتریهای تولیدکننده گاز باشد، البته این مطالعات نتوانستهاند این نظریه که رشد بیشازحد باکتری در روده باریک، مسبب شکایات بیماران IBS است را به اثبات رسانند.
علاوه بر این، مطالعه دیگری در مورد رشد بیشازحد باکتری در روده باریک با روش تست تنفسی لاکتولوز انجام شده است، اما این مطالعه نتوانسته است بین بیماران IBS و افراد سالم، تفاوت معناداری پیدا کند، بنابراین طرح موضوعاتی مانند رشد بیشازحد باکتری، فواید مصرف آنتیبیوتیک، و روشهای بررسی رشد بیشازحد باکتری نیازمند بررسیهای تکمیلی است.
– درمانهای جایگزین: برخی درمانهای جایگزین از قبیل گیاهان دارویی، پروبیوتیکها، طب سوزنی و مکملهای آنزیمی در درمان بیماران IBS مطرح گردیدهاند اما این درمانها تابحال، نامطمئن بودهاند.
راهنماهای عمده درمانی (Guide lines)
راهنماهای اداره بیماران مبتلا به IBS بهوسیله انجمنها و سازمانهای متعددی از جمله انجمن گاستروانترولوژی امریکا پیشنهاد شده است.
مسیرهای درمانی سندرم روده تحریکپذیر
درمان بیماران IBS براساس شدت بیماری و نیز شکایت اصلی بیمار، متفاوت است:
– شکایات خفیف: بیماران با علائم خفیف و گهگاه، معمولاً اختلال عملکردی یا روانی عمدهای ندارند، بنابراین توصیه مناسب در مورد این گروه از بیماران، ارتباط مناسب پزشک– بیمار، آموزش، اطمینانبخشی، رعایت رژیم غذایی و استفاده از فیبر (درصورتیکه از نفخ شاکی نباشند) میباشد و درمان دارویی در این گروه از بیماران توصیه نمیشود.
– شکایات متوسط: این گروه از بیماران علاوه بر اینکه به دلیل شدت شکایاتشان دچار اختلال عملکرد در فعالیتهای روزانهشان میباشند، ممکن است از مشکلات روانی نیز در رنج باشند. توصیه میشود شکایات این بیماران و فاکتورهای تشدیدکننده آن از قبیل عدم تحمل شیر، مصرف کافئین و استرسورهای خاص بمدت چند هفته تحتنظر باشند. اصلاح رژیم غذایی، تغییرات رفتاری و رواندرمانی ممکن است در این بیماران مفید باشد.
در مورد این گروه از بیماران، مطالعات تصادفی نشان داده است که دارودرمانی مؤثرتر از تجویز دارونما است. گرچه مطالعات دیگری به این نکته تأکید دارند که درمانهای غیردارویی مانند فیبر هم میتواند در کنار دارودرمانی مؤثر باشند توصیه مناسب در این گروه از بیماران، دارودرمانی به جهت کنترل علائم بیماران است، مضافاً بر اینکه داروهایی مانند ضدافسردگیها باید ماهها یا سالها ادامه یابند. انتخاب دارویی مناسب در این گروه از بیماران براساس شکایت غالب و نیز پاسخ آنها به درمان است.
– شکایات شدید: بخش کوچکی از بیماران IBSدچار علائم شدید و غیر بهبود یابنده میباشند که اغلب همراه با مشکلات عمده روانی و مراجعات مکرر است. توصیه مناسب در این گروه از بیماران استفاده از رفتاردرمانی و داروهای روانپزشکی است.
References:
- Hulisz D (2004). “The burden of illness of irritable bowel syndrome: current challenges and hope for the future”. J Manag Care Pharm. 10 (4): 299–309.
- Whitehead WE، Palsson O، Jones KR; Palsson; Jones (2002). “Systematic review of the comorbidity of irritable bowel syndrome with other disorders: what are the causes and implications?”. Gastroenterology. 122 (4): 1140–56.
- Spiller R، Garsed K; Garsed (May 2009). “Postinfectious irritable bowel syndrome”. Gastroenterology. 136 (6): 1979–88.
- Moayyedi، P; Quigley، EM; Lacy، BE; Lembo، AJ; Saito، YA; Schiller، LR; Soffer، EE; Spiegel، BM; Ford، AC (September 2014). “The effect of fiber supplementation on irritable bowel syndrome: a systematic review and meta-analysis.”. The American journal of gastroenterology. 109 (9): 1367–74.
- Maxion-Bergemann S، Thielecke F، Abel F، Bergemann R; Thielecke; Abel; Bergemann (2006). “Costs of irritable bowel syndrome in the UK and US”. PharmacoEconomics. 24 (1): 21–37.
- Schmulson MW، Chang L; Chang (1999). “Diagnostic approach to the patient with irritable bowel syndrome”. Am. J. Med. 107 (5A): 20S–26S.
- Tamparo، Carol (2011). Fifth Edition: Diseases of the Human Body. Philadelphia، PA: F.A. Davis Company. p. 407.
- Ohman L، Simrén M; Simrén (2010). “Pathogenesis of IBS: Role of inflammation، immunity and neuroimmune interactions”. Nature Reviews Gastroenterology & Hepatology. 7 (3): 163–73.
- Shanahan F، Quigley EM; Quigley (May 2014). “Manipulation of the microbiota for treatment of IBS and IBD-challenges and controversies”. Gastroenterology. 146 (6): 1554–63.
- Fukudo S، Nomura T، Muranaka M، Taguchi F; Nomura; Muranaka; Taguchi (1993). “Brain-gut response to stress and cholinergic stimulation in irritable bowel syndrome. A preliminary study”. J. Clin. Gastroenterol. 17 (2): 133–41.
- Barreau F، Ferrier L، Fioramonti J، Bueno L; Ferrier; Fioramonti; Bueno (September 2007). “New Insights in the Etiology and Pathophysiology of Irritable Bowel Syndrome: Contribution of Neonatal Stress Models”. Pediatric Research. 62 (3): 240–245.
- Spiller، R; Aziz، Q; Creed، F; Emmanuel، A; Houghton، L; Hungin، P; Jones، R; Kumar، D; Rubin، G; Trudgill، N; Whorwell، P (1 December 2007). “Guidelines on the irritable bowel syndrome: mechanisms and practical management”. Gut. 56 (12): 1770–1798.
- Fukudo، Shin (19 January 2007). “Role of corticotropin-releasing hormone in irritable bowel syndrome and intestinal inflammation”. Journal of Gastroenterology. 42 (S17): 48–51.
- Ghoshal، UC.; Srivastava، D. (Mar 2014). “Irritable bowel syndrome and small intestinal bacterial overgrowth: meaningful association or unnecessary hype.”. World J Gastroenterol. 20 (10): 2482–91.
- Collins، SM (August 2014). “A role for the gut microbiota in IBS.”. Nature reviews. Gastroenterology & hepatology. 11 (8): 497–505.
- Santelmann، H; Howard، JM (January 2005). “Yeast metabolic products، yeast antigens and yeasts as possible triggers for irritable bowel syndrome.”. European journal of gastroenterology & hepatology. 17 (1): 21–6.
- Amin OM (2002). “Seasonal prevalence of intestinal parasites in the United States during 2000”. Am. J. Trop. Med. Hyg. 66 (6): 799–803.
- Stark D، van Hal S، Marriott D، Ellis J، Harkness J; Van Hal; Marriott; Ellis; Harkness (2007). “Irritable bowel syndrome: a review on the role of intestinal protozoa and the importance of their detection and diagnosis”. Int. J. Parasitol. 37 (1): 11–20.
- Yakoob J، Jafri W، Jafri N، Khan R، Islam M، Beg MA، Zaman V; Jafri; Jafri; Khan; Islam; Beg; Zaman (2004). “Irritable bowel syndrome: in search of an etiology: role of Blastocystis hominis”. Am. J. Trop. Med. Hyg. 70 (4): 383–5.
- Giacometti A، Cirioni O، Fiorentini A، Fortuna M، Scalise G; Cirioni; Fiorentini; Fortuna; Scalise (1999). “Irritable bowel syndrome in patients with Blastocystis hominis infection”. Eur. J. Clin. Microbiol. Infect. Dis. 18 (6): 436–9.
- Cremon C، Carini G، De Giorgio R، Stanghellini V، Corinaldesi R، Barbara G; Carini; De Giorgio; Stanghellini; Corinaldesi; Barbara (May 2010). “Intestinal dysbiosis in irritable bowel syndrome: etiological factor or epiphenomenon?”. Expert Rev. Mol. Diagn. 10 (4): 389–93.
- Su YC، Wang WM، Wang SY، Lu SN، Chen LT، Wu DC، Chen CY، Jan CM، Horowitz M; Wang; Wang; Lu; Chen; Wu; Chen; Jan; Horowitz (August 2000). “The association between Helicobacter pylori infection and functional dyspepsia in patients with irritable bowel syndrome”. Am. J. Gastroenterol. 95 (8): 1900–5.
- Gerards C، Leodolter A، Glasbrenner B، Malfertheiner P; Leodolter; Glasbrenner; Malfertheiner (2001). “H. pylori infection and visceral hypersensitivity in patients with irritable bowel syndrome”. Dig Dis. 19 (2): 170–3.
- Vernia P، Ricciardi MR، Frandina C، Bilotta T، Frieri G; Ricciardi; Frandina; Bilotta; Frieri (1995). “Lactose malabsorption and irritable bowel syndrome. Effect of a long-term lactose-free diet”. The Italian journal of gastroenterology. 27 (3): 117–21.
- Brandt LJ، Chey WD، Foxx-Orenstein AE، Schiller LR، Schoenfeld PS، Spiegel BM، Talley NJ، Quigley EM; Brandt; Chey; Foxx-Orenstein; Schiller; Schoenfeld; Spiegel; Talley; Quigley (January 2009).
- Simrén M، Axelsson J، Gillberg R، Abrahamsson H، Svedlund J، Björnsson ES; Axelsson; Gillberg; Abrahamsson; Svedlund; Björnsson (2002). “Quality of life in inflammatory bowel disease in remission: the impact of IBS-like symptoms and associated psychological factors”. Am. J. Gastroenterol. 97 (2): 389–96.
- Minderhoud IM، Oldenburg B، Wismeijer JA، van Berge Henegouwen GP، Smout AJ; Oldenburg; Wismeijer; Van Berge Henegouwen; Smout (2004). “IBS-like symptoms in patients with inflammatory bowel disease in remission; relationships with quality of life and coping behavior”. Dig. Dis. Sci. 49 (3): 469–74.
- García Rodríguez LA، Ruigómez A، Wallander MA، Johansson S، Olbe L; Ruigómez; Wallander; Johansson; Olbe (2000). “Detection of colorectal tumor and inflammatory bowel disease during follow-up of patients with initial diagnosis of irritable bowel syndrome”. Scand. J. Gastroenterol. 35 (3): 306–11.
- Corazziari E، Attili AF، Angeletti C، De Santis A; Attili، AF; Angeletti، C; De Santis، A (2008). “Gallstones، cholecystectomy and irritable bowel syndrome (IBS) MICOL population-based study”. Dig Liver Dis. 40 (12): 944–50.
- Tietjen GE، Bushnell CD، Herial NA، Utley C، White L، Hafeez F; Bushnell; Herial; Utley; White; Hafeez (2007). “Endometriosis is associated with prevalence of comorbid conditions in migraine”. Headache. 47 (7): 1069–78.
مروری بر درمان تکیاختهای رودهای
برای دانلود پی دی اف بر روی لینک زیر کلیک کنید
ورود / ثبت نام