مروری بر تومورمارکرها
دکتر سیدمهدی زرگریان
نقش تومورمارکرها طی دهه اخیر در انکولوژی بالینی شدیداً افزایش یافته است. با پیشرفت تکنولوژی و افزایش دانش ما در خصوص بدن انسان و روند بیماریها این نقش پررنگتر شده است. تومورمارکرها نقش گستردهای در غربالگری، انتخاب روش درمان و ارزیابی پیشآگهی و نیز پایش درمان سرطان ایفا میکنند. از میان تعداد بیشمار تومورمارکرهای شناختهشده، تعداد معدودی از آنها کاربرد روتین بالینی یافتهاند و از آن میان هم فقط چند مورد دارای دستورالعمل مورد اجماع جهت استفاده در مورد بیماران هستند. در این مقاله به موارد استفاده از تومورمارکرها، طبقهبندی، برخی تومورمارکرهای متداول و نیز اصول کلی استفاده بهینه از آنها خواهیم پرداخت.
مقدمه
تومورمارکرها مولکولهایی هستند که فراتر از غلظت طبیعی در بافت، سرم، ادرار یا سایر مایعات بدن فرد مبتلا به سرطان یافت میشوند. از این مولکولها میتوان در غربالگری، ارزیابی پیشآگهی، انتخاب درمان و پایش روند درمان بیماران سرطانی استفاده کرد. در شرایط بالینی صحیح، استفاده از این مارکرها میتواند به درمان سرطان کمک کند اما باید محدودیتهای استفاده از آنها هم مورد توجه واقع گردد.
تومورمارکر ایدهآل
گرچه ویژگیهای یک تومورمارکر ایدهآل تاحدودی به طبقهبندی و کاربرد آنها بستگی دارد، معالوصف ویژگیهای عمومی چنین مارکری میتواند به شرح ذیل باشد:
- بهطور خاص توسط بافت سرطانی یا پیشسرطانی در مراحل اولیه ایجاد بیماری تولید گردد.
- در تمام بیماران مبتلا به یک سرطان خاص در حدی که قابل تشخیص باشد، تولید شود.
- مختص به عضو خاصی باشد.
- بهراحتی قابل دسترس از طریق مایعات بدن باشد و یا اینکه در بافتهایی باشد که دسترسی به آنها به سهولت انجام شود و نیاز به نمونهگیری تهاجمی نباشد.
- میزان آن از لحاظ کمی متناسب با اندازه تومور، رفتار بیولوژیک تومور یا پیشرفت بیماری باشد.
- نیمهعمر نسبتاً کوتاهی داشته باشد تا بر اساس آن بتوان رشد تومور یا پاسخ به درمان را مشخص نمود.
- برای سنجش آن روشهای استاندارد، تکرارپذیر و معتبر وجود داشته باشد.
موارد استفاده از تومورمارکرها
- غربالگری سرطان در مراحل اولیه
- کمک به تشخیص سرطان
- پیشگویی کارآیی درمان؛ به عنوان مثال مارکرهای بافتی نظیر گیرندههای استروژن و HER-2
(human epidermal groth factor receptor-2) پاسخ به درمان هورمونی و trastuzumab را پیشگویی میکنند. - پایش درمان در سرطانهای پیشرفته
- برآورد پیشآگهی سرطان
- پایش بعد از جراحی تومور و شناسایی عود بیماری
محدودیتهای تومورمارکرها
- تومورمارکرها فاقد ویژگی کافی برای تشخیص بدخیمی هستند و نمیتوان آنها را جایگزین تشخیص هیستوپاتولوژیک (بیوپسی) کرد.
- موارد مثبت کاذب آنها منجر به اضطراب بیهوده و آزمایشهای غیرضروری متعاقب آن میگردد.
- موارد منفی کاذب آنها منجر به آسودگی خیال کاذب، تأخیر در تشخیص و پیشرفت بدخیمی میشود.
- ممکن است در شرایط خوشخیم هم افزایش داشته باشند.
- پیامدهای مالی و اقتصادی دارند.
طبقهبندی تومورمارکرها
تومورمارکرها را میتوان بر اساس نوع بافت به شرح ذیل طبقهبندی نمود:
الف- مارکرهای اپیتلیال
- مارکرهای سطحی سلول – Histocompatibility
- مارکرهای داخل سلولی – سیتوکاینها
- مارکرهای غشاء پایه – کلاژن نوع 4
- مارکرهای ماتریکس – Tenascin
- آنتیژن غشایی – آنتیژنهای گروه خون
ب- مارکرهای بافت پیوندی
- پروتئینهای فیلامان اینترمدیت – Desmin
- سایر پروتئینهای فیلامان – Laminin
- آنزیمهای سلولی – آمیلاز، لیزوزیم
- پروتئینهای غیرفیلامانی – غیرآنزیمی سیتوپلاسم – میوگلوبین، پروتئین S100
- آنتیژن غشایی – آنتیژن اختصاصی لکوسیت
ج- مارکرهای غدد بزاقی
- مارکرهای اپیتلیال – سیتوکراتینها
- مارکرهای سلولی میواپیتلیال – اکتین، میوزین
- مارکرهای سرمی سلول آسینار- آمیلاز بزاقی
- سلولهای میواپیتلیال + سلولهای آسینار – پروتئین S100
طبقهبندی تومورمارکرها بر اساس عملکرد
تومورمارکرها را میتوان بر اساس عملکرد آنها به شرح ذیل طبقهبندی نمود:
مارکرهای تشخیصی: این مارکرها در تشخیص بیماری و با آزمایش نمونه بیمار (سرم، مایعات بدن، بافتها و …) مفید هستند. تشخیص کروموزوم فیلادلفیا در لوسمی میلوژن مزمن از طریق تکنیک FISH مثالی برای این نوع مارکرها است.
مارکرهای پیشآگهی: مارکرهای پیشآگهی در برآورد سرانجام بیماری مستقل از اقدامات درمانی مفید هستند. موتاسیون P53 مثالی از مارکرهای پیشآگهی است که مرتبط با تهاجم بیماری و پیشآگهی ضعیف است.
مارکرهای پیشبینیکننده: این مارکرها پاسخ تومور را به نوع خاصی از درمان پیشبینی میکنند و لذا در طراحی فرآیند درمان کارآیی دارند؛ به عنوان مثال در سرطان سینه کسانی که HER2 مثبت هستند به درمان با trastuzumab پاسخ بهتری میدهند.
تومورمارکرهای تشخیصی Companion: این تومورمارکر ممکن است تشخیصی، پیشآگهی یا پیشبینیکننده باشد ولی برای شناسایی زیرگروهی از بیماران بهکار میروند که نوع خاصی از درمان برای آنها مفید است (موتاسیون V600E BRAF در ملانوما).
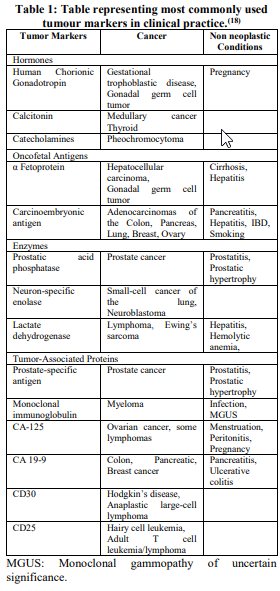
تومورمارکرهای متعددی با کارآیی تشخیصی، پیشآگهی و پیشبینی بهطور روزمره برای بیماریهای نئوپلاستیک بهکار میروند. متداولترین این مارکرها در جدول یک نشان داده شدهاند.
مبنای مولکولی تومورمارکرها:
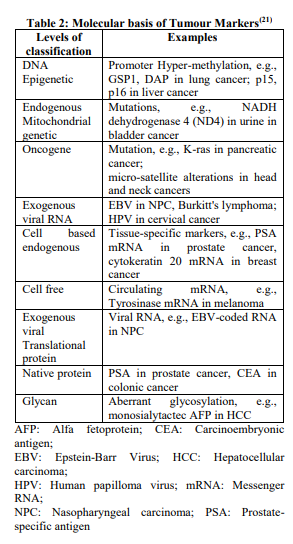
تغییرات ژنتیکی در سلول تومورال بهطور مستقیم یا غیرمستقیم الگوی بیان ژن را در سلول تومورال یا بافتهای اطراف آن تغییر میدهد. این تغییرات ژنتیکی به صور مختلف مشاهده میشوند (جدول 2)، که از جمله آنها اختلالاتی همچون موتاسیون، حذف ژن و ادغام ژن در ژنوم ویروس است که نهایتاً اساس مولکولی تومورمارکرها را تشکیل میدهند.
روشهای شناسایی تومورمارکرها:
روشهای متعددی جهت شناسایی تومورمارکرها وجود دارند که از بین آنها روشهای سرولوژیک سنجش آنزیمی متداولتر هستند. روشهایی چون ایمونوهیستوشیمی (IHC)، رادیوایمونواسی (RIA) یا الیزا (ELISA) هم برای شناسایی تومورمارکرها بهکار میروند. مبنای شناسایی ایمونولوژیک، اتصال اختصاصی آنتیبادی منوکلونال به اپیتوپهای تومورمارکر است که پس از آن در روش IHC به کمک رنگ، در RIA بهوسیله ماده نشاندار رادیواکتیو و در روش ELISA بهوسیله آنزیم، آشکارسازی میگردد. از فلوسیتومتری هم برای آنالیز حضور و درصد سلولهای نشاندارشده با آنتیبادی در یک سوسپانسیون استفاده میشود.
روشهای پیشگفت بسیار حساس بوده و در برآورد نیمهکمی یا کمی تومورمارکرها مفید هستند. روش ایمونوهیستوشیمی ((IHC متداولترین روش شناسایی تومورمارکرها در حال حاضر است. از IHC در انکولوژی جهت طبقهبندی تومورهای تمایزنیافته، لوسمی و لنفوم و نیز تعیین منشأ تومورهای متاستاتیک و همچنین شناسایی مولکولهای پروگنوستیک یا تراپوتیک استفاده میشود.
منشأ تومورمارکرها:
تومورمارکرها را میتوان در بافت (بافت توپر، غدد لنفاوی، مغز استخوان) و یا مایعات بدن همچون مایع آسیت یا پلور و یا سرم شناسایی نمود.
تومورمارکرهای بافتی برای پاتولوژیستها حائز اهمیت بیشتری هستند ولی تومورمارکرهای سرولوژیک توسط پزشکان بالینی بیشتر مورد استفاده واقع میشوند.
تومورمارکرهای اختصاصی در نئوپلاسمهای دهان
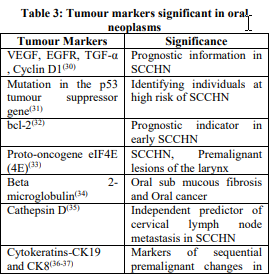
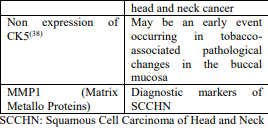
گرچه به لحاظ تئوریک تومورمارکرهای متعددی به نظر جالب میآیند، ولی هیچکدام از آنها ویژگی و حساسیت لازم جهت غربالگری انبوه در جمعیت کمریسک را ندارند. برخی از این تومورمارکرها و اهمیت آنها درنئوپلاسمهای دهانی در جدول 3 آمدهاند.
بیومارکرهای بزاقی
با روشهای جدید شناسایی مقادیر کم اجزای بزاق همچون پروتئینها و mRNA، تقریباً هر چیزی که در سرم قابل اندازهگیری باشد را در بزاق هم میتوان اندازه گرفت، لذا بزاق را میتوان همچون جریان خون در داخل حفره دهانی تصور کرد. نوسان در مقادیر پروتئینها و mRNAهای خاص در سرطانهای مختلف از جمله سرطانهای حفره دهانی مشاهده شده است، لذا میتوان تصور کرد که از این تغییرات بتوان در شناسایی و پایش سرطان استفاده نمود. تومورمارکرهایی همچون CA 15-3، HER2/neu و CA125 در بزاق یافت میشوند.
در موارد سرطان سینه، HER2/neu اولین بیومارکری است که در بزاق گزارش شد. مقدار CA 15-3، HER2/neu افزایش یافته و مقدار P53 کاهش مییابد. افزایش مقدار CA125بزاق در سرطان تخمدان قابل توجه است.
از بزاق میتوان در شناسایی سرطانهای دهان نیز استفاده کرد. ژن P53 در DNA بزاق بیماران مبتلا به سرطان دهان جهش مییابد. IL-8،SAT ،IL-1B ،OAZ1 ، H3F3A، DUSP و S100 از جمله RNAهای مرتبط با کارسینوم سنگفرشی دهان هستند که در بزاق میتوان مشاهده نمود. در مبتلایان به سرطان دهان، افزایش پروتئینهای تنظیمکننده سیکل سلولی همچون Cyclin D1 و Ki67 و نیز افزایش LDH و (MMP) matrix metalloproteinase و کاهش آنـزیم ترمیم DNA ،
glycosylase (OGG1) DNA 8-oxoquanineو پروتئین سرکوب تومور، Mapsin قابل توجه است.
پروتئوم پلاسمای انسانی
اگر چالشهای موجود در پروتئومیکس برطرف شود، پروتئوم پلاسمای انسان میتواند در تشخیص بیماری و پایش درمان، انقلابی ایجاد کند.
پلاسما بزرگترین منبع پروتئوم انسانی است و علاوه بر اینکه واجد “پروتئینهای پلاسمایی” است، دارای پروتئینهای بافتی (بعلت نشت) و سکانسهای مناطق مختلف ایمونوگلوبینها نیز هست. پیشرفتهای جاری در زمینه پروتئومیکس عمدتاً بعلت پیشرفتهای اخیر در اسپکترومتری جرمی (MS) است. تکنیکهای جدید برای یونیزه کردن پروتئینها و پپتیدها همچون
matrix assisted laser desorption- ionization (MALDI) و (ESI) Electrospray ionization به همــــــراه (TOF) Time of flight و نیز اسپکترومتر جرمی هیبرید ابزار انتخابی برای تعیین مشخصات پروتئینها هستند.
ادرار
Lida W Chan و همکارانش در سال 2004 ارزش پیشگویی دو فاکتور آنژیوژنیک در ادرار یعنی VEGF و MMPS در میزان بقای یک ساله بدون گسترش سرطان را در یک مطالعه طولی بررسی کردند. این مطالعه کوچک پیشنهاد میکرد که تغییرات دو فاکتور مذکور در پیشبینی بقای بدون سرطان بعد از اتمام رادیوتراپی میتوانند مفید باشند.
استفاده معقول از تومورمارکرها
به هنگام درخواست آزمایش تومورمارکرها باید به موارد ذیل توجه داشت:
- تومورمارکرها ممکن است در شرایط متعدد خوشخیم و غیرنئوپلاستیک هم افزایش یابند.
- به لحاظ پایین بودن حساسیت و ویژگی تشخیصی غربالگری جمعیت بدون علامت با بیشتر تومورمارکرهای سرمی توصیه نمیگردد.
- خطاهای ارزیابی پیشآگهی: نتایج در محدوده طبیعی امکان بدخیمی یا پیشرفت بیماری را نفی نمیکنند.
- در تشخیص اولیه سرطان نمیتوان از تومورمارکرها بهجای بیوپسی و بررسی هیستوپاتولوژی استفاده کرد.
- نتایج تومورمارکرها اغلب بستگی به روش اندازهگیری دارند، لذا بهتر است بیماران با یک روش پایش شوند و نوع روش در گزارش قید گردد.
- تفسیر نتایج تومورمارکرها باید در بستر تمام اطلاعات موجود همچون یافتههای بالینی، تصویربرداری و سایر آزمایشهای خونی انجام شود.
نتیجه:
با ارتقاء شناخت از مبانی ژنتیک و مولکولی بدخیمیهای انسانی، تومورمارکرها هم بهتر شناخته شدند و بهطور فزایندهای در شناسایی خطر تومورها و نیز راهکارهای درمانی بهکار میروند.
تومورمارکرهای متعددی شناخته شدهاند اما تعداد معدودی از آنها به لحاظ بالینی مفید واقع میشوند، لذا نباید تومورمارکرها تکیهگاه اولیه در تشخیص و درمان سرطان محسوب گردند بلکه باید در کنار سایر ابزارهای تشخیصی بهکار گرفته شوند.
برگرفته از:
Tumor Markers- A Review
International Journal of Oral Health Dentistry; January-March 2017;3(1):1-5
مارکرهای آزمایشگاهی COVID-19 خفیف و شدید
برای دانلود فایل pdf بر روی لینک زیر کلیک کنید
ورود / ثبت نام