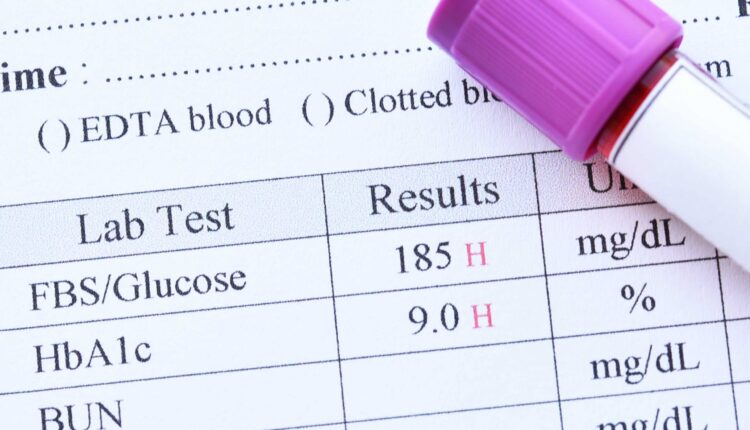
مروری بر تشخیص آزمایشگاهی HbA1c
دکتر حمیدرضا هجرانی، دکترای علوم آزمایشگاهی
درصد هموگلوبین گلیکوزیله A1c (HbA1c%) در خون کامل انسان، نشاندهنده میانگین غلظت گلوکز پلاسما در یک دوره زمانی طولانی است و برای تشخیص دیابت استفاده میشود. در حال حاضر، روشهای متداول آزمایشگاهی برای تشخیص پروتئینهای گلیکهشده (glycated)، کروماتوگرافی مایع با کارایی بالا (HPLC) ، ایمونواسی و الکتروفورز هستند. صحت و دقت روشهای سنجش A1c، حداقل در حد دقت و صحت سنجش گلوکز است؛ در نتیجه انجمن دیابت آمریكا، انجمن اروپایی مطالعات دیابت و فدراسیون بینالمللی دیابت تصمیم گرفتند كه سنجش A1c باید بهعنوان روش اصلی تشخیص دیابت شناخته شود. در سالهای اخیر در دسترس بودن آزمایشهای سریع، قابل اعتماد و با قابلیت انجام آسان برای تشخیص HbA1c، تشخیص سریع دیابت را امکانپذیر ساخته است، ازاینرو این مقاله مروری، اطلاعات کنونی در مورد ابعاد حال و آینده روشهای تشخیصی برای HbA1c را خلاصه میکند.
مقدمه
هموگلوبین گلیکهشده (هموگلوبین A1c ،HbA1c ، A1C یا Hb1c که همچنین بهعنوان HbA1c یا HGBA1c نیز شناخته میشود) نوعی از هموگلوبین است که در درجه اول برای تعیین میانگین غلظت گلوکز پلاسما در دورههای طولانی اندازهگیری میشود. مشاهده شده است که HbA1c از مجاورت هموگلوبین با گلوکز پلاسما، طی یک مسیر گلیکاسیون غیر آنزیمی ایجاد میشود.
HbA1c معیاری از جزء بتا- N- 1داکسی فروکتوزیل در هموگلوبین است. HbA1c بهعنوان هموگلوبینی تعریف شده است که بهطور برگشتناپذیر در یک یا هر دو والین انتهای N زنجیرههای بتا گلیکه میشود. HbA1c تست پرکاربرد و پذیرفتهشده برای پایش کنترل قند در افراد مبتلا به دیابت بوده است. هنگامی که یک مولکول هموگلوبین گلیکه میشود، واحد قندی در باقی طول عمر گلبول قرمز (120روز) همچنان روی آن باقی میماند.
از تستهای آزمایشگاهی HbA1c برای پایش کنترل دیابت استفاده میشود. کروماتوگرافی هموگلوبین A1 و هموگلوبین A1c در خون طبیعی بزرگسالان به دو بخش تقسیم میشــــود: HbA (HbA0) 92-94% و HbA1 (6-8%) که در آن زنجیره B یک گروه گلوکز اضافی دارد.
HbA1 سه گلیکاسیون مختلف دارد؛ HbA1c معمولاً با ایزوالکتریک فوکوسینگ یا الکتروفورز اندازهگیری میشود. گلیکاسیون هموگلوبین در طی زمان، در طول عمر گلبولهای قرمز که 120 روز است به میزانی متغیر (میزان غیرخطی) رخ میدهد. سهم نسبی HbA1c، به میانگین سطح گلوکز در طی 120 روز گذشته بستگی دارد. دامنه آزمایشگاهی طبیعی، بسته به اینکه HbA1 یا HbA1c اندازهگیری شود و بسته به روش مورد استفاده، متفاوت است.
HbA1c یک شاخص قابلاعتماد برای کنترل دیابت بهشمار میرود، بهجز شرایطی که میانگین طول عمر RBC بهطور قابلتوجهی کمتر از 120 روز باشدکه معمولاً منجر به پایین بودن نتایج HbA1c خواهد شد زیرا 50% گلیکاسیون در روزهای 120-90 رخ میدهد. علل شایع این وضعیت عبارتند از:
الف) افزایش تخریب و نوسازی گلبولهای قرمز: از دست دادن خون، همولیز، هموگلوبینوپاتیها و اختلالات گلبولهای قرمز، بیماری میلودیسپلاستیک
ب) تداخل در آزمایش {این امر به روش استفادهشده بستگی دارد: باقی ماندن هموگلوبین جنینی و واریانتهای هموگلوبین، هموگلوبین کاربامیله شده (بیماران اورمیک)}
ج) در بیمارانی که قندخونشان بین مقادیر بسیار بالا و بسیار پایین نوسان دارد، هموگلوبین گلیکهشده میتواند گمراهکننده باشد (پزشک باید نتایج را با اطلاعات بهدستآمده ازنتایج آزمایشهای خانگی گلوکز مقایسه کند).
د) HbA1c میتواند در شناسایی بیمارانی که ممکن است گزارشی غیرواقعی از آزمایش خانگی گلوکز خون خود ارائه میدهند، مفید باشد.
پیشینه تاریخی
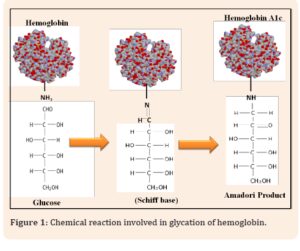
در سال 1955، محققان برای اولین بار اظهار داشتند كه هموگلوبین بالغ حاوی مولكولهایی ناهمگن است. در اواسط دهه 1970، ماهیت واکنش شیمیایی مشخص شد. گلیکاسیون، یک واکنش غیرآنزیمی خودبهخودی است که در آن گلوکز با پیوند کووالانسی به انتهای آمینی زنجیره B گلوبین در هموگلوبین متصل میشود. بعدها پیشنهاد شد که در مولکول گلوکز، اتم کربن نوع دوم به کربن نوع سوم تبدیل میشود؛ بدین ترتیب در گلبول قرمز، گلوکز یک پیوند آلدیمین با NH2– والین زنجیره β تشکیل میدهد، سپس تحت بازآرایی آمادوری قرار میگیرد که باعث تشکیل پیوند پایدار کتوآمین میشود، این فرایند در شکل 1 نشان داده شده است. در سال 1976، HbA1c بهعنوان ابزاری مفید برای پایش کنترل گلایسمی در بیماران دیابتی توصیف شد. در اوایل دهه 1980، آزمایش HbA1c در عرصه بالینی بهطور گسترده مورد پذیرش قرار گرفت.
کاربردهای بالینی HbA1c
بیش از 220 میلیون نفر در سراسر جهان مبتلا به دیابت تشخیص داده شدهاند، اگرچه احتمالاً تعداد واقعی مبتلایان به دیابت به دلیل شروع موذیانه دیابت نوع 2 بیشتر است. بسیاری از افرادی که اختلال در تحمل گلوکز دارند، بیرون از جامعه تشخیص دادهشده بیماران باقی میمانند. دیابت نوع 2، 90 تا 95% از کل موارد دیابت را تشکیل میدهد؛ بهعلاوه، T2DM (دیابت شیرین نوع دو) خطر ابتلا به بیماریهای قلبی و سکته را افزایش میدهد، در واقع 50% از افراد مبتلا به دیابت در اثر بیماریهای قلبی عروقی فوت میکنند.
HbA1c بهعنوان بهترین معیار تعیین گلایسمی در طی 3 ماه گذشته پذیرفته شده است. روشهای مختلفی برای بررسی گلایسمی وجود دارد [بهعنوان مثال، سابقه علائم آشکار (تکرر ادرار، تشنگی زیاد و غیره)، سنجش گلوکز ادرار و گلوکز پلاسما بهصورت تصادفی یا ناشتا]. بررسی گاهبهگاه گلوکز خون، بیشترین استفاده را در بین این روشهای ارزیابی دارد و میتواند بهصورت منطقی منعکسکننده میانگین گلیسمی در دیابت نوع 2 پایدار باشد، اما این روش، صرفاً معیاری صحیح از قند خون در آن لحظه است. قابل اطمینانترین روش سنجش HbA1c که در آزمایشگاههای بالینی با کیفیت بالا انجام میشود، روش استانداردشده بر اساس برنامه ملی استانداردسازی گلیکوهموگلوبین (NGSP) است.
اصلیترین مزیت انجام آزمایش بر بالین بیمار، این واقعیت است که پزشکان میتوانند فوراً در همان لحظه ویزیت بیمار از نتیجه آزمایش مطلع شوند. مزیت دیگر این است که انجام آزمایش بر بالین بیمار در محلهایی که دسترسی آسان به آزمایشگاه ندارند، بهراحتی مورد استفاده قرار میگیرد. از معایب آزمایش بر بالین بیمار میتوان به ضرورت نگهداری معرفها در شرایط صحیح و احتمال کاهش کنترل کیفی در صورت انجام آزمایش توسط پرسنل فاقد آموزشهای کافی اشاره کرد. نقطه ضعف دیگر که مخصوصاً در مورد آزمایش خانگی HbA1c توسط بیماران صدق میکند این واقعیت است که دادهها همیشه بهطور دقیق و کامل وارد پرونده الکترونیکی پزشکی بیمار نمیشوند. بدون در نظر گرفتن این معایب، شواهدی وجود دارد که آزمایش بر بالین بیمار روشی مؤثر است.
گلیکاسیون غیرآنزیمی در برابر دگلیکاسیون آنزیمی
بیشتر پروتئینها (از جمله هموگلوبین) با قندها واکنش داده و بدون دخالت آنزیمها ترکیبات کووالانسی را تشکیل میدهند. این فرآیند شیمیایی گلیکاسیون غیرآنزیمی نامیده میشود. تجمع حاصل از محصولات نهایی گلیکاسیون پیشرفته، با پیشرفت عوارض دیابت همراه است. دگلیکاسیون آنزیمی، فرآیند گلیکاسیون غیرآنزیمی را معکوس میکند و باعث ایجاد گروههای آمینوی آزاد میشود. دگلیکاسیون آنزیمی یک سیستم دفاعی نیرومند در برابر گلیکاسیون غیرآنزیمی در سلولهای پستانداران است. این سیستم با استفاده از فروکتوزآمین- ۳- کیناز (FN3K)، ریشه فروکتوزلیزین بر روی پروتئینهای گلیکهشده را فسفریله میکند و در نتیجه ترکیب را ناپایدار میسازد که در نهایت باعث تجزیه پروتئینهای گلیکهشده میشود. این فرآیند دگلیکاسیون آنزیمی در اپیزودهای هایپرگلایسمی شدید در افراد مبتلا به دیابت با شکست مواجه میشود، زیرا گلیکاسیون غیرآنزیمی بدون توقف ادامه مییابد. در طولانی مدت، این مسئله پایداری ساختار پروتئین را تغییر میدهد و در نهایت منجر به اختلال عملکرد سلولی میشود.
محصولات نهایی گلیکاسیون پیشرفته Advanced Glycation End products (AGEs)، بهطور مستقیم و غیرمستقیم (از طریق گیرندهها) باعث شکلگیری بیماری قلبی عروقی میشوند. آنها در قسمتهای مختلف بدن انباشته میشوند و با گیرندههای محصولات نهایی گلیکاسیون پیشرفته (RAGE) واکنش ایجاد میکنند و باعث القای استرس اکسیداتیو، افزایش التهاب و افزایش رسوب در ماتریکس خارج سلولی میشوند و در نتیجه روند مختل شدن عملکرد اندوتلیال را تسریع میکنندو منجر به تشکیل سریعتر پلاک و درنهایت آترواسکلروز در دیابت میشوند. هموگلوبین گلیکهشده، ترکیبی حد واسط و برگشتپذیر است، اما پس از برخی بازآراییهای داخلی در این ترکیب، HbA1c پایدار تشکیل میشود. چندین جایگاه گلیکاسیون در مولکول HbA وجود دارد؛ ریشه والین انتهای N زنجیره b، عمدهترین جایگاه گلیکاسیون است که ۶۰% گلوکز متصلشده را تشکیل میدهد. از سه نوع HbA1 یعنی HbA1a، HbA1b و HbA1c، نوع HbA1c بیشترین گونه گلیکهشده است.
چرا استانداردسازی اندازهگیری HbA1c ضرورت دارد؟
عدم استانداردسازی منجر به ایجاد تغییرات زیاد در نتایج (4% تا 8/1%) یک نمونه میشود و این امر مقایسه نتایج بیماران در آزمایشگاهها را دشوار میسازد. این عدم تطابق همواره موجب بروز نگرانی در بین ارائهدهندگان مراقبتهای سلامتی شده است؛ به خصوص در عصر حاضرکه مهاجرتهای زیادی صورت میگیرد و مردم مسافتهای طولانی را طی میکنند و نتیجه آزمایش قبلی خود را نیز با خود میبرند؛ بنابراین، برخورداری از روش و واحد یکسان برای اندازهگیری HbA1c نیاز روز است.
برای غلبه بر این مشکل، در سال 1995 فدراسیون بینالمللی شیمی بالینی (IFCC)، توسعه استانداردسازی بینالمللی یکپارچه برای HbA1c را بر عهده گرفت. برای کالیبراسیون روش مرجع، مخلوطی از HbA1c خالص و HbAo خالص ساخته شد. یک شبکه آزمایشگاهی نیز راهاندازی شد که از دو روش مرجع استفاده میکرد و کروماتوگرافی مایع فاز معکوس با کارایی بالا را با طیفسنجی جرمی یا الکتروفورز کاپیلاری ادغام کرده و از همان مخلوط بهعنوان کالیبراتور استفاده میکرد، سپس IFCC، HbA1c را بهعنوان هموگلوبینی تعریف کرد که بهطور برگشتناپذیر در یک یا هر دو والین انتهای N زنجیرههای بتا گلیکه میشود.
این تعریف همچنین هموگلوبینی را که علاوه بر این، در هریک از ریشههای لیزین زنجیره b گلیکه میشود را نیز در برمیگیرد. قبل از تعریف IFCC، HbA1c بهصورت یک پیک (peak) مشخص در HPLC تعریف شده بود که بهوضوح چندان علمی بهنظر نمیرسید. هموگلوبینی که فقط در یک جایگاه لیزین گلیکه شده است، در اندازهگیری HbA1c لحاظ نمیشود. از آنجا که اندازهگیری IFCC بسیار اختصاصی است، فقط یک گونه مولکولی HbA1c را اندازهگیری میکند؛ بنابراین، اجزای غیر HbA1c در نتایج نهایی گنجانده نشدهاند؛ در نتیجه مقادیر HbA1c بهدستآمده با استفاده از روش IFCC به میزان 1/5 تا ۲ درصد، کمتر از نتایج NGSP ردیابیشده به DCCT و همچنین روشهای مقایسه تعیینشده سوئدی و ژاپنی است.
نگرانیهایی در مورد تأثیر این تغییر مقادیر در مراقبت از بیمار مطرح شده است چرا که میتواند منجر به کنترل کمتر از حد مطلوب گلایسمی در بیماران دیابتی شود. برای غلبه بر این مشکل، «معادله اصلی» برای فرمولیزه کردن ارتباط بین روش مرجع IFCC و هر سه روش مقایسه تعیینشده (DCMs)، یعنی برنامه ملی استانداردسازی گلیکوهموگلوبین ایالات متحده (NGSP)، انجمن دیابت ژاپن/ انجمن شیمی بالینی ژاپن (JDS/ JSCC) و Mono-S در سوئد شکل گرفت. معادله اصلی امکان تبدیل نتایج IFCC به نتایج HbA1c مرسومتر که میتواند در نتایج حاصل از DCCT و مطالعه آیندهنگر دیابت انگلستان (UKPDS) قابل ردیابی باشد را فراهم میآورد.
در سال 2004، کارگروه سنجش HbA1c با شرکت انجمن دیابت آمریکا، انجمن اروپایی مطالعه دیابت و فدراسیون بینالمللی دیابت، با هدف هماهنگسازی سیستمهای گزارشدهی شکل گرفت. در این کارگروه اعضایی ازADA ،IDF ،EASD ، NGSP و IFCC شرکت داشتند. در سال 2007، IFCC توصیه كرد كه نتایج HbA1c بهجای درصد HbA1c بهصورت mmol HbA1c/mol Hb نمایش داده شود. بیمارانی که برای خودنظارتی (self-monitoring) روزانهی گلوکز از mmol/l یا mg/dl استفاده میکنند، درک این مقادیر برایشان دشوار است چرا که پزشکانشان در هنگام صحبت با آنها مقادیر هموگلوبین را به درصد بیان میکنند.
برای از بین بردن این سردرگمیها و کاهش این عدم تطابقها، بیانیه اجماع (consensus statement) در مورد استانداردسازی جهانی اندازهگیری هموگلوبین A1c در ماه می 2007 توسطADA ،EASD ، IDF و IFCC به تصویب رسید. مطابق این بیانیه، سیستم مرجع جدید IFCC تنها مرجع معتبر برای اجرای استانداردسازی اندازهگیری HbA1c است. علاوه بر این، نتایج HbA1c در سراسر جهان باید با اســـــتفاده از معادله اصلی IFCC-NGSP، مطابق واحدهای IFCC (Hb گلیکهشده برحسب mmol بهHb کل برحسب mol) و واحدهای منشأ گرفته از NGSP گزارش شوند؛ بنابراین بازه 25 تا 42 (mmol/mol) افراد غیردیابتی را نشان میدهد، همانگونه که بر اساس واحدهای منشأ گرفته از NGSP نیز بهطور مشابه، بازه مربوط به افراد دیابتی 2/5 تا 4/2 درصد (HbA1c) است. همچنین معین شد كه میتوان از میانگین گلوکز متناظر با HbA1C نیز به عنوان تفسیری از نتایج HbA1c استفاده نمود.
ارتباط بین میانگین گلوکز خون و HbA1c
تلاشهایی برای تعریف ارتباط واقعی بین میانگین گلوکز پلاسما و سطح HbA1c در برخی موارد انجام شده است، اما این پژوهشها به دلیل اندازهگیریهای کمتر مقادیر گلوکز و محدود بودن تعداد شرکتکنندگان، کارایی محدودی داشتند. این روش، مستعد خطا است و هیچ نمونهای در شب جمعآوری نمیشود، بنابراین بهطور واقعی نشاندهنده گلایسمی 24 ساعته نیست. Nathan و همكاران از پایش مداوم گلوکز که طی آن سطح گلوکز را هر 5 دقیقه یکبار به مدت 3 ماه در افراد غیردیابتی و افراد دیابتی با گلایسمی نسبتاً پایدار اندازهگیری میشود، استفاده کردند.
آنها یک رابطه ریاضی بین HbA1c و میانگین گلوکز خون را گزارش کردند به این معنی که HbA1c میتواند بهصورت معادلی از میانگین سطح گلوکز (یعنی با استفاده از همان واحدهای خودنظارتی بیماران) بیان شود. با این حال، این مطالعه به دلیل کم بودن تعداد نمونهها محدودیت دارد. یک آنالیز دادهای گذشتهنگر از DCCT نیز همبستگی خطی بین HbA1c و میانگین گلوکز خون را نشان داد، اما جمعیت مورد مطالعه فقط شامل T1DM بود و DCCT برای تعیین چنین ارتباطی طراحی نشده است.
یک اصطلاح جدید برای جایگزینی HbA1c
مطالعه میانگین گلوکز مشتق از A1c در 10 مکان مختلف در آمریکای شمالی، اروپا و آفریقا انجام شد. دو کشور بزرگ یعنی هند و چین با جمعیت مبتلا به دیابت بسیار زیاد کنار گذاشته شدند. جامعه مورد مطالعه شامل 507 بیماربود که 268 بیمار مبتلا به T1DM و 159 بیمار T2DM و 80 فرد غیردیابتی را دربر میگرفت. محققان به دنبال بررسی رابطه میانگین گلوکز خون با HbA1c در یک بازه گسترده بودند (یعنی HbA1c بین ۵ تا 13%). آنها طی 3 ماه تقریباً 2700 قرائت قند خون را از هر شرکتکننده جمعآوری کردند که تا به امروز بیشترین تعداد قرائت قند خون در هر فرد در یک مطالعه واحد است.
هدف از این مطالعه گزارش نتایج هموگلوبین گلیکهشده نه در قالب معمول درصد HbA1c، بلکه بهصورت میانگین مشتق از A1c و با همان واحدهای مورد استفاده درارزیابیهای خودنظارتی (یعنی mg/dl یا mmol/l) است. این مطالعه اینچنین نتیجهگیری کرد که اکنون میتوان میانگین گلوکز تخمین زدهشده (eAG) را با استفاده از یک معادله رگرسیون خطی، از روی HbA1c محاسبه کرد. در حال حاضر از eAG میتوان برای پایش گلایسمی در بیماران دیابتی استفاده نمود. همانگونه که از میزان فیلتراسیون گلومرولی تخمینزده شده (eGFR) بر اساس اندازهگیری کراتینین سرم برای پایش بیماری مزمن کلیوی استفاده میشود.
مقادیر هدف HbA1c در درمان دیابت
در عرصه بالینی، مقادیر هدف مربوط به HbA1c توسط سازمانهای رسمی توصیه میشوند و گایدلاینها مقدار کمتر از 6/5% یا 7% – با اندکی احتیاط- را پیشنهاد میکنند. هر کدام از این سطوح HbA1c، نشاندهنده پایین بودن خطر ابتلا به عوارض میکروواسکولار پیشرونده است. بین کنترل درازمدت در سطح 6/5% یا ۷% به لحاظ وضعیت ریسک، اختلاف کمی وجود دارد؛ اما شخصیسازی مقادیر هدف میتواند تفاوت قابلتوجهی ایجاد کند. در بیماران سالخورده با وجود چندین همابتلایی، کنترل قندخون مزایای اندکی دارد. یک فرد جوان و با ثبات مبتلا به دیابت که بهخوبی از خود مراقبت میکند ممکن است بتواند به کنترل بهتری از قندخون دست یابد.
HbA1c چگونه اندازهگیری میشود؟
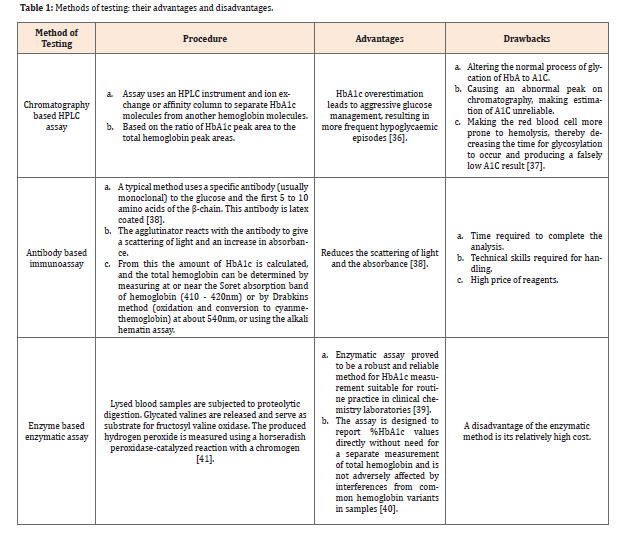
بر روی مولکول HbA1c یک بار الکتریکی وجود دارد که مقدار آن با بارهای موجود بر روی اجزاء هموگلوبینهای دیگر متفاوت است. بر این اساس و نیز اختلاف اندازهHbA1c با سایر هموگلوبینها و با استفاده از روشهای شناختهشدهای مانند کروماتوگرافی مایع با فشار (یا کارایی) بالا (HPLC)، می توان آن را جدا نمود. HPLC اجزاء مختلف مخلوطها (بهعنوان مثال خون) را با افزودن آنها به مایعات مخصوص و عبور دادن تحت فشار آنها از خلال ستونهای خاص جدا میکند. این ستونها مملو از مادهای هستند که مولکولهای مختلف یک مخلوط را از هم جدا میکنند. از آنجا که HbA1c تحت تأثیر نوسانات کوتاهمدت غلظت گلوکز خون- بهعنوان مثال به دلیل صرف وعدههای غذایی- قرار نمیگیرد، میتوان نمونه خون برای آزمایش HbA1c را بدون توجه به زمان غذا خوردن جمعآوری کرد. در حال حاضر 3 روش اصلی برای اندازهگیری HbA1c در آزمایشگاههای بالینی وجود دارد:
الف. روش HPLC مبتنی بر کروماتوگرافی
ب. ایمونواسی مبتنی بر آنتیبادی
ج. روش آنزیمی مبتنی بر آنزیم
روشهای مبتنی بر کروماتوگرافی
HPLC
در سنجش کروماتوگرافیک، از دستگاه HPLC و ستون تعویض یون یا ستون تمایلی (affinity) برای جدا کردن مولکولهای HbA1c از دیگر مولکولهای هموگلوبین استفاده میشود. مقدار HbA1c بر اساس نسبت مساحت سطح پیک HbA1c به مساحت سطح پیک هموگلوبین کل اندازهگیری میشود.
کروماتوگرافی Boronate affinity:
این روش برای جداسازی و آنالیز آنالیتهای خاص در یک نمونه بر اساس استفاده از «واکنشی بیولوژیک» عمل میکند. در مورد HbA1c، کروماتوگرافی میل ترکیبی بورونات، یک روش اختصاصی گلیکاسیون است که اساس آن اتصال بورونات به گروه cis- diol حاصل از اتصال پایدار گلوکز به Hb است؛ بنابراین، این روش هر چهار گونه پایدار را اندازهگیری میکند. اندازهگیری ترکیبی تنها برای این چهار گونه پایدار تحت عنوان «HbA1c کل» یا در برخی موارد «HbA1c واقعی» نامیده میشود. به این دلیل که در این روشها تنها دو بخش وجود دارد (گلیکهشده و غیرگلیکه)، بخش گلیکهشده با کل مقایسه میشود و نتایج بهصورت HbA1c% بیان میشود. بازه خطی بودن برای شناسایی HbA1c، 5.3 % تا 17% است.
روش ایمونواسی تقویتشده با لاتکس:
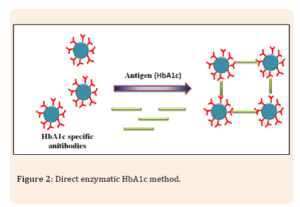
روش ایمونواسی تقویتشده با لاتکس برای HbA1c مبتنی بر واکنش بین مولکولهای آنتیژن (HbA1c) و آنتیبادیهای اختصاصی HbA1c که روی دانههای لاتکس پوشیده شده است، میباشد. این واکنش باعث تغییر در کدورت محلول میشود و این کدورت با مقدار آنتیژن موجود در نمونه متناسب است که در شکل 2 نشان داده شده است. مشخص شده است که این تست در بازه 2/0% تا 16/0% خطی است.
روش سنجش آنزیمی HbA1c:
نوآوریهای اخیر، یک سنجش آنزیمی مستقیم HbA1c را به ارمغان آورده است که از یک آزمایش منفرد استفاده میکند و مقادیر HbA1c% را مستقیماً و بدون نیاز به اندازه گیری هموگلوبین توتال در یک مرحله محاسبه و گزارش میکند.
اصول سنجش
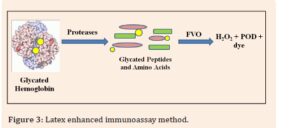
مواد اکسیدکننده موجود در بافر لیزکننده با نمونه خون واکنش نشان میدهند تا مواد مداخلهکننده در سیگنال با وزن مولکولی کم و با وزن مولکولی زیاد را از یکدیگر جدا کنند. بعد از لیز شدن، نمونههای خون تحت تجزیه پروتئولیتیک قرار میگیرند. این فرآیند، آمینواسیدها، از جمله والینهای گلیکهشده را از زنجیرههای بتای هموگلوبین آزاد میکند. در سنجش آنزیمی مستقیم HbA1c، والینهای گلیکهشده بهعنوان سوبستراهایی برای یک آنزیم اختصاصی نوترکیب به نام فروکتوزیل والین اکسیداز (FVO) عمل میکنند.
FVO نوترکیب بهصورت اختصاصی، والینهای انتهای N را جدا کرده و سپس در حضور عوامل انتخابی (selective agents) هیدروژن پراکسید تولید میکند. این فرایند با استفاده از واکنش کاتالیزشده توسط پراکسیداز متعلق به گیاه ترب کوهی (horseradish) (POD) و یک کروموژن مناسب اندازهگیری میشود. سیگنال تولید شده در واکنش با استفاده از یک منحنی کالیبراسیون خطی، HbA1c را مستقیماً بهصورت درصد HbA1c موجود بیان میکند. اصول سنجش آنزیمی مستقیم HbA1c در شکل 3 به تصویر کشیده شده است.
سنجش آنزیمی مستقیم HbA1c، از تمامی مزایای روشهای HPLC و ایمونواسی از نظر دقت، اختصاصیت، قابلیت استفاده در آنالایزرهای شیمی برخوردار است و در عین حال مقرونبهصرفه و سادهتر است و نیازمند به مداخلات کمتری است. سنجش آنزیمی مستقیم HbA1c از دو معرف مایع پایدار آمادهی مصرف استفاده میکند. از آنجا که اندازهگیری هموگلوبین کل موجود در نمونهها بهصورت جداگانه موردنیاز نیست، سنجش آنزیمی مستقیم HbA1c، برای انجام آزمایش در آنالایزرهای شیمی فقط به یک کانال واحد نیاز دارد درحالیکه برخی ایمونواسیها نیازمند اندازهگیری هموگلوبین کل بهصورت جداگانه هستند و به دو کانال برای انجام آزمایش در آنالایزرهای شیمی نیاز دارند.
روش سنجش آنزیمی مستقیم HbA1c ساده و عاری از پیچیدگی است؛ پس از افزودن معرف R1، نمونه و معرف R2، نتیجه HbA1c% ظرف دو دقیقه گزارش میشود. علاوه بر این، معرفها حاوی ذرات لاتکس نیستند و ازاینرو کووتها و لاینهای آنالایزر را نمیپوشانند. از همه مهمتر، سنجش آنزیمی HbA1c بالاترین اختصاصیت را در بین کلیه روشهای سنجش HbA1c دارد. سنجش آنزیمی مستقیم HbA1c دارای بازه خطی بودن از 4 تا 16% است.
همانطور که در جدول 1 ذکر شده است، واریانتهای تغییریافته ژنتیکی یا شیمیایی هموگلوبین در سنجشهای آنزیمی HbA1c تداخل ایجاد نمیکنند؛ بنابراین تستهای آنزیمی Hb1c تستهای قابلاعتمادی هستند و فارغ از واریانتهای مختلف هموگلوبین بیمار، نتایج کاذب ارائه نمیدهند. بهطور خلاصه، سنجش آنزیمی مستقیم HbA1c، نسبت به HPLC و ایمونواسی از مزایای زیر برخوردار است:
الف) دو معرف پایدار مایع
ب) عدم نیاز به اندازهگیری هموگلوبین کل
ج) استفاده از یک کانال منفرد در آنالایزرها که سریعتر، سادهتر و مقرونبهصرفهتر است.
د) عدم مداخله واریانتهای هموگلوبین
ه) قابل اجرا در اکثر آنالایزرها
و) همبستگی خوب با HPLC و ایمونواسی
الکتروفورز کاپیلاری
اساساً، بهمنظور جداسازی HbA1c در الکتروفورز کاپیلاری (CE)، با توجه به نسبت بار به جرم، دو امکان وجود دارد؛ امکان اول، آنالیز Hb بهعنوان کاتیون در بافرهای اسیدی با pH کمتر از pI هموگلوبین که تقریباً 0/7 است. جداسازی هموگلوبینهای A1C و A0 به دلیل اختلاف بار ناشی از حذف یک گروه آمینوی دارای بار مثبت در مولکول HbA1c به دلیل اتصال به گلوکز رخ میدهد. امکان دوم، آنالیز Hb بهعنوان آنیون در شرایط قلیایی، با گزینشپذیری (selectivity) برای HbA1c است که این گزینشپذیری از طریق یک واکنش cis- diol بین بخش گلوکز HbA1c و آنیون بورات حاصل از الکترولیت پسزمینه (background electrolyte; BGE) القا میشود.
بیوسنسور الکتروشیمیایی برای هموگلوبین گلیکهشده (HbA1c)
اولین حسگرهای زیستی تجاری موفق بر اساس حسگرهای الکتروشیمیایی برای آنالیتهای چندگانه بنا شده بودند. پژوهشها در مورد حسگرهای زیستی الکتروشیمیایی برای مدت طولانی ادامه داشته است. در حال حاضر، مبدلهای (transducer) مبتنی بر الکترودهای نیمهرسانا و الکترودهای صفحهای (screen printed electrods)، یک پلتفرم رایج برای توسعه حسگرهای زیستی هستند. آنزیمها یا آنتیبادیهای نشاندارشده با آنزیم، پرکاربردترین اجزاء زیستشناساگر در حسگرهای زیستی هستند. بیوالکتروآنالیز با حسگرهای زیستی الکتروشیمیایی، یک عرصه جدید برای توسعه سریع در الکتروآنالیز است. در ساخت بیوسنسور باید مولکول گیرنده زیستی (bioreceptor)، روش بیحرکت کردن و مبدل بهدرستی انتخاب شوند و برای هدف مورد نظر مناسب باشند.
سنسورهای مربوط به بیوالکتروآنالیز، آنالیزی اختصاصی، با تکنیکی سریع، حساس، انتخابی و ارزانقیمت را ارائه میدهند. تفاوت حسگرهای زیستی و حسگرهای فیزیکی یا شیمیایی در این است که جزء شناساییکننده این حسگرها، یک عنصر بیولوژیک است. حسگرهای زیستی الکتروشیمیایی دارای مزایایی هستند که میتوانند بدون آسیب رساندن به سیستم، مواد را حس کنند. بهمنظور محاسبه سطح گلوکز روزانه برای کنترل میزان مصرف مواد غذایی و انسولین، حسگرهای زیستی الکتروشیمیایی بهعنوان سنجشگرهای گلوکز، علیرغم برخی مشکلات موجود، بهکار میآیند؛ بهعنوان مثال توصیه می شود اندازهگیری سطح گلوکز خون سه تا چهار بار در روز انجام شود. با توجه به نوسانات زیاد سطح گلوکز که بهطور طبیعی در طی یک روز اتفاق میافتد، اندازهگیریهای در زمان خالی بودن معده و طی 2 ساعت بعد از خوردن غذا، برای اهداف متفاوتی موردنیاز است.
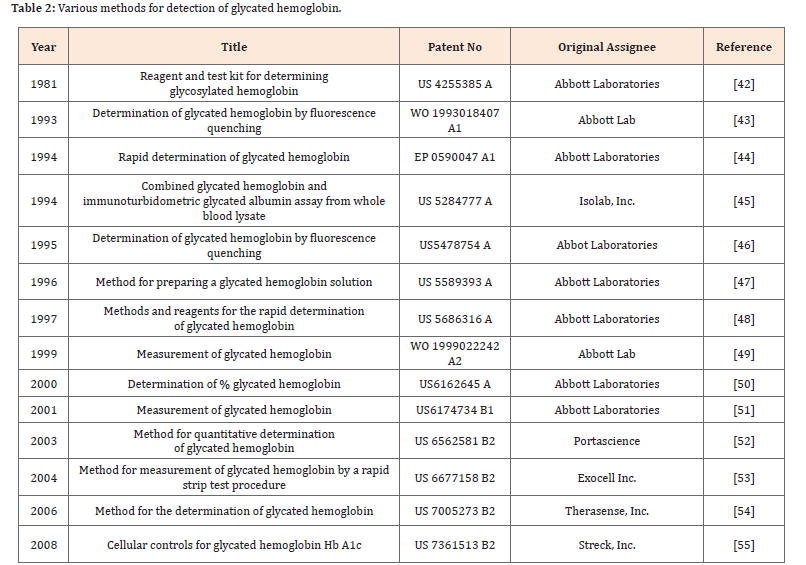
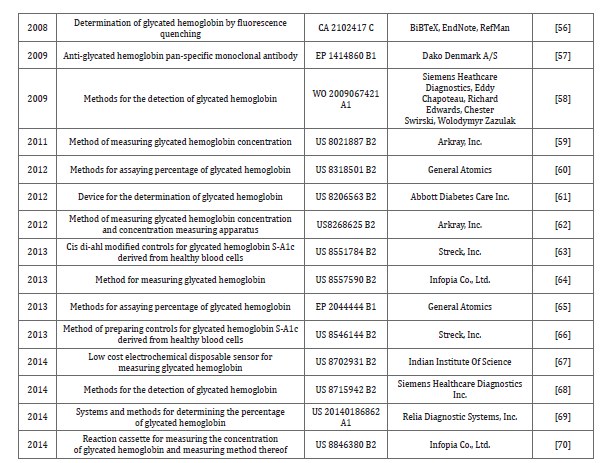
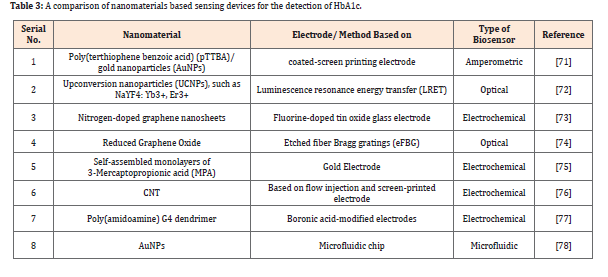
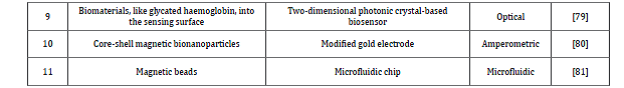
این مشکلات برای تشخیص دیابت و بررسی ارتباط بین سبک زندگی و دارو پس از تشخیص ابتلای یک فرد به این بیماری، برجستهتر است. مطالعات مختلف برای تشخیص هموگلوبین گلیکهشده که پیشتر انجام گردیده است در جدول 2 خلاصه شده است، همچنین، نانومواد مختلفی همچون نانوذرات طلا، نانولولههای کربنی (CNT)، نانوذرات زیســــــــتی مغناطیسی هسته- پوسته (core-shell)، گرافم آلاییده doped grapheme با نیتروژن و مواردی از این دست وجود دارند که میتوانند در ساخت حسگرهای الکتروشیمیایی و همچنین دیگر انواع مختلف حسگرهای زیستی بهعنوان مثال حسگر میکروفلوئیدیک یا حسگر نوری برای تشخیص هموگلوبین گلیکهشده مورد استفاده قرار گیرند؛ بنابراین مقایسهای بین دستگاههای حسگر مبتنی بر نانومواد برای تشخیص HbA1c نیز در جدول 3 آورده شده است.
پاسخ خطی بودن این حسگرها به سطوح HbA1c، 2/5% تا 15% است. در سناریوی کنونی بازار، روشهای آزمایشگاهی (سنجش HPLC مبتنی بر کروماتوگرافی، ایمونواسی مبتنی بر آنتیبادی و سنجش آنزیمی مبتنی بر آنزیم) در محدوده 700 تا 1400 روپیه هند هزینه دارد. با استفاده از نانوذرات و قابلیت استفاده چندگانه آن، هزینه محصول در طولانی مدت نسبت به سیستمهای تشخیصی فعلی کاهش مییابد.
ابهامات آینده: چالشها و راهحلها
روشهای شناسایی HbA1c را میتوان به دو گروه ابزارهای آزمایشگاهی و ابزارهای مراقبت بر بالین بیمار (POCT) تقسیم کرد. عملکرد آنالیزی ابزارهای آزمایشگاهی از عملکرد ابزارهای POCT بهتر است، اما ابزارهای POCT این مزیت را دارند که نتایج را در هنگام مراجعه بیمار به پزشک فراهم میآورند (بنابراین نیاز بالینی را بهراحتی برآورده میکند). توسعه ابزار POCT اخیراً به یک روند تبدیل شده است. چالش نهایی، یافتن دستگاه آنالیتیک با اختصاصیت خوب و دقت کافی دستگاهها در ارتباط با کاربرد بالینی آنها است. توسعه بیوسنسورهای آرایهای ارزان و یکبار مصرف برای شناسایی همزمان مارکرهای مهم دیابتی کماکان موردنیاز است. استفاده از بیومولکولها برای رشد نانوذرات، چشمانداز روشنی را برای حسگرهای زیستی و طراحی سیستمهای بیوالکتریک در آینده در پی دارد.
نتیجهگیری
بررسی خون توسط بیمار بهصورت روزانه، با واحدهای mmol/L یا mg/dl انجام میشود و اندازهگیری HbA1c بهصورت درصد تا حدودی گیجکننده است. با توجه به باریک بودن دامنه درصدها، درک برخی از پیامدهای حتی یک درصد افزایش یا کاهش HbA1c برای بیماران دشوار است. بیماران و پزشکان آنها به این موضوع عادت کردهاند که سطح HbA1c در بیماران دیابتی باید کمتر از 7 درصد باشد. یک قرائت بالاتر سطح گلوکز نشان میدهد که کنترل گلایسمی از دست خارج شده است. در حال حاضر نتایج IFCC بهصورت میلیمول HbA1c در هر مول هموگلوبین بیان میشود. تداوم بیان نتایج NGSP بهصورت درصد، همراه با نتایج IFCC باعث میشود این تفاوت کمتر گیجکننده باشد.
هدف ما این بود که در یک مطالعه آیندهنگر، عملکرد بالینی روش مرجع و یک روش جایگزین برای اندازهگیری سطح هموگلوبین گلیکهشده خون را مقایسه کنیم. تشخیص سریع و دقیق آزمایشگاهی HbA1c با استفاده از انواع روشهای آزمایشگاهی یک امر ضروری است. چنین آزمایشهایی تاکنون توسط HPLC، ایمونواسی و واکنشهای آنزیمی، انجام شده است اما همه این روشها دارای محدودیتهایی هستند. حسگر زیستی HbA1c به دلیل کمهزینه بودن، سریع بودن و فاکتورهای دارای حساسیت بالا ممکن است گزینه بهتری باشد.
ترجمه از:
Laboratory Diagnosis of HbA1c: A Review
J Nanomed Res 2017, 5(4): 00120
HbA1c: مروری بر جنبههای آنالیتیکی و بالینی
اندازهگیری HbA1c در نمونههای Dried Blood Spot (DBS) به روش LPLC با استفاده از دستگاه DS5
https://www.medicinenet.com/hemoglobin_a1c_test/article.htm
برای دانلود فایل pdf بر روی لینک زیر کلیک کنید
ورود / ثبت نام

در جامعه آزمایشگاهی کار نکرده بسیار است
مجموعه پارس پیوند اقدام به انتشار مقالات آزمایشگاهی نموده است
از همراهی شما در بازدید از مقالات مرتبط سپاسگزاریم
http://gph.ir/AB6C