باكتريهاي شكارچي انقلابي در در مان بيولوژيك
سعيد شعاع: دانشجوي كارشناسي ارشد ميكروبيولوژي
دلوويبريو
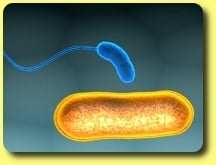
چكيده: دلوويبريو باكتريووروس[1] باكتري شكارچي از كلاس دلتا پروتئوباكتريا[2] ميباشد كه شكار خود را از ميان باكتريهاي گرم منفي انتخاب ميكند. اين باكتري داراي 2 سيكل زندگي مرحله حمله و مرحله رشد[3] ميباشد كه در نهايت باعث مرگ سلول شكار (ميزبان) ميشود. اين خاصيت باكتري به عنوان شكارچي طبيعي ميتواند به عنوان يك عامل كنترل طبيعي آن را مطرح سازد. اين باكتري توانايي حمله به باكتريهاي پاتوژن– انساني، گياهي و حيواني را دارا ميباشد، با اين مزيت كه هيچگونه زياني به سلولهاي انساني– گياهي– حيواني وارد نميسازد.
| Bdellovibrio | |
| Scientific classification | |
| King dom | : Bacteria |
| Phylum | : proteobacteria |
| Class | : Delta proteobacteria |
| Order | : Bdellovibrionales |
| Family | : Bdellovibrionaceae |
| Genus | : Bdellovibrio |
| Species | : B. bacteriovorus |
| Bdellovibrio bacteriovorus | |
مقدمه
دلوويبريو باكتريووروسها، گرم منفي، متحرك با يك فلاژل غلافدار قطبي هستند كه بوسيله شكار كردن ساير باكتريهاي گرم منفي مشخص ميشوند.
دلوويبريوها داراي دو سيكل زندگي[4] ميباشند؛ يك مرحله حمله[5] و يك مرحله رشد[6] كه در درون باكتري گرم منفي و در فضاي پريپلاسمي رخ ميدهد (stolp H, starr MP, 1963). دلوويبريوها اولين بار در سال 1963 بوسيله استالپ[7] و استار[8] كه بر روي باكتريهاي صياد مطالعه ميكردند، كشف شدند (stolp and starr, 1963). اين باكتري در فضاي پريپلاسمي باكتري شكار رشد ميكند و فرمي ساختماني كه به آن دلوپلاست[9] ميگويند را ايجاد ميكند. در فاز حمله[10] باكتري تقسيم نميشود و براي اينكار بايد يك سلول ميزبان را آلوده كند تا بتواند تقسيم را در درون سلول ميزبان انجام دهد.
سيكل زندگي دلوويبريو شكارچي
الف- (مرحله حمله)
در مرحله و فاز حمله باكتـــــري با سرعت باور نكردني 160mm در ثانيه حركت ميكند (Lambert, C et al, 2006)، كه اين حركت بوسيله يك فلاژل قطبي غلافدار ايجاد ميشـــــود (Thamashow Ls, Rittenberg SC, 1978). مشخص نيست كه چه عاملي باعث جذب اين صيادان به محل شكار ميشود ولي مواردي مثل اكسيژن و آمينواسيدها را احتمال ميدهنــــــــــــــــــــــــد كه تأثيرگذار باشند (Straley sc, conti SF, 1977).
به محض اينكه دلو ويبريو باكتريووروس[11] با سلول شكار تماس پيدا كرد، آنزيمهاي هيدروليتيك شروع به هضم ديواره سلول شكار (ميزبان) ميكنند (Rendulic et al, 2004). اولين حمله بوسيله آنزيمهاي هيدروليتيك[12] باعث ميشود كه ديواره سلولي شكار بطور ناقص هضم شود، اين تضعيف ديواره و ساختمان سلولي باعث بوجود آمدن فرمي ميشود كه به آن دلوپلاست[13] گويند (Thomashow and Rittenborg, 1987). تماس با سلول ميزبان در ابتدا قابل برگشت است و باكتري ميتواند از سلول شكار جدا شده و به راه ديگر براي شكار ديگر برود، اما بعد از مرحله شناسايي و تشخيص[14] كه چند دقيقه طول ميكشد مرحله حمله به سلول ميزبان شروع ميشود (Burnham jc, et al, 1968).
ب- مرحله تماس و ورود باكتري دلوويبريو به سلول شكار:
دلوويبريو باكتريووروس[15] وارد سلول ميزبان ميشود، در اين زمان اين عمل را بوسيله كم كردن سرعت و به هم فشردن خود و ايجاد يك روزنه در ديواره خارجي سلول ميزبان با استفاده از پيلي نوع 4[16] انجام ميدهد (Evans et al, 2007).
ج– مرحله رشد[17]:
بعضي از اولين آنزيمهايي كه بوسيله دلوويبريو آزاد ميشود باعث حل شدن 15-10% از ديواره سلولي ميزبان ميشود و باعث تغيـــير شكل از شـــــــــــــكل ميلهاي به كروي ميگردد (Themashow and Rittenberg , 1978).
اين تغيير ساختمان و رشد در درون سلول ميزبان و كروي شدن سلول ميزبان را دلوپلاست[18] گويند كه اولين بار در سال 1973 توسط كسل و وارون[19] مشخص گرديد (Kessel and Varon, 1973).
د- مرحله تقسيم شدن دلوويبريو در فاز رشد[20]:
استفاده دلو ويبريو از اجزاي هضم شده در درون سلول ميزبان باعث افزايش طول و پيچ خوردن آن به شكل در بطري باز كن[21] ميشـــــــــــــــــود كه طول آن 3-5 برابر زمان فاز حمله ميشود (starr & Baigent, 1966).
ه– از بين رفتن دلوپلاست[22] و آزاد شدن باكتريها[23]:
زماني كه ذخاير داخل دلوپلاست تمام شد، دلو ويبريوها شروع به ترشح آنزيمهاي ليز كنندهاي كرده كه باعث ميشود كه باقيمانده غشاء ميزبان پاره شده و سلولهاي جديد ساخته شده به محيط رها شوند. اين سلــــولها كامل بوده و قابليت حمله به باكتريهاي ديگر را دارا ميباشند (Thomushow and Rittenberg, 1978).
استفاده از دلوويبريوها در مصارف پزشكي
تحقيقات اخير بر روي دلوويبريو اين اصل را روشن ميسازد كه ميتوان از اين خاصيت باكتري در درمان بيماريهاي باكتريايي اســـــتفاده كرد و آنها را بعنوان «آنتيبيوتيكهاي زنده»[24]مطرح ميسازد (R. Elizabeth socket et al., 2004).
چندين مطالعه بر روي دلوويبريوها نشان ميدهد كه اين باكتري ميتواند بر روي بسياري از باكتريهاي پاتوژن انساني مثل اشرشــــــــــــــياكلي و سالمونلا و لژيونلا[25] اثر كند (Richordson I. R., 1990).
يك گروه در فرانسه استفاده از دلوويبريو را در درمان بيماري گاستريت بطور برجستهاي نشان دادند (Markelova, N. Y., 2010). مطالعات دو سال گذشته دلوويبريوها بر روي حيوانات ميزبان مثل گاو، جوجه و ارزيابي تأثيرات اين باكتري بر روي پاتوژنهاي مختلفي از جمله هليكوباكتر پيلوري و سالمونلا و پاتوژنهاي دهــــــــــــــــــــــــــــــــاني مثل پروفيروموناس ژينژيواليس[26] (Boileau, M. j., and clinken beard, K. D., 2011) نشان داده كه از باكتريووروس ميتوان به عنوان يك عامل آنتيباكتريال در محيط، صنعت و پزشكي در آينده نگاه كرد.
باكتريهاي بيماريزاي مورد حمله دلوويبريو
از باكتري دلوويبريو باكتريووروس ميتوان براي حمله به بسياري از باكتريهاي گرم منفي استفاده كرد؛ براي مثال از دلوويبريو j 109 ميتوان براي حمله به باكتريهاي اشرشيا[27] و سودوموناس[28] و اسپريليوم[29] استفاده كرد، همچنين مطالعات گروه كادوري[30] نشان داده كه از همين استرين ميتوان در حمله به پاتوژنهاي ديگري مانند اسينتوباكتر[31] و آئروموناس[32] و بردتلا[33] و بورخلدريا[34]و سيتروباكتر[35] و انتروباكتر[36] و كلبسيلا[37] و مورگانلا[38] و پروتئوس[39] و سراشيا[40] و سالمونلا[41] و شيگلا[42]و ويبريو[43]و يرسينيا[44] بهره برد (Dashiff, A, et al, 2011).
اگرچه طبق نتايج بدست آمده دلوويبريو j 109 نميتواند به كمپيلوباكتر[45]حمله كند، ولي بر اساس مطالعات انجام شده بوسيله ماركلووا[46] نشان داده شده كه استرين ديگري از دلوويبريو بنام 100 NCB ميتوانـــــــــد به كمپيلوباكتر ژوژني و هليـــــــــــــــــكوباكترپيلوري[47] حمله كند (Markelova, and kerzhentser, 2010).
مطالعات و تكنيكهاي مختلف نشان داده كه دلوويبريوها هيچ زياني براي انسان و حيوان ندارند. در سال 1973 مطالعات انجام شده بوسيله وركلووا نشان داد كه دلوويبريو نميتواند اثرات بيماريزايي بر روي موش، خرگوش و خوكچه هندي داشته باشد (Verklova Z. S., 1973). وي به وسيله وارد كردن استرينهاي مختلف از باكتريهاي شكارچي به درون فضاي سيتوپلاسمي سلول تخم خرگوش و ارزيابي اينكه آيا اين باكتريها ميتوانند در صورت ورود به اين فضا در آنجا رشد كنند، نشان داد كه اين باكــــــــــــــــــــــــتريها هيچگونه رشد قابل تشخيصي بعد از 18 ساعت نداشتهاند (Lenz, R. W. and Hespell, R. B, 1978).
استفاده از دلوويبريوها در مصارف غيرپزشكي
در يكي از اين مطالعات نشان داده شده است كه دلوويبريو را ميتوان در صنايع غذايي بكار برد و با اضافه كردن آن به مواد غذايي كنسروي از بروز و افزايش درصد مسموميتهاي غذايي جلوگيري كرد.
كشاورزي
دلوويبريو همچنين شكارچي تــــعداد زيادي از پاتــــــــــــــــوژنهاي گياهي است (jukevitch,E, Minz, D,. Et al, 2000). اولين كوششها در كاربرد دلوويبريو در بيماريهاي گياهي و كنترل آنها بوسيله شرف[48] در سال 1973 انجام گرفت (Scherff, R, H, 1973). در اين مطالعه دلوويبريو استرين Bd – 17 كه از ناحيه ريزوسفر[49] ريشه گياه سويا جدا شده بود براي كنترل بيماري ناشي از سودوموناس گليسينا[50] بكار رفت. نتيجه نشان داد كه Bd-17 توانايي جلوگيري از رشد بيماري گياهي را دارا ميباشد.
ايمنيزايي دلوويبريوها
مطالعات ايمني بر روي دلوويبريوها نشان دهنده آيندهاي اميدبخش است؛ اولاً مطالعات انجام شده بر روي لايه ليپوپليساكاريد اين باكتريها نشان داده كه آن يك لايه منحصر بفرد ليپيد A ميباشد كه به جاي آلفا–دي– مانوز[51] گروههاي فسفات قرار گرفته و باعث ميشود كه هيچگونه شارژ منفي اين گروهها نداشته باشند، نهايتاً اين باكتريها كمترين گرايش اتصال به رسپتورهاي ليپو پليساكاريدي[52] در سلولهاي انساني را دارا ميباشند و از آن بهتر كمترين خاصيت فعاليت اندوتوكسيني را در مقايسه با اشرشياكلي[53] دارا ميباشند و در آخر اين مسئله با پايين بودن سطح TNF-a و IL– 6 ترشح شده از ماكروفاژهاي انساني مورد تأييد قرار گرفته است.
در آخرين مرحله، مطالعات انجام شده بر روي اين باكتريها اين نكته بزرگ را مورد توجه قرار ميدهد كه اين باكتريها داراي خاصيت بيماريزايي و سمي براي انسان و حيوان نميباشند.
توانايي حمله دلوويبريو به بيوفيلم
در حدود %80 از بيماريهاي مزمن التهابي باكتريايي و بيماريهاي عفوني در اثر بيوفيلم در انسان بوجود ميآيد (Wood, T. K, et al, 2011) كه اينها شامل بيوفيلمهايي است كه بوسيله يوروپاتوژنيك اشرشياكلي در عفونتهاي ادراري و انتروهموراژيك E-coli در عفونت گاسترواينتستينال و زخم و سوختگي و عفونت دستگاه تنفسي در اثر سودوموناس آئروژينوزا[54] ايجاد ميشوند.
عموماً مشكل اصلي در اين بيماريها ايجاد بيوفيلم توسط اين باكتريها در عضو درگير ميباشد كه اين بيوفيلم باعث محافـــــــــــــــــظت خوب در برابر درمانهاي آنتيبيوتيكي ميشود (Stewart, P. S. and costerton, J. W. , 2001).
يكي از شاخصهاي مــــهم دلوويبريو توانايي حـــــــــــــــــــــــمله به بيوفيلم است (Kedouri, D. and O’Tool, G. A.,2005) كه ميتواند بدين وسيله باعث كاهش باكتريها شود. مطالعه ديگري نيز كه بوسيله همين گروه انجام شده درباره حمله باكترويووروس[55] به بيوفيلم ايجاد شده توسط باكتريهاي حفره دهان ميباشد. مورد ديگر كه ميتوان مورد توجه قرار داد استفاده از اين باكتريها در درمان بيــــــــــــــماريهايي است كه بصورت عفونتهاي مخلوط[56] ميباشند (Aaron, et al., K. , 2007).
استفاده از دلوويبريو در صنايع غذايي[57]
استفاده از دلوويبريو در حيوانات: اخيراً استفاده از اين باكتريها در صنعت مرغداري مورد توجه قرار گرفته است و ميتوان از اين باكتريها به جاي استفاده از آنتيبيوتيكها به عنوان يك پروبيوتيك استفاده كرد (Atterbury, R. J., Hobley L., 2011).
بوسيله دلوويبريو استرين (Bdc-1) ميتـــوان از عفونت ماهيها در استخرها توسط A.hydrophiliaj-1 جلوگيري كرد (chu, w. H. and Zhu, w. , 2010).
نتيجهگيري
تمامي اين نتايج نشان ميدهد كه استفاده از دلوويبريوها به عنوان يك عامل آنتيباكتريال نه تنها در پزشكي بلكه در بسياري از صنايع و موارد و موضوعات محيطي ميتواند مورد توجه قرار گيرد.
همچنين ميتوان از اين باكتريها در صنايع غذايي و موارد صنعتي به عنوان آنتيبيوتيك و پروبيوتيك استفاده كرد.
:References
1-Aaron, S. D., Denis, M.S., Ramotar, K., et al (2007) infection with Burkhoderia cepacia complex bacteri and pulmonary exacerbation of cystic fibrosis.chest 131, 1188 – 1196.
2-Atterburg, R.j., Hobley, L. et al (2011) effect of oraly Adminsteread Bdellovibrio bacterio vorus on the well – Being and salmonella calonization of young chicks. Appl. Environ. Microb . 77, 5794-5803.
3-Boileau, M. j. and clinkenbeard, K. D. (2011) Assesment of Bdellovibrio bacteriovorus 109j viability in bovin tears. j. Vet. Intern. Med. 25, 759-760.
4-Burnham, J. C., hashimoto, T. Conti, S. F. (1968) Electron microscopic observation on the penetration of Bdellovibrio bacteriovorus in to gram negative bacterial host. J, Bacterial 96, 1366-81.
5-Chu, W. H. and Zhu, W. (2010) isolation of Bdellovibrio as biological Therapeutic agent used for the treatment of Aeromonas hydrophilia infection in fish. Zoonoses public Hlth. 57, 258-264.
6-Dashiff, A. , Junka, R. A., Libera, M. and kadouri, D. E. (2011) predation of human pathogens by the predatory bacteria Micavibrio aeruginosavorus and Bdellovibrio bacteriovorus. Appl. Environ. Microb. 77, 2224-2231.
7-Evans et al, (2007) predation by Bdellovibrio bacteriovorus HD 100 requires type IV pili.
8-Jukevitch, E., Mins, D., Ramati, B. et al (2000) prey Range characterization ribo typing. Appl Environ Microbiol66, 2365 – 71.
9-Kadouri, D. and O’Toole, G. A. (2005) Susceptibility of biofilms to Bdellovibrio bacteriovorus attack. Appl. Environ. Microb. 71, 4044-4051.
10-Kessel and varon, M. (1973) Development of bdellophage Vl – 1 in parasitic and saprophytic bdellovibrios.
11-Lambert, C., et al. (2006) characterizing the flagellar filament and the role of Motility in bacterial prey – penetration by Bdellovibrio bacteriovorus.
12-Lenz, R. W. and Hespell, R. B. (1978) Attempts to Growth Bdellovibrios Micurgically- injected in to Animal- cells. Arch. Microbiol. 119, 245-248.
13-Mar Kelova, N. Y. and kerzhentsev, A. S. (2010) interaction of Bdellovibrio bacteriovorus with bacteria campylobacter jejuni and helicobacter pylori. Microbiology 79, 777-779.
14-R. Elizabeth socket and carey Lambert (2004) Bdellovibrio as therapeutic agent: a predatory renaissance? Nature reviews, Microbioloy Vol 2 Agust 2004- 669-675.
15-Rendulic et al. (2004) A predator unmasked: Life cycle of Bdellovibrio bacteriovorus from a genomic perspective.
16-Richardson, I. R. (1990) the incidence of Bdellovibrio spp. In man – made water systems. J Appl Bacteriol 69,134-40.
17-Scherff, R. H. (1973) control of bacterial Blight of soybean by Bdellovibrio – bacteriovorus. Phytopathology 63, 400-402.
18-Schwudke, D. et al (2003) the obligate predatory Bdellovibrio bacteriovorus. The j. Biol. Chem. 278, 27502 – 27512.
19- Stewart, P. S. and costerton, j.w. (2001) Antibiotic resistance of bacteria in biofilms. Lancet 358-138.
20- STolp, H. and starr, M. D. (1963) Bdellovibrio Bacteriovorus Gen. Et sp. N., a predatory, Ectoparasitic, and bacteriolytic Microorganism.
21- Straley, S. C. and Conti, S. F. (1977) Chemotaxis in Bdellovibrio bacteriovorus.
22- Strarr and baigent, N. L. (1966) parasitic interaction of Bdellovibrio bacteriovorus with other bacteria.
23- THomashow, M. F. and Ritten berg, S. C. (1978) Intraperiplasmic growth of Bdellovibrio bacteriovorus 109 j, j. Bacteriol. 133, 1484-1491.
24- Verklova, I. S. (1973) A Study of virulence toxicity and immunogenicity of various strain of Bdellobivrio bacteriovorus. Gig. Sanit. 38,4.
25- Wood, T. K., Hong, S. H. and Ma, Q. (2011) Engineering biofilm formation and dispersal. Trend. Biotechnol. 29, 87-94.
[1] – Bdellovibrio bacteriovorus
[2] – delta proteobacteria
[3] – attack phase , Growth phase
[4] – (biphasic life – cycle)
[5] – (attack – phase)
[6] – (growth – phase)
[7] – Stolp
[8] – Starr
[9] – bdelloplast
[10] – attack – phase
[11] – B. bacteriovorus
[12]– hydrolytic enzymes
[13] – Bdelloplast
[14] – recognition
[15] – B. heateriovous
[16] – Type IV pili
[17] – Growth phase
[18] – bdelloplast
[19] – Kessel و Varon
[20] – Growth phase – Bdellovibrio septation
4-(Corksrew)
[22] – Bdelloplast lysis
[23] – Bdelloplast lysis
[24] – living antibiotic
[25] – E. coli , Salmonella , Legionella
[26] – prophyromonas gingivalis
[27] – Eshcherichia
[28] – Pseudomonas
[29] – spirillum
[30] – Kadouri
[31] – Acintobacter
[32] – Aeromonas
[33] – Bordetella
[34] – Burkholderia
[35] – Citrobacter
[36] – Enterobacter
[37] – Klebsiella
[38] – Morganella
[39] – Proteus
[40] – Serratia
[41] – Salmonella
[42] – Shigella
[43] – Vibrio
[44] – Yersinia
[45] – Campylobacter
[46] – Markelova
[47] – C. Jejuni و H. Pylori
[48] – Scherff
[49] – rhizosphere
[50] – glycinea
[51] – a-D- mannose
[52] – LPS
[53] – E-coli
[54] – P. aeroginosa
[55] – B. bacteriovorus
[56] -(Mixed infection)
[57] – Food Industry
برای دانلود پی دی اف بر روی لینک زیر کلیک کنید
ورود / ثبت نام