ابتلا به کووید 19 در زمینه بیماریهای التهابی آتوایمیون
دکتر حبیباله گلافشان1، پریسا تندل2
1– هیئت علمی دانشکده پیراپزشکی دانشگاه علوم پزشکی شیراز
2-کارشناسی ارشد خونشناسی آزمایشگاهی و بانک خون دانشکده پیراپزشکی دانشگاه علوم پزشکی شیراز
سندرم نارسایی حاد تنفسی و نارسایی حاد چند ارگانه از مهمترین عوامل مرگومیر در مبتلایان به کووید 19 (SARS.COV-2) است. گرچه شیوع بالا و غیرمعمول اختلالات ترومبوتیک مشاهده میگردد، ولی چگونگی سازوکار آن در رابطه با ویروس کووید هنوز مبهم است. گزارشهای زیادی از همراهی سندرم ضد فسفولیپید با آلودگیهای ویروسی به ویژه HIV، HBV، HCV و EBV و پاروویروس 19 B وجود دارد.
سندرم ضد فسفولیپید یک بیماری آتوایمیون با عیار بالای آنتیبادیهای ضد فسفولیپیدی بهصورت طولانی مدت و مستعد به ترومبوآمبولی مکرر شریانی و وریدی است. آزمایشهای استاندارد که در گروه معیارهای تشخیصی هستند شامل ACLA و Antiβ2 GPI و LA است. جالب اینکه آنتیبادیهای ضد فسفولیپیدی در یک تا 5% جمعیت نرمال به ویژه افراد مسن با بیماریهای مزمن مشاهده شدهاند. سندرم ضد فسفولیپید داری علائم بالینی بسیار ناهمگون است و از بدون علائم تا ترومبوز ناگهانی عروق بزرگ و ترومبوز میکرو واسکولار پیشرونده و تهدید به مرگ جلوه میکند. نوع نادر و شدید آن سندرم فاجعهبار ضد فسفولیپید است که در کوتاهمدت با نارسایی چند ارگانه و انسداد مویرگی و با عیار بالای آنتیبادی ضد فسفولیپیدی ظاهر میشود. در حدود 50% موارد، عامل شروعکننده، عفونتهای ویروسی یا میکروبی و جراحی و بدخیمیها هستند.
آنکسین 5 لایه محافظتی بر روی سطح سلولهای اندوتلیال است. این پروتئین با پیوند به فسفولیپیدهای شارژ منفی، مانع از گردهمایی فاکتورهای فعال انعقادی بر سطح فسفولیپیدهای با شارژ منفی میگردد که نتیجه آن جلوگیری از لخته شدن خون است. آنتیبادیهای ضد فسفولیپیدی با تخریب آنکسین 5 روی سلولهای اندوتلیال و جفت، موجب لختگی در عروق میگردند. گفتنی است CRP(C-reactive protein) شبیه آنکسین دارای میل ترکیبی برای فسفولیپیدها به ویژه فسفاتیدیل کولین (PC) است که مهمترین لیگاند آن است. البته CRP با فسفولیپیدهای دیگر مانند فسفاتیدیل اتانول آمین (PE) نیز میتواند پیوند دهد.
آنتی 2 β گلیکوپروتئین (Anti β2 GPI) I نوعی آنتیبادی در پلاسماست که با اپیتوپهایβ2 GPI واکنش میدهد. این پروتئین تمایل بسیاری برای پیوند به فسفولیپیدهایی با شارژ منفی دارد. آنتیبادیهای ضد فسفولیپیدی، ایمونوگلوبولینهایی از جنس IgG یا IgM هستند که اغلب علیه فسفولیپیدها فعالیت نمیکنند، بلکه با پروتئینهایی که به فسفولیپیدهایی با شارژ منفی پیوند دادهاند، واکنش میدهند که در میان آنها، میتوان به پروتئینهای β2 GPI، پروترومبین، پروتئین C، پروتئینS، فاکتور ۵، آنکسین A2 (آنکسین II) و آنکسین A5 اشاره کرد. بیشترین تارگت آنتیژنی این آنتیبادیها، β2 GPI و پروترومبین است.
CRP یک پروتئین فاز حاد است که نهتنها در مبتلایان به کووید بلکه در پروسههای التهابی تحت اثر اینترلوکین 6 از کبد ترشح میشود و غلظت آن با وسعت التهاب رابطه مستقیم دارد. اتصال CRP به فسفولیپیدهای شارژ منفی، تستهای انعقادی به ویژه آزمایشهای aPPT و LAC (بازدارنده لوپوس) را تحت تأثیر قرار داده و باعث جلوگیری از تجمع فاکتورهای فعال انعقادی بر سطح فسفولیپیدها گشته و بهطور کاذب موجب طولانی شدن تستهای PTT-LA و Staclot-LA میگردد. آزمایشهای فوق برای تشخیص بازدارنده لوپوس (LA) به کار میروند که بهطور معمول از فسفولیپیدهایی در تست استفاده میشود که حساس به حضور CRP در پلاسما هستند. از طرف دیگر حضور CRP میتواند آزمایش PTT را در رابطه با نوع فسفولیپید بهکار گرفتهشده در تست، بهطور کاذب طولانی کند. آزمایش بازدارنده لوپوس (LAC) بر پایه آزمایش dRVVT (آزمایش سم افعی رقیقشده) کمتر تحت اثر CRP قرار میگیرد.
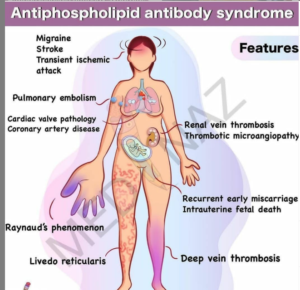
علائم بالینی مرتبط با سندرم ضد فسفولیپید
- سیستم عروقی: ترومبوز سیستم عروقی؛
- اختلالات حاملگی: سقط مکرر، پره اکلامپسی، جدا شدن نابهنگام جفت، تولد نوزاد نارس، عقبافتادگی رشد جنینی؛
- نورولوژیک: سکته، حملات ایسکمی موقت، میگرن، تشنج، کرهآ، سندرم گیلن باره، نوروپاتی؛
- سیستم قلبی عروقی: انسداد ترومبوتیک عروق کرونر، سکته، آترواسکلروز زودرس، اختلال دریچهای؛
- سیستم گردش خون: ترومبوسیتوپنی، کاهش پروترومبین، کاهش پروتئین S، مقاومت به پروتئین C فعال، حضور بازدارندههای انعقاد؛
- ریوی: افزایش فشار ریوی ناشی از انسداد عروقی؛
- کلیوی: ترومبوز ورید یا سرخرگ کلیه، گلومرولونفریت؛
- پوستی: زخمهای پوستی بهعلت نکروز ناشی از انسداد مویرگی، لیویدو رتیکولاریس، بثورات قرمز، نوجولهای دردناک، لوپوس دیسکوئید؛
- چشمی: نوروپاتی اپتیک، انسداد عروق شبکیه، ایسکمی و اختلال موقتی در دید؛
- شکمی: نکروز مری با پارگی، ایسکمی روده، انسداد عروق صفراوی، انسداد عروق مزنتریک، سیروز صفراوی؛
بیماریهای آتوایمیون التهابی روماتیسمی فاکتورهای خطر بیشتری در ابتلا به کووید دارند. شانس 46% بستری و مرگومیر 9 درصدی در میان بیماران مبتلا به لوپوس و واسکولیت گزارش گردیده است. علاوه بر بیماریهای قلبی عروقی و سن بالا، فاکتورهایی از قبیل درمان با گلوکواستروئید بیشتر از 10 میلیگرم در روز و تجویز ریتاکسی ماب (Rituximab) و سایر سرکوبگرهای ایمنی در ارتباط با مرگومیر و ترومبوآمبولی وریدی بوده است.
در گزارش دیگر، مصرف استروئیدها، مایکوفنولیت (Mycophenolate mofetil) و ریتاکسی ماب در ارتباط با شدت بیماری کووید بوده است. ارتباط بین لوپوس و شدت بیماری کووید در سطح پاتولوژی مربوط به اختلال در پاسخ تایپ یک اینترفرون گزارش گردیده است.
آنتیبادیهای خنثیکننده علیه تایپ یک اینترفرون در بیماری شدید کووید 19 و برخی از بیماران مبتلا به لوپوس مشاهده شده است در حالی که در شخص مبتلای بدون علامت یا علائم خفیف گزارش نشده است و این ممکن است آسیبپذیری بیماران لوپوس در برابر ابتلا به کووید را مطرح کند. عفونت با کووید 19 نهتنها موجب القای تولید آنتیبادیهای ضد فسفولیپیدی میگردد، بلکه موجب شعلهور شدن سندرم ضد فسفولیپید در بیماران بدون علامت نیز میشود و اینکه آیا واکسیناسیون قادر به تولید و یا علامتدار کردن سندرم ضد فسفولیپید است و اینکه آیا فرد قبل از واکسینه شدن لزومی به چک کردن آنتیبادیهای ضد فسفولیپیدی دارد، مورد پرسش است.
دوره شدید بیماری کووید 19 علاوه بر بیماریهای لوپوس (SLE) در (PSS (Primary systemic sclerosis پیشرونده و گرانولوماتوز پلیآنژیت (Polyangiitis) به علت بیماری زمینهای ریوی و درمان با استروئید و ریتوکسی ماب مشاهده شده است. ریزش طولانی مدت ویروس زنده در ترشحات تنفسی بیماران با کاهش ایمنی ارثی هومورال و سلولار، بیماران با مصرف داروهای سرکوبکننده ایمنی و بیماران با پیوند کلیه مشاهده گردیده و از این رو دوره قرنطینه را بایستی با توجه به نوع بیماری زمینه تنظیم کرد. اختلالات ارثی و اکتسابی اینترفرون (Interferonopathies) با بیماری شدید و طولانیتر کووید همراه است.
عفونت با کووید 19 گاهی همراه با یک سری علائم روماتیسمی است که در این میان میتوان شایعترین آنها از قبیل میالژی و خستگی را نام برد. گزارشهای موردی از بیماری گیلن باره (Guillain-Barre) و انسفالیت در مبتلایان و شبه کاواساکی در بچهها مشاهده شده است و گزارشهایی از مثبت شدن آزمایشهای ANA و Anti SSA و آنتی فسفولیپید در دست است. پاسخ هومورال و سلولار در پی واکسیناسیون بیماران با زمینه آتوایمیون التهابی بهجز در بیماری که دوز بالای استروئید و یا ریتوکسی ماب استفاده میکند شبیه به جمعیت عادی است و سفارش میشود که 6 ماه بعد از آخرین تزریق ریتوکسی ماب واکسن کووید تزریق شود تا از پاسخ ایمنی مناسب اطمینان حاصل گردد.
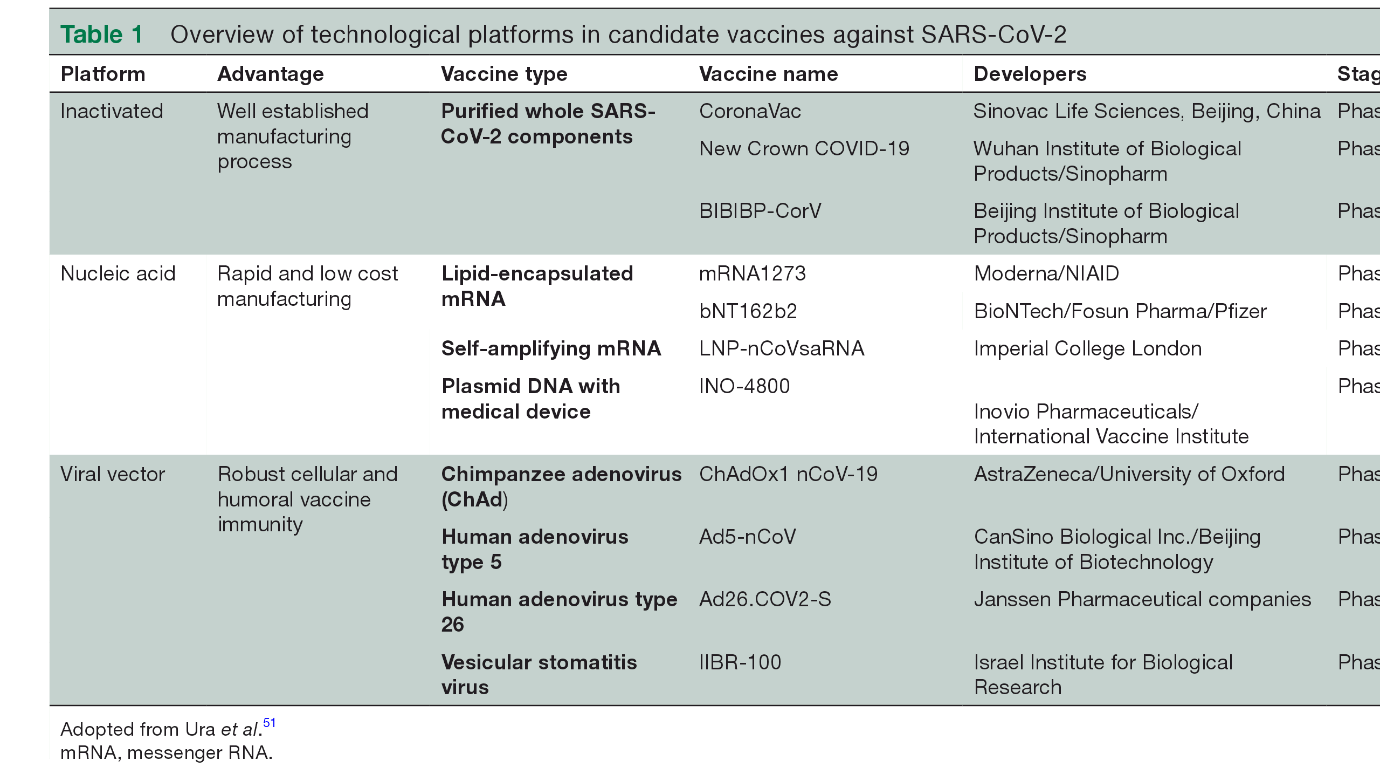
دورههای واکسنهای کووید را باید بهتنهایی تزریق کرد و چنانچه نیاز به تزریق واکسن دیگر از قبیل آنفلوانزا و استرب پنومونی باشد، حداقل 14 روز بایستی فاصلهدار باشد. تزریق واکسنهای ویروس کشته و بر پایه mRNA برای این دسته از بیماران سودمند است.
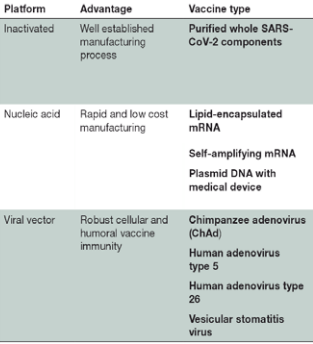
پلتفرمهای رایج واکسن کووید 19
اختلالات انعقادی ترومبوتیک در مبتلایان به نوع شدید بیماری کووید 19 شبیه به سندرم آنتی فسفولیپید فاجعهبار (CAPL) است. کاهش لنفوسیتهای T هلپر و ترومبوسایتوپنی و افزایش دایمر D ولی با افزایش فیبرینوژن شباهت به سندرم ضد فسفولیپید فاجعهبار در ترومبوتیک میکروآنژیوپاتی دارد.
از سازوکارهای کلیدی که ممکن است در پاتوفیزیولوژی آسیبهای چند ارگانه خارج از ریوی در ابتلا به کووید 19 نقش داشته باشند میتوان به اثرات سمی مستقیم ویروس، آسیب به سلولهای اندوتلیال، التهاب ترومبوتیک، رها شدن سیستمیک سایتوکاینها و واسطههای التهابی و از تنظیم خارج کردن سیستم ایمنی و محور رنین-آنژیوتنسین-آلدوسترون نام برد
در بیش از 60% موارد ابتلا به کووید 19، افزایش شدید فریتین (Hyperferritinemia) مشاهده شده است و این اساس کاربرد داروی Tocilizumab (مهارکننده گیرنده اینترلوکین 6) برای مهار طوفان سایتوکاینهاست. جالب اینکه افزایش فریتین در سندرم ضد فسفولیپید فاجعهبار، عفونتهای خون، سندرم تحریک ماکروفاژها و بیماری استیل مشاهده شده است. این پروتئین فاز حاد با القای بیان واسطههای التهابی دیگر مانند IL-1β، موجب خیز مجدد افزایش فریتین میگردد. سکته قلبی و پوشش فیبرینی دریچههای قلب (Vegetation) در کووید 19 شبیه به سندرم ضد فسفولیپید مشاهده گردیده است. در حدود 20 تا 30 درصد بیماران، افزایش آنزیمهای قلبی و حتی الکتروکاردیوگرام با بلندی ( ST (ST elevation با آنژیوگرافی نرمال گزارش شده است.
شباهتهای سندرم ضد فسفو لیپید فاجعهبار با بیماری شدید کووید 19
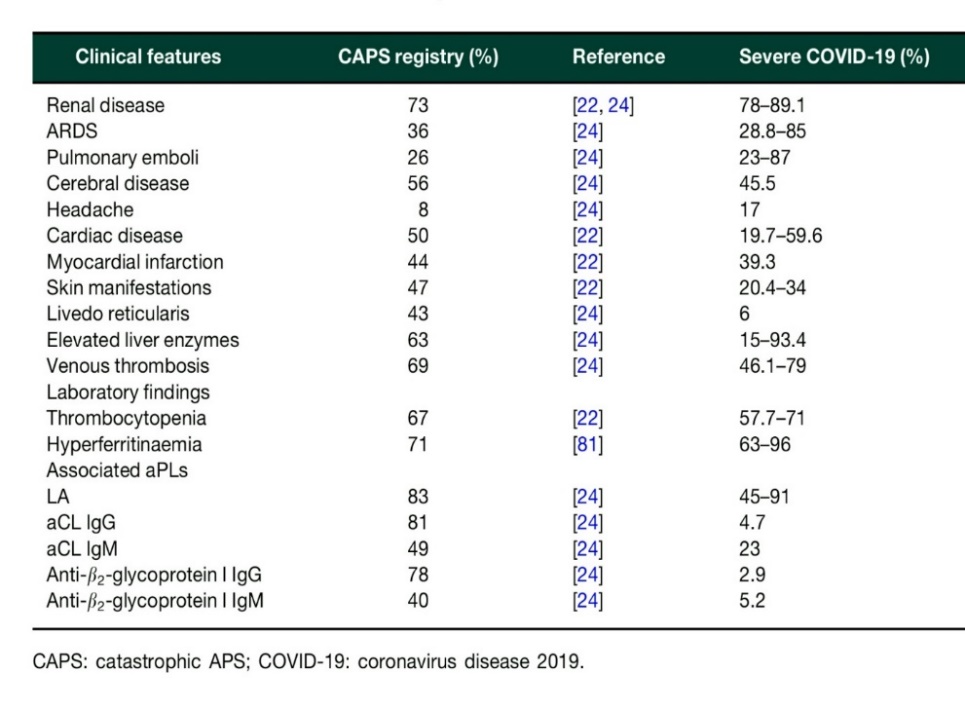
بنظر میرسد که از نقطهنظر پاتولوژی بالینی، شباهتهایی بین سندرم ضد فسفولیپید فاجعهبار (CAPS) و بیماری شدید کووید 19 وجود دارد و در این راستا تجویز ضد انعقادها سنگ بنای درمان در پیشگیری از ترومبوز است و ممکن است آزمایشهای ضد فسفولیپید در بیماران کووید 19 برای جداسازی گروه پرخطر و کمخطر لازم باشد. جدول زیر علائم بالینی و آزمایشگاهی ثبتشده در کمیته بینالمللی سندرم آنتی فسفولیپید فاجعهبار (CAPS registry) و مقایسه آن با عفونت شدید کووید را نشان میدهد.
سندرم ضد فسفولیپید بسیار پیشرونده که با نارسایی چند ارگانی همراه است، با عنوان سندرم ضد فسفولیپید فاجعهبار نامگذاری شده است که حدود ۴۴ درصد منجر به مرگومیر میشود و در حدود یک درصد بیماران مبتلا به سندرم ضد فسفولیپید رخ میدهد. انسداد عروقی در حداقل سه ارگان یا بافت در طول یک هفته (طوفان ترومبوتیک) با آزمایشهای مثبت سندرم ضد فسفولیپید، از معیارهای حالت فاجعهآمیز است. طوفان سایتوکاینی موجب نارسایی حاد تنفسی در بیماران میشود. سندرم ضد فسفولیپید فاجعهبار باید از میکروآنژیوپاتی ترومبوتیک، ترومبوسیتوپنی ناشی از هپارین و سندرم هلپ افتراق داده شود به نظر میرسد که از نقطهنظر پاتولوژی بالینی شباهتهایی بین سندرم ضد فسفولیپید فاجعهبار (CAPS) و بیماری شدید کووید 19 با ترومبوز حاد وجود دارد
نکات قابل توجه، افزایش شدید فریتین، آزمایش بازدارنده لوپوس (LA) و نارسایی حاد چند ارگانه در هر دو مورد است. سندرم آنتی فسفولیپیدی فاجعهبار نوع نادر از تظاهرات سندرم ضد فسفولیپید است و نارسایی چند ارگانه در مدت کوتاه با هیستولوژی انسداد مویرگها و عیار بالای ضد فسفولیپید همراه است. در حدود 50% موارد، عامل شروعکننده عفونتهای میکروبی، ویروسی، جراحی و بیماریهای بدخیم بوده است. استرسهای اکسیداتیو، تولید سوپر اکسید، فعال شدن پلاکتها، تخریب لایه محافظتی انکسین 5 و کاهش فعالیت سیستم فیبرینولیتیک (Down regulation) در ایجاد ترومبوز نقش دارند.
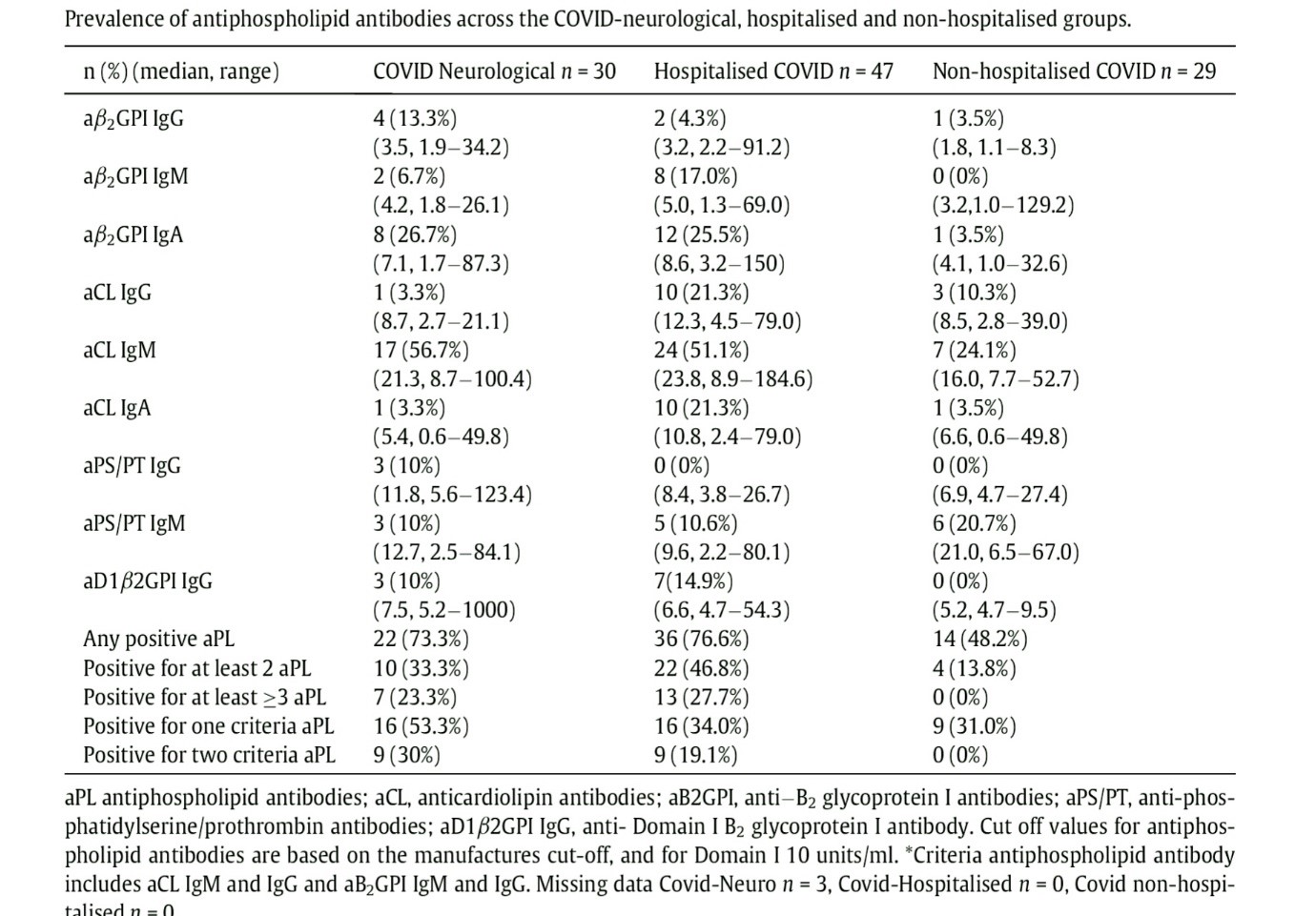
در یک مطالعه مقطعی (Cross sectional) که بر روی 30 بیمار مبتلا به کووید با علامت نورولوژیک و 47 بیمار بستری بدون علائم نورولوژیک و 29 بیمار مبتلا بدون علامت صورت گرفته، شیوع آنتیبادیهای ضد فسفولیپیدی در مبتلایان به کووید در گروه با علائم نورولوژی و بستری به شرح زیر بوده است:
ACLA IgM > aβ2 GPI > aPS/PT IgM > aD1 β2 GPI
آزمایش ACLA به مفهوم آنتیکاردیولیپین، آنتی β2 گلیکوپروتئین I، آنتیبادی علیه فسفاتیدیل سرین و پروترومبین و آنتیبادی علیه میدان D1 از β2GPI است.
آزمایش مثبت با عیار بالا از نوع IgG و IgA در بیماران بستری مبتلا به کووید 19 با افزایش انعقادپذیری و افزایش دایمر D، درگیری تنفسی و کلیه و افزایش کراتینین همراهی داشته است.
آنتیبادی علیه فسفاتیدیل سرین، واکنش متقاطع با مایلین داشته و افزایش عیار آن در بیماران با علامت نورولوژیک مشاهده شده است.
انسفالیت یا التهاب و تورم بافت مغز توسط ویروس یا واکنشهای ایمونولوژیک
انسفالیت یا التهاب و تورم بافت مغز توسط ویروس یا واکنشهای ایمونولوژیک با علائم سردرد، سفتی گردن، گیجی و تشنج و آنسفالوپاتی با تغییرات رفتاری، عدم تمرکز و حرکات غیر ارادی و آنسفالومیلیت (Encephalomyelitis) با حمله التهابی به مغز و طناب نخاعی و تخریب بافت مایلین از علائم نورولوژیک کووید 19 مشاهده شده است.
جداول زیر حاصل مطالعه مقطعی بیماران مبتلا به کووید 19 از نظر علائم بالینی و آزمایشهای ضد فسفولیپیدی را نشان میدهد:
شیوع آنتیبادیهای ضد فسفولیپیدی در اختلالات نورولوژیک ناشی از ابتلا به کووید 19 در یک مطالعه مقطعی
Refrences:
1-Katrien M.J. Devreese*, Charlotte J. Verfaillie, Frank De Bisschop and Joris R. Delanghe Interference of C-reactive protein with clotting Time
2-Point of view on the vaccination against COVID-19 in patients with autoimmune inflammatory rheumatic diseases Victoria Furer, Christien Rondaan,3 Nancy Agmon-Levin,
3-Antiphospholipid antibodies and neurological manifestations in acute
COVID-19: A single-centre cross-sectional study Laura A. Benjamin,Ross W. Paterson,Rachel Moll, Charis Pericleous\
4-Assessment of Lupus Anticoagulant Positivity in Patients With Coronavirus Disease 2019 (COVID-19) Morayma Reyes Gil, MD, PhD.
5-Thrombosis Research Lupus Anticoagulant (LAC) testing in patients with inflammatory status: Does C-reactive protein interfere with LAC test results?
6-Extrapulmonary manifestations of COVID-19 Nature Medicine | VOL 26 | July 2020 | 1017–1032 | www.nature.com/naturemedicine
برای دانلود پی دی اف بر روی لینک زیر کلیک کنید
ورود / ثبت نام