تشخیص آزمایشگاهی آسپرژیلوزیس تهاجمی
دكتر سهیلا محمودپور1، روژین جمشیدی2*، فرزانه ناطقی3، صادق خداويسي4
1. مسئول فنی آزمایشگاه تشخیص طبی پاستور، دانشگاه علوم پزشكي کردستان
2. دانشجوي كارشناسي علوم آزمایشگاهی، دانشگاه آزاد اسلامی بروجرد
3. دانشجوي كارشناسي ارشد میکروب شناسی، دانشگاه آزاد اسلامی ورامین
4. دانشجوي دکترای تخصصی قارچ شناسی پزشکی، دانشگاه علوم پزشكي تهران
مقدمه
آسپرژیلوس از قارچهای رشتهای با انتشار بسیار وسیع در طبیعت است. مطالعات صورت گرفته در این زمینه توزیع وسیعی از گونههای این قارچ بخصوص گونه آسپرژیلوس فومیگاتوس و فلاووس در محیطهای مختلف مثل وسایل و تجهیزات بیمارستانی و خاک گلدانهای موجود در بیمارستانها را نشان داده است. آسپرژیلوزيس تهاجمی (IA)[1] بیماری شدید و کشنده ناشی از گونههای مختلف قارچ فرصت طلب آسپرژیلوس ميباشد. این بیماری با میزان مرگ و مير بسيار بالا در بيماران با ضعف در سيستم ايمني مثل بیماران دچار نوتروپنی شدید، گرانولوماتوز مزمن، بدخیمیهای خونی، دریافت کنندگان پیوند مغز استخوان، سلولهای بنیادی و ساير بافتها، دریافت کنندگان داروهای استروئیدی و آنتیبیوتیکهاي وسیعالطیف به مدت طولانی مشاهده میشود.
بیماران در بخشهای اونکولوژی و ICU از طریق منابع مختلفی بخصوص از طریق دستگاه تنفسی در تماس با گونههای قارچی میباشند که در صورت عدم پیشگیری و تشخیص و درمان به موقع، منجر به پیشرفت بیماری در این بیماران میشود. بقای بيماران مبتلا به این بیماری به طور کلی کم و در حدود 50-30% است که اكثراً بعلت عدم تشخیص بیماری در مراحل اوليه آلودگی و عدم شروع زود هنگام درمانهاي ضد قارچي براي بهبود وضعيت بیماران است، لذا در این مقاله سعي شده تا سودمندی و محدودیتهاي روشهای رایج و در دسترس جهت تشخيص بیماری IA مورد بررسی قرار گيرد.
روشهای تشخیصی:
براي تشخیص به موقع IA در بیماران مبتلا باید از ترکیبی از علائم بالینی، فاکتورهای خطر و روشهای تشخیصی استفاده شود. با توجه به اینکه علائم بالینی مرتبط با IA اختصاصي نبوده و به همین خاطر پزشكان به تكنيكهای تشحیصی معتبر و باارزش براي مراقبت صحيح و درمان بيماران آلوده نيازمند هستند، روشهاي مختلف كشتي و راههاي سريع غير كشتي برای تشخیص بیماری IA به كار برده ميشوند.
علائم باليني IA شامل وجود تب، افزايش ترشحات تنفسي، افزايش نياز به اكسيژن و خلط خوني ميباشد كه اختصاصي بيماري نيست، همچنین تشخيص بيماري با استفاده از تصاوير راديولوژي نیز در اثر تظاهرات غيرطبيعي مثل آتلاكتازي و همچنين تنفس مصنوعي در اكثر بيماران محدود بوده و علائم اختصاصی در سیتیاسکن مثل creasent sign air و halo sign كه بيشتر در بيماران داراي نوتروپني نیز مشاهده ميشود داراي حساسيت كم و حدود 5% ميباشد. استفاده روتين از این روشها در مراحل ابتدايي IA جهت تشخيص اوليه و همچنین نشاندادن فرآيند بهبودي در بيماران لازم است و محل عارضه برای انجام برونكوسكوپي و بيوپسي از ريه مفيد ميباشد.
به دلیل تمایل تهاجم آسپرژیلوس به رگهای خونی و انتشار بیماری و در صورت درگیری احتمالی سیستم اعصاب مرکزی نیز میتوان از تکنیکهای CT و MRI[2] جهت بررسی انتشار بیماری به مغز استفاده نمود. روشهاي تشخیصي بررسي هیستوپاتولوژیک نمونههای بافتي (روش استاندارد طلايي[3]) نیز با مشاهده هایفهای با انشعابات دارای زاویه حاد و دارای دیواره عرضی، بدون پیگمان و تقریباً با قطر 3 میلیمتر در نمونههاي بافتي همراه با نتايج مثبت كشت از لحاظ گونههاي آسپرژيلوس تائيدكننده IA ميباشد، ولی استفاده از این روشها بعلت وضعیتهاي زمينهاي بیماران مثل ترومبوسیتوپنی و شرایط وخیم کلینیکی كه مانع استفاده از روشهاي تهاجمی مثل بيوپسي میشود غیرعملی است.
كشت مثبت در تشخیص IA بسیار کمک کننده بوده و اغلب اولین کلید تشخیصی در بیماران با وضعیت وخیم میباشد. جدا کردن گونههای آسپرژیلوس از نمونههای به دست آمده از سیستم تنفسی بیماران، بغیر از آلودگیهای احتمالی در حین نمونهگیری میتواند به سه صورت نشان دهنده بیماری واقعی، وجود یک کلونیزاسیون و یا اینکه نشانهای از وجود یک بیماری تهاجمی در نظر گرفته شود. اين روش قادر به تفريق بين فرمهاي تهاجمي و كلونيزاسيون از هم نبوده و ارزش اخباري مثبت آن نيز متفاوت بوده و بیشتر بستگي به وضعيت سيستم ايمني بيمار دارد؛ بعنوان مثال در بيماران فاقد نوتروپني از 20% تا 60% ميباشد. زمان مورد نياز براي بررسي اكثر كشتها حداقل 48 ساعت است كه جهت تشخيص بيماري به صورت سریع و در مراحل اوليه بیماری مناسب نيست.
تشخیص بر اساس نتایج کشت مثبت از نمونههای نواحی غیر استریل بدن در بیمارانی که کمتر در معرض IA بوده دارای حساسیت و اختصاصیت پایین میباشد، فقط در 30-10درصد بیماران دچار HIV، 20% بیماران دریافت کننده پیوند اعضا و 10 درصد بیماران بدون بیماریهای زمینهای نتایج کشت از لحاظ گونههای آسپرژیلوس مثبت بودند. اهميت جداسازي گونههاي آسپرژيلوس از نمونههای بالینی بیشتر به وضعيت سيستم ايمني بستگي دارد. جداسازي این عوامل از بيماران با وضعيت سيستم ايمني كامل و بدون علائم بیشتر به مفهوم كلونيزاسيون و عدم عفونت ميباشد، اما بايد توجه شود كه درصورت جداسازي گونههاي آسپرژيلوس از نمونههاي بيماران داراي سيستم ايمني ضعيف بايد بررسيهاي تشخيصی كاملتر جهت پیگیری IA در اين افراد صورت گيرد.
نتايج مثبت كشت مايع BAL به ترتيب دارای حساسيت و اختصاصيتی در حدود 50% و 97% ميباشد. آزمایش مستقیم میکروسکوپی نیز درصورت مثبت بودن کشت با ارزش است و دیدن هایف با تیغههای میانی احتمال بیماری تهاجمی را افزایش میدهد. این پروسههاي تشخیصی بیشتر به اطلاعات غیر مستقیمی که نشان دهنده احتمال بالای بیماری تهاجمی باشند، وابسته هستند.
بعلت محدودیت اين روشهای تشخیصی و كشندگي بسيار بالاي بيماري، استفاده از روشهاي غیر کشتي بر پایه تعيين آنتیژنهای قارچ آسپرژیلوس بسيار مفيد است. از روشهای تشخیصی غير كشتي، سرولوژی و مولکولی جهت تعیین آنتیبادی و مارکرهای تشخیصی گونههای آسپرژیلوس مثل آنتیژن گالاکتومانان(GM)[4]، بتا 1 و 3 دیگلوکان[5] و تعیین DNA به وسیله روش PCR جهت تشخیص بیماری استفاده میشود.
این روشها غیر تهاجمی، سريع و با حساسيت بالا هستند که پزشكان را در تشخيص بيماري در مراحل اوليه و شروع هرچه سريعتر درمانهاي مؤثر، اصلاح نوع درمان، پيگيري پيشرفت بيماري و اثر داروهاي تجويزي و ساير اقدامات كلينيكي توانمند ميسازند .با توجه به اینکه تولید آنتیبادی در بیماران دچار نقص ایمنی مبتلا به IA کم است، بنابراین تشخیص آنتیبادیهای ضد آسپرژیلوس در افراد با سیستم ایمنی مهار شده انجام پذیر نبوده و این تستها جهت تشخیص بیماری در بیماران غیر نوتروپنیک با وضعیت وخیم مورد استفاده قرار نمیگیرند.
آنتیژن بتا 1 و 3 دیگلوکان که ترکیب دیوارهی سلولی قارچ میباشد جهت تشخیص بیماریهای قارچی مهاجم مثل كاندیدیازیس، فوزاریوزیس و آسپرژیلوزیس استفاده میشود. نتیجه مثبت این تست، عامل اختصاصی عفونت تهاجمی قارچی را مشخص نمیکند و تفسیر نتایج این روش جهت تشخیص IA در بیماران با فاکتورهای خطر غیرنوتروپنی به دلیل ارزش اخباري مثبت پايين و نتايج مثبت كاذب زياد ناشي از همودیالیز، ديگر عوامل باكتريايي و قارچي، استفاده از آلبومین، داروهای با دوز بالای ایمنوگلوبولین و استفاده از گازهای زخم دشوار میباشد. هماکنون این تست به صورت تجاری قابل دسترس است و امروزه این روش، در حال بررسی و توسعه بوده و به همین منظور به انجام تحقیقات گستردهتری بر روی جمعیتهایی از بیماران خاص نیازمند میباشد.
آنتیژن گالاكتومانان پلیساکاریدی است که در ترکیبات دیواره سلولی آسپرژیلوس وجود دارد و در طی تهاجم به بافت از هایف قارچ آزاد ميشود. از آنجا كه اين آنتیژن یک کربوهیدرات محلول درآب است میتوان آن را علاوه بر سرم در ساير نمونههای بدست آمده از بیمار مثل ادرار، مايع مغزي نخاعي، مایع پلور، لاواژ برونكوآلوئولار و نمونههای بافتی تعيين كرد. جهت تعیین این آنتیژن از روشهای دیگر سرولوژی مثل آزمایش رادیو ایمنواسی (RIA)[6] و لاتکس آگلوتیناسیون (LA)[7] نیز استفاده میشود ولی مطالعات نشان دادهاند که این روشها فقط در طی مراحل پیشرفته عفونت در بیشتر بیماران مشکوک به IA مثبت شده و علاوه بر این، آنتیژن GM در نمونههای سرمی در آزمایش الایزا بیشتر و بسیار زودتر از سایر روشها شناسایی میشود.
امروزه كيت Pletelia™ Aspergillus EIA توسط شركت Bio-Rad جهت بررسی آنتیژن در نمونه سرم مورد تأييد سازمان كل غذا و دارو (FDA)[8] قرار گرفته است. اين روش در مقايسه با روشهاي تشخيصي ديگر از حساسيت و اختصاصيت بالاتري به ترتيب معادل 94 و 85 درصد برخوردار ميباشد و حتی در بسیاری از موارد سریعتر از علائم کلینیکی و یافتههای رادیولوژی مثبت میشود.
روش تعيين آنتيژن GM داراي نتايج مثبت و منفي كاذب است كه دلایل اين واکنشها تقريباً ناشـــــــــــــــــناخته باقی مانده است، ولی مصرف آنتیبیوتیکهای بتالاکتام مثل پایپراسیلین- تازاباکتام[9] در بزرگسالان، نوع رژيم غذايي در نوزادان، واکنش متقاطع با اپیتوپهای گونههای بیفیدوباکتریوم، استافیلوکوک، سودوموناس، درمان با سیکلوفسفامید، تولید اتوآنتیبادیها در GVHD، آلودگیهای آزمایشگاهي و مشکلات تکنیکی مثل سلولز سوابهاي پنبهاي در آزمايش LA از دلايل نتایج مثبت کاذب در اين تست بيان شدهاند.
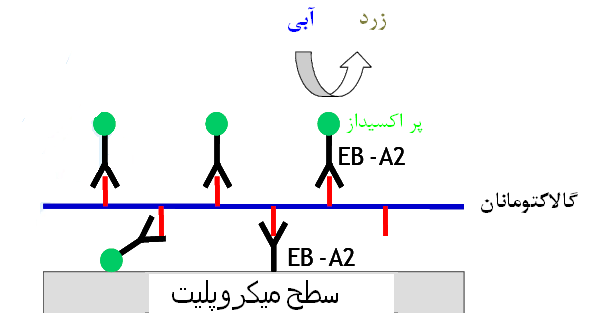
شماي كلي تست تعيين آنتیژن گالاكتومانان به وسيله آزمایش الايزا
امروزه از روش PCR نیز برای تعیین DNA اختصاصی آسپرژیلوس به فراواني استفاده میشود. مطالعات مختلف در ارزیابی آسپرژيلوس تهاجمي به وسیله روش Real time-PCR در نمونه لاواژ برونكوآلوئولار نشان دادهاند که این روش نيز در تشخیص بیماری دارای اختصاصیت بسیار بالا ميباشد. مزیتهای عمدۀ PCR، توانایی مشخص نمودن تراکم کم مادۀ ژنتیکی قارچی است که میتواند وجود احتمالی IA را نشان دهد. کمترین حد تشخیــــصی گزارش شده برای آسپرژیلوس فومیگاتوس برابر 10-100 CFU در هر نمونه است. مطالعات نشان داده که روش PCR در نمونه خون، جهت تشخيص IA دارای حساسیت 100-67% و اختصاصيت 95-55% میباشد، البته از آنجا که این تست قادر به افتراق بین کلونیزاسیون با عفونت واقعی نیست دارای نتایج مثبت کاذب است.
نتیجه گیری: از آنجا که به تأخیر افتادن تشخیص قطعی، عدم درمان مناسب و به موقع و وجود بیماریهای مختلف زمینهای از دلایل بالا بودن مرگ و میر این بیماری میباشند، استفاده از این روشهاي سريع و اختصاصي جهت شروع هرچه سريعتر درمانهاي مؤثر و مدیریت بیماری بسيار ضروري است.
البته جهت به دست آوردن نتايج دقيق، این آزمايشها بايد به طور تخصصي انجام شود و همچنين پزشكان نيز بايد از محدوديتها و نتایج کاذب آنها مطلع باشند تا از آن در مديريت وضعيت بيمار استفاده كنند و نكته مهمي كه بايد به آن توجه شود این است که يك تست منفي نميتواند تشخيص آسپرژيلوس تهاجمي را رد كند و همچنين يك تست مثبت نيز دلالت بر تشخيص قطعی عفونت ندارد، از این رو آزمايشها بايد بهصورت مرتبط باهم و نه بطور جداگانه تفسیر شوند، بنابراین وجود یک تعریف مشخص و واضح از این عفونتها جهت مطالعات کلینیکی و تحقیقاتی بسیار لازم و مفید است.
سازمان اروپایی درمان و تحقیقات سرطان (EORTC) [10]و مؤسسه بینالمللی آلرژی و گروه مطالعهای بیماریهای قارچی (MSG)[11] با هدف تشخیص بیماریهای تهاجمی در افراد در معرض خطر و همچنین طراحی مطالعات کارآزمایی بالینی جهت بررسی داروهای جدید و استراتژیهای مدیریتی، تعریف استاندارد شدهای جهت عفونتهای تهاجمی قارچی برای تحقیقات اپیدمیولوژیکی و کلینیکی وضع نموده است؛ در این تعریف افراد مورد شک به IA بر اساس فاکتورهای میزبان، معـــــــیارهای کلینیکی و قارچ شناسی در سه گروهProven ،possible و probable دسته بندی میشوند.
دسته بندی افراد مورد شک به بیماری IA بر اساس پروتکل EORTC
| Proven | مشاهده هایف قارچی در بررسیهای هیستو پاتولوژی، سایتولوژی و آزمایش مستقیم نمونههای به دست آمده از طریق آسپیراسیون یا بیوپسی، کشت مثبت از نمونههای به دست آمده با روشهای استریل از نواحی استریل و مشکوک به عفونت از طریق مشاهدات رادیولوژی وکلینیکی (این موارد شامل نمونههاي برداشت شده از BAL[12]، حفرات سینوسی بینی و ادرار نمی شود)، کشت خون مثبت با عدم تغییر عامل پس از تکرار |
| Probable | حداقل يك معیار فاکتور میزبان، يك معیار کلینیکی و يك معیار قارچ شناسی |
| Possible | حداقل يك معیار فاکتور میزبان و يك معیــــــــار کلینیکی با عدم حضور معیار قارچ شناسی |
نکات:
| فاکتورهای میزبان | – نوتروپنی (نوتروفیل کمتر از 109 ×5/0 در لیتر برای بیشتر از 10 روز)
– دریافت کنندگان پیوند Stem cellآلوژنیک – استفاده طولانی مدت ازکورتیکو استروئیدها (بجز بیماران با آسپرژیلوزیس برونکوپولمونر آلرژیک (ABPA) با میانگین حداقل دوز 3/. میلیگرم برای هر کیلوگرم در روز پردنیزولون به مدت بیشتر از 3 هفته – درمان با دیگر داروهای تضعیف کننده سیســـــــــــــــــتم ایمنی نظیر Cyclosporin ,TNF-α blockers و آنتیبادیهای منوکلونال اختصاصی یا آنالوگهای nucleoside در طول 90 روز قبل |
| معیارهای بالینی | * بیماری قارچی قسمتهای تحتانی دستگاه تنفسی:
ماژور: وجود حداقل يك علامت از علائم CT: – ضایعات متراکم، با محدوده و دیواره مشخص با یا بدون علامت Halo sign – نشانه Air –Crescent مینور: وجود حداقل 2 علامت از علائم شامل سرفه، درد قفسه سینه، هموپتزی، دیسپنه، پلورال راب، پلورال افیوژن |
| * تراکئوبرونشیت:
– اولسر تراکئوبرونشیال، ندول، غشاء کاذب، پلاک یا اسکار مشاهده شده در بررسیهای برونکوسکوپی |
|
| * عفونتهای سینوسی بینی:
تصویر نشان دهنده سینوزیت و وجود حداقل یکی از 3 علامت زیر: – دردهای حاد موضعی (شامل دردهای کشیده شده به سمت چشم) – زخم بینی با اسکار سیاه – گسترش از سینوس پارانازال به استخوانهای مجاور، از جمله به درون حدقه چشم |
|
| * عفونت CNS:
وجود حداقل یکی از 2 علامت: – مشاهده زخمهای کانونی در تصویر – افزایش (enhancment) مننژیتی درCT یا MRI |
|
| معیارهای قارچ شناسی | * آزمایش مستقیم (سیتولوژی، مشاهده مستقیم یا کشت)
قارچهای رشتهای در نمونههای خلط، BAL، شستشوی برنشی یا نمونه آسپیره سینوس که با یکی از موارد زیر نمایان شود: – وجود عناصر قارچی نشان دهنده قارچهای رشتهای – مثبت شدن کشت مجدد قارچ رشتهای مشخص *آزمایشات غیر مستقیم (جستجوی آنتیژن یا ترکیبات دیواره سلولی) – جستجوی آنتیژن گالاکتومانان در پلاسما، سرم، BAL یا CSF – جستجوی β-D Glucan در سرم |
[1]-Invasive Aspergilosis
[2] Magnetic Resonsnce Imaging
[3] gold standard
[4]Galactomannan
[5]β1-3-D-Glucan
[6] Radio Immune Assay
[7] Latex Agglotination
[8] Food and drug Administratron
[9] piperacillin–tazobactam
[10] European Organization for Research and Treatment of Cancer
[11] Mycosis Study Group
[12] Bronchoalveolar Lavage Fluid
راهکارهای کاهش ابتلا به عفونتهای ناشی از قارچ آسپرژیلوس
https://www.cdc.gov/fungal/diseases/aspergillosis/index.html
برای دانلود پی دی اف بر روی لینک زیر کلیک کنید
ورود / ثبت نام