مقاله مروری
رهنمودهای ICSH برای استانداردسازی نمونهها و گزارشهای مغز استخوان (1)
دکتر طاهره اسلاممنش، استادیار پاتولوژی دانشگاه علوم پزشکی رفسنجان
بررسی مغز استخوان یک بررسی ضروری برای تشخیص و پیگیری بسیاری از اختلالات خونی و مغز استخوان است.نمونههای آسپیراسیون و بیوپسی مکمل همدیگر هستند و زمانی که هر دوی آنها را داشته باشیم، امکان ارزیابی جامع مغز استخوان فراهم میشود. تفسیر نهایی نیازمند جمعبندی یافتههای خون محیطی، آسپیراسیون و بیوپسی مغز استخوان همراه با نتایج تستهای تکمیلی مثل ایمونوفنوتایپ، آنالیز سایتوژنتیک و مطالعات ژنتیک مولکولی مناسب در زمینه بالینی بیمار است. روشهای آمادهسازی، پردازش و گزارش نمونههای آسپیراسیون و بیوپسی مغز استخوان بسیار متغیر است. این تفاوتها منجر به تناقضات در تشخیص یا طبقهبندی بیماریها میشود که احتمال دارد روی درمان و نتایج بالینی بیمار اثر گذارد. با تشخیص نیاز به استانداردسازی در این زمینه، یک گروه کاری بینالمللی برای استانداردسازی نمونهها و گزارشهای مغز استخوان توسط کمیته بینالمللی استانداردسازی در هماتولوژی (ICSH) برای آمادهسازی مجموعهای از دستورالعملها بر اساس بهترین شیوهها و اقدامات تشکیل شد. دستوراالعملها در مجامع عمومی ICSH مورد بحث قرار گرفت و توسط یک هیات بینالمللی از کارشناسان برای رسیدن به اتفاق نظر بیشتر، بررسی شد.
مقدمه
بررسی بیوپسی و آسپیراسیون مغز استخوان برای تشخیص اختلالات مغز استخوان ضروری است. یک تشخیص جامع اختلال مغز استخوان اغلب نیازمند راههای تشخیصی مختلف است که شامل ارزیابی اسمیر و شمارش سلولهای خون محیطی، اسمیر آسپیراسیون مغز استخوان، برش لخته ذرات (particle clot section)، بیوپسی مغز استخوان و مورفولوژی نقشگذاری(imprint) همراه با نتایج حاصل از بررسیهای مرتبط دیگر مثل سیتوشیمی، آنالیز ایمونوفنوتیپ، تکنیکهای سیتوژنتیک و ژنتیک مولکولی و همچنین نتایج تستهای بیوشیمی و میکروبیولوژیک در صورت لزوم است. تفسیر نهایی باید در چارچوب یافتههای کلینیکی و تشخیصی مقدماتی اولیه باشد. روشهای فعلی برای آماده سازی، پردازش و گزارش نمونههای مغز استخوان بسیار متغیر است. فقدان یکسانسازی میتواند منجر به تناقض در طبقهبندی و تشخیص بیماریها شود و در نتیجه روی درمان و نتایج بالینی بیمار اثر گذارد. در تلاش برای استانداردسازی اندیکاسیونهای بررسی مغز استخوان، نمونههایی که مورد نیاز است و چارچوب گزارش، یک گروه کاری بینالمللی برای استانداردسازی نمونهها و گزارشهای مغز استخوان توسط اعضای خود و بنیاد مستقل از کمیته جدید بینالمللی برای استانداردسازی در هماتولوژی (ICSH) در ایالات متحده در آوریل 2007 تشکیل شد. توسط کنفرانس الکترونیکی پیشنویس کارگروه که مجموعهای از دستورالعملهای مورد توافق بود در مجامع عمومی ICSH در انگلستان در اکتبر 2007 و در استرالیا در می 2008 ارائه شد. پس از انجام اصلاحات لازم، دستورالعملها به یک هیات بینالمللی از کارشناسان برای اظهار نظر بیشتر قبل از انتشار ارائه شد. اگرچه گروه کاری توصیههای زیر را بر اساس بهترین شیوه ارائه داده است ولی تغییراتی در عمل به دلیل هزینهها یا محدودیتهای عملی وجود دارد و این تغییرات در آن منطقه خاص قابل قبول است.
اندیکاسیونهای بررسی مغز استخوان
اندیکاسیونهای بررسی BM در جدول شماره 1 لیست شده است. آسپیراسیون و بیوپسی اطلاعات مفید و تکمیلی را ارائه میکند. توصیه میشود هم آسپیراسیون و هم بیوپسی مغز استخوان به طور روتین انجام شود، به طوری که یافتههای ایندو میتواند با هم ارتباط داشته باشند. اگرچه در بعضی شرایط کلینیکی، امکان دارد یک آسپیره به تنهایی کافی باشد. اگر بیوپسی اندیکاسیون دارد ولی انجام نشده است و یا قابل دستیابی نیست، نمونه لخته ذرات(particle clot) توصیه میشود. اگر آسپیره قابل دستیابی نباشد (مثلاٌ در آسپیره خشک) نقشگذاری بیوپسی تهیه شود.
| جدول 1: اندیکاسیونهای بررسی مغز استخوان |
| -بررسی آنمی غیرقابل توجیه، شاخصهای غیرطبیعی گلبول قرمز، سایتوپنی یا سایتوزیس
-بررسی مورفولوژی غیرطبیعی اسمیر خون محیطی که مطرح کننده پاتولوژی مغز استخوان است -تشخیص، مرحلهبندی و پیگیری اختلالات هماتولوژیک بدخیم (مثل لوکمی حاد و مزمن، سندرمهای میلودیسپلاستیک، اختلالات میلوپرولیفراتیو مزمن، لنفوما، میلوم پلاسماسل، آمیلوئیدوز، ماستوسیتوز) -بررسی متاستازهای مغز استخوان مشکوک -ضایعات استخوانی کانونی غیرقابل توضیح در تصویربرداری رادیولوژی -ارگانومگالی غیرقابل توجیه یا وجود ضایعات تودهای غیرقابل دسترس برای بیوپسی -کشت میکروبیولوژیک برای بررسی تب با منشا ناشناخته یا عفونتهای خاص مثل سل ارزنی، لیشمانیوز، مالاریا -ارزیابی ذخایر آهن -بررسی اختلالات ذخیرهای چربی/گلیکوژن -رد بیماری هماتولوژیک در اهداء کنندگان بالقوه پیوند سلول ریشهای آلوژنیک |
روشهای مقدماتی
مهم است که اپراتور از اندیکاسیونهای کلینیکی بررسی BM و نمونههایی که مورد نیاز است گرفته شود آگاهی داشته باشد. همچنین اپراتور باید از نیاز به آرامبخش و تسکین درد کافی و مباحث ایمنی با توجه به ترومبوسیتوپنی یا خطرات انعقادی آگاه باشد که امکان دارد نیازمند انتقال پلاکت یا برگشت ضدانعقادی باشد. ملاحظات خاص از محل بررسی BM و وضعیت قرارگیری بیمار باید برای بیماران بیحرکت، بیماران چاق، کودکان یا شیرخواران، بیماران با ضایعات استخوانی لیتیک یا نکروز BM و یا افرادی که پرتوتابی قبلی داشته اند لحاظ شود. قبل از بررسی BM، اقدامات زیر لحاظ شود:
- روش کار با جزئیات برای بیمار توضیح داده شود. تاریخچه کلینیکی گذشته بیمار گرفته شود. هرگونه آلرژی و ناخوشیهای همزمان مستند شود و هر گونه مصرف دارویی توضیح داده شود.
- رضایت آگاهانه باید از بیمار گرفته شود. همچنین بر اساس دستورالعملهای محلی برای استفاده از هر کدام از نمونهها برای اهداف غیرتشخیصی مثلا پژوهشی تحقیقاتی، بانک بافتی، آموزشی یا تضمین کیفیت باید رضایت گرفته شود.
- یک اسمیر خون محیطی و شمارش سلولهای خونی باید تهیه شود، در صورتی که طی 2 روز گذشته جمع آوری نشده است.
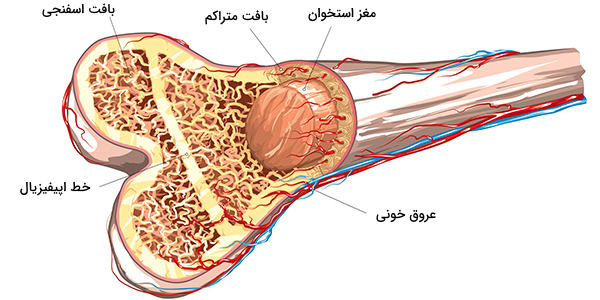
محل آناتومیک
محل آناتومیک ترجیحی برای آسپیراسیون و بیوپسی BM، ستیغ ایلیاک خلفی است. ستیغ ایلیاک قدامی برای بیمارانی که قادر به حرکت نیستند استفاده میشود. سطح داخلی تیبیا در شیرخواران استفاده میشود. آسپیره استرنوم در برخی شرایط خاص مناسب است مثلا اگر بیمار قادر به حرکت نیست، پرتوتابی به لگن یا محلهای دیگر داشته است که منجر به آسپیره خشک میشود یا اگر بیوپسی مورد نیاز نیست. آسپیراسیون استرنوم فقط باید توسط یک اپراتور باتجربه که از خطر تامپوناد قلبی باخبر است انجام شود. اگر یک ضایعه استخوانی کانونی شناخته شده وجود دارد (در تصویربرداری رادیولوژی)، احتمال تشخیص ضایعه از طریق آسپیراسیون سوزنی و بیوپسی استخوانی در محل ضایعه وجود دارد.
آسپیراسیون یا بیوپسی هر کدام ممکن است اول انجام شوند. اگر ابتدا آسپیراسیون انجام شود، بیوپسی از راه همان انسیزیون، تقریبا نیم تا یک سانتی متر دور از محل آسپیراسیون برای اجتناب از به دست آوردن یک بیوپسی آسیب دیده یا خونریزی دهنده انجام میشود. اگر ابتدا بیوپسی انجام شود، سوزن آسپیراسیون روی سطح استخوان نیم تا یک سانتی متر دور از محل بیوپسی قرار میگیرد تا نمونه آسپیراسیون لخته نشود. توصیه میشود که آسپیراسیون و بیوپسی با استفاده از سوزنهای مربوطه جداگانه و نه از طریق یک سوزن بیوپسی به دست آید. اگر آسپیراسیون با سوزن بیوپسی انجام شود، امکان رقیق شدن نمونه آسپیره با خون وجود دارد. اگر بیوپسی بعداً با همان سوزن انجام شود، امکان دارد نمونه بیوپسی آسیب دیده و خونریزی دهنده باشد.
آسپیراسیون مغز استخوان
جمعآوری نمونههای آسپیراسیون
توصیه میشود که آسپیراسیون با یک سرنگ پلاستیکی 10 یا 20 سیسی متصل به سوزن آسپیراسیون، برای به دست آوردن فشار منفی کافی، کشیده شود. برای حفظ مورفولوژی، سرنگ نباید حاوی ضدانعقاد باشد. تقریباً نیم سیسی از اولین نمونه آسپیراسیون برای تهیه اسمیرهای BM در کنار بالین بیمار جمعآوری میشود. با افزایش حجم آسپیراسیون BM رقیق شدن پیشرونده آسپیراسیون با خون محیطی دیده میشود. آسپیرههای اضافی باید در لوله حاوی اتیلن دی آمین تترا استیک اسید (EDTA) ریخته شود، در مواردی که نمونه سریعاً لخته میشود برای کاهش آرتیفکت ناشی از EDTA مقدار آسپیراسیون باید متناسب با مقدار EDTA در لوله باشد. ICSH نمک دی پتاسیم EDTA با غلظت خونی 0/25±1/50 میلیگرم در میلیلیتر را توصیه میکند. امکان دارد حجم مناسب آسپیراسیون به یک لوله حاوی EDTA ایزوتونیک اضافه شود تا غلظت مورد نظر به دست آید. در روش دیگر حجم مناسب از آسپیراسیون به یک لوله EDTA کودکان اضافه میشود.
سرنگ دوم به سوزن آسپیراسیون برای کشیدن نمونههای بیشتر برای تستهای تکمیلی مثل فلوسیتومتری، آنالیز سیتوژنتیک و مطالعات ژنتیکی مولکولی، میکروبیولوژی، میکروسکوپ الکترونی یا کشت BM متصل میشود. در صورت آسپیره خشک یا زمانی که قطعات بافتی وجود ندارد، آسپیره BM در یک زاویه مختصر متفاوت یا در یک محل دیگر میتواند تکرار شود. پیشنهاد میشود که نمونههای فلوسیتومری، سیتوژنتیک و بررسی ژنتیکی مولکولی با تمام آسپیرههای BM جمعآوری شود. امکان دارد نمونهها دور انداخته شود در صورتی که اسلایدهای BM مرور شود و بررسیها نشان دهد که وجودشان غیر ضروری است.
نمونههای آسپیره مغز استخوان باید برای تست های تکمیلی جمعآوری شود، به روشی که توسط آزمایشگاه محلی توصیه شده است. آسپیراسیون مغز استخوان برای فلوسیتومتری باید در لوله حاوی هپارین سدیم ریخته شود. EDTAدیپتاسیم نیز میتواند استفاده شود، اگرچه نمونهها باید عرض 12 تا 24 ساعت آنالیز شوند. در صورت آسپیره خشک، یک قطعه بیوپسی که مجموعا به طول 2 تا 3 سانتیمتر باشد برای آنالیز فلوسیتومتری در یک محیط کشت بافتی مثل RPMI در یک ظرف استریل ارسال میشود. اگرچه به علت افزایش سلولهای مرده و ذرات سلولی کیفیت سوسپانسیون سلولی به دست آمده توسط دوباره معلقسازی نمونه بیوپسی نسبت به آسپیراسیون پایینتر است. آسپیرههای BM برای آنالیز سیتوژنتیک یا هیبریدیزاسیون در جای فلورسنت(FISH) باید به همان صورتی که آزمایشگاه سیتوژنتیک توصیه میکند جمعآوری شود. ترجیحاً نمونهها داخل لولههای استریل با محیط کشت بافتی مثل RPMI یا سرم جنین گاو 10% برای زنده ماندن سلولی خوب یا به داخل لولههای حاوی هپارین سدیم برای انتقال بعدی به داخل محیط کشت بافتی در آزمایشگاه ریخته می شود. اگر امکان آسپیراسیون مغز استخوان وجود ندارد یک نمونه بیوپسی در محیط کشت بافتی استریل یا سالین برای آنالیز سیتوژنتیک قرار میگیرد. نمونههای آسپیراسیون برای مطالعات مولکولی مثل PCR یا RT-PCR نیز باید بر اساس دستورالعمل آزمایشگاه مولکولار، معمولاً داخل لولههای حاوی EDTA، جمعآوری شود. نمونهها برای میکروبیولوژی باید در ظرف استریل قرار داده شود یا به داخل محیط کشت مناسب که توسط آزمایشگاه میکروبیولوژی توصیه میشود تلقیح گردد. اگر نمونهها برای کشت BM یا میکروسکوپ الکترونی مورد نیاز است باید به داخل محیط مناسب به صورتی که آزمایشگاههای مربوطه مشخص کردهاند جمعآوری شود. آسپیرههای اضافی را میتوان برای تهیه “لخته ذرات” استفاده کرد یا در لوله حاوی EDTA برای اهدافی مثل تهیه اسمیرهای بیشتر، فلوسیتومتری، بررسیهای ژنتیک مولکولی، انجماد و بانک بافتی استفاده کرد.
ادامه دارد….
:Reference
S.-H. Lee, W. N. Erber, A. Porwit, M. Tomonaga, L. C. Peterson– For The International Council For Standardization In Hematology. ICSH guidelines for the standardization of bone marrow specimens and reports. Int. Jnl. Lab. Hem. 2008, 30, 349–364
برای دانلود پی دی اف بر روی لینک زیر کلیک کنید
ورود / ثبت نام