آشنایی با مَس اسپکترومتری Mass Spectrometry
حسن منصوری طرقبه دانشجوی دکترای تخصصی آلرژی
آنچه خواهید خواند:
تاریخچه مس اسپکترومتری/ اصول کلی مس/ قسمتهای مختلف دستگاه مس/ توصیف یک گراف سادهء مس/ انواع مختلف مس/ کاربردهای مس/ مالدی تاف/ اصول کار ملدی تاف/ سلدی تاف/ اصول کار سلدی تاف/ صفحات کاربردی مختلف در سلدی تاف/ کاربردهای سلدی تاف/ مروری بر کمیت مقالات چاپ شده / خلاصه/ نتیجه گیری.
اهداف آموزشی:
درک اصول حاکم بر مس/ شناخت قسمتهای مختلف دستگاه مس/ توانایی درک گراف مس/ آشنایی با انواع مس/توانایی ذکر کاربردهای مس/ آشنایی با ملدی تاف/ درک اصول کار مادی تاف/ درک اصول کار سلدی تاف/ آشنایی با سطوح کاربردی در سلدی تاف.
مقدمه:
همواره یکی از مشکلات محققین و دانشمندان در حیطههای مختلف علوم اندازهگیری مواد و شناسایی آنها در مواد بیولوژیک بوده است. در طی دهههای گذشته راهکارها و روشهای آزمایشگاهی متعددی جهت پوشش این مشکل پیشنهاد شده است و برخی از آنان به صورت دستگاههای آزمایشگاهی به بازار آمده و برخی با گذر زمان بهبود یافتهاند. یکی از این روشها و دستگاهها روش مس اسپکترومتری است. مس اسپکترومی یک روش شیمیایی تجزیهای است که به ما در تعیین مقدار و شناسایی مواد موجود در یک نمونه بیولوژیک با سنجش نسبت جرم به بار الکتریکی یونهای فاز گازی کمک میکند. در سال ۱۸۸۶میلادی یوگن گولدشتین مشاهده نمود که گازها در شرایط فشار پایین از خود اشعه ساطع میکنند.
متعاقب آن ویلهلم وین متوجه گردید که میدانهای قوی مغناطیسی و یا الکتریکی اشعه را منحرف میکنند و در سال ۱۸۹۹ وی دستگاهی ابداع نمود که میتوانست اشعه را بر اساس نسبت جرم به بار جداسازی نماید (تصویر ۱). پس از ویلهم وین دانشمند دیگری به نام تامسون با ایجاد خلاء کارهای وی را بهبود بخشیده و ارتقاء داد.1
تصویر ۱) دستگاه ابتدایی ویلهلم وین که اکنون در موزه نگهداری می شود
اصول کلی حاکم بر دستگاههای مس اسپکترومتری
تمامی دستگاههای مس اسپکترومتری صرف نظر از نوع و مدل در اصول اولیه زیر مشترک هستند:
- در همه دستگاهها نیاز به ایجاد یونهای گازی از اتمها یا مولکولهای ماده مورد نظر میباشد.
- جداسازی یونها بر اساس نسبت جرم به بار آنها حاصل میآید.
- سنجش نهایی بر اساس فراوانی یونهای ردیابی شده میباشد.
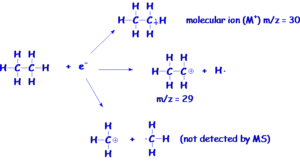
در برخی دستگاههای مس اسپکترومتری از الکترونهای پر انرژی برای شکستن مولکولها به قطعات کوچکتر استفاده میشود. جداسازی و تجزیه و تحلیل این قطعات اطلاعاتی در مورد وزن مولکولی و ساختمان این قطعات برای ما فراهم میآورد. مولکولهای ماده مورد بررسی در مواجهه با الکترونهای پر انرژی دچار یونیزاسیون میگردند، یعنی ممکن است پس از برخورد الکترون پر انرژی به مولکول هدف، الکترونی از آن جدا شده و یون باردار مولکول هدف با بار مثبت باقی بماند که رادیکال کاتیون نامیده میشود.
M– + e– → M●+ + 2e
یونهای بارداری که جرم یکسانی دارند و دارای یک واحد بار الکتریکی هستند براحتی بر اساس وزن مولکولیشان در دستگاه مشخص میگرندد. برای نیل به این هدف نرمافزارهای موجود در دستگاه با استفاده از محاسبات ریاضی و الگوریتمی این اعمال را انجام میدهند. مولکولهای ماده مورد آزمایش میتوانند دچار یونیزاسیون الکترونی گردند. اگر M ماده مورد آزمایـش و –e الکترون پر انرژی باشد ●+M الکترون یونیزه است.
●+M مولکول یونیزه شده ماده مورد آزمایش است که یون مولکولی نامیده میشود. مولکول کاتیون با از دست دادن یک الکترون پدید میآید. یونهای باردار که دارای وزن مولکولی متفاوت و بار الکتریکی یکسانی هستند در دستگاه مس براحتی شناسایی میگردند. نرمافزار دستگاه که اطلاعات را از طریق آشکارساز دریافت میکند با استفاده از الگوریتمهای ریاضی این اعمال را انجام میدهد. بایستی یادآوری نمود که در دستگاه مس تنها یونهای دارای بار مثبت امکان شناسایی را دارند. تاثیر طیفی از الکترونهای پر انرژی بر روی یک مولکول نسبتا بزرگ میتواند طیفی از رادیکال کاتیونها و قطعات حاصل از شکست مولکول را پدید آورد. به مثال زیر (تصویر2) که نتیجه شکست مولکول سادهای را به تصویر کشیده است توجه فرمایید.1و2
تصویر 2) محصولات حاصل از برخورد الکترون پر انرژی به مولکول C2H6
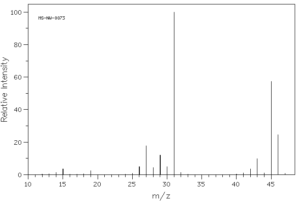
در گراف یا تصویر حاصل از دستگاه مس با دو موج (Peak) مواجه میشویم: 1- یون والد که عبارت است از فراوانی کاتیون یونی که جرمی معادل مولکول اصلی مادهء مورد بررسی ما دارد و با +M نشان داده می شود. 2- موج پایه (Base peak) که مربوط به فراوانترین یون ردیابی شده است و معمولا فراوانی آن توسط دستگاه 100 در نظر گرفته میشود و فراوانی سایر کاتیون یونها بر اساس آن تعیین و عدددهی میشود. در گراف مس محور عمودی فراوانی کاتیون یونها و محور افقی نسبت جرم به وزن کاتیون یونهای مختلف را به نمایش میگذارد. تصویر 3 نشان دهنده نتیجه بررسی مولکول اتانول در دستگاه مس میباشد.
تصویر 3) نتیجه بررسی مولکول اتانول در دستگاه مس
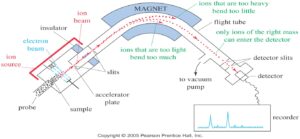
بایستی توجه داشت که بسیاری از موادی که در دستگاه مس مورد بررسی قرار میگیرند دارای چندین مولکول از مواد مختلف میباشند. وجود مقادیر زیادی از ایزوتوپهای سنگین منجر به ظهور موجهای کوچکی در گراف مس میشود که از یون والد جرم بیشتری دارند. تصویر 4 نمای شماتیک دستگاه مس را به نمایش گذاشته است. براساس این نما مولکولهای گازی ماده مورد بررسی از طریق پروب وارد دستگاه شده و در محل منبع یونی تحت بمباران الکترونهای پرانرژی که عمود بر مسیر حرکت مولکولهای ماده مورد آزمایش میتابند قرار میگیرند. در این قسمت مولکولهای ماده مورد آزمایش شکسته شده به انواع کاتیونها، آنیونها و قطعات حاصل از شکست تبدیل میگردند. سپس در قسمت بعدی که شتاب دهنده دستگاه است شتاب و سرعت گرفته و ادامه مسیر میدهند و پس از عبور از روزنه وارد کانال مس میگردند.
تصویر 4) نمای شماتیک دستگاه مس
در این تونل در مسیر یونهای کاتیونی یک میدان مغناطیسی تعبیه شده است که به یونها نیرو وارد میکند. این نیرو سبب انحراف مسیر حرکت کاتیون یونها میگردد. میزان انحراف مسیر یونهایی که دارای یک بار الکتریکی مثبت هستند و یا به عبارتی نسبت جرم به وزن آنها برابر جرمشان است (جرم تقسیم بر یک بار مثبت مساوی است با جرم) بستگی به جرم مولکولها دارد. به عبارت دیگر هرچه ماده سنگینتر باشد کمتر تحت تاثیر نیروی میدان قرار میگیرد و منحرف میگردد و هرچه سبکتر باشد بیشتر منحرف میگردد. از بین تمامی یونهایی که تحت تاثیر این میدان قرار میگیرند تنها یک یون مستقیما در مسیر درست قرار میگیرد و قادر است از روزنه آشکار ساز عبور کرده و شناسایی گردد.
سایر کاتیون یونها به جدارهء تونل برخورد کرده شتاب خود را از دست میدهند و امکان رسیدن به آشکارساز را پیدا نخواهند کرد. ضمنا در طول مسیر توسط پمپ، خلا ایجاد شده است و مولکولها و کاتیونهای برخورد کرده با جداره توسط خلا از مسیر خارج میگردند. در ادامه با تغییر شدت میدان (کم و زیاد شدنهای متوالی شدت انرژی مغناطیسی) کاتیونهای دیگر توسط دستگاه شناسایی شده و اطلاعات آن از آشکارساز به قسمت نرمافزاری دستگاه جهت رسم گراف هدایت میشود.
الگوی شکست و تولید قطعات مختلف هر نمونه و همچنین انواع یونهای کاتیونی هر نمونه ثابت است. نرمافزار دستگاه با داشتن این الگو میتواند آنرا از حافظه خود بازخوانی کرده و مولکول ماده مورد آزمایش را شناسایی نماید. این فرآیند به مثابه داشتن اطلاعات پازل عکس یک فیل است که منحصر به فرد میباشد و با ترکیب قطعات پازل تصویر دیگری در نرمافزار به دست نمی آید و در بازخوانی تک تک قطعات پازل نرمافزار مجددا به شکل فیل میرسد (تصویر 5). 3و4
تصویر 5) نمایی از یک پازل فیل جهت درک بازخوانی اطلاعات در نرم افزار مس
قطعات اصلی یک دستگاه مس:
قطعات اصلی دستگاه مس معمولا بدون توجه به نوع دستگاه شامل قسمتهای زیر است:
- قسمت تزریق نمونه
- منبع یونساز
- بخش تجزیه و تحلیل یونها
- آشکارساز
- پمپهای ایجاد کنندهء خلاء
- بخش نرمافزاری
انواع مختلف دستگاه مس اسپکترومتری:
دستگاههای مس اسپکترومتری دارای انواع مختلفی هستند. در ذیل به چند نمونه آنها اشاره شده است:
- دستگاه مس با تکنولوژی یونیزاسیون مواد با الکترون Electron impact ionization (EI)
- دستگاه با تکنولوژی یونیزاسیون مواد با الکترون و انتقال انرژی به کمک واکنشهای شیمیایی Chemical ionization (CI)
- دستگاه مس با تکنولوژی بمباران سریع الکترونی Fast atomic bombardment (FAB)
- دستگاه مس با تکنولوژی یونیزاسیون با لیزر و استفاده از سطوح فعال شده Matrix-assisted laser desorption ionization (MALDI)
- دستگاه مس ملحق شده به دستگاه کروماتوگرافی مایع LC-Mass
در این دستگاه تفکیک اولیه مواد توسط دستگاه کروماتوگرافی مایع انجام میشود و مواد تفکیک شده بتدریج که از خروجی دستگاه خارج میگردند به ورودی دستگاه مس وارد میشوند.
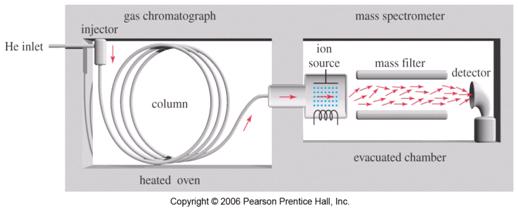
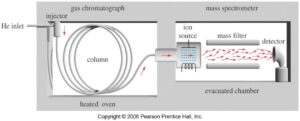
- دستگاه مس ملحق شده به دستگاه کروماتوگرافی گازی GC-Mass (تصویر6)
در این دستگاه تفکیک اولیه مواد توسط دستگاه کروماتوگرافی گازی انجام میشود و مواد تفکیک شده بتدریج که از خروجی دستگاه خارج میگردند به ورودی دستگاه مس وارد میشوند.
- دستگاه مس ملحق شده به دستگاه کروماتوگرافی مایع با کارایی بالا HPLC-Mass
در این دستگاه تفکیک اولیه مواد توسط دستگاه کروماتوگرافی مایع با کارایی بالا انجام میشود و مواد تفکیک شده بتدریج که از خروجی دستگاه خارج میگردند به ورودی دستگاه مس وارد میشوند.
- دستگاه مس با میدانهای مغناطیسی متعدد جهت جداسازی بهتر Tandem Mass
- دستگاه مس با تکنولوژی میدان مغناطیسی و الکتریکی متناوب Quarrupole
- دستگاه مس با تکنولوژی به دام اندازی یونها در گرداب مغناطیسی Obitrap
تصویر 6) نمای شماتیک دستگاه مس در سمت راست که با دستگاه کروماتوگرافی گازی در سمت چپ ادغام شده است
کاربردهای مس اسپکترومتری:
کاربردهای مختلف مس را میتوان در دو گروه بررسیهای کمی و کیفی تقسیمبندی نمود اما به طور کلی کاربردهای مس عبارتند از شناسایی ترکیبات ناشناخته، تعیین میزان و درصد ایزوتوپها در یک مولکول و تعیین ساختمان یک ترکیب و مشاهده قطعات حاصل از شکست آن که به ما در درک ساختمان فضایی مولکول کمک مینماید.
دستگاههای مس مطرح در علوم پزشکی:
در ذیل از بین انواع مختلف دستگاه مس به دو نوع آن که در علوم پزشکی کاربرد فراوانتری دارند اشاره میشود.
1: دستگاه مس با تکنولوژی یونیزاسیون با لیزر و استفاده از سطوح فعال شده Matrix-assisted laser desorption ionization (MALDI)
این دستگاه با تکنولوژی لیزر جهت تولید یون کار مینماید و نوع آشکارساز آن از نوع زمان پرواز (Time of flight) می باشد. این تکنولوژی در سال 1991 توسط هیلنکامپ معرفی گردید و امروزه در حد وسیعی برای بررسی و تجزیه و تحلیل پروتئینها، پپتیدها، گلیکوپروتئینها، اولیگوساکاریدها و اولیگونوکلئوتیدها به کار میرود.
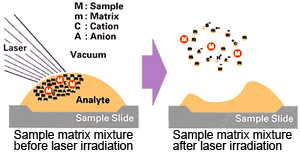
در این تکنیک نمونه با حلال و ماتریکس مخلوط شده و بر روی سطح کاری (probe) قرار داده میشود.
با گذشت زمان حلال تبخیر شده و نمونه به همراه ماتریکس به صورت کریستالیزه شده در میآید (تصویر 7). سپس تابش اشعه لیزر کریستال حاصله را شکسته و خورد مینماید و قطعات حاصل از شکست و کاتیون یونهایی را برای بررسی تولید میکند.5
تصویر 7) نحوه یونیزاسیون در دستگاه MALDI
2: دستگاه مس با تکنولوژی سطوح فعال شده و آشکارساز زمان پرواز SELDI-TOF
واژهء SELDI-TOF مخفف کلمات Surface-Enhanced Laser Desorption/Ionization- time of flight میباشد. این تکنولوژی در سال 1993 توسط ویلیام هوتچن معرفی شد و پس از چهار سال توسط شرکت بیولب تجاریسازی گردید. در حقیقت این تکنولوژی زیر ردهای از تکنیک مالدی است که در بالا بدان اشاره شد. این تکنیک روش بسیار مناسبی برای بررسی و تجزیه و تحلیل پروتئینهای پیچیده در نمونههای خون، ادرار، نمونههای بافتی و سایر نمونههای بیولوژیک میباشد.
در این تکنیک نمونه حاوی پروتئینهای مختلف بر روی سطحی قرار میگیرد که با استفاده از یک سری شاخصهای از قبل تعیین شده پوشانیده و فعال شده است. پس از قرارگیری نمونه بر روی سطح فعال شده با شاخصهای مد نظر (که سطح جهت گزینش آنها طراحی شده است) پروتئینهای هدف به آن متصل شده و بقیه پروتئینها شسته میشوند. پس از شستشو سطح فعال شده حاوی نمونه به صورت کریستاله در میآید. اتصال پروتئین هدف به سطح فعال شده در واقع نقش جداسازی و تفکیک کنندهگی را بر عهده دارد لذا بررسی مولکول پروتئینهای هدف در مرحله بعدی مس راحتتر میشود.
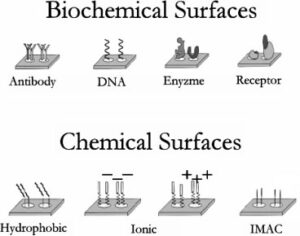
سطوح فعال شدهای که بطور شایع در سلدی-تاف مورد استفاده قرار میگیرند عبارتند از سطوح CM10, H50, IMAC30, Q10, که به ترتیب دارای خاصیت تعویض یونی مثبت ضعیف، سطح با خاصیت آبگریزی، سطح با قابلیت اتصال به فلز و سطح متصل شونده به آنیون قوی میباشند. همچنین این سطوح را میتوان با مواد شیمیایی و یا بیوشیمیایی فعال نمود. مواردی از این دست در تصویر 8 به نمایش گذاشته شده است.
تصویر 8) برخی از سطوح فعال شده که در دستگاه سلدی مس مورد استفاده قرار میگیرند
متعاقب این مرحله نمونه تحت تاثیر اشعه لیزر قرار می گیرد (تصویر 9) و به مولکولها یا قطعاتی با وزن مولکولی مختلف با بار مثبت تبدیل میگردد. این قطعات بایستی فاصله بین سطح فعال شده تا آشکارساز را طی نمایند و در این خصوص شتاب دهندهای در دستگاه تعبیه شده است که به مولکولها شتاب میدهد. از آنجایی که نیروی وارد شده به مولکولهای مختلف برابر است و از طرفی بار الکتریکی آنها یکسان است، سرعت حرکت مولکولها به جرم آنها بستگی پیدا میکند.
به عبارت دیگر قطعات سنگینتر دارای زمان پرواز طولانیتری جهت طی فاصله فرودگاه مبدا تا مقصد را خواهند داشت و مولکولهای کوچکتر زمان پرواز کوتاهتری دارند و زودتر به مقصد میرسند. این فرآیند همانند این است که سه هواپیما از یک مدل با نیرو و انرژی برابر ولی یکی خالی از بار، دیگری پر از بار و سومی نیمه پر بخواهند مسیر مشترکی را طی کنند. قطعا هواپیمای خالی زمان پرواز کوتاهتری دارد و زودتر به مقصد میرسد (زمان پرواز Time of flight).
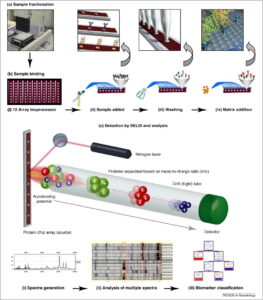
تصویر 9) نمای شماتیک از نحوهء عملکرد مس با سطوح فعال شده و آشکارساز زمان پرواز
کاربردهای مس اسپکترومتری نوع سلدی-تاف در علوم پزشکی:
1- بررسی تجمع پروتئینها
2- مطالعات میکروبشناسی
3- بررسیهای مختلف بافتی
4- بررسیهای ژنتیکی
5- بررسی تومورهای بدخیم و سرطانهای خون
6- بررسیهای انعقادی
7- شناسایی شاخصهای حیاتی (Biomarkers) جدید برای ردیابی و شناسایی بیماریها6-9
در این مورد ابتدا پروتئینهای مختلف در نمونههای بیولوژیک یک فرد مبتلا به بیماری خاص بررسی میشود و سپس نمونههای بیولوژیک یک فرد سالم نیز مورد آزمایش قرار میگیرد. از مقایسه الگوهای پروتئینهای مختلف (کاهش یا افزایش پروتئینها) میتوان شاخصهای جدیدی برای بیماری مورد نظر پیدا نمود. نمونهای از کاربرد در تحقیقات مرتبط با ایدز بسیار کمک کننده بود. به مدت حدود 15 سال محققین ایدز پژوه درگیر حل این معما بودند که چرا برخی افراد HIV مثبت به سندروم ایدز مبتلا نمیگردند. تنها یافته موثر در این سالها کشف CAF (CD28 antiviral factor) بود. پس از معرفی دستگاه سلدیتاف و بررسی این افراد گروهی از پروتئینها تحت عنوان آلفا دفنسین 1، 2 و 3 که خاصیت ضد تکثیر ویروسی داشتند شناسایی گردیدند.
مروری بر مقالات چاپ شده در حوزه سلدی تاف در موتور جستجوی پاب مد
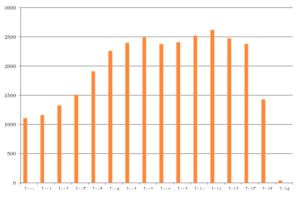
بررسی مقالات مرتبط با تکنیک سلدی تاف در موتور جستجوی پاب مد در محدوده زمانی ژانویه سال 2000 میلادی تا ابتدای ژانویه 2015 نشان دهنده چاپ 28812 مقاله است. توزیع فراوانی این مقالات در جدول 1 نشان داده شده است و بیانگر اوجگیری چاپ مقالات تا سال 2012 است هرچند پس از آن شاهد افت انتشار مقالات در این زمینه هستیم.
خلاصه:
مس اسپکترومتری تکنیکی جهت تعیین کیفی و کمی مواد بطور دقیق است. برای بررسی یک ماده در مس اسپکترومتری احتیاج به تولید رادیکال یونهایی از ماده مورد بررسی است تا دستگاه قادر به بررسی آنها باشد. امروزه انواع مختلفی از این دستگاه با ویژگیهای مختلف به بازار عرضه شده است که در حیطههای مختلف علوم کاربرد دارد.
نتیجه گیری:
امروزه در بسیاری از دانشگاهها و مراکز علمی دستگاه مس بصورت گسترده در مطالعات فیزیکی، شیمیایی، بیولوژیک برای طیف وسیعی ترکیبات بکار گرفته میشود. شکی نیست که در آینده شاهد پیشرفتهای بیشتر در بهبود تکنیکی این روش و توسعه آن در علوم مختلف پروتئومیک در علوم پزشکی خواهیم بود.
منابع:
- Volker Seibert. Et al. Surface-enhanced laser desorption ionization time-of-flight mass spectrometry (SELDI TOF-MS)and Protein Chips technology in proteomics research. Pathology– Research and Practice 200 (2004) 83–94.
- Chibo Liu. The Application of SELDI-TOF-MS in Clinical Diagnosis of Cancers. Journal of Biomedicine and Biotechnology. Volume 2011, Article ID 245821, 6 pages.
- Emanuel F Petricoin. et al. SELDI-TOF-based serum proteomic pattern diagnostics for early detection of cancer. Current Opinion in Biotechnology 2004, 15:24–30.
- Ning Tang, et al. Current development in SELDI affinity technology. Mass Spectrometry Reviews, 2004, 23, 34–44.
- Bischoff SR, et al. SELDITOF-MS analysis of transcriptional activation protein binding to response elements regulating carcinogenesis enzymes. Int J Mol Sci 2002. 3:1027–1038.
- Bane TK, et al. DNA affinity capture and protein profiling by SELDI-TOF mass spectrometry: Effect of DNA methylation. Nucleic Acids Res 2002.30:e69/1–e69/6.
- Hinshelwood J, et al. Identification of the C3b binding site in a recombinant vWF A domain of complement factor B by surface-enhanced laser desorption-ionization affinity mass spectrometry and homology modelling: Implications for the activity of factor J Mol Biol 294:587–599.
- Wright GL. SELDI Proteinchip MS: A platform for biomarker discovery and cancer diagnosis. Exp Rev Mol Diagn 2002.2:549–563.
https://www.google.com/url?sa=t&rct=j&q=&esrc=s&source=web&cd=&cad=rja&uact=8&ved=2ahUKEwjgzbnuxJz0AhVcQ0EAHcdABGgQFnoECB4QAQ&url=https%3A%2F%2Fwww.britannica.com%2Fscience%2Fmass-spectrometry&usg=AOvVaw3gYDDk2ELYr9eEhGt29Ysk
https://www.britannica.com/science/mass-spectrometry
برای دانلود پی دی اف بر روی لینک زیر کلیک کنید
ورود / ثبت نام



هزینه رپورتاژ آگهی توی سایت شما
چنده؟ ❤️❤️❤️
تسلایوپی اس
لطفا با شماره 55004855 تماس بگیرید