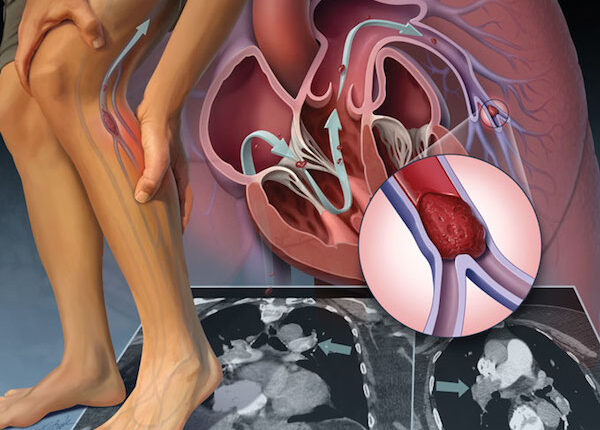
پایش آزمایشگاهی مقاومت دارویی به داروهای رایج ضد لختگی در بیماران قلبی و عروقی
قسمت دوم
دکتر حبیباله گلافشان عضو هیئت علمی دانشگاه علوم پزشکی شیراز
وارفارین:
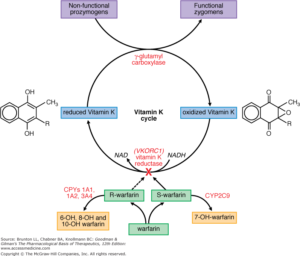
وارفارین یک ضدانعقاد خوراکی و مخلوطی راسمیک از ایزومرهای S,R میباشد که در این راستا ایزومر S توانایی بیشتری برای ضد لختگی دارد. وارفارین با ممانعت از عملکرد آنزیم احیاگر ویتامین K یا VKOR (Vitamin K epoxide reductase) خاصیت ضد انعقادی خود را ایفا میکند. گفتنی است که فاکتورهای انعقادی 2،7، 9، 10 و پروتئین های Z ,S ,C که تنظیمگر سیستم انعقاد بوده و نقش مهمی در جلوگیری از گسترش انعقاد دارند برای کارامد شدن نیاز به ویتامین K دارند. آنزیم کاربوکسیلاز کبدی در همراهی با ویتامین K به فرم احیا شده یک گروه کربوکسیل (-Carboxylationɤ) را به واحدهای مخصوص گلوتامیک اسید در فاکتورهای وابسته به ویتامین K پیوند داده و از این رو واحدهای ویژه گلوتامیک اسید که خود دارای یک گروه کربوکسیل هستند دارای یگ گروه کربوکسیل اضافی دیگر میگردند و درنتیجه هر واحد گلوتامیک اسید دارای دو شارژ منفی میشود (میدان GLA) و امکان پیوند فاکتورهای وابسته به ویتامین K با کمپلکس سطوح فسفولیپیدی با یون کلسیم (Ca++/phospholipid) را در پروسه انعقاد فراهم میسازد. این پروسه جهت انعقاد خون ضروری بوده و چنانچه اختلال در کربوکسیلاسیون فاکتورهای فوق رخ دهد سیستم انعقاد خون غیرکارامد میگردد. ویتامین K در فرایند کربوکسیلاسیون به شکل اکسیده شده در میآید که دوباره توسط آنزیم VKOR احیا شده و چرخه ادامه مییابد. داروی وارفارین با ممانعت از آنزیم VKOR و احتباس ویتامین K در شکل اکسید شده از کربوکسیلاسیون فاکتورهای وابسته به ویتامین K جلوگیری کرده و فاکتورهای 2،7، 9 و 10 را غیرکارآمد میکند.
فاکتورهای انعقادی 2، 7، 9 و 10 و پروتیینهای تنظیمکننده انعقاد (پروتیینهای C,S,Z) وابسته به ویتامین K میباشند. بدین مفهوم که برای کارآمد شدن نیازمند به افزایش یک گروه کربوکسیل به 12 تا 18 واحد اسید گلوتامیک در یک آرایش خطی در پایانهی آمینی هستند. فرآیند کاربوکسیلاسیون واحدهای اسید گلوتامیک تولید میدانی به نام GLA میباشد که در آن هر گلوتامیک اسید دارای دو شارژ منفی است و فاکتورها را قادر میسازد تا از طریق یون Ca2+ با سطوح فسفولیپیدی آنیونیک ارتباط برقرار کند. واکنش کاربوکسیلاسیون توسط آنزیم کربوکسیلاز کبدی صورت میگیرد و ویتامین K بصورت احیا شده کوفاکتور آن میباشد. در این فرآیند ویتامین K به فرم اکسیدشده یا اپوکسی در میآید که توسط آنزیم ردوکتاز کبدی دوباره احیا و در چرخه قرار میگیرد. وارفارین با تداخل در احیای دوباره ویتامین K از کارآمد شدن فاکتورهای وابسته به ویتامین K جلوگیری کرده و فاکتورهای انعقادی خون را رقیق میکند.
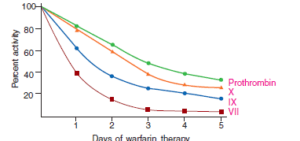
اثرات ضد لختگی وارفارین با سنجش زمان پروترومبین (PT) است. آزمایش زمان پروترومبین مسیر خارجی انعقاد را ارزیابی میکند و با توجه به اینکه سه فاکتور از 4 فاکتور وابسته به ویتامین K(2،7 و 10) در این مسیر قرار دارند از این رو آزمایشی مناسب جهت ارزیابی اثرات ضد لختگی وارفارین است. وارفارین به سرعت فاکتور 7 را به علت کوتاهترین نیمعمر بیولوژیک (4 تا 6 ساعت) ناکارآمد میکند و از آن پس فاکتور 10 با نیمعمر 24 تا 48 ساعت و فاکتور 2 با نیمه عمر 72-48 ساعت را ناکارآمد میکند. از این رو اثرات کامل وارفارین برای رسیدن به سطح یکنواخت ضد انعقادی پس از 4 تا 6 روز از شروع درمان مشخص میشود. طولانی شدن اولیه زمان PT با شروع درمان ناشی از افت سریع فاکتور 7 میباشد.
با شروع درمان وارفارین سطح فاکتور 7 پس از 6 ساعت به حدود 50% افت میکند و آزمایش PT طولانی میشود. ولی اثرات کامل وارفارین پس از 3 تا 5 روز از شروع درمان که تمام فاکتورهای وابسته به ویتامین K کاهش یافتند ظاهر میگردد. اولین آزمایش PT حدود 24 ساعت پس از درمان انجام میشود و از آن پس روزانه تکرار میشود تا زمانی که حداقل دو جواب پشت سرهم در طیف درمانی باشد و از آن پس هر 4 تا 12 هفته تا پایان درمان نیاز به چک کردن آزمایش است. برای یک حادثه ترومبوز درمان تا 6 ماه و جلوگیری از سکته مغزی و فیبریلاسیون دهلیزی درمان به صورت نامحدود ادامه مییابد.
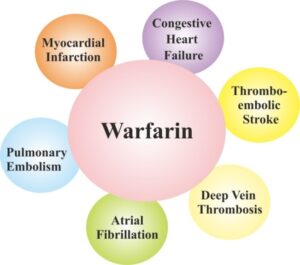
وارفارین اثرات ضدانعقادی خود را از طریق آنتاگونیست با ویتامین K ایجاد میکند و یک داروی مهم در جلوگیری از پدیدههای ترومبوآمبولی در بیماران مستعد به لختگی عروقی و نیز جلوگیری از پدیدههای ترومبوآمبولی ناشی از فیبریلاسیون دهلیزی و دریچه مصنوعی در قلب میباشد. وارفارین در پیشگیری از آمبولی بعد از سکته قلبی و نیز کاهش عود سکته قلبی کاربرد دارد.
کاربرد های گسترده وارفارین
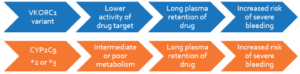
اثرات ضد انعقادی وارفارین وابسته به ژنتیک شخص بوده و فاکتورهایی مانند جنس، سن و وزن پیشبینی کننده ضعیف درمان هستند. ژنهای کنترل کننده فعالیت و متابولیسم وارفارین بیش از 50% نوسان اثر وارفارین را در بین بیماران عهدهدار میباشند. وارفارین با هدف قرار دادن آنزیم VKORC1 اثرات ضدانعقادی خود را اعمال کرده و آنزیم CYP2C9 با متابولیسم وارفارین سطح دارویی را تنظیم میکند. ایزومر S وارفارین توسط آنزیم CYP2C9 و ایزومر R آن توسط آنزیمهای CYP1A2 و CYP3A4 متابولیزه و از بدن پاکسازی میشوند. سه پلیمورفیسم تکنوکلئوتیدی (SNPS) که دو تای آن در ژن CYP2C9 و یکی در ژن VKORC1 رخ میدهد دارای اثرات کلیدی در تعیین دوزاژ وارفارین میباشند. گونه نرمال و اصلی
(Wild type) آنزیم CYP2C9 را با نشانه 1* و پلیمورفیسمهای دیگر با نشانه 2* و 3* علامتگذاری میشود. هر شخص میتواند دو آلل از پلیمورفیسمهای مختلف (SNP) را مانند 1*/1* یا 3*/1* یا 3*/3* و غیره را به ارث ببرد. شیوع پلیمورفیسمها در نژادها و جمعیتهای مختلف یکسان نمیباشد.
فراوانی پلی مورفیسم های CYP2C9 و VKORC1
پلی مورفیسم CYP2C9*1 به وارفارین حساس بوده و به طور طبیعی آنرا متابولیزه میکند در حالیکه سرعت متابولیسم وارفارین با گونه 2* تا 30% و در گونه 3* تا 90 درصد کاهش مییابد. از اینرو در واریانهای 2* و 3* با توجه به کاهش سرعت متابولیسم نیاز به دوزاژ کمتر و پیگیری بیشتری با آزمایش PT/INR میباشد.
وراثت گونه های *2 و*3 موجب انباشتگی وارفارین در بدن و افزایش نامتناسب PT/INR و میل به خونریزی میگردد.
آنزیم VKORC1 دارای دو پلیمورفیسم مهم A و G میباشد. آلل A یا هاپلوتیپ A مقدار کمتری از آنزیم VKOR را نسبت به الل G تولید میکند و از این رو دوزاژ وارفارین کمتری برای جلوگیری از عملکرد آن لازم است.
تنظیم دوزاژ وارفارین با توجه به پلیمورفیسمهای آنزیم احیاگر ویتامین K (VKORC1)
بیماران با هاپلوتیپ های CYP2C9*2 و C9YP2C9*3 به طور میانگین به ترتیب به کاهش 19% و 33% به ازای هر الل نسبت به الل 1* دارند. وراثت هاپلوتیپ A از ژن VKORC1 به طور میانگین نیاز به کاهش 28% در دوزاژ وارفارین به ازای هر الل نسبت به افرادی که الل A ندارند میباشد.
درمان استاندارد وارفارین در بیمار با اللهای 2* و 3* و نیز الل A با پاسخ آزمایشگاهی PT/INR خارج از طیف درمانی (INR>4) بروز میکند. فنوتیپهای G/G و 1*/1* حساسیت کمتری به وارفارین داشته و برای دستیابی به INR مطلوب نیاز به افزایش دوزاژ وارفارین نسبت به حالت استاندارد دارند. به نظر میرسد تنظیم وارفارین بر اساس فارموژنتیک زمانی لازم است که بیمار به صورت طولانی مدت پاسخ غیرمنتظره و نامتناسب با آزمایش PT/INR بدهد. بیمارانی که با دو دوزاژ وارفارین، PT/INR بیشتر از 1/5 می گردد، ممکن است در گروه متوسط تا خفیف حساس به وارفارین باشند و به دوزاژ کمتری نسبت به استاندارد درمان نیاز داشته باشند.
داروهای گوناگون با تحریک آنزیم CYP2C9 و یا افزایش سرعت پاکسازی و یا کندکردن سرعت پاکسازی روی غلظت وارفارین اثر میگذارند برای مثال استفاده از چای سبز، آووکادو و سبزیجات با برگهای پهن یک منبع غنی از ویتامین K بوده و موجب کاهش اثر وارفارین میگردد و یا آنتیبیوتیکها با کاهش دادن فلورهای روده که منبع تولید ویتامین K میباشند موجب تقویت اثر وارفارین میگردند. به نظر میرسد که معرفی بعضی از داروها برای پزشک و مسئول فنی آزمایشگاه برای تفسیر نتیجه PT/INR ضروری میباشد.
مهمترین داروهایی که اثر وارفارین را کاهش داده و موجب کاهش PT/INR میگردند
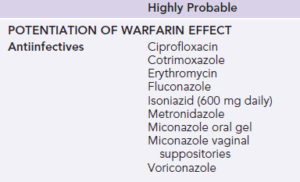
مهمترین داروهای ضدمیکروبی و ضدقارچی که اثرات وارفارین را افزایش داده و موجب افزایش PT/INR حتی به دو تا سه برابر میگردند
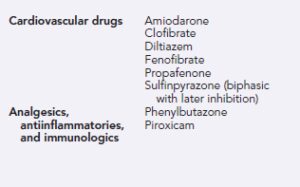
مهمترین داروهای قلبی و ضدالتهابی که اثرات وارفارین را افزایش داده و موجب افزایش PT/INR میشوند
مهمترین داروهای عصبی و گوارشی که اثرات وارفارین را افزایش داده و موجب افزایش PT/INR میشوند
|
|
|
|
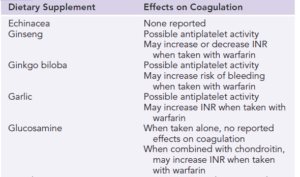
مهمترین داروهای گیاهی اثرگذار بر سیستم انعقادی که احتمال تداخل آنها در تستهای آزمایشگاهی میباشد |
|
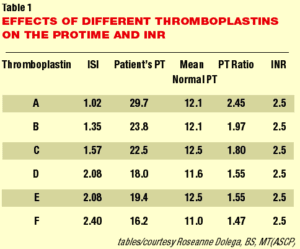
معرف فاکتور بافتی که در آزمایش PT به کار میرود، بر اساس منبع دارای حساسیت متفاوتی در کمبود فاکتورهای مسیر وابسته به ویتامین K است. درجه حساسیت معرف فاکتور بافتی با ISI (International Sensitivity index) یا نشانه حساسیت بینالملل مشخص میشود. معرف PT با ISI کمتر از 1.4 (بین 1/4-1) بسیار حساس و بین 1/4 تا 1/7 دارای حساسیت متوسط و بیشتر از 2 دارای حساسیت کم است. وقتی گفته میشود حساسیت معرف PT برای مثال ISI=1/2 است، بدین مفهوم است که آزمایش PT در کمبود فاکتورهای انعقادی به سرعت طولانی میشود، برای مثال اگر PT بیماری با ISI=2 برابر 17 ثانیه باشد با ISI=1 ممکن است حدود 25 تا 30 ثانیه گردد.
چنانچه گزارش آزمایش PT بر مبنای INR (نسبت همسو شده بینالملل) باشد وابستگی آزمایش PT به حساسیت معرف از بین میرود. برای محاسبه INR نسبت PT بیمار بر حسب ثانیه به میانگین PT پلاسمای نرمال به توان ISI میرسد. هنگامی که PT بیمار بر اساس INR گزارش شود مثل این است که نسبت PT بیمار به کنترل با معرف PT مرجع بینالملل انجام شده است.
آزمایش PT بیمار با دو معرف PT که یکی دارای ISI=1.24 و دیگری دارای ISI=2.46 بوده است انجام شده است. همانطور که مشاهده میشود جواب PT/INR برای هر دو معرف یکسان بوده و وابستگی آن به حساسیت معرف از بین رفته است. توجه داشته باشید که معرف PT با ISI نزدیک به یک در کمبود فاکتورهای انعقادی طولانیتر از معرف PT با ISI بالاتر از 2 میگردد. (16/2 ثانیه در مقابل 22 ثانیه)
سازمان بهداشت جهانی معرف PT شرکت سازنده را با معرف مرجع که از مغز انسان تهیه و دارای ISI یک است مقایسه کرده و ضریب ISI را به معرف شرکت سازنده میدهد. ضریب ISI ممکن است به صورت عمومی و یا با توجه به نوع تجهیزاتی که آزمایش با آن انجام می شود اختصاصی باشد.
در جدول فوق از یک نمونه پلاسمای بیمار که روی درمان با وارفارین بوده است با شش نوع معرف PT که دارای ISI های متفاوت از 1/02 تا 2/4 بوده است آزمایش PT انجام گرفته و جوابهای آزمایش از 29/7 ثانیه تا 16/2 ثانیه متغییر بوده است و این تفاوت ناشی از تفاوت در حساسیت معرف PT است. بدین مفهوم که معرف PT با ISI نزدیک به یک در کمبود فاکتورهای انعقادی بسیار طولانی و با ISI بالا چندان طولانی نمیگردند ولی جواب INR برای معرفهای PT با حساسیت های مختلف یکسان است.
پلیمرفیسمی از فاکتور هفت به نام فاکتور هفت Padua وجود دارد که تنها با فاکتور بافتی انسانی در پروسه انعقاد شرکت میکند و پاسخ PT نرمال با معرف بافتی انسانی میدهد در حالی که با استفاده از فاکتور بافتی تهیه شده از خرگوش جواب طولانی بدست میدهد. سفارش میشود که جهت آزمایش روتین PT برای بیمارانی که چکآپ میشوند و یا عمل جراحی دارند و وارفارین مصرف نمیکنند از معرف PT با حسایت متوسط حدود 1/7 استفاده شود، در غیر این صورت استفاده از PT با ISI نزدیک به یک جواب PT را حتی در مواردی که کمبود فاکتورهای انعقادی جزیی بوده و ارزش بالینی ندارد طولانی کرده و اقدام به تزریق غیر ضروری پلاسما میگردد. گفتنی است که سطح فاکتورهای انعقادی حدود 20% تا 50% برای ثبات انعقادی کافی است.
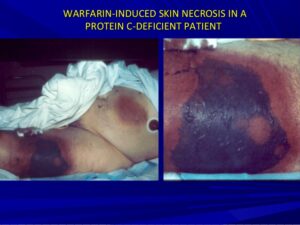
با مصرف وارفارین سطح پروتیینهای تنظیمگر انعقادخون که جلوگیری از گسترش انعقاد میکنند کاهش مییابد که در این میان پروتیین C که نیمه عمر حدود 6 ساعت دارد و وابسته به ویتامین K است دارای اهمیت ویژه است. با کاهش پروتیینهای تنظیمگر در 2 تا 3 روز اول از شروع درمان با وارفارین بیمار در خطر ابتلا به ترومبوز قرار میگیرد و از این رو درمان با وارفارین گاهی برای 5 روز اول با هپارین همراه میگردد. رعایت نکردن این روند درمانی به ویژه در بیماران با کمبود پروتیین C موجب نکروز پوستی ناشی از وارفارین (warfarin skin necrosis) گردیده که یک واکنش شدید ترومبوتیک پوست همراه با خارش شدید است که نیاز به برداشتن بافتهای مرده (debridement) با جراحی است.
بیماران مبتلا به ترومبوز عروق عمقی (DVT) که برای مدت 7 تا 10 روز هپاریندرمانی میشوند بایستی چند روز قبل از قطع هپارین داروی وارفارین نیز همزمان تجویز شود و با قرار گرفتن PT/INR در سطح درمانی، تجویز هپارین قطع گردیده و مصرف وارفارین ادامه مییابد. با توجه به اینکه هپارین میتواند آزمایش PT را طولانی کند سفارش میشود که در این گونه موارد از کیتهای PT حاوی جاذب هپارین یا با آنزیم هپاریناز استفاده شود تا بتوان میزان PT را تنها با توجه به سطح دارویی وارفارین بدست آورد.
کنترل کیفی تستهای معمول انعقادی
آشنایی با آزمایشهای انعقادی PTT & APTT
برای دانلود پی دی اف بر روی لینک زیر کلیک کنید
ورود / ثبت نام