اهمیت تشخیصی میکروآر.ان.ایها در دیابت
سیدآرمان مهدوی[1] و ستار گرگانی فیرزجایی 2
1- دانشجوی کارشناسی ارشد بیوتکنولوژی پزشکی، مرکز تحقیقات بیولوژی مولکولی، دانشگاه علوم پزشکی بقیه ا…(عج)، تهران، ایران (نویسنده مسئول) (livesnuff@gmail.com)
2- استادیار بیوشیمی بالینی، گروه علوم آزمایشگاهی، دانشکده پیراپزشکی، دانشگاه علوم پزشکی ارتش، تهران، ایران
چکیده:
دیابت بهعنوان رایجترین بیماری مزمن جهان شناخته میشود. این بیماری بهعنوان یک بیماری چندعاملی در دو گروه 1 و 2 طبقهبندی شده و مکانیسمهای اصلی بیماریزایی آن ناشناخته باقی مانده است. با کشف اخیر میکروRNAها، این Ribonucleotides کوچک بهعنوان نشانگرهای جدید در پاتوژنز دیابت و عوارض دیابت و همچنین شناسایی آن نقش دارند. همچنین نقش MiRNA برای تنظیم تولید و ترشح انسولین مورد توجه قرار گرفته است. در این مقاله خلاصهای از جدیدترین یافتهها و دستاوردها در مورد بیماریزایی و عوارض دیابت و اهمیت تشخیصی میکروRNAها در دیابت مورد بررسی قرار گرفته است.
کلمات کلیدی: دیابت، مقاومت به انسولین و میکرو RNA
ﻣﻘﺪﻣﻪ و تاریخچه
از زﻣﺎن ﮐﺸﻒ اوﻟﯿﻦ ﻣﻮﻟﮑﻮل ﻣﯿﮑﺮوRNA ﺗﺎ ﺑﻪ اﻣﺮوز، ﺣﺪود 20 ﺳﺎل میگذرد و ﺗﺤﻘﯿﻘﺎت در اﯾﻦ زﻣﯿﻨﻪ رﺷﺪ قابلملاحظهای داﺷﺘﻪ اﺳﺖ. ﻣﯿﮑﺮوRNAﻫﺎ مولکولهای ﮐﻮﭼﮑﯽ ﻫﺴﺘﻨﺪ ﮐﻪ در ﻓﺮآﯾﻨﺪﻫﺎي ﻓﯿﺰﯾﻮﻟﻮژﯾﮏ، ﭘﺎﺗﻮﻟﻮژﯾﮏ، رﮔﺰاﯾﯽ، آﭘﻮﭘﺘﻮزیس و ﺳﺮﻃﺎن ﻧﻘﺶ ﮐﻠﯿﺪي دارﻧﺪ. اﯾﻦ مولکولها 25-18 ﻧﻮﮐﻠﺌﻮﺗﯿﺪ ﻃﻮل داﺷﺘﻪ و حفاظتشده ﻫﺴﺘﻨﺪ و از ﻃﺮﯾﻖ ﻣﻬﺎر ﺗﺮﺟﻤﻪ ﯾﺎ اﻟﻘﺎء ﺗﺠﺰﯾﻪ mRNA ﻣﮑﺎﻧﯿﺴﻢ ﺧﻮد را اﻋﻤﺎل میکنند.
ﮐﺸﻒ ﻣﯿﮑﺮوRNAﻫﺎ در دﻫﻪ 1990 ﻣﻨﺠﺮ ﺑﻪ اﻧﻘﻼﺑﯽ ﻋﻈﯿﻢ در ﺗﺤﻘﯿﻘﺎت زﯾﺴﺘﯽ ﺷﺪ، اﻣﺎ ﺑﺎ ﮔﺬﺷﺖ ﺣﺪود 20 ﺳﺎل از اﯾﻦ ﮐﺸﻒ ﺗﺎرﯾﺨﯽ، ﻣﮑﺎﻧﯿﺴﻢ ﺗﻨﻈﯿﻢ ژﻧﯽ اﯾﻦ مولکولهای ﮐﻮﭼﮏ ﻫﻤﭽﻨﺎن بهصورت سؤالی اﺳﺎﺳﯽ ﻣﻄﺮح است. ﺗﺎ ﺑﻪ اﻣﺮوز مقالات متعددی منتشر شده ﮐﻪ ﻣﺤﻮرﻫﺎي اﺻﻠﯽ ﺗﺤﻘﯿﻘﺎت ﺑﺎﻟﯿﻨﯽ و ﻣﻮﻟﮑﻮﻟﯽ را ﭘﻮﺷﺶ میدهد و ﻧﻘﺶ اﯾﻦ مولکولهای ارزﺷﻤﻨﺪ در ﺗﻨﻈﯿﻢ ﺑﯿﺎن ژن ﻏﯿﺮﻗﺎﺑﻞ اﻧﮑﺎر اﺳﺖ. ﯾﮏ ﻣﻮﻟﮑﻮل ﻣﯿﮑﺮو RNA میتواند بهتنهایی ﺑﺎ اﺗﺼﺎل ﺑﻪ ﻧﺎﺣﯿﻪ ﺗﺮﺟﻤﻪ ﻧﺸﺪﻧﯽ ‘3 ﻣﺎﻧﻊ از ﺗﺮﺟﻤﻪ ﺻﺪﻫﺎ ﻣﻮﻟﮑﻮل mRNA ﺷﻮد. ﻣﻄﺎﻟﻌﺎت ﺑﯿﻮاﻧﻔﻮرﻣﺎﺗﯿﮏ بیانگر کنترل بیش از ﯾﮏﺳﻮم ژﻧﻮم اﻧﺴﺎﻧﯽ توسط ﻣﯿﮑﺮوRNAﻫﺎ است و آنها تقریباً در ﺗﻤﺎم پروسههای زﯾﺴﺘﯽ نظیر ﺗﮑﺜﯿﺮ سلولی، آﭘﻮﭘﺘﻮزیس، ارﮔﺎﻧﺰاﯾﯽ و ﺧﯿﻠﯽ ﻣﻮارد دﯾﮕﺮ دﺧﯿﻞ ﻫﺴﺘﻨﺪ.
ﺩﺭ ﺳﺎﻝ 1993 ﺍﻭﻟﻴﻦ ﻣﻴﻜﺮﻭRNA ﺑﻪ ﻧﺎﻡ lineage-4) Lin-4) ﺩﺭ Caenorhabditis elegans ﻛﺸﻒ ﺷﺪ، ﺍﻣﺎ ﺍﻫﻤﻴﺖ این مولکول ﺑﻪﻋﻨﻮﺍﻥ ﻳﻚ ﺗﻨﻈﻴﻢﻛﻨﻨﺪﻩﻱ ﺯﻳﺴﺘﻲ ﺗﺎ ﺳﺎﻝ 2001 ﻛﻪ ﻧﻤﻮﻧﻪﻱ ﺩﻳﮕﺮﻱ ﺑﻪ ﻧﺎﻡ Let-7 ﺷﻨﺎﺳﺎﻳﻲ ﺷﺪ، ﻣﺸﺨﺺ نگردید. ﺩﺭ ﺳﺎﻝ 2001 ﻓﻘﻂ 5 ﻣﻘﺎﻟﻪ ﺩﺭ ﻣﻮﺭﺩ ﻣﻴﻜﺮﻭRNAﻫﺎ ﻧﻮﺷﺘﻪ شده بود، درحالیکه ﺗﺎ ﺳﺎﻝ 2008 ﺣﺪﻭﺩ 3500 ﻣﻘﺎﻟﻪ ﺩﺭ ﭘﺎﻳﮕﺎﻩ ﺩﺍﺩﻩﻫﺎﻱ Pubmed ﻣﻨﺘﺸﺮ ﺷﺪ ﻛﻪ 1500 ﻣﻘﺎﻟﻪ ﻓﻘﻂ ﻣﺮﺑﻮﻁ ﺑﻪ ﺳﺎﻝ 2008 ﺑﻮﺩ. ﺗﻮﺟﻪ ﺑﻴﺶ ﺍﺯ ﭘﻴﺶ ﺑﻪ ﺳﺎﺧﺘﺎﺭ ﻭ ﻋﻤﻠﻜﺮﺩ ﻣﻴﻜﺮﻭRNAﻫﺎ ﺑﻪ ﻋﻠﺖ تأثیر ﺁﻥﻫﺎ ﺩﺭ ﻓﺮﺍﻳﻨﺪﻫﺎﻱ ﻣﺘﻨﻮﻉ ﺗﻜﻮﻳﻨﻲ ﻭ ﻓﻴﺰﻳﻮﻟﻮژﻳﻜﻲ ﻣﺎﻧﻨﺪ ﺁﭘﻮﭘﺘﻮﺯیس، ﺗﺮﺷﺢ ﺍﻧﺴﻮﻟﻴﻦ، خونسازی، ریختزایی ﻣﻐﺰ ﻳﺎ ﺗﻤﺎﻳﺰ ﺑﺎﻓﺘﻲ ﻭ ﺩﺭﮔﻴﺮﻱ ﺁﻥﻫﺎ ﺩﺭ ﺩﻓﺎﻉ ﺍﻳﻤﻨﻲ ﻭ ﺑﻴﻤﺎﺭﻱﻫﺎﻱ ﻭﻳﺮﻭﺳﻲ ﺍﺳﺖ [1].
تعریف میکرو RNA
میکروآر.ان.ایﻫﺎ زﯾﺮﮔﺮوه ﺑﺰرﮔﯽ از ﺧﺎﻧﻮاده RNAﻫﺎي ﻏﯿﺮﮐﺪﮐﻨﻨﺪه 25-18 ﻧﻮﮐﻠﺌﻮﺗﯿﺪي ﻫﺴﺘﻨﺪ ﮐﻪ ﺑﯿﺎن ژن را ﭘﺲ از روﻧﻮﯾﺴﯽ با ﺗﺠﺰﯾﻪ ﯾﺎ ﻣﻬﺎر ﺗﺮﺟﻤﻪ mRNA از ﻃﺮﯾﻖ ﻣﮑﺎﻧﯿﺴﻢ RNAi اﻟﻘﺎء میکنند. RNAi ﻧﻮﻋﯽ ﻣﮑﺎﻧﯿﺴﻢ خاموشکننده ﭘﺲ از روﻧﻮﯾﺴﯽ است ﮐﻪ ﺑﺎ اﺗﺼﺎل ﺟﺰﺋﯽ ﻣﯿﮑﺮوRNA ﺑﻪ ﻧﺎﺣﯿﻪ ‘3-UTR در mRNA ﻫﺪف ﺳﺒﺐ ﻣﻬﺎر ﺗﺮﺟﻤﻪ ﯾﺎ ﺗﺠﺰﯾﻪ آن میگردد. ﭘﺮﺍﻛﻨﺪﮔﻲ ژﻥﻫﺎﻯ ﻣﻴﻜﺮﻭRNA ﺩﺭ ژﻧﻮﻡ بهصورت ﻣﻨﻔﺮﺩ ﻳﺎ خوشهای بوده ﻭ ﺑﺮﺧﻰ ﺩﺭ ﻧﻮﺍﺣﻰ ﺑﻴﻦ ژﻧﻰ ﻭ ﺣﺪﺍﻗﻞ ﻧﻴﻤﻰ ﺍﺯ ﺁﻥﻫﺎ ﺩﺭ ﻭﺍﺣﺪﻫﺎﻯ ﺭﻭﻧﻮﻳﺴﻰ ﻣﻌﻴﻨﻰ ﻣﺜﻞ ﺍﻳﻨﺘﺮﻭﻥ ﻭ ﺍﮔﺰﻭﻥﻫﺎﻯ ﻛﺪﻛﻨﻨﺪﻩ ﭘﺮﻭﺗﺌﻴﻦ ﻭ ﺭﻭﻧﻮﺷﺖﻫﺎﻳﻰ ﻛﻪ ﭘﺮﻭﺗﺌﻴﻦ را ﻛﺪ نمیکنند، ﻳﺎﻓﺖ شدهاند [1].
اهمیت و کاربرد
در دهه اخیر مطالعات بیانگر نقش مهم و حیاتی miRNAs در تنظیم بیان ژنهای مرتبط با سرطان هستند. این مولکولهای تکرشتهای قادر به تحمل نوع خاصی از اصلاح مولکولی هستند که از نتایج فیزیولوژیکی ویژهای برخوردار است. حدود یک میلیون میکروآر.ان.ای در سلولهای بدن وجود دارد که ۲۵۰۰۰ مورد باعث مهار تولید پروتئینها میشوند. با توجه به اینکه میکروآر.ان.ایها با بیماریها ارتباط مستقیم دارند، بهسرعت وارد فاز کلینیکی (تولید دارو و درمان و تشخیص) شدهاند، بهگونهای که کمپانیهای بزرگ دارویی در دنیا به تحقیقات، ساخت دارو و درمان با استفاده از میکروآر.ان.ایها توجه ویژهای دارند [2].
ﭼﯿﺪﻣﺎن ژنهای ﻣﯿﮑﺮوRNA ﺑﺮ روي ﮐﺮوﻣﻮزوم
اﮐﺜﺮ ژنهای ﻣﯿﮑﺮوRNAﻫﺎ بهصورت خوشهای بر روي کروموزومها ﻗﺮار گرفتهاند. ﺗﺎ ﺑﻪ اﻣﺮوز ﺗﺤﻘﯿﻘﺎت زﯾﺎدي ﺑﯿﺎن کردهاند ﮐﻪ خوشههای ﮔﻮﻧﺎﮔﻮﻧﯽ ﺑﺮ روي کروموزومهاي ﻣﺨﺘﻠﻒ وﺟﻮد دارﻧﺪ. ﺑﺮﺧﯽ از اﯾﻦ خوشهها بهصورت ﭼﻨﺪ ﺳﯿﺴﺘﺮوﻧﯽ ﻫﺴﺘﻨﺪ و در ﻣﻮارد دﯾﮕﺮ ﭘﺲ از ﭘﺮدازش از روي ﭼﻨﺪﯾﻦ ﻣﯿﮑﺮوRNA ﺗﻨﻬﺎ ﯾﮏ روﻧﻮﺷﺖ اوﻟﯿﻪ ﺗﻬﯿﻪ میشود ﮐﻪ ﺑﻪ ﭼﻨﺪﯾﻦ ﻣﯿﮑﺮوRNA ﺗﺒﺪﯾﻞ میگردد. علاوه بر این ﻣﻄﺎﻟﻌﺎت دﯾﮕﺮي اﻧﺠﺎم ﺷﺪه اﺳﺖ ﮐﻪ ژنهای ﻣﯿﮑﺮوRNA را در دو گروه ﺑﯿﻦ ژﻧﯽ و درون ژﻧﯽ ﺗﻘﺴﯿﻢ میکنند و ﮔﺮوه دوم ﺧﻮد ﺑﻪ ﭼﻬﺎر زﯾﺮﮔﺮوه ﺗﻘﺴﯿﻢ میشوند (ﺟﺪول 1).
ﺟﺪول 1: ﭼﯿﺪﻣﺎن ژنهای ﻣﯿﮑﺮوRNAها
| ردیف | نام گروه | نام زیر گروه | درصد |
| 1 | میکروRNAهای بین ژنی | 46.5 | |
| 2
|
میکروRNAهای درون ژنی
|
میکروRNAهای اینترونی
میکروRNAهای اگزونی میکروRNAهای ناحیه ‘3-UTR میکروRNAهای ناحیه ‘5-UTR |
44 7 1.5 1 |
ﭘﺮدازش و ﺗﻮﻟﯿﺪ (Biogenesis) ﻣﯿﮑﺮوRNAﻫﺎ
تولید زیستی میکرو RNAشامل چندین مرحله مختلف است. ژن کدکنندۀ میکروآر.ان.ای ها ابتدا توسط RNA پلیمراز II رونویسی شده و رونوشت میکرو RNA اولیهPri-miRNA را ایجاد میکند. سپس پردازش و بلوغ آنها توسط دو آنزیم اندونوکلئاز و ریبونوکلئاز RNase III که Drosha و Dicer نام دارند، انجام میشود. میکروآر.ان.ایها از یک مولکول RNA ابتدایی بلند و تکرشتهای (ssRNA) که توانایی تبدیل به یک مولکول دو رشتهای (dsRNA) را دارد، تولید میشوند. آنزیم شرکتکننده در این فرایند تغییر ساختار یک RNase III از خانوادهی Drosha/Dicer است.
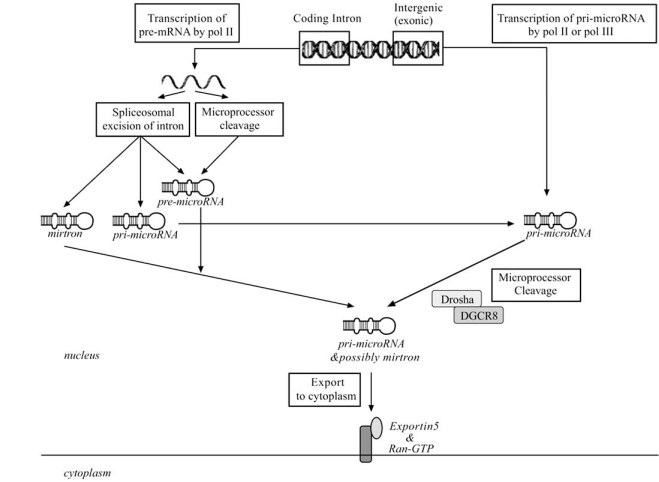
ﺑﻴﻮژﻧﺰ ﻣﻴﻜﺮﻭ RNAﻫﺎ ﺩﺭ ﻫﺴﺘﻪ ﻭ ﺳﻴﺘﻮﭘﻼﺳﻢ ﺻﻮﺭﺕ میگیرد. ﻣﻴﻜﺮﻭ RNAﻫﺎ ﭼﻨﺪﻳﻦ ﻛﻴﻠﻮ ﺟﻔﺖ ﺑﺎﺯ ﺭﻭﻧﻮﺷﺖ آغازین طول ﺩﺍﺭند ﻭ ﺗﻮﺳﻂ RNA ﭘﻠﻴﻤﺮﺍﺯ II ﺭﻭﻧﻮﻳﺴﻰ ﺷﺪﻩ ﻭ ﭘﻠﻰﺁﺩﻧﻴﻠﻪ ﻣﻰﺷﻮند که دارای دو مرحله است؛ یک مرحلهی هستهای و یک مرحلهی سیتوپلاسمی. این دو مرحله توسط دو آنزیم اندونوکلئاز III به نامهای Drosha و Dicer انجام میشود. ابتدا Drosha که یک ریبونوکلئاز هستهای است و پروتئین همراه 8، تشکیل مجموعهای به نام DGCR8 را میدهند که در هسته سلول،Pri-miRNA را به پیشساز ساقه- حلقه به نام Pre-miRNA پردازش میکنند و این ساختار حدود 110 -60 نوکلئوتید دارد. ژنهای miRNA پس از بیان، یک miRNA اولیه به نام pri-miRNA تولید میکنند که ویرایش شده و پیشساز miRNA به نام pre-miRNA را در نهایت ایجاد میکند، سپس Pre-miRNA توسط مکانیسمی که توسط Exportin5 وابسته به Ran-GTP انجام میشود و بهطور ویژه ساختار مولکولهای Pre-miRNA را شناسایی میکند، از هسته به سیتوپلاسم منتقل میشود. در مرحلهی بعد miRNA دو رشتهای ساخته شده و در نهایت این miRNA دو رشتهای، miRNA بالغ و تکرشتهای را به وجود میآورد (شکل 1).
شکل 1: مراحـل تولیـد زیسـتی میکـرو RNA از هسـته تـا سیتوپلاسم
پـس از رونویسـی از ژن میکــرو RNA، رونوشــت اولیهای بــه نــام Pri-miRNA در هســته تولیــد میشود و تحت تأثیر آنزیـم ریبونوکلئـاز هستهایDrosha به Pre-miRNA پـردازش میشود کـه توسـط Exportin-5 بـه سیتوپلاسم منتقـل میگردد. آنزیـم Dicer ریبونوکلئـاز سیتوپلاسـمی بوده وPre-miRNA را بـه میکـرو RNA دو رشتهای 21 نوکلئوتیـدی بـرش میدهد و سـپس یـک رشـته از آن بـرای بارگـذاری بـر روی کمپلکـس خامـوشکننـده القـاشـده توسـطRNA (RISC) انتخــاب میگردد. ایــن کمپلکــس، میکــرو RNA را بــه ناحیه ʹUTR 3 در mRNA هــدف هدایــت میکند و سـبب تجزیـه mRNA ی هـدف و یـا مهـار ترجمـه آن میشود (http://www.nature.com/ncb/journal/v11/n3/full/ncb0309-228.html)
نقش میکرو RNAها در تشخیصهای آزمایشگاهی
ميكروRNAهاي گردش خون، کاندید بیومارکری جديد هستند. از مزيتهاي اين ميكروRNAها میتوان به سهولت نمونهگيري، پايداري در شرايط مختلف، سنجش بهوسیله روشهای حساس، اختصاصيت و تكرارپذيری اشاره كرد.
آشکار شدن سریع تغییرات حاصل از بیان یا عدم بیان ژن مذکور بهطور سریع و قاطع قابل شناسایی است، بهطوریکه با طراحی روشهای PCR Real-time میتوان به آشکار شدن بسیاری از بدخیمیها و یا بیماریهای خودایمن پی برد و امروزه با کشف میکروآر.ان.ای های مرتبط با هر نوع اختلال و تحت نظر گرفتن شدت بیان یا کاهش بیان آن جهت درمان یا پیشگیری اقدام کرد. امروزه با توجه به محافظت زیاد در برابر تغییرات محیطی، این مولکولها در جهت درمان بسیاری از بیماریها قابل استفاده هستند [1].
ميكروRNAها با مكانيسمي دقيق از طریق ناحيه `3 ترجمه نشده (`3-UTR) توالي mRNA هدف را در مرحله بعد از رونويسي يا ترجمه خاموش مينمايند.
آزمایشهای زﯾﺎدي ﻧﺸﺎن داده اﺳﺖ ﮐﻪ ﺑﺮﺧﻼف mRNAﻫﺎ، ﻣﯿﮑﺮوRNAﻫﺎ در دﻣﺎي اﺗﺎق و ﻫﻤﭽﻨﯿﻦ در چرخههای ﭘﯿﺎﭘﯽ اﻧﺠﻤﺎد- ذوب میتـــــوانند ﭘﺎﯾﺪار ﺑﻤﺎﻧﻨﺪ. فرضیههای ﮔﻮﻧﺎﮔﻮﻧﯽ ﺑﺮاي ﺑﯿﺎن اﯾﻦ ﭘﺎﯾﺪاري ﻣﯿﮑﺮوRNAﻫﺎ ﻣﻄﺮح ﺷﺪه اﺳﺖ ﮐﻪ اوﻟﯿﻦ آﻧﻬﺎ ﭘﺎﯾﺪاري ﻣﯿﮑﺮوRNAﻫﺎ را ﺑﻪ ﺧﺎﻃﺮ ﻃﻮل ﮐﻮﭼﮏ آﻧﻬﺎ میدانند، اما طی آزمایشها مشخص شد اﺿﺎﻓﻪ ﮐﺮدن ﻣﯿﮑﺮوRNAﻫﺎي ﺳﻨﺘﺰﺷﺪه ﯾﺎ خالصشده ﺑﻪ ﭘﻼﺳﻤﺎ ﺳﺒﺐ اﻟﻘﺎی ﺗﺠﺰﯾﻪ آﻧﻬﺎ میگردد، همچنین ﻣﻬﺎر ﻓﻌﺎﻟﯿﺖ RNAase ﻗﺒﻞ از اﺿﺎﻓﻪ ﮐﺮدن ﻣﯿﮑﺮوRNAﻫﺎي خالصشده ﺳﺒﺐ ﻣﻬﺎر ﺗﺠﺰﯾﻪ آﻧﻬﺎ میشود، ازاینرو طول کوچک ﻣﯿﮑﺮوRNAﻫﺎ نمیتواند ﻋﺎﻣﻞ ﭘﺎﯾﺪاري آﻧﻬﺎ ﺑﺎﺷﺪ، ﺑﻨﺎﺑﺮاﯾﻦ ﻋﻠﺖ ﭘﺎﯾﺪاري ﻣﯿﮑﺮو RNAﻫﺎ ﻫﻨﻮز ﯾﮏ سؤال ﺑﺎﻗﯽ ﻣﺎﻧﺪه و ﻧﯿﺎزﻣﻨﺪ ﺗﺤﻘﯿﻘﺎت ﺑﯿﺸﺘﺮي اﺳﺖ [3].
میکروآر.ان.ایها در سلولهای بافتهای مختلف، مایع پلاسما و دیگر مایعات بدن مانند ادرار، اشک و مایع آمنیون به شکل پایدار و بهصورت متصل به کمپلکس خاموشکننده القاشده توسط RNA یافت میشوند. به این ترتیب، میکروآر.ان.ایها از دسترس فعالیت RNaseهای با منشأ داخلی محافظت میشوند و به همین دلیل است که میکروآر.ان.ایها به شرایط سخت مقاوماند [2].
میزان میکروآر.ان.ای تعیینشده در سرم و ردههای سلولی متفاوت است که این اختلاف به این دلیل است که میکروآر.ان.ای موجود در سرم، محصول تخریب سلول تومور یا شکل فعال اگزوزونهای در حال انتقال است. تفاوت مشاهدهشده بین میزان میکروآر.ان.ای بافت و سرم نیز به مکانیسم آزادسازی میکروآر.ان.ایهای بافت به جریان خون نسبت داده میشود. الگوی سرمی میکروآر.ان.ای در سرم مردان و زنان سالم یکسان است که نشاندهنده عدم ارتباط این الگوی سرمی با جنسیت است. ارزیابی و سنجش میکروآر.ان.ایها از جهت کنترل فعالیتها با روشهای مختلــــــفی انجــــــام میپذیــــرد کـــه مهـــمترین آنها
QPCR-TAQ MAN ARRAY است [4].
ميكروRNAها بهعنوان بيوماركرهاي جديد بيماري دیابت
دیابت ملیتوس بیش از 350 میلیون نفر را در سرتاسر دنیا تحت تأثیر قرار داده است. ديابت نوع 1 (T1D) يك اختلال اتوايميون است كه در آن سلول بتاي پانكراس توسط سيستم ايمني مورد حمله قرار میگیرند، درحالیکه در دیابت نوع 2 (T2D) بافتهای کبد، اسکلتی و چربی حساسیت به انسولین را از دست میدهند. از سنجش اتوآنتیبادیهای موجود در سرم برای تشخیص T1D استفاده میشود. در T2D نیز نیاز به ترکیبی از بیومارکرهای کلاسیک و فاکتورهای خطر است تا بتوان احتمال بروز بیماری را در افراد پیشبینی کرد، در نتیجه برای ارتقای شناسایی افراد در معرض خطر ابتلا به دیابت و عوارض مرتبط با آن، غربالگري و ارزیابی کارایی روشهای درمانی نیاز به بیومارکرهای جدیدی است.
سلولهای بتای پانکراس و بافتهای هدف انسولین مجموعهای از ميكروRNAها را بیان میکنند. برای مثال mir-375 که بیان ژنهای درگیر در ترشح هورمون انسولين و توسعه توده سلولهای بتا در پاسخ به مقاومت به انسولین را تنظیم میکند، بهطور زیادی در جزایر لانگرهانس بیان میشود [3]. همچنین ثابت شده است که بیان miRNAهای سلولهای بتا و بافتهای هدف انسولین در بیماران مبتلا بهT1D و T2D دچار تغییر شده که احتمالاً به دلیل عملکرد ناقص این بافتها تحت شرایط بیماری است، برای مثال جزایر لانگرهانس موشهای دیابتیک غیرچاق (مدلی از (T1D حاوی سطح افزایشیافتهای از چندین miRNA شامل ,miR-21 miR-34a ,miR-29 و miR-146a بودند که اثرات زیانباری روی عملکرد سلولهای بتا دارند [5]، علاوه بر این، بیش از 60miRNA با بیان تغییریافته در نمونه بیوپسی عضله اسکلتی بیماران T2D شناسایی شده كه شامل mir-143 که بیان بالایی داشـــــته و mir-206 و mir-133a که بیان پایینی دارند، است [7]. سطح حدود 15% از این miRNAها پیش از این در افراد با اختلال تحمل گلوکز نیز تغییر کرده که این موضوع نشانه این است که miRNAها در فاز ابتدایی پروسه بیماری درگیر هستند [6]. miRNAها علاوه بر تنظیم بیان ژن درون سلولهایی که آنها را تولید میکنند، در خون و سایر مایعات بدن بهصورت متصل به پروتئینها، لیپوپروتئینها و یا درون اگزوزمها یافت میشوند. در این صورت این miRNAها در برابر ریبونوکلئازها، چرخه فریز و دفریز شدن و سایر شرایط آزمايشگاهي پایدار و مقاوم هستند. در نتیجه نمونه سرم یا پلاسما میتواند در منهای 20 درجه یا منهای 80 درجه برای بیش از چندین ماه بدون تجزیه miRNAها ذخیره شود، بعلاوه miRNAهای گردشی نهتنها در خون، بلکه در سایر مایعات بیولوژیکی مانند ادرار، بزاق و مایع آمنیوتیک نیز یافت میشوند. همچنین میتوان از این بیومارکر جدید برای پیشبینی عوارض ناشی از دیابت هم استفاده کرد. تحقیقات نشان داده که کاهش سطح سرمي mir-126 ارتباط قوی با بروز بیماریهای شریانی و عوارض میکروواسکولار دیابتی دارد، چراکه این miRNA در سلولهای اندوتلیال بيان قابل توجهي دارد.
بهطور نمونه در مطالعات انجامگرفته در ارتباط با میکرو RNA و سرطان معده، نتایج حاصل نشان از افزایش بیان میکرو RNA-25 و درگیر کردن چرخههای ترشح اسید معده دارد [6].
در مطالعه دیگری نشان داده شد که کاهش بیان میکرو RNA-101 در ارتباط نزدیکی با کارسینومای کبد است [4].
مطالعات دیگر ارتباط بین سطح miRNAهای گردشی معینی مانند ,miR-16 ,miR-21 ,miR-210 miR-638 و میزان فیلتراسیون گلومرولی، یک پارامتر شناختهشده برای پیشرفت بیماریهای کلیوي، مشاهده شده است و میتوان از این بیومارکر جدید در غربالگري پیشرفت نفروپاتی دیابتی استفاده کرد [7].
نقش میکروآر.ان.ایها در دیابت و اختلالات متابولیک
تعییــــــن نقش و ردیابی عملکرد miRs در برخی از بیماریها دستاورد بزرگی همانند ردیابی نقش میکروآر.ان.ایها در اختلالات متابولیسم، سرطان، بیماریهای قلبی، نقصهای نوزادی و … برای علم پزشکی درپی داشت. میکروآر.ان.ایهای مورد مطالعه و تأثیرگذار در دیابت در مقالات علمی بهطور خلاصه بدین شرح است:
miR-375 بیان ژنهای درگیر در ترشح هورمون انسولين و توسعه توده سلولهای بتا در پاسخ به مقاومت به انسولین را تنظیم میکند. این miR بهطور زیادی در جزایر لانگرهانس بیان میشود و احتمالاً از طریق مهار کردن مسیر سیگنالینگ میوتروپین انسولین در بیان ژن انسولین نقش دارد، همچنین موجب کاهش بیان PDK1 و فسفاتیدیل اینوزیتید وابسته به پروتئین کیناز 1، جزء اصلی مسیر سیگنالینگ PIP3 میگردد [5]، همچنین نقش miR-9 در ترشح انسولین و بیان فاکتور Onecut-2 که در تنظیم Granuphilin نقش دارد، مورد مطالعه قرار گرفته است [3]. میکرو RNA-96 موجب کاهش بیان پروتئین کمپلکس هستهای 2 شده (Noc2)، همچنین موجب افزایش بیان Granuphilin میگردد [8].
در گذشته تصور میشد miR-124a در بلوغ سلولهای بتا پانکراس نقش دارد، اما با مطالعات جدید نشان داده شد این میکروآر.ان.ای بر روی Box protein A2 که در ترشح انسولین نقش دارد، تأثیر میگذارد [9].
همچنین شواهد زیادی نشاندهنده نقش ماکروفاژها، منوسیتها و سلولهای مرتبط با آنها در بیماریزایی هنگام بروز اختلال متابولیک (MetS) و دیابت تیپ 2 است، بهطور مثال در بیماران دچار چاقی درجه 3 از نظر BMI، درصد ماکروفاژها را از 15-10 درصد به 60-50 درصد شاهد هستیم [2]. بدنبال افزایش درصد تراکم و پراکنش این سلولها در بافت، شاهد بروز واکنشهای التهابی و بدنبال آن بروز علائم بیماریهای اتوایمیون با شدت بیشتر هستیم، بهطور مثال سلولهای ماکروفاژ تیپ M1 با ترشح سایتوکاینهای مختلف نظیر (TNF-α ,IL-1β ,IL-6 ,CCL-4) و کموکاینهای اختصاصی نظیر (CCL2) در بروز واکنشهای التهابی منجر به اختلالات سیستماتیک اتوایمیون مانند مقاومت به انسولین نقش دارند. بدنبال افزایش مزمن کلسترول (dyslipidemia) و قند خون (hyperglycemia)، تعداد منوسیتهای در گردش و بدنبال آن واکنشهای التهابی در بیماران دچار سندرم اختلالات متابولیک و بیماران دیابت تیپ 2 افزایش مییابد [9].
مجموعاً در بیماریهای ذکرشده شاهد تغییر بیان الگوهای ژنی منوسیتها و پروفایلهای آنها در جایگاههای مرتبط با فعالیتهای التهابی بوده و بررسیها بیانگر افزایش بیان عوامل التهابی متعددی بوده که در دو گروه اصلی فاکتورهای التهابی مانند IL-1B ,IL-6 ,TNF ,TNFAIP3 ,PGS2 ,CCL20, PTX3 ,PDE4B ,DUSP2 ,ATF3 ,CXCL2,BCL2A1) و فاکتورهای کموتاکسی و تمایز سلولهای التهابی مانند,CCL2 ,CCL7 ,MAPK6 ,NAB2 ,CD9 ,STX1A ,EMP-1 CDC42 ,PTPN7 ,DHRS3 ,FABP5 ,HSPA1A قرار میگیرد. بیان هر دو خانواده (کلاستر ژنی) نقش اساسی در دیابتهای بزرگسالان و تیپ 1 دارند، اما نکته مهم تنظیم بیان و بروز این ژنها تحت کنترل miR-146a، miR-155 و miR-34c-5p است. بهعنوان مثال در بیماران دیابتی الگوها و مقدار این میکروآر.ان.ایها در سلولهای تکهستهای خون محیطی (PBMC) و منوسیتهای گردش خون کاهش مییابد [10].
نتیجهگیری:
عليرغم پیشرفتهای قابلتوجه در مورد نقش بيوماركري ميكروRNAها در بيماري ديابت، اين مبحث در مراحل ابتدايي بوده و نياز به اطلاعات بيشتر در اين خصوص است. هنوز چندين سؤال مهم وجود دارد كه بايستي در خصوص اهميت بيوماركري ميكروRNAها در بيماري ديابت پاسخ داده شود. بايستي كارايي اين بيوماركر جديد در پیشآگهی بيماري و همچنين عوارض بيماري در مقايسه با بيوماركرهاي موجود بررسي گردد. هنوز اجماع در مورد نقش بيوماركري ميكروRNAها وجود ندارد كه اين به دلیل نتايج متناقض بدستآمده از چند مطالعه مختصر در نژادهاي مختلف است.
منابع:
1– Parvini, N. and S. Ahmadi, Role of MicroRNAs in Development of Immune Cells and Nervous System and their Relation to Multiple Sclerosis. The Neuroscience Journal of Shefaye Khatam, 2015. 3(1): p. 131-144.
2- Fernandez-Valverde, S.L., R.J. Taft, and J.S. Mattick, MicroRNAs in β-cell biology, insulin resistance, diabetes and its complications. Diabetes, 2011. 60(7): p. 1825-1831.
3- Kantharidis, P., et al., Diabetes complications: the microRNA perspective. Diabetes, 2011. 60(7): p. 1832-1837.
4- Trajkovski, M., et al., MicroRNAs 103 and 107 regulate insulin sensitivity. Nature, 2011. 474(7353): p. 649-653.
5- Ryu, H.S., et al., The induction of microRNA targeting IRS-1 is involved in the development of insulin resistance under conditions of mitochondrial dysfunction in hepatocytes. PloS one, 2011. 6(3): p. e17343.
- Caporali, A., et al., Deregulation of microRNA-503 contributes to diabetes mellitus–induced impairment of endothelial function and reparative angiogenesis after limb ischemia. Circulation, 2011. 123(3): p. 282-291.
- Pullen, T.J., et al., miR-29a and miR-29b contribute to pancreatic β-cell-specific silencing of monocarboxylate transporter 1 (Mct1). Molecular and cellular biology, 2011. 31(15): p. 3182-3194.
- Greco, S., et al., MicroRNA dysregulation in diabetic ischemic heart failure patients. Diabetes, 2012. 61(6): p. 1633-1641.
- Bao, L., et al., MicroRNA-185 Targets SOCS3 to Inhibit Beta-Cell Dysfunction in Diabetes. PloS one, 2015. 10(2): p. e0116067.
- Nichols, G.A., et al., The incidence of congestive heart failure in type 2 diabetes an update. Diabetes care, 2004. 27(8): p. 1879-1884.
- He, A., et al., Overexpression of micro ribonucleic acid 29, highly up-regulated in diabetic rats, leads to insulin resistance in 3T3-L1 adipocytes. Molecular Endocrinology, 2007. 21(11): p. 2785-2794.
دیابت؛ گذشته، حال و چالشهای پیش رو
نکات مهم آزمایشگاهی در آزمایشهای تشخیص دیابت (2)
microRNAها در هموستاز و ترومبوز
Micro M.RNA، مارکری برای تشخیص سرطان
تشخیص مقاومت به انسولین با آزمایش HOMA-IR.index و یا TyG index
برای دانلود پی دی اف برروی لینک زیر کلیک کنید
ورود / ثبت نام