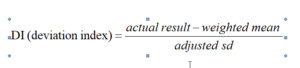اساس كار،کنترل کیفی و کالیبراسیون آنالیزورهای خون شناسی
دکتر حبیباله گلافشان، عضو هیئت علمی دانشگاه علوم پزشکی شیراز
قسمت دوم
کالیبراسیون آنالیزورها
راهاندازی اولیه آنالیزور خون شناسی ، تعویض قطعاتی که در اندازهگیری پارامترها نقش دارند، استفاده از معرفهای با سری ساخت متفاوت، رخداد الگوهای خطای سیستمیک مانند شیفت یا گرایش در نمودار کنترل کیفی و سفارش شرکت سازنده همه از مواردی است که نیاز به کالیبراسیون دستگاه دارد.
یک آنالیزور خوب نه تنها بایستی تکرار پذیر باشد بلکه باید جوابهای صحیح را ارائه دهد و از این رو قبل از کالیبراسیون بایستی از تکرار پذیری و شمارش زمینهای آنالیزور آگاهی داشت.
آنالیزور را میتوان با استفاده از نمونه کالیبراتور تجارتی با دامنه کوتاه SDیا با استفاده از خون تازه بیماران کالیبره کرد. کالیبراتورها بایستی بدون لخته باشند و قبل از مصرف به دمای اتاق رسیده باشند. و بمدت 20-15 دقیقه روی روتاتور مخلوط شوند. برای ارزیابی تکرار پذیری میتوان یک یا دو نمونه خون تازه EDTAدار را حداقل 11 بار به دستگاه داد و برای هر پارامتر مقدار CV (ضریب تغییرات) را محاسبه کرد. ضریب تغییرات قابل قبول برای شمارش RBC و MCV و Hb کمتر از 2 درصد برای شمارش گلبول سفید و هماتوکریت کمتر از 3 درصد و برای شمارش پلاکت کمتر از 5 درصد است. چنانچه کالیبراتور تجارتی در دسترس ندارید بایستی 10 تا 20 نمونه خون تازه ترجیحاً در ضد انعقاد K2EDTA را تهیه کرده و هر نمونه را برای هر پارامتر سه بار با روش دستی مرجع تعیین مقدار کرد.
روش مرجع اندازهگیری هموگلوبین روش سیانمت هموگلوبین است. هماتوکریت در لولههای کاپیلاری اندازه گرفته شده و برای 3% پلاسمای بدام افتاده تصحیح میگردد، برای مثال چنانچه هماتوکریت 44 درصد باشـــــــد مقدار تصحیح شده آن 0/42= 0/013 – 0/44 خواهد بود. گلبولهای قرمز و سفید با استفاده از آنالیزورهای تک کاناله (مانند کولتر مدل Z) شمرده شده و اندکسهای خون با فرمول محاسبه میگردند. گفتنی است که آنالیزورها از نظر پارامترهای قابل کالیبراسیون با هم متفاوتند به طوری که در برخی از مدلها تنها هموگلوبین و هماتوکریت توسط کاربر میتوانند کالیبره شوند. بهرحال تعداد 10 تا 20 نمونه خون تازه را انتخاب کرده و هر کدام را سه بار به آنالیزور غیر کالیبره داده و سه بار با روش مرجع تعیین مقدار میکنیم.
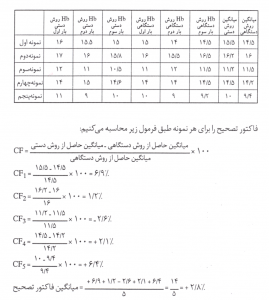
نکته مهم اینکه اگر روشهای مرجع در اختیار نیست نمونههای انتخابی را هر کدام سه بار با سلکانتر مرجع که در آزمایشگاه رفرانس مرکز استان یا بیمارستانی که تحت نظارت آزمایشگاه رفرانس است تعیین مقدار کنید و دادهها معادل روش دستی مرجع گرفته شود، برای مثال به محاسبه فاکتور تصحیح (CF) برای پارامتر هموگلوبین بر اساس 5 نمونه خون تازه توجه کنید.
مثال: برای کالیبراسیون پارامتر هموگلوبین، 5 نمونه خون تازه را هر کدام سه بار با روش دستی مرجع و روش دستگاهی به شرح زیر تعیین مقدار کردهایم:
میانگین فاکتور تصحیح برای هموگلوبین در مثال فوق 2/8 درصد است و چون علامت آن مثبت است به مفهوم آن است که دستگاه 2/8درصد کمتر از روش مرجع دستی هموگلوبین را گزارش میکند، بنابراین باید 2/8 درصد مقدار Hb آنالیزور را افزایش داد. برای مثال اگر Hb یک نمونه خون توسط دستگاه 16 گرم درصد گزارش شود، آن را به 16/4 تغییر داده و دستگاه را روی این مقدار تنظیم میکنیم یا فاکتور کالیبره هموگلوبین دستگاه را 2/8 درصد بالا میبریم.
اگر میانگین فاکتور تصحیح 2/8- درصد بود میزان هموگلوبین دستگاه را 2/8 درصد کاهش داده و آن را روی 15/6 گرم درصد تنظیم میکنیم و یا اینکه فاکتور کالیبره هموگلوبین آنالیزور را 2/8% کاهش میدهیم.
از 10 تا 20 نمونه خون 10 تا 20 فاکتور کالیبره (CF) برای هر پارامتر بدست میآید. میانگین فاکتور تصحیح برای هر پارامتر محاسبه میشود، برای مثال اگر میانگین فاکتور تصحیح برای هماتوکریت 5/5+ درصد باشد به آن مفهوم است که آنالیزور هماتوکریت نمونهها را 5 درصد کمتر از روش مرجع (روش دستی یا آنالیزور کالیبره مرجع) گزارش میکند و بایستی فاکتور کالیبره دستگاه را 5/5 درصد بالا برد، برای مثال اگر فاکتور کالیبره 93 درصد باشد بایستی آنرا در سطح 98/5 درصد تنظیم کرد و یا اگر برای MCV میانگین فاکتور تصحیح 3- درصد باشد و هم اکنون فاکتور کالیبراسیون دستگاه برای MCV عدد 110 است بایستی این فاکتور را 3 درصد کاهش داد چون 3 درصد بیشتر از روش مرجع گزارش میکند.
در این حالت عدد کالیبره MCV آنالیزور روی عدد 106/7= 3/3- 110 تنظیم میشود. فاکتور کالیبره برای غالب آنالیزورهای نو عدد 100% است که این عدد میتواند در محدوه 125% – 75% توسط کاربر تغییر پیدا کند. گاهی که نیاز به تغییرات زیاد فاکتور کالیبره است بایستی فاکتور کالیبره را طی چند مرحله تغییر داد.
تهیه رتیکولوسیت مصنوعی جهت کنترل
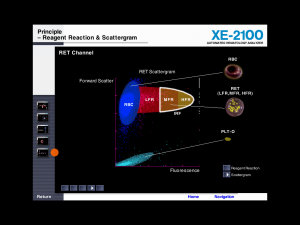
با قرار دادن گلبولهای قرمز تازه در محیط هایپوتونیک با فشار اسمزی پایین و اضافه کردن RNA (مثلاً از منبع مخمر) میتوان رتیکولوسیت تهیه کرد. در این حالت منافذی در غشای گلبول بوجود میآید که موجب ورود آب و رشتهای RNA بداخل گلبول میگردد.
روزنههای غشاء با طبیعی کردن فشار اسمزی محیط بسته شده و RNA در داخل گلبول محبوس میگردد و از این رو میتوان رتیکولوسیت مصنوعی تهیه کرد.
با بکارگیری رنگ فلورسانس تیازول نارنجی میتوان رتیکولوسیتها را بر مبنای شدت فلورسانس در سه دسته جای داد. رتیکولوسیت با فلورسانس بالا (HFR) بیانگر رتیکولوسیتهای نارس و یا رتیکولوسیتهای تحت استرس میباشد. با شمارش پلاکتها به روش اپتیک (PLT-O) میتوان پلاکتها را از گلبولهای قرمز شکسته جدا کرد.
شمارش زمینه
قبل از آنالیز خون بیماران بایستی شمارش زمینهای (back ground) محلولهای رقیق کننده را کنترل کرد. شمارش زمینه قابل قبول برای برخی از پارامترهای هماتولوژی عبارتند از :
| شمارش گلبول قرمز کمتر از | 20000 در میلیمتر مکعب |
| شمارش گلبول سفید کمتر از | 200 در میلیمتر مکعب |
| مقدار هموگلوبین کمتر از | 0/1گرم در دسیلیتر |
| شمارش پلاکت کمتر از | 5000 در میلیمتر مکعب |
کنترل کیفی(Quality control) روشی برای حصول اطمینان از کیفیت کالا یا خدمت ارائه شده میباشد و جواب آزمایش یک نوع خدمت محسوب میشود و از این رو تضمین کیفیت در تمامی مراحل فرایند تولید جواب از قبیل قبل از آنالیز، هنگام آنالیز و بعد از آنالیز بایستی صورت گرفته و سعی در رفع خطا به منظور بهبود جواب آزمایش (بهبود کیفیت) نمود.
روشهای کنترل کیفی
روشهای کنترل کیفی به دو دسته کنترل کیفی داخلی (IQC) و کنترل کیفی خارجی (EQC) طبقه بندی میشود. کنترل کیفی داخلی به طور اولیه دقت و تکرار پذیری آزمایشهای روزانه را کنترل میکند و دارای روشهای گوناگونی میباشد.
کنترل کیفی خارجی از طریق سازمانهای منطقهای مانند آزمایشگاه مرجع کشوری و یا آزمایشگاه رفرانس استان انجام گرفته و هدف آن نظارت بر کنترل کیفی داخلی آزمایشگاه است. در این روش نمونههای مشخص به تمامی آزمایشگاهها ارسال شده و از آزمایشگاه درخواست میگردد که نمونه را همراه با نمونههای بیماران مورد آزمایش قرار داده و جوابها را به آن سازمان عودت دهد.
کنترل کیفی قبل از آنالیز مربوط به نمونهگیری میشود، گرچه مسئول فنی آزمایشگاه بایستی آموزشهای لازم را به کادر پرستاری یا نمونهگیر بدهد ولی مسئولیت شرایط اولیه از قبیل مصرف دارو، ناشتا بودن و … به عهده پرستار یا خونگیر است.
هنگامی که با یک نتیجه آزمایش بسیار بالا روبرو میشوید برای رفع خطای خطی (Linearity) بایستی آزمایش را روی رقت یک به دو یا یک به سه انجام داده و یا جواب آزمایش را با جواب قبلی بیمار مقایسه کنید. با بازرسی داخلی میتوان از خطاهای فاحش جلوگیری کرد. برگههای لیست کاری (work list) و برگههای چاپ نتایج دستگاه میبایست تا یک سال در بایگانی آزمایشگاه ذخیره شوند ولی سوابق بانک خون تا 5 سال و ذخیرههای کامپیوتری با تهیه لوح فشرده (CD) بک آپ تا 10 سال بایگانی شوند.
خطاهای سیستمیک و اتفاقی
خطای سیستمیک قاعدهمند است و تا زمانی که علتیابی نشود نتایج تمام آزمایشها را با الگوی یکسان تحت تأثیر قرار میدهد و از این رو در چارت کنترل کیفی از نظم برخوردار است و معمولاً به صورت شیب کاهنده یا افزاینده (Trend) و یا الگوی جابجایی (Shift) نمایان میشود و برخلاف خطای راندوم با تکرار آزمایش برطرف نمیشود. ضعیف شدن منبع نوری آنالیزور، خرابی پمپها، گرد و غبار روی منبع نوری، خطای درجه حرارت، خرابی آشکارساز(detector)، فساد تدریجی معرفها، معرفهای تاریخ گذشته، مشکلات در سیستمهای نوری (optic) همه موجب بروز خطای سیستمیک میگردند. برای مثال انسداد تدریجی روزنه دستگاه (aperture) با لاشههای سلولی و پروتئین موجب خطای افزایش حجم سلولی و کاهش شمارش سلولی میگردد که با الگوی گرایش (ترند) منفی در شمارش و ترند مثبت در افزایش حجم سلولی نمایان میگردد.
برای کشف خطای سیستمیک نیاز به دادههای خون کنترل در چندین روز است. خطاهای راندوم یا تصادفی یک سری از نتایج را تحت تأثیر قرار میدهند و اثرات قابل توجهی روی میزان انحراف معیار دارند. تکرار آزمایش غالباً پاسخ درست میدهد. نوسان درجه حرارت، تغییرات ناگهانی ولتاژ ، تشکیل حباب هوا در حین آنالیز و خطای انتقال از موارد خطای راندوم است که به صورت نقاط بسیار پراکنده در چارت کنترل کیفی بروز میکند.
کنترل کیفی داخلی دارای روشهای گوناگون است که برخی از آنها عبارتند از:
- تست دوبل (duplicate)
برای انجام این روش نمونههای 10 یا 20 نفر از بیماران را در یک نوبت کاری انتخاب کرده و هر کدام به صورت پشت سر هم دوبار به آنالیزور داده میشود. با محاسبه اختلاف جوابهای دوتایی (d) مقدار انحراف معیار از روی معادله مربوطه محاسبه میشود. بعد از محاسبه انحراف معیار (SD) عدد d یا اختلاف آزمایشهای مضاعف نبایستی خارج از محدوده ±2SD باشد. این روش تکرار پذیری آزمایشها را کنترل کرده و استفاده از آن مشروط به کالیبراسیون دستگاه است.
برای رسم چارت کنترل دوبل از قدر مطلق اختلاف جوابهای دوبل(dها) میانگین گرفته و عدد حاصل را در 2/45 ضرب کرده و بدین ترتیب محدوده 95% اطمینان بدست آورده میشود. عدد حاصل را بر روی محور y منتقل کرده و از آن نقطه خطی موازی محور X رسم میشود. سطح زیرین این مرز محدوده 95% اطمینان است.
محور X بیانگر دفعاتی است که اختلاف جوابهای دوبل محاسبه میشود. روزانه از هر 20 تست انجام شده یکی را به طور شانسی انتخاب کرده و دوبار به دستگاه داده و سپس قدر مطلق d برروی نمودار برده میشود که نبایستی از خط 95% اطمینان تجاوز کند.
آزمایش چک تست یا آزمایش بازبینی شبیه آزمایش دوبل است با این تفاوت که بجای نمونههای همان دوره کاری (Run) جوابهای آزمایش نمونه بیماران انتخابی در دو سری کاری مورد مقایسه قرار میگیرند. برای مثال مقایسه جوابها در ساعت 8 صبح و 12 ظهر (سری اول و دوم) مورد آنالیز قرار میگیرد. نمونهها را بایستی در شرایط مناسب نگهداری کرد و تا 6 ساعت از بین دو سری کار (Run) مورد آنالیز قرار داد.
تست دوبل (duplicate)
- دلتا تست یا دلتا چک
در این روش نتایج کنونی آزمایشات یک بیمار با نتایج قبلی وی (یک تا دو هفته قبل) مقایسه میشود و یا در بیمارستان میتوان نتایج روزانه بیمار را با هم مقایسه کرد.
با دلتا چک برخلاف چک تست نتایج آزمایش بیمار در روزهای مختلف مقایسه میشود. در این روش فاصله زمانی بین دو آزمایش نبایستی بیش از دو تا سه هفته باشد و از اینرو ثبت کامپیوتری نتایج قبلی الزامی است. چنانچه بیمار در شرایط خاص بالینی نباشد و یا داروهای خاصی مانند شیمی درمانی، تزریق G- CSF و خونریزی و … نداشته باشد. تنها تغییرات فیزیولوژیک میتواند موجب اندکی اختلاف در نتیجه آزمایشها باشد. دلتا چک به خطاهای نمونهگیری از قبیل نمونه جابجا شده، برچسب اشتباه، نمونه همولیز شده، ذرات لخته در نمونه و … بسیار حساس است.
از دلتا چک نمیتوان در بیمارانی که تحت درمان فعال بوده و یا سیر بیماری در آنها ایجاد تغییرات فاحش در نتایج آزمایشها … میکند استفاده کرد.
نتیجه دوم / 100 × ( نتیجه دوم – نتیجه اول) = درصد دلتا
اختلاف دو نتیجه = مقدار دلتا
مقادیر دلتا برای پارامترهای CBC
| پارامتر | مقدار دلتا |
| Hb | کمتر از 10 درصد |
| HCT | کمتر از 5 درصد |
| MCV | کمتر از 6 فمتولیتر |
| MCH | کمتر از 5 پیکوگرم |
| PIT | تغییرات بیش از 50% خارج از محدوده دلتاست |
| RBC | کمتر از 10 درصد |
| WBC | طبیعی به غیر طبیعی و یا غیر طبیعی به غیر طبیعی فاحش خارج از محدوده دلتاست (تغییرات بیش از 20 تا 25%) |
همبستگی و همخوانی نتایج آزمایش با وضعیت بالینی و همچنین ارتباط آنها با سایر یافتههای آزمایشگاهی نیز نقش مهم در کنترل نمونه بیمار دارد، برای مثال انتظار زمان سیلان طولانی در بیماری که آسپرین مصرف میکند وجود دارد و یا مشاهده رولکس در گستره محیطی با افزایش ESR همراه است و یا طولانی شدن آزمایش PT با مصرف وارفارین و یا کاهش شکاف آنیون در بیمار مبتلا به مالتیپل میلوما مورد انتظار است. نتایج آزمایشگاه بایستی به پزشک در تشخیص بیماری کمک کند و به طور کلی مقدار CV آزمایشگاه نبایستی از CV معاینات بالینی بیشتر باشد، بدین مفهوم که اگر پزشکی با ضریب خطای 10% امکان مننژیت را مطرح کند نتایج آزمایشگاه نبایستی با ضریب خطای 20% احتمال مننژیت را مطرح کند.
آزمایش تکرار تست (Replicate test)
با این روش تکرار پذیری و دقت دستگاه یا روش کار مورد بررسی قرار میگیرد و نتیجه مطلوب بیانگر پایداری و عدم نوسان است. برای انجام تست یک نمونه خون را 11 بار به دستگاه داده و میانگین و انحراف معیار (SD) و ضریب تغییرات برای هر پارامتر محاسبه میشود. برای مثال مقدار CV قابل قبول برای آزمایش هموگلوبین در یک آزمایشگاه روتین بین 2 تا 3 درصد و برای آزمایشگاه تخصصی حدود 1/5 درصد و برای یک مرکز تحقیقاتی و استاندارد بایستی کمتر از یک درصد باشد. با آزمایش تکرار تست علاوه بر پایداری نتایج میتوان دقت عملکرد آنالیزور را مورد بررسی قرار داد.
برای این کار میتوان از دو یا سه خون تازه EDTAدار استفاده کرد و هر کدام را چندین بار به آنالیزور داد و از نتایج هر نمونه میانگین، مقدار انحراف معیار و ضریب تغییرات را محاسبه کرد.
CV = ×100 و SD=
SD انحراف معیار و X نتیجه یک آزمايش و X میانگین نتیجه آزمایش و N دفعاتی است که نمونه خون به آنالیزور داده شده است. حروف CV به مفهوم ضریب تغییرات (coefficient of variation) است که حاصل تقسیم انحراف معیار بر میانگین در عدد 100 ضرب میشود.
چنانچه مقدار CV پارامترها در محدوده جدول باشد آنالیزور از تکرار پذیری خوب برخوردار است و در غیر این صورت بایستی قبل از کالیبره کردن بررسی فنی دستگاه انجام شود.
| مقادیر قابل قبول ضریب تغییرات برای پارامترها | |
| پارامتر | دامنه CV |
| RBC | 2% > |
| MCV | 2% > |
| HCT | 3% > |
| Hb | 2% > |
| WBC | 3% > |
| P Lat | 5% > |
روش کنترلی بریتین
مشاهدات بریتین نشان داده است که پارامترهای مهم آزمایش CBC از قبیل شمارش سلولی و اندکسها (MCV و MCH و MCHC) تا 24 ساعت در خون EDTAدار در حرارت 4 درجه پایدارند.
در روش کنترلی بریتین یا پایداری کالیبراسیون از فرمول آماری t (آزمون گوست) استفاده میشود. تعداد 5 تا 10 از نمونههای خون بیماران که امروز توسط آنالیزور آزمایش شده و مقادیر پارامترها در محدوده طبیعی است را انتخاب کرده و در یخچال برای کنترل فردا گذاشته میشود.
به عبارت دیگر از نمونههای خون امروز جهت کنترل تکرار پذیری آنالیزور براي فردا استفاده میشود.
انحراف معیار و مقدار tn برای هر پارامتر CBC بر اساس فرمول مخصوص محاسبه میشود، برای مثال مقدار tn برای 5 نمونه عدد 2/7 با توجه به جدول آماری t است. چنانچه برای مثال مقدار tn برای پارامتر هموگلوبین بیشتر از 2/7 باشد با 95% اطمینان میتوان گفت اختلاف معنیداری بین دو روز متوالی در پارامتر مورد سنجش وجود دارد و ممکن است نیاز به کالیبراسیون مجدد آنالیزور باشد.
آزمون آماری میانگین متحرک بول (Bull Moving Average)
آزمون میانگین متحرک بول (Bull) برای کنترل کیفی داخلی اندکسهای خونی ارائه گردیده است. طرح آزمون آماری فوق بر این اساس است که مقادیر اندکسهای خون برای هر آزمایشگاه که بیماران مناطق مخصوص را میپذیرد تقریباً ثابت است، بنابراین اگر میانگین اندکسهای خون در جمعیت آن ناحیه مشخص شده باشد میتوان از نمونههای خون بیماران که روزانه به دستگاه داده میشود برای کنترل کردن کالیبراسیون استفاده کرد.
برای شروع چنین برنامهای دستگاه شمارشگر را طبق روش معمول کالیبره کرده و بعد از آنالیز حداقل 500 نمونه بیمار، میانگین پارامترها حساب میشود.
میانگین بدست آمده برای هر پارامتر به روش فوق به عنوان پایه برای چک کردن کالیبراسیون و انحراف دستگاه به کار میرود. بول (Bull) نشان داد که با محاسبه میانگینهای متحرک MCV، MCHو MCHC هر 20 نمونه متوالی که به طور راندوم پشت سرهم به دستگاه داده میشود، میتوان وضعیت کالیبراسیون را بررسی کرد. البته نباید نمونه 20 بیمار که به عنوان مثال مبتلا به کمخونی یا لوسمی هستند را پشت سر هم به دستگاه داد. اگر مقادیر میانگین اندکسها که برای هر 20 نمونه به دست میآید 3% از میزان پایه تغییر کند کالیبراسیون دستگاه باید بررسی شود. قبل از اقدام به کالیبراسیون مجدد باید حداقل میانگین اندکسهای سه دسته 20 تایی از نمونهها بیشتر از 3% ±از میانگین پایه اختلاف داشته باشد. مزایای آزمون میانگین متحرک این است که از خون تازه جهت کالیبراسیون دستگاه استفاده میشود.
در آزمایشگاهی که روزانه حداقل 100 نمونه دارد نبایستی اختلاف چشمگیری در میانگین روزانه اندکسهای گلبول قرمز دیده شود. البته بایستی از یک جمعیت پایدار استفاده کرد و برای مثال نباید از نمونههای مربوط به بیماران خاص که موجب تغییر ناگهانی در میانگین میشوند استفاده کرد. با این پیش فرض که نمونههای با وضعیت پایدار به دستگاه داده شده است، هر تغییر چشمگیری بیانگر تغییر در کالیبراسیون یا اختلال درعملکرد دستگاه است. بنظر میرسد که این روش کنترل کیفی حساسیت ویژهای نیز برای به کنترل در آوردن شمارش گلبولهای قرمز داشته باشد.
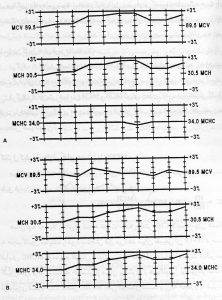
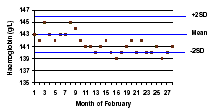
میانگین متحرک بول به شمارش گلبولها و اندکسهای خونی حساس بوده و انسداد تدریجی روزنه موجب میشود که گراف از محدوده کنترل خارج شود.
در گراف A افزایش همزمان در میزان MCV و MCH مشاهده میشود که احتمالاً به علت گرفتگی روزنه دستگاه با مواد پروتئینی و کاهش شمارش گلبولهای قرمز است.
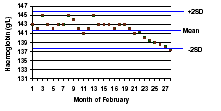
در گراف B افزایش همزمان MCH و MCHC گویای خطای کاذب در شمارش گلبولهای قرمز یا خطای اندازهگیری در هموگلوبین و افزایش کاذب آن مثلاً به علت کدر شدن محلول سنجش هموگلوبین است.
پایش عملکرد آنالیزورها با استفاده از خون کنترل
استفاده از خون تازه بیماران جهت کنترل روزانه گرچه هزینهبر نیست ولی توانایی تشخیص همزمان خطاهای سیستمیک و راندوم را ندارد و نمیتوان با تحلیل جوابها احتمال فساد تدريجي معرفها و يا نقص فنی آناليزور را پيشبيني كرد.
امكان قضاوت و مقايسه ماهانه جوابها وجود ندارد ولي با خون كنترل كه پارامترهاي هماتولوژي آن ثابت باشد ميتوان با انتقال دادههاي خون كنترل به طور روزانه یا هر نوبت کاری روي نمودار لوي– جنينگ الگوهاي پراكندگي از نظر خطاهاي راندوم و الگوهاي جابجايي و گرايش براي شناخت خطاهاي سيستميك را مورد مطالعه قرار داد.
نمودار كيو سام با استفاده از خون كنترل امكان شناخت بهتر خطاهاي سيستميك را فراهم ميآورد. خون كنترل پايدار را ميتوان به صورت تجاري و يا در آزمايشگاه تهيه كرد. چنانچه خون كنترل براي سه سطح كنترلي پايين، نرمال و بالا در دسترس باشد در مدت كوتاهتري ميتوان خطاهاي راندوم و سيستميك را كشف كرد.
چگونه میتوان خون کنترل تهیه کرد؟
برای تهیه خون کامل فیکس شده و پایدار که برای چندین ماه دارای پارامترهای ثابت بوده تا با آن بتوان چارت کنترل کیفی را ترسیم کرد، بایستی نخست محلول فیکساتیو را به شرح زیر تهیه کرد:
تهیه محلول فیکساتیو
| فرمالدئید 37 تا 40 درصد | 6/75 سیسی |
| گلوتارالدئید 50 درصد | 0/75 سیسی |
| تری سدیم سیترات | 26 گرم |
| آب مقطر | 100 سیسی |
محلول فیکساتیو را در یخچال نگه دارید. چنانچه گلوتارالدئید 25 درصد در اختیار دارید 1/5 سیسی از آنرا بکار ببرید.
تهیه خون کنترل
- از خون کامل در نگهدارنده CPD یا ACD استفاده میشود، میتوان خون کامل را از کیسههای تازه اهدا شده از سازمان انتقال خون تهیه کرد. خون بایستی تازه بوده و هرگز بیش از 3 روز از نگهداری آن نگذشته باشد.
- آنتیبیوتیکهای گسترده طیف یا مخلوط آنتیبیوتیک و ضد قارچ به نمونه خون اضافه و مخلوط کنید.
برای مثال میتوان از یک ویال 800000 واحد پنيسیلین و یک گرم استرپتومایسین به ازای تهیه هر 500 سیسی خون کنترل استفاده کرد، یا میتوان از ترکیب پنيسیلین و جنتامایسین استفاده کرد. مقادیر آنتیبیوتیک را با توجه به حجم خون کنترل تنظیم کنید.
- برای تهیه هر 50 سیسی از حجم خون کنترل یک سیسی محلول فیکساتیو اضافه کرده و بمدت یک ساعت در حرارت اتاق مخلوط کرده و سپس در یخچال 4 درجه نگه دارید.
- خون کنترل را بمدت 10-7 روز در یخچال قرار داده و هر روز بمدت یک ساعت آن را بیرون آورده و روی روتاتور قرار دهید. پس از آن خون کنترل فیکس شده را در ویالهای 2 تا 3 سیسی ریخته و در 4 درجه نگهداری کنید.
- تعداد 5 نمونه (ویال) از خون کنترل را به طور راندوم انتخاب کرده و دادههای هماتولوژی آن را مانند شمارش سلولی و پارامترها با یک دستگاه کالیبره بدست آورید. میزان CV پارامترهای خونی در ویالهای راندوم انتخابی نبایستی بیشتر از 2 درصد باشد.
- میانگین و انحراف معیار پارامترهای هماتولوژی را بدست آورده و از این خون کنترل برای رسم چارت روزانه کنترل کیفی استفاده کنید.
چنانچه آناليزور كاليبره باشد ميتوان خون كنترل را چندين بار به آناليزور داد و ميانگين جواب هر پارامتر و دامنه مورد انتظار را با محاسبه انحراف معيار تعيين كرد و يا ممكن است از ميانگين و دامنه مندرج در بروشور استفاده كرد. ولي توجه داشته باشيد كه همه آناليزورها ممكن است پاسخ قابل انتظار با توجه به دادههاي بروشور نداشته باشند.
در نمودار لوي جنينگ مقادير ميانگين و محدودههاي كنترلي X ±2SD و X ±3SD روي محور Y و تعداد دفعاتي كه خون كنترل به آناليزور داده ميشود- براي مثال برحسب روز يا در هر سري (Run)- بر روي محور x مشخص ميگردد.
خط ميانگين به صورت خط پررنگ در مركز و محدودهها با خطوط كمرنگ و يا نقطه چين در دو طرف رسم ميشود. براي هر سطح كنترلي بايستي نمودار جداگانه ترسيم شود. چنانچه جواب خون كنترل در محدوده مورد انتظار باشد آناليزور تحت كنترل بوده و پاسخ خارج از كنترل نياز به بررسي دارد و تا رفع اشكال نبايستي جواب بيمار را گزارش كرد.
تحليل نمودار لوي جنينگ (L- J)
با انتقال دادههاي خون كنترل برروي نمودار L-j ميتوان الگوهاي پراكندگي (dispersion)، جابجايي (shift) و گرايش (Trend) را مشخص كرد. الگوي پراكندگي با قرار گرفتن نتايج خون كنترل خارج از محدوده ±2SD غالباً بيانگر خطاهاي راندوم است. در الگوي گرایش يا شيفت هر چند جوابها ممکن است در محدوده كنترلي باشند ولي داراي شیب نزولي يا صعودي هستند. در الگوي جابجايي بدنبال يك تغيير ناگهاني جوابها در یک طرف خط ميانگين منتقل شده و مثل اين است كه جوابها اطراف يك خط ميانگين فرضي دیگر قرار دارند.
الگوهای جابجایی و گرایش بیانگر خطای سیستمیک میباشد.
نمودار كيوسام
نمودار كيوسام به كشف خطاي سيستميك بسيار حساس است زيرا در اين نمودار خطاهاي راندوم يكديگر را حذف ميكنند، از اين رو اين نمودار جهت تشخيص خطاهايي است كه به تدريج موجب افزايش يا كاهش پاسخها ميشوند و نشانه خرابي معرفها و يا دستگاه ميباشد. در نمودار كيوسام جمع جبري (تجمعي) تفاوت بين نتايج بدست آمده از ميانگين هدف در هر سري كاري (RUN) محاسبه ميشود، براي مثال اگر هموگلوبين يك نمونه كنترل 15 و دستگاه امروز 16 قرائت كند تفاوت X-X برابر 1+ است و چنانچه فردا (سري دوم كاري ) 14 قرائت كند تفاوت X-X برابر 1- است و جمع نتایج اين دو روز كاري يا دو سري كار صفر (1+ 1-) است. اگر كنترل در سري سوم كاري يا روز سوم براي مثال 15/8 خوانده شود تفاوتهاي اين سه روز 8/0 +0 ميباشد.
در گراف كيوسام محور Y از -10 SD تا +10SD با فاصله 1SD تقسيم بندي ميشود و يك خط افقي از نقطه صفر محور Y به سمت راست رسم ميشود كه در بالا و پايين داراي محدودههاي ±10SD است. محور X بر حسب دفعاتی که مجموع تفاوتهاي دوره كاري نتایج كنترل از ميانگين بر روی چارت برده میشود تقسیم بندی شده است. چنانچه نتايج در محدوده كنترل باشد نقاط نمودار اطراف خط صفر قرار ميگيرند و شيب نقطهها به طرف بالا و پايين بيانگر خطاي سيستميك است. در روش غير كامپيوتري حد آستانه يعني ±1SD و محدوده يعني SD2/7 ± محاسبه ميشود. هنگامي كه پاسخ خون كنترل به حد آستانه كيوسام برسد پيگيري آغاز و با بازگشت آن به پايين حد آستانه پيگيري خاتمه مييابد و چنانچه پاسخهاي كنترل از محدوده كنترل فراتر رود نتايج خارج از كنترل ميباشد.
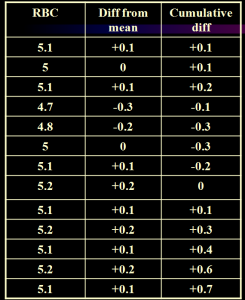
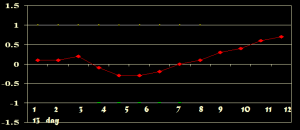
رسم نمودار کیوسام برای شمارش گلبولهای قرمز. میانگین شمارش گلبولهای قرمز 5 میلیون در میلیمتر مکعب است. این نمودار با الگوی گرایش(ترند) مثبت بیانگر خطای سیستمیک در شمارش گلبولهای قرمز است.
کنترل کیفی خارجی (External Quality Control)
عبارت است از ارزیابی نتایج روی یک نمونه خاص که توسط آزمایشگاههای مختلف آزمایش میشود. ارزیابی کنترل کیفی خارجی توسط یک مرکز صورت گرفته و منظور آن مقایسه نتایج پارامترهای یک نمونه مانند Hb در سطح آزمایشگاههای استان یا کشور و حتی بین کشورهاست. اگر چنین نمونهای در آزمایشگاه رفرانس تعیین مقدار شده باشد امکان بررسی صحت آزمایشهای انجام شده توسط آزمایشگاههای مختلف را نیز فراهم میسازد.
اصول کار کنترل کیفی خارجی برای یک پارامتر مخصوص مثلاً بررسی نتایج مقدار هموگلوبین در استان به شرح زیر است:
- نمونههای یکسان خون کنترل برای اندازهگیری Hb، به تعداد زیادی از آزمایشگاهها در سطح استان از طرف آزمایشگاه مرکز رفرانس ارسال میشود.
- مقادیر اندازه هموگلوبین از طرف آزمایشگاهها به مرکز عودت داده میشود.
- میانگین و انحراف معیار اندازهگیری هموگلوبین با استفاده از جوابهای ارسالی محاسبه میشود.
- آن دسته از نتایج اندازهگیری هموگلوبین که خارج از محدوده SD2 ± باشد حذف شده و از مابقی نتایج، برای بار دوم میانگین و انحراف معیار گرفته میشود که در این حالت به ترتیب میانگین سنجیده (وزین) (Weighted mean) و انحراف معیار سنجیده (Weighted SD) نامیده میشود.
- با استفاده از رابطه زیر ایندکس انحراف برای هر نتیجه ارسالی محاسبه میشود
چنانچه میزان شاخص انحراف (Deviation Index) کمتر از 0/5 باشد نمره آزمایشگاه عالی (excellent) و بین 1-0/5 باشد، رضایتبخش، و اگر 2-1 باشد هنوز قابل قبول و چنانچه بیش از 2 باشد بیانگر وجود اشکال در کار آزمایشگاه است که به توجه و پیگیری نیاز دارد.
چنانچه انحراف معیار نتایج ارسالی از آزمایشگاههای با دقت بالا محاسبه گردد، معمولاً کمتر از انحراف معیار نتایج شرکت کنندگان در برنامه کنترل کیفی خواهد بود.
داوری در مورد نتایج به دست آمده از آزمایشگاههای مختلف از طریق محاسبه میزان انحراف معیار از نتایج به دست آمده توسط آزمایشگاه مرجع انجام میگیرد.
انحراف با یک SD دارای درجه عالی، بین SD1-2 درجه رضایتبخش و بین SD2-3 به عنوان اخطار و بیشتر از SD3 بیانگر نقص کار و توجه فوری است.
https://pubmed.ncbi.nlm.nih.gov/3827540/
https://www.elitecme.com/resource-center/laboratory/calibration-control-of-hematology-analyzers
کنترل کیفی در آزمایشگاه خونشناسی(در تب جدید مرورگر باز می شود )
برای دانلود فایل pdf بر روی لینک زیر کلیک کنید
ورود / ثبت نام