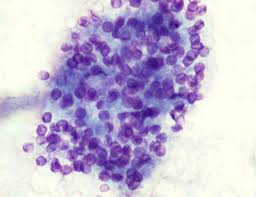
پنومونی پنوموسیستیس
دکتر سهیلا محمود پور1، فرزانه ناطقی2، روژین جمشیدی1، صادق خداویسی3
1 آزمایشگاه تشخیص طبی پاستور، سنندج
2 کارشناسی ارشد میکروبیولوژی، دانشگاه آزاد اسلامی ورامین
3 دانشجو دکتری تخصصی قارچ شناسی پزشکی، دانشگاه علوم پزشکی تهران
پنومونی پنوموسیستیس[1](PCP) یک بیماری خطرناک در اکثر بیماران با نقص سیستم ایمنی نظیر افراد مبتلا به HIV میباشد. عامل این بیماری Pneumocystis jirovecii است که تنها قارچی است که به طور مستقیم از انسان به انسان منتقل میشود و سایر پستانداران توسط گونههای مخصوص به خود مبتلا میشوند. انتقال انسان به انسان بیشتر در اوایل زندگی اتفاق میافتد. برخی افراد احتمالاً بطور کامل عاری از این ارگانیسم هستند در حالیکه سایر افراد حامل این قارچ با درجههای مختلف میباشند.
در حدود 20% افراد بالغ کلونیزه شدهاند ولی بیشترین مقدار کلونیزاسیون در کودکان و افراد بالغ با نقص سیستم ایمنی میباشد. تشخیص و درمان به موقع آن امکان نجات بیمار را بالا میبرد. ارتباط بین قومیت و ژنتیک با کلونیزاسیون به مقدار کمی شناخته شده است. وقوع همزمان سایر عفونتهای تنفسی میتواند موجب انتقال شود. این بیماری به شدت مسری میباشد و پیشگیری با کوتریموکسازول بطور وسیعی در جلوگیری از عفونت موثر میباشد.
وقوع PCP کشنده در مردان همجنسگرا در ایالات متحده یکی از اولین نشانههای اپیدمی قریبالوقوع AIDS در دهه 1980 را فراهم کرد. افراد دارای نقص شدید در سیستم ایمنی بخصوص نقص و عدم کارایی در T-cell اولین گروه در خطر PCP میباشند. در اوایل اپیدمی AIDS،PCP عامل تشخیص این بیماری در حدود 60% افراد بود. این فراوانی در کشورهای توسعه یافته اتفاق افتاد ولی بخاطر کمبود ظرفیت تشخیصی در اکثر کشورهای کم توسعه یافته، عفونت بطور ضعیفی در این کشورها ثبت شده است. میزان افراد آلوده شده با HIV در کشورهای مختلف (به دلیل استفاده از تکنیک های تشخیصی مختلف) در واقع در حال تغییر است.
PCP در افراد بدون HIV:
گروههای مختلفی از افراد نظیر گیرندگان عضو و بیماران درمان شده با کورتیکواستروئیدها و عوامل تنظیم کننده سیستم ایمنی در خطر آلودگی با PCP میباشند. در میان کودکان خصوصاً کودکان دارای سوء تغذیه، کودکان دارای سندرم نقص سیستم ایمنی وراثتی و سرطان، مستعد PCP میباشند. سندرم مرگ ناگهانی کودکان اخیراً در ارتباط با عفونت اولیه P. jirovecii میباشد. نقش P. jirovecii در تشدید COPD یا پیشرفت بیماری ریه به وضوح مشخص نیست ولی P. jirovecii بطور معمول یافت میشود . 42% از ریههای بیمارانCOPD پیشرفته، حامل میکروارگانیسم هستند. این بیماری در افراد HIV منفی، دارای نشانهها و علائم بیشتر، رادیولوژی وخیمتر و 50% مرگ و میر بیشتر با وجود درمان میباشد.
تشخیص PCP:
تشخیص میکروسکوپی اساس شناسایی P.jirovecii میباشد. این ارگانیسم در محیط رشد نمییابد. در سالهای اخیر بیومارکرهای مولکولی نقش مهمی را در تشخیص سریع و حساس این بیماری ایفا کردهاند.
جدول 1: مقایسه تکنیکهای میکروسکوپی و PCR در شناسایی P.jirovecii
| Real time-PCR | ایمونوفلورسنس | GMS | تولوئیدن بلو-O | رنگ آمیزی گرم | گیمسا | Diff-Quick | |||
|
هدف |
فرم کیستی، فرم تروفوزوئیتی |
فرم کیستی |
فرم کیستی | فرم کیستی | فرم کیستی، فرم تروفوزوئیتی | فرم تروفوزوئیتی | فرم تروفوزوئیتی | ||
| حساسیت | +++++ | +++++ | ++++ | ++++ | ++++ | +++ | ++ | ||
| اختصاصیت | ++++ | ++++ | ++++ | ++++ | ++ | +++ | ++++ | ||
| زمان روش بر حسب دقیقه |
150 |
200 |
100 |
50 |
60 |
80 |
33 |
||
GMS=Gomori Methenamine Silver؛ فرم کیستی=asci؛ فرمهای تروفوزوئیتی مشابه دیواره سلولی ناقص مخمر؛ نامگذاری جدید برای کیست، تروفوزوئیت ها و اسپوروزوئیت ها.
+ =0-25 %؛ ++ =26-26% ؛ +++ =75-51% ؛ ++++ =85-76% ؛ +++++ =95-86%.
از بین این روشها، Real time PCR، GMS و تلوئیدن بلو–O بهترین روشهای تشخیصی میباشند. مطالعات نشان دادهاند که حساسیت PCR 15-20% بیشتر از روشهای میکروسکوپی است. در Real time PCR نیاز به مهارت در استفاده از میکروسکوپ نیست ولی این روش نیز نیازمند تجهیزات مخصوص میباشد. به نظر میرسد که روش تشخیص سریع و حساس موجب کاهش تلفات میشود. با این حال در روش میکروسکوپی به دلیل خطای کار میکروسکوپیست حدود 25% از موارد اثبات شده، بخاطر خطا از دست میرود.
تشخیص با آنتیژن بتا –D گلوکان در خون بسیار حساس میباشد ولی اختصاصی نیست، این تست روش مناسبی برای اکثر آزمایشگاهها نیست حتی در کشورهایی که بطور وسیعی گسترش یافتهاند روش کارآمدی در ارزیابی پاسخ به درمان نمیباشد. تمام نمونههای تنفسی برای PCR و تشخیص میکروسکوپی قابل استفادهاند ولی شستشوی برونکوآلوئولار (BAL) در کشورهای توسعه یافته ترجیح داده میشود. بزاق و شستشوی دهانی نیز در برخی مطالعات ارزشمند میباشند ولی از اعتبار کمتری برخوردار هستند.
درمان PCP:
دوز بالای کوتریموکسازول (سولفامتوکسازول/تری متوپریم) به عنوان درمان استاندارد برای مرحله اول درمان PCP، بهترین درمان درون وریدی(IV) داده شده برای افراد بسیار بیمار میباشد. تغییر نوع مصرف دارو از تزریقی به خوراکی بعد از 3 تا 10 روز معمول میباشد که به پیشرفت و شدت بیماری بستگی دارد. در PCP متوسط و شدید اگر کورتیکواستروئیدها بطور همزمان برای 10 روز تا 3 هفته استفاده شوند، بیمار پاسخ بهتری را در درمان میگیرد. عوارض معمول درمان شامل حالت تهوع، استفراغ، راش های پوستی، نوتروپنی و تست فعالیت کبدی غیرعادی میباشد. موارد خفیف بیماری قابل درمان با داروهای خوراکی میباشد که از کوتریموکسازول و یا ترکیبی از تریمتوپریم و داپسون استفاده میشود.
مرحله دوم درمان شامل تزریق درون وریدی یا عضلانی پنتامیدین و ترکیبی از دوز بالای کلیندامایسین و پریماکوئین میباشد. PCP در صورتیکه درمان نشود، کشنده خواهد بود. مدیریت این بیماری توسط متخصصین بالینی با تجربه منجر به نجات 90-85%ی بیماران مبتلا به AIDS و حدود 50% در بیماران HIV منفی شده است. در کودکان آفریقایی نتایج حاصل حتی با درمان مناسب ضعیف میباشد بطوریکه میزان مرگ و میر 50 تا 75% میباشد. در افراد مبتلا به ایدز هنگامی که بهبودی در مورد PCP حاصل میشود، این بیماران میتوانند تحت درمان ضد ویروسی قرار گیرند که اکثراً این بیماران تحت مراقبتهای کلینیکی خوبی قرار میگیرند.
پیشگیری اولیه و ثانویه با کوتریموکسازول خوراکی است و در صورتیکه مصرف دارو منظم باشد و پیشیگیریهای لازم در مقابل توکسوپلاسموز و برخی عفونتهای باکتریایی صورت گیرد، بسیار موثر است. بطور معمول این دارو به بیماران HIV مثبت با شمارش سلولی CD4 ml200 > و گیرندگان عضو داده میشود. ظهور مقاومت نسبت به کوتریموکسازول، کارآمدی آن را در برخی بیماران محدود کرده است. در برخی جوامع و گروههای بیمار، عدم موفقیت در پیشگیری با کوتریموکسازول وجود دارد. انتقال مستقیم از طریق بیمارانی که ارگانیسم در بدن آنها کلونیزه شده است نیز انجام ميشود.
P. jirovecii در هوای بازدمی بیماران PCP وجود داشته و با افزایش فاصله از بیمار، مقدار میکروارگانیسم کاهش مییابد. انتقال مستقیم فرد به فرد، در حال حاضر ثبت شده است و برخی از سویهها ممکن است بسیار مسری یا بدخیم نسبت به سایر سویهها باشند. همه بیماران PCP بیمارستانی باید در اتاقهای یک نفره ایزوله شوند و بیماران آسیبپذیر باید از آنها دور بمانند.
تحقیقات مورد نیاز در خصوص پنومونی پنوموسیستوزیس:
- روشهای تشخیصی مولکولی ارزان قیمت (نظیر Real time-PCR) باید برای تشخیص سریع و موثر PCP گسترش یابند.
- ابزارهای تشخیصی جایگزین کارآمد برای بیمارانی که بزاق کافی ندارند و در افرادی که برونکوسکوپی امکانپذیر نمیباشد.
- نسبت مشابه موارد PCP در مقابل سایر جوامع دارای پنومونی، هم در افراد بالغ و هم در کودکان، از روش های تشخیصی حساس باید برای کشورهای با موارد بالای HIV مشخص و ثابت استفاده شود.
- تاثیر درمانی کمکی کورتیکواستروئیدها باید در کشورهای با بار TB بالا مورد مطالعه قرار گیرند تا عواقب منفی آن معلوم گردد و اینکه آیا معیارهای یکسانی که برای تشخیص PCP متوسط و شدید در کودکان و افراد بالغ مورد استفاده قرار میگیرد قابل پذیرش است.
- انجام ارزیابی مقاومت نسبت به دارو کوتریموکسازول
منابع:
- 1. Thomas Jr CF, Limper AH. Pneumocystis pneumonia. New England Journal of Medicine. 2004;350(24):2487-98.
- 2. Morris A, Norris KA. Colonization by Pneumocystis jirovecii and its role in disease. Clin Microbiol Rev 2012;25:297-317.
- 3. Tipirneni R, Daly KR, Jarlsberg LG, Koch JV, Swartzman A, Roth BM, et al. Healthcare worker occupation and immune response to Pneumocystis jirovecii. Emerging infectious diseases. 2009;15(10):1590.
- 4. Maskell N, Waine D, Lindley A, Pepperell J, Wakefield A, Miller R, et al. Asymptomatic carriage of Pneumocystis jiroveci in subjects undergoing bronchoscopy: a prospective study. Thorax. 2003;58(7):594-7.
[1] Pneumocystis pneumonia
https://www.webmd.com/hiv-aids/guide/aids-hiv-opportunistic-infections-pneumocystis-pcp-pneumonia
https://medlabnews.ir/%d8%a7%db%8c%d8%af%d8%b2/
برای دانلود پی دی اف بر روی لینک زیر کلیک کنید
ورود / ثبت نام