پرسش و پاسخهای آزمایشگاهی و کاربردی در طب انتقال خون
قسمت اول
دکتر حبیباله گلافشان1، پریسا تندل2
1: عضو هیئت علمی دانشگاه علوم پزشکی شیراز
2: کارشناسی ارشد خونشناسی و بانک خون دانشکده پیراپزشکی
مقدمه
سمینارهای طب انتقال خون و هموویژولانس بهطور مکرر در بیمارستانهای استان برای پرسنل علوم آزمایشگاهی، پرستاران و پزشکان برگزار میگردد. توفیق الهی نصیب اینجانب در برگزاری سمینارها در طی سالیان متمادی گردید و موفق به جمعآوری پرسشهای کلیدی و کاربردی از طرف عزیزان علوم آزمایشگاهی گردیدم که در حد بضاعت علمی با توجه به رفرانسهای مرجع و معتبر که در بخش آخر خواهد آمد، پاسخ داده شده است. این پرسش و پاسخ در چند قسمت تقدیم شما عزیزان میگردد به این امید که گره مشکلات آزمایشگاهی در رابطه با تزریق خون و فرآوردههای آن گشوده گردد.
پرسش 1) آزمایشهای قبل از تزریق خون شامل چه تستهایی است؟
پاسخ: گروهبندی سیستم ABO و RH، آزمایش اسکرین آنتیبادی و کراس مچ از آزمایشهای قبل از تزریق هستند.
پرسش 2) شرایط نمونهگیری از بیمار برای تزریق خون چگونه است و مفهوم قانون 3 در نمونهگیری چیست؟
پاسخ: نمونهگیری شامل تهیه 10 سیسی خون بدون ضد انعقاد و 2 سیسی خون EDTAدار است. نمونهها نباید با محلول قندی تزریق وریدی مخلوط و رقیق شده باشند. لولههای نمونه بایستی با نام و نام خانوادگی، شماره پرونده، تاریخ و ساعت خونگیری و اوایل نام و نام خانوادگی خون گیرنده نشانهگذاری گردد.
از سرم جداشده برای کراس مچ و از نمونه EDTAدار برای گروهبندی استفاده میشود. قانون 3 بدین مفهوم است که چنانچه بیماری تا 3 ماه پیش خون یا پلاکت دریافت کرده باشد و یا این که خانمی تا 3 ماه پیش حامله بوده است، از این نمونه فقط تا 3 روز میتوان برای کراس مچ یا تشخیص آنتیبادی استفاده کرد و در صورت نیاز به کیسههای بیشتر، بایستی نمونهگیری مجدد بهعمل آید. گفتنی است که اگر خون به بیماری تزریق گردد، آنتیژنهای جدیدی وارد گردش خون میگردند و شانس ساختن آنتیبادی بین 3 روز تا 3 ماه پس از تزریق است.
از این رو فرض بر این نهاده شود که وضعیت ایمنی شخصی که تا 3 ماه پیش خون گرفته یا حامله بوده است ممکن است 3 روز به 3 روز عوض شود؛ برای مثال چنانچه از بیماری نمونهگیری روز شنبه انجام شود، از این نمونه تا ساعت 12 شب روز سهشنبه میتوان برای کراس مچ و یا تشخیص آنتیبادی استفاده کرد.
مثال دیگر، چنانچه برای بیماری 5 کیسه خون کراس مچ و آماده شده باشد و به بیمار 3 کیسه تزریق شود و 3 روز از تزریق بگذرد، بایستی دو کیسهای که از قبل آماده شده با نمونه جدید، بنا به قانون 3، دوباره برای بیمار کراس مچ شود چون با تزریق، وضعیت ایمونولوژیک بیمار تغییر کرده است. روز اول نمونهگیری روز صفر محسوب میشود. نمونههای خون هپارینه بهویژه از بخش همودیالیز که دیر لخته میشود و اغلب سرم ژلاتینه میدهد را میتوان با افزایش یک تا دو قطره سولفات پروتامین یک درصد به لوله آزمایش هپارین آن را خنثی و انعقاد را تسریع کرد.
چنانچه قانون 3 در مورد بیماری صادق باشد، وضعیت ایمونولوژیک بیمار ممکن است هر 3 روز تغییر کند و در آمادهسازی خون بایستی تمام فازهای کراس مچ را بهدقت انجام داد
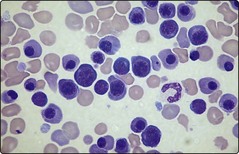
یک مثال از قانون 3 که از بیمار با سابقه تزریق خون، نمونهگیری برای کراس مچ و تشخیص آنتیبادی انجام شده است
پرسش 3) شیوه انتخاب خون و فرآوردهها برای بیمار چگونه است؟
پاسخ: هر بیمار بایستی خون همگروه ABO و RH را دریافت کند، ولی چنانچه همگروه در دسترس نباشد به نکات زیر توجه کنید:
- گلبول قرمز O فشرده، دهنده همگانی است و با همگروهی ارهاش به بیمار تزریق میشود. در زمانی که فرصت گروهبندی نیست –O دهنده همگانی است.
- بیمار با گروه خونی AB گیرنده همگانی خون فشرده است ولی بهتر است در درجه اول چنانچه گروه AB در دسترس نباشد از خون فشرده A استفاده کرد زیرا عیار آنتی A در گروههای B و O بالاست و توجه داشته باشید که هر کیسه خون فشرده حدود 50 سیسی پلاسما دارد.
- تزریق خون ارهاش منفی به ارهاش مثبت بلامانع است و چنانچه کیسههای ارهاش منفی به تاریخ انقضا نزدیک میشود بهتر است که برای افراد ارهاش مثبت هم کراس مچ شود.
- در صورت در دسترس نبودن پلاسمای همگروه میتوان از پلاسمای گروه AB بهعنوان دهنده همگانی استفاده کرد. در تزریق پلاسما نیازی به همگروهی ارهاش نیست.
- بیمار با گروه O، گیرنده همگانی پلاسما است و میتوان پلاسما از گروههای A،B و AB را به بیمار تزریق کرد ولی پلاسمای AB را بهتر است برای بیمار با گروههای A، B و AB نگه دارید چون برای این افراد غیر از گروه AB شانس دیگری وجود ندارد.
- تزریق کرایو بدون در نظر گرفتن ABO و RH صورت میگیرد چون دارای حجم کم حدود 10 سیسی است.
- در تزریق پلاکت همگروهی ABO و RH لازم است. هر کیسه پلاکت راندوم تقریباً حاوی 50 سیسی پلاسماست و تزریق غیر همگروه بهویژه در کودکان موجب واکنش حاد همولیتیک میگردد. در صورت در دسترس نبودن پلاکت همگروه بایستی گروهی انتخاب کرد که سازگاری پلاسما رعایت شده باشد و از این رو پلاکت گروه AB، دهنده همگانی و بیمار با گروه O، گیرنده همگانی پلاکت است. گرچه سیستم ارهاش روی پلاکتها بیان نمیشود ولی تهیه فرآورده پلاکتی با مقداری از گلبول قرمز (کمتر از 0/3سیسی)، با گلبول قرمز آلوده میشود و از این رو همگروهی ارهاش در تزریق این فرآورده بایستی در نظر گرفته شود. آنتیژنهای ABO بهطور ضعیف روی پلاکتها بیان میشوند.
پرسش 4) بیماری با کاهش شدید پلاکت، نیاز به پلاکت دارد. همگروه بیمار و پلاکت گروه AB که دهنده همگانی است در دسترس نیست چه کار باید کرد؟
پاسخ: چنانچه پلاکت غیر همگروه در دسترس است میتوان چند کیسه را با هم مخلوط کرد (مخلوط کردن بایستی از یک گروه باشد) و با دور g 500-800 سانتریفیوژ نموده و قسمت بیشتر پلاسمای ناسازگار را برداشت و جایگزین آن پلاسمای AB یا محلول نگهداری پلاکت(PAS) اضافه کرد و به اصطلاح کاهش حجم پلاسما داد و سپس برای تزریق استفاده نمود.
پرسش 5) در چه سطحی از شمارش پلاکت نیاز به تزریق پلاکت است؟ اگر مجبور به تزریق پلاکت گروه مثبت به منفی باشیم چه کار باید کرد؟
پاسخ: شمارش پلاکت کمتر از 20000 فرد را مستعد خونریزی میکند، بهویژه اینکه با فاکتورهای خطر دیگر مانند تب و عفونت همراه باشد. برای ثبات انعقادی برای بیماری که به علت کاهش پلاکت خونریزی دارد، رساندن پلاکت به سطح 50000 کافی است ولی برای عمل جراحی بین 50000 تا 100000 و برای جراحیهای چشم و مغز و ریه سطح 100000 پیشنهاد میگردد.
تزریق هر کیسه پلاکت راندوم که از 500 سیسی خون تهیه میشود به ازای هر 10 کیلوگرم وزن، 50000 پلاکت را در میلیمتر مکعب افزایش میدهد؛ برای مثال تزریق 7 کیسه پلاکت به فرد 70 کیلوگرمی 50000 و تزریق 4 کیسه به فرد 40 کیلوگرمی 50000 در میلیمتر مکعب پلاکت را افزایش میدهد. هر کیسه پلاکت که به روش آفرز تهیه میشود معادل 6 کیسه پلاکت راندوم است و تزریق هر واحد آن 30000 تا 50000 پلاکت را در یک شخص 70 کیلوگرمی افزایش میدهد. توجه داشته باشید که این افزایش مقدار برای بیماری است که آنتیبادی علیه HLA و آنتیژنهای پلاکتی نداشته باشد.
چنانچه به دختربچه با گروه منفی یا خانمی با گروه منفی که در سن بارداری است نیاز به تزریق پلاکت باشد و مجبور به تزریق پلاکت با گروه مثبت به منفی باشیم، میتوان با تزریق یک آمپول 300 میکروگرمی روگام در ابتدا اقدام به تزریق 30 تا 36 کیسه پلاکت کرد. برخی عقیده دارند که تا زمانی که روگام (آنتی D) در خون بیمار قابل شناسایی است میتوان پلاکت گروه مثبت را به منفی تزریق کرد. نیمهعمر روگام 21 روز است و از این رو میتوان تزریق پلاکت مثبت به منفی را حتی 2 تا 3 ماه ادامه داد و در صورت نیاز بیشتر اقدام به تزریق یک آمپول روگام دیگر کرد. گفتنی است که پلاکت آفرز آلودگی بسیار کمتری به RBC دارد و شاید یک میکرو دوز روگام در این حالت لازم باشد.
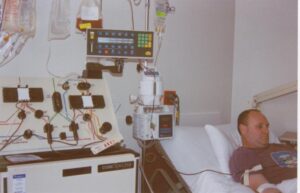
در تهیه پلاکت به روش آفرز خون اهداکننده وارد دستگاه شده و پس از جداسازی پلاکت بر اساس وزن مخصوص بقیه خون از ورید دیگر به گردش خون بازمیگردد
پرسش 6) از بخشهای بیمارستان چند واحد پلاکت و خون مصرفنشده زماندار به بانک خون بیمارستان عودت دادهاند، آیا مجاز به نگهداری مجدد آن هستیم؟
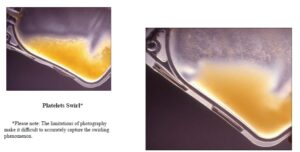
پاسخ: آزمایش حرکت گردابی یا Swirling آزمایشی ساده برای اطمینان یافتن از زنده بودن پلاکتها و PH بالای 6/2 است، از این رو با مثبت شدن حرکت Swirling و اطمینان از اینکه پلاکتها در یخچال قرار نگرفتهاند میتوان برای بیماران دیگر استفاده کرد. برای مشاهده حرکت گردابی کیسه پلاکت را در برابر منبع نور تکان داده و بایستی شاهد حرکت گردابی ابری مانند پلاکتها بود. کیسههای خون به شرطی برای نگهداری در بانک خون مورد قبول قرار میگیرند که بیش از نیم ساعت در بیرون از یخچال نبوده باشند که در این حالت دمای کیسه نبایستی از 10 درجه سانتیگراد متجاوز گردد.
مثبت شدن حرکت گردابی کیسه پلاکت بیانگر زنده بودن و PH بالای 6/2 است. کیسه سمت راست دارای حرکت گردابی منفی است
پرسش 7) چنانچه خون با گروه ارهاش منفی در دسترس نباشد آیا میتوان به بیمار خون ارهاش مثبت تزریق کرد؟
پاسخ: اگر تزریق خون جنبه اورژانس دارد، بهتر است که در انجام آن تأخیری رخ ندهد. چنانچه یک کیسه خون ارهاش مثبت به شخص سالم ارهاش منفی تزریق شود، شانس ساختن آنتیبادی 70% است ولی این شانس در بیمار بدحال ترومایی حدود 30% است. از طرف دیگر در تزریق خون ارهاش مثبت به منفی چنانچه آنتیبادی شکل گیرد، موجب فعال شدن کمپلمان نمیگردد و از این رو برخلاف آنتیبادیهای سیستم ABO موجب فعال شدن انعقاد خون (DIC) و شوک نمیگردد و همولیز بهصورت خارج عروقی رخ میدهد. البته یادآوری میشود که بهطور کلی هر بیمار ارهاش منفی شاید یکبار بتواند خون ارهاش مثبت دریافت کند و نباید بهآسانی این شانس را از بیمار سلب کرد چون اگر آنتی ارهاش بسازد بار دیگر شانس گرفتن خون ارهاش مثبت را ندارد.
با تزریق خون ارهاش مثبت به منفی چنانچه آنتیبادی شکل گیرد، ممکن است بیمار زرد شود و در گستره خون محیطی بهطور موقت اسفروسیت مشاهده شود و یا ممکن است اتفاقی رخ ندهد. چنانچه بیماری با گروه ارهاش منفی نیاز به تعداد زیادی کیسه خون دارد و کیسههای گروه منفی محدود هستند و با تمام شدن کیسههای منفی باز مجبور به تزریق خون ارهاش مثبت میشوید، سفارش میشود که از همان اول تزریق را با کیسههای ارهاش مثبت شروع کنید و منبع ذخیره گروه منفی را برای افراد ارهاش منفی حفظ کنید. اگر به دختربچهای با گروه منفی یا خانمی که در سن بارداری است و شوهرش گروه مثبت دارد به اشتباه خون ارهاش مثبت تزریق شد، بایستی با تزریق روگام از تحریک ارهاش جلوگیری کرد.
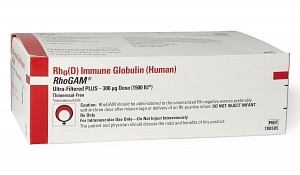
هر آمپول روگام جهت جلوگیری از تحریک 15 سیسی خون فشرده یا 30 سیسی خون کامل با گروه مثبت به منفی است. برای مثال اگر به دختربچهای با گروه منفی 50 سیسی خون فشرده مثبت تزریق شود، نیاز به 4 آمپول روگام است که تا 72 ساعت از تزریق خون بایستی تزریق شود.
در محاسبه روگام چنانچه عدد اعشاری زیر نیم یا عدد بدون اعشار بود یک عدد اضافه میکنیم و چنانچه عدد اعشاری نیم یا بالاتر بود ابتدا به طرف عدد بالا گرد میشود و سپس یکی اضافه میشود برای مثال 3/8 آمپول روگام عدد 5 میگردد.
البته بایستی یادآوری شود که چنانچه تزریق خون ارهاش مثبت به منفی در حجمی زیاد رخ داده باشد، تزریق روگام باعث همولیز میشود و سودی ندارد چون روگام از جنس آنتی D است و با گلبولهای قرمز واکنش میدهد؛ برای مثال اگر به خانمی با ارهاش منفی، اشتباهاً 300 سیسی خون فشرده مثبت تزریق گردد، نیاز به 20 آمپول روگام بنا بر محاسبه میشود که یکی هم اضافه میگردد. این حجم از روگام منجر به همولیز میگردد. چنانچه در موارد فوق مجبور به جلوگیری از تحریک ارهاش باشیم، بایستی نخست با یک حجم خون ارهاش منفی، تعویض خون انجام شود. با هر حجم تعویض، 30% از خون تزریقی در بدن بیمار باقی میماند که در این حالت 100 سیسی میشود و با تزریق 7 آمپول روگام از ایمونوزاسیون جلوگیری میگردد.
چنانچه با دو حجم ارهاش منفی تعویض خون صورت گیرد، فقط 30 تا 35 سیسی خون ارهاش مثبت در بدن بیمار باقی میماند که با 3 آمپول روگام میتوان از تحریک ارهاش جلوگیری کرد.
هر ویال روگام حاوی 300 میکروگرم یا 1500 واحد اینترنشنال آنتی D است
پرسش 8) بیماری مبتلا به کمخونی آپلاستیک و دچار ترومبوسیتوپنی شدید کمتر از 20000 است و تعداد زیادی کیسههای پلاکت به بیمار تزریق شده ولی خونریزی بند نمیآید و افزایش شمارش پلاکت مشاهده نمیشود. چه باید کرد؟
پاسخ: هنگامی که بیماری به تزریق پلاکت پاسخ ندهد، گفته میشود که بیمار به تزریق رفراکتوری یا مقاوم است. از مهمترین علت مقاومت به تزریق پلاکت ساخته شدن آنتیبادی علیه آنتیژنهای HLA و آنتیژنهای پلاکتی است. برای ارزیابی پاسخ بیمار به تزریق پلاکت میتوان پارامتر cci را پس از یک ساعت از تزریق پلاکت محاسبه کرد و چنانچه مقدار آن پس از دو بار از تزریق پلاکت کمتر از 7500 شود، پدیده رفراکتوری تأیید میگردد. گفتنی است که همیشه شمارش پایین پلاکت، راهنمایی برای تزریق پلاکت نیست؛ برای مثال در بیماری TTP (ترومبوتیک ترومبوسایتوپنی پورپورا) و ترومبوسایتوپنی ناشی از تزریق هپارین (HIT) علیرغم کاهش شدید پلاکت، تزریق آن قدغن است چون به ایجاد لخته پلاکتی میانجامد. در ترومبوسایتوپنی ایمونولوژیک عمر پلاکتهای تزریقی در حد چند دقیقه و کوتاه است، مگر اینکه به همراه IVIg به بیمار تزریق شود.
هر کیسه پلاکت راندوم حداقل حاوی 1010×5/5 و هر کیسه پلاکت آفرز حاوی 1011×3 عدد پلاکت است
در کمخونیهای آپلاستیک و بیمارانی که شیمیدرمانی میشوند بایستی از روز اول فرآوردههایی به بیمار تزریق شود که از پدیده رفراکتوری جلوگیری کند، زیرا این دسته از بیماران نیاز مزمن به تزریق پلاکت دارند؛ برای مثال چنانچه بیمار مبتلا به آنمی آپلاستیک نیاز به خون دارد باید LR-RBC (خون کم لکوسیت) تزریق کرد تا از تحریک آنتیژن HLA جلوگیری شود. وقتی که بیماری به تزریق پلاکت مقاوم میشود، بهتر است از خواهران و برادران و یا اقوام درجه اول، آزمایش تطابق آنتیژنی HLA-A و HLA-B بین دهنده و بیمار بهعمل آید و سپس اهداکنندهای که شباهت آنتیژنی به بیمار را دارد انتخاب کرده و به طریقه آفرز از دهنده پلاکت تهیه گردد.
اهداکننده میتواند در سال 24 بار به طریقه آفرز، پلاکت اهدا نماید. هر کیسه پلاکت آفرز معادل 6 کیسه پلاکت راندوم و حاوی 1011×3 عدد پلاکت است. پلاکت آفرز پس از اشعه دادن به بیمار تزریق میشود. اشعه دادن از آن رو انجام میگیرد که قرابت بیمار و اهداکننده ممکن است موجب واکنش گرافت گردد. در پلاکت اشعهدیده تمام لنفوسیتها غیرفعال گشته و از پدیده گرافت که مرگ به دنبال دارد جلوگیری میکند.
پرسش 9) برای بیماری با گروه +A هر کیسه خونی که کراس مچ میکنیم ناسازگار است. علت چیست و چکار باید کرد؟ اتفاقی مشابه فوق با گروههای دیگر هم داشتهایم. در این موارد چگونه خون سازگار یافت میشود؟
پاسخ: وقتی که تعداد زیادی کیسه خون برای بیماری کراس مچ میکنید و ناسازگار است، گفته میشود حالتی است که همه اهداکنندگان ناسازگارند. این حالت در موارد زیر دیده میشود:
- مبتلا به کمخونی آتوایمیون همولیتیک
- حضور آنتیبادی در بیمار علیه آنتیژنی با شیوع فراوان
- تزریق ایمونوگلوبولین وریدی IVIg) به بیمار)
- حضور رولکس یا پدیده آگلوتیناسیون سرد
در این مورد آزمایش کومبز مستقیم بر روی نمونه بیمار انجام دهید. چنانچه آزمایش مثبت باشد و گستره محیطی اسفروسیتوز و پلیکروماژی و افزایش رتیکولوسیت نشان دهد، بیمار مبتلا به کمخونی آتوایمیون است. در این موارد چندین کیسه را کراس مچ کرده و کیسههایی که کمترین ناسازگاری را میدهد برای بیمار انتخاب کنید. البته به یاد داشته باشید چنانچه بیمار در یکی دو ماه گذشته تزریق خون داشته و آزمایش کومبز بهصورت میکس فیلد مثبت باشد، این دال بر حضور آتوآنتیبادی نیست و ممکن است پدیده میکس فیلد به علت ساخته شدن آلوآنتیبادی علیه گلبولهای تزریقی باشد که بایستی حتماً خون سازگار برای بیمار پیدا کرد.
گفتنی است که آتوآنتیبادی با تمام سلولهای اسکرین و پانل واکنش میدهد، در حالی که آلوآنتیبادی با برخی واکنش مثبت و با برخی واکنش منفی دارد. چنانچه آزمایش کومبز مستقیم بیماری منفی است و تمام کراس مچها ناسازگارند، احتمال حضور آنتیبادی علیه آنتیژنی با شیوع بالا مطرح میشود؛ برای مثال آنتی k یک آنتیبادی علیه آنتیژنی با شیوع فراوان است. در این موارد امکان دارد اهداکننده سازگار را در میان اقوام درجه اول بیمار جستجو کرد زیرا احتمال داردکه اقوام نزدیک بیمار مانند بیمار از نظر آن آنتیژن با شیوع فراوان منفی باشند. ایمونوگلبولینهای تزریق وریدی از حوضچههای مخلوط صدها پلاسما تهیه میشوند و از این رو تزریق آن با تناقض گروهبندی و آزمایش مثبت کومبز بهطور موقت همراه میشود. در این حالت کیسه خون O را برای تزریق به بیمار در نظر بگیرید، گرچه کراس مچها ناسازگار باشند.
چنانچه بیماری آگلوتیناسیون سرد قوی دارد مانند برخی از بیماران مبتلا به لنفوم یا عفونت به میکروب مایکوپلاسما یا مونونوکلئوز عفونی از روش کراس مچ پیشگرمایی استفاده کنید. در کراس مچ پیشگرمایی، سرم و گلبولهای قرمز اهداکننده را بهطور مجزا هر کدام 10 دقیقه در 37 درجه گذاشته میشود و سپس در همان 37 درجه با هم مخلوط میگردند. شستشوی گلبولها برای فاز کومبز با سالین 37 درجه انجام میگیرد.
رولکس تجمع غیراختصاصی گلبولهای قرمز ناشی از حضور پروتئینهای غیرطبیعی است که بهطور معمول در مالتیپل مایلوما به علت گاماپاتی و بیماریهای التهابی بهعلت افزایش پروتئینهای فاز حاد و حاملگی به علت افزایش فیبرینوژن رخ میدهد. در این حالت اگر یکی دو قطره خون بیمار روی اسلاید ریخته شود، تجمع گلبولهای قرمز دیده شده که با افزایش چند قطره سرم فیزیولوژی گلبولها پخش میگردند، در حالی که در آگلوتیناسیون سرد پخش نشده و چنانچه اسلاید در 37 درجه به مدت 3-2 دقیقه قرار گیرد واکنش ناپدید میگردد. چنانچه در کراس مچ شاهد واکنش رولکس و حل شدن واکنش با سرم فیزیولوژی بودید، مانعی برای تزریق خون وجود ندارد.
پرسش 10) نوزادی احتیاج به تعویض خون به علت افزایش بیلیروبین دارد، خون انتخابی و شیوه کراس مچ چگونه است؟ اگر خون سازگار یافت نشد چه باید کرد؟
پاسخ) اگر بیلیروبین از سطح بحرانی تجاوز کند با نفوذ به مغز موجب یرقان مغزی (kernicterus) میگردد که ضایعات مغزی غیر قابل برگشت یا مرگ به دنبال دارد. سطح بیلیروبین یا محاسبه نسبت بیلیروبین به آلبومین و وزن نوزاد از معیارهای مهم برای تعویض خون هستند. چنانچه کومبز مستقیم نوزاد مثبت باشد ناسازگاری سیستم ارهاش یا سایر گروههای خونی مطرح است. امروزه آنتی K و آنتی c از مهمترین علل کمخونی همولیتیک جنین- نوزادی است. در یک برهه زمانی آنتی D عامل مهم کمخونی همولیتیک نوزادی بوده است که با تزریق روگام به خانمهای ارهاش منفی در 28 هفتگی حاملگی و بعد از زایمان از شیوع آن کاسته شده است. در ناسازگاری ارهاش، گروه خون مادر منفی و نوزاد دارای گروه مثبت است و آزمایش کومبز مستقیم نوزاد مثبت است. آزمایش اسکرین مادر از نظر آنتیبادی حضور آنتی D را نشان میدهد.
چنانچه سرم مادر با سه گلبول +O واکنش مثبت و با سه گروه –O واکنش منفی بدهد، به احتمال 95% ناسازگاری RH اثبات میگردد. خون انتخابی جهت تعویض در ناسازگاری ارهاش بایستی حتماً از نظر ارهاش منفی و از نظر ABO با مادر و نوزاد جور باشد؛ برای مثال اگر مادر – A و نوزاد +A باشد خون –A یا –O در نظر گرفته میشود. اگر ناسازگاری ارهاش مطرح نباشد، برای مثال مادر +O و نوزاد +O باشد و تست کومبز مستقیم مثبت باشد، بایستی به ناسازگاری در سیستمهای دیگر گروه خون فکر کرد. در این حالت ممکن است در پرونده پزشکی مادر آنتیبادی حائز اهمیت بالینی که در دوران حاملگی اسکرین شده است، مشخص شده باشد؛ برای مثال اگر سرم مادر حاوی آنتی K باشد، خون +O–K برای نوزاد در نظر گرفته میشود.
چنانچه آزمایش در دوران حاملگی انجام نشده باشد، بایستی سرم مادر را با سلولهای پانل مجاور ساخت و آنتیبادی مسئول همولیز را مشخص کرد و خون آنتیژن منفی را با توجه به آنتیبادی برای تعویض در نظر گرفت.
گفتنی است که آنتی K علاوه بر همولیز قادر به ایجاد ترومبوسایتوپنی نوزاد نیز هست. آزمایش کراس مچ برای تعویض خون با سرم مادر انجام میشود و سرم مادر با گلبولهای دهنده در سه فاز حرارت اتاق، 37 درجه و کومبز مورد آزمایش قرار میگیرد. در موارد اورژانس که خون سازگار یافت نمیشود، میتوان خون مادر را به شرط همگروهی یا سازگار بودن با نوزاد برای خارج کردن آنتیبادی شست و برای تعویض خون استفاده کرد.
چنانچه مادر گروه O و نوزاد گروه A یا B با بیلیروبین بالا باشد، ناسازگاری ABO مطرح میگردد. یادآوری میشود که افراد گروه O دارای Anti AB میباشند که 50% آن از جنس IgG است و قابلیت عبور از جفت را دارد. با عبور Anti AB از جفت، گلبولهای قرمز A یا B جنین، آلوده به آنتیبادی شده و همولیز میگردد. در ناسازگاری ABO تصویر خون محیطی نوزاد اسفروسیتوز را نشان میدهد. در ناسازگاری ABO بایستی حتماً از خون O و ارهاش شبیه نوزاد جهت تعویض استفاده کرد؛ برای مثال اگر مادر +O و نوزاد +A یا +B است از خون فشرده O با پلاسمای AB جهت تعویض استفاده میشود. چنانچه مادر O–و نوزاد +A یا +B باشد هم ناسازگاری RH و هم ABO در نظر گرفته شده و خون O– جهت تعویض بهکار میرود.
در ناسازگاری ABO آزمایش کومبز مستقیم نوزاد به علت خنثی شدن بخش بزرگی از AntiAB توسط مواد ترشحی و سلولهای دیگر نوزاد ممکن است منفی یا مثبت ضعیف شود. توجه داشته باشید که آنتیژنهای ABO روی تمام سلولهای بدن قرار دارند. چنانچه با دو برابر حجم خون (2 volume exchange) نوزاد تعویض خون صورت گیرد، حدود 90% از گلبولهای قرمز آغشته به آنتیبادی نوزاد با گلبولهای دهنده جایگزین میگردد و حدود 45 تا 50 درصد بیلیروبین گردش خون کاهش مییابد؛ برای مثال نوزادی با وزن 3 کیلوگرم احتیاج به 510 سیسی خون برای تعویض دو حجم دارد. نوزاد رسیده 85 سیسی خون و نوزاد نارس 100 سیسی خون به ازای هر کیلوگرم وزن دارد و 2 برابر حجم خون نوزاد 510 سیسی میشود.
برای تعویض معمولاً از مخلوط O فشرده و پلاسمای AB استفاده میشود. گروه O، دهنده همگانی گلبول قرمز و گروه AB دهنده همگانی پلاسماست. در صورت در دسترس نبودن پلاسمای AB میتوان از پلاسمای همگروه نوزاد استفاده کرد. چنانچه هماتوکریت خون فشرده 80% باشد برای دستیابی به هماتوکریت 50% برای تعویض، هر 100 سیسی خون فشرده با 30 سیسی پلاسما مخلوط میشود.
در گستره محیطی نوزاد مبتلا به کمخونی همولیتیک انبوهی از گلبول قرمز هستهدار دیده میشود که به آن اریتروبلاستوز فتالیس گفته میشود
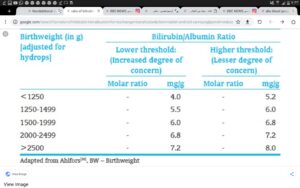
آستانه پایین و بالای نسبت بیلیروبین به آلبومین در تعویض خون نوزاد بر اساس وزن برحسب گرم
درباره اهدای خون بیشتر بدانیم (قسمت اول)
https://onlinelibrary.wiley.com/journal/15372995
برای دانلود پی دی اف بر روی لینک زیر کلیک کنید
ورود / ثبت نام