تکنولوژی کاهش پاتوژنها در فرآوردههای خون
دکتر حبیبالله گلافشان
عضو هیئت علمی دانشگاه علوم پزشکی شیراز
سالم بودن خون و فرآوردههای آن رکن اساسی طب انتقال خون است. بکارگیری یک سیستم پاتوژنزدایی که خطر انتقال بیماریهای مسری را به صفر برساند از ایدهآلهای تکنولوژی است.
ضرورت کاهش پاتوژنها
آلوده شدن خون و فرآوردههای آن به ویروس نقص ایمنی اکتسابی (HIV) در سال ۱۹۸۰ تهدیدی جدی و تجربهای تلخ در طب انتقال خون بود. تا پیدایش روشهای تشخیصی در جداسازی فرآوردههای سالم از آلوده، شرایط دشواری برای بیماران نیازمند که زندگی آنها وابسته به فرآوردهها بود بوجود آمد و متأسفانه تعداد چشمگیری از بیماران به این ویروس خطرناک مبتلا گردیدند.
با پدیدار شدن پاتوژنهای جدید، مسافرتهای بینالمللی، آداب و رسوم گوناگون و خرید و فروش کالا، ضرورت به کار گرفتن روشی که پاتوژنزدایی کند را اساسی کرده است.
روشهای تشخیصی پاتوژنها بر اساس ایمونولوژیک و اسید نوکلئیک (NAT)، گرچه سرایت برخی از بیماریهای خطرناک را کاهش داده است اما موفق به ریشهکنی کامل آنها نبوده است.
دوران دریچهای (Window Period) که در آن دوران بیماری قابل انتقال بوده ولی تشخیص آزمایشگاهی داده نمیشود و نیز مشکل در دایر کردن روشهای مناسب برای تشخیص میکروبها و انگلها مانند مالاریا از عوامل نبود موفقیت بوده است.
هدف تکنولوژی کاهش پاتوژنها به حداقل رسانیدن سرایت بیماریهای مسری با حداکثر راندمان در تخریب عوامل بیماریزاست.
این تکنولوژی بایستی سمی و موتاژن نبوده و بتواند کارآمدی گلبولهای قرمز، پلاکت و پروتئینهای پلاسما را تضمین کند. گلبولهای سفید در این تکنولوژی ناکارآمد و فاقد قدرت تکثیر میگردند و ازاینرو میتواند جایگزین خون اشعهدیده گردد.
تکنولوژی کاهش پاتوژنها برای بار نخست در پاتوژنزدایی پلاسما و مشتقات آن بکارگرفته شده است. هزاران واحد از پلاسمای اهداکنندگان در تهیهی فرآوردههای پلاسمایی مخلوط میگردند و بیمار را در خطر جدی سرایت بیماریها قرار میدهند، مانند سرایت هپاتیت و HIV که در بیماران مبتلا به هموفیلی رخ داد.
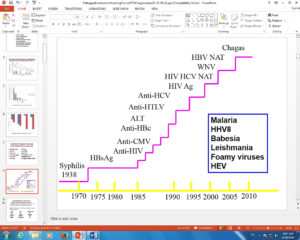
روند تاريخي آزمایش بیماریهای مسری روی فرآوردههای خون
مجاور ساختن و تیمار حوضچه ۲۵۰۰ واحد پلاسما با مواد حلال و پاککننده (Solvent detergent) یا پلاسمای S/D شیوهی مؤثر در غیرفعال کردن ویروسهای با پوشش لیپیدی مانند HIV، ویروسهای هپاتیت B و C، ویروس مولد لوسمی سلولهای T (HTLV)، EBV، ویروس سیتومگال و ویروس هرپس است. این روش قادر به غیرفعالسازی ویروسهای هپاتیت A و پاروویروس که فاقد پوشش لیپیدی هستند نیست. در تهيه پلاسماي S/D، ترکیبات تریانبوتیلفسفات و تریتون ۱۰۰-X برای کاهش پاتوژنها به کار میروند. کاهش پروتئین S و افت چند درصدی فاکتورهای انعقادی از موارد منفی این شیوه و کاهش دادن واکنشهای آسیب حاد ریوی و آلرژی به علت رقیق شدن آنتیبادیها و آلرژنها از موارد مثبت فرآورده پلاسمای S/D است. با انکوبه کردن پلاسمای S/D با ماتریکس جاذب پریونها میتوان فرآورده پلاسمایی با کاهش سرایت پریونها تهیه کرد.
متیلنبلو (MB)
متیلنبلو یک رنگ فنوتیازیني است که در برابر تابش نور مرئی (visible) فعال میشود و چنانچه به کیسهی پلاسما اضافه و در معرض تابش قرار گیرد قادر به غیرفعال کردن ویروسهای با پوشش لیپیدی است. فرآوردهی MB-Plasma (Therafley) بیش از ۲۰ سال است که در اروپا استفاده میشود.
متیلنبلو توانایی غیرفعالسازی ویروسهای داخل سلولی را ندارد و بنابراین روی فرآورده پلاسمایی غیرمنجمدشده بایستی نخست مرحلهی انجماد یا مرحلهی کاهش لکوسیت انجام گیرد و سپس در مجاورت متیلن بلو قرار گیرد. گرچه گزارش موردی از آلرژی به متیلنبلو گزارش گردیده ولی سلامت تزریق و کیفیت فرآورده مورد تأیید است.
کاربرد نور ماوراء بنفش در تکنولوژی کاهشدهندههای پاتوژن
(Ultra violet-activated photosensitive)
در سالهای اخیر از موادی مانند ریبوفلاوین (ویتامین B2) و آموتوسالن (Amotosalen) که با تابش اشعه ماوراء بنفش فعال میشوند برای کاهش خطر سرایت پاتوژنها در کیسههای پلاکت و پلاسما استفاده شده است.
در هر دو تکنولوژی برای غیرفعالسازی پاتوژنها و گلبولهای سفید کیسه از هدف قرار دادن اسید نوکلئیک استفاده میشود.
در سیستم کاهشدهنده میرازول (Mirasol PRT)، ریبوفلاوین به فرآورده پلاسما یا پلاکت اضافه شده و با اشعهی U.V در طول موج ۴۰۰ – ۲۸۰ نورافشانی میشود.
در این تکنولوژی، آسیب انتخابی غیرقابل برگشت که به گوانین وارد میشود قابلیت تکثیر و ترمیم را از گلبولهای سفید و عوامل پاتوژن سلب میکنــــــــــــــــــــــــــــد. در سیستم میرازول (Pathogen Reduction Technology) ویروسهای با پوشش و بدون پوشش لیپیدی، میکروبها و پروتوزوا حتی در تراکمی نزدیک به دوران دریچهای غیرفعال میگردند. سلامتی و کیفیت این فرآوردهها با تزریق بیش از 220000 واحد پلاسما و پلاکت تا سال ۲۰۱۴ موفقیتآمیز بوده است.
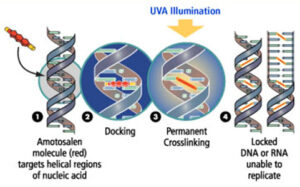
در تکنولوژی اینترسپت (PRT Intercept) از آموتوسالن (Amotosalen) استفاده میشود که با پیوند به اسید نوکلئیک در میان آنها جای گرفته و با پرتوافشانی ماوراء بنفش در طول موج ۴۰۰ -۳۲۰ نانومتر فعال شده و منجر به تشکیل پیوندهای کووالانس بین بازهای پیرامیدین میگردد که نتیجهی آن جلوگیری از تکثیر و نسخهبرداری است.
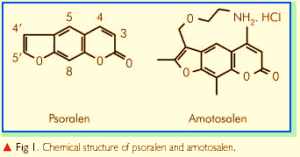
ساختار شیمیایی پسورالن و آموتوسالن
در این سیستم مادهی آموتوسالن و مشتقات تجزیهشدهی نوری آن توسط ماده جاذب از کیسه برداشت میشود. این سیستم توانایی غیرفعالسازی ۲ تا ۶ لگاریتم (۹۹/۹99۹-۹۹ درصد) از ویروسهای پوششدار و بدون پوشش و میکروبها را دارا میباشد.
سازوکار آموتوسالن در مسدودسازی اسید نوکلئیک در رونویسی و ترجمه
توانایی تکنولوژی کاهش دهنده پاتوژن (PRT)
| نوع پاتوژن | کارآمدی |
| ویروسها (با پوشش لیپیدی، بدون پوشش، داخل سلولی، خارج سلولی) |
2-6 لگاریتم 99-99/9999 درصد |
| انگلها (مالاریا، چاگاس، بابزیا، لیشمانیا) |
۶ ≤ تا ۳ ≤لگاریتم 99/9999< تا ≤ 99 درصد |
| میکروبهای گرام مثبت و منفی |
حدود 6-2 لگاریتم 99-99/9999 درصد |
تکنولوژی کاهش پاتوژنها در غیرفعالسازی گلبولهای سفید در دوزاژ بهکارگرفتهشده
| کارامدی | تکنولوژی میرازول (ریبوفلاوین) | تکنولوژی اینترسپت (آموتوسالن) |
| کاهش گلبولهای سفید | ۶ لگاریتم کاهش گلبولهای سفید زنده | 5/4-6 < لگاریتم کاهش گلبولهای سفید زنده |
| تغییرات مولکولی | یک حادثه تغییر گوانین به ازای هر ۳۵۰ جفت باز | قرارگرفتن یک مولکول آموتوسالن به ازای هر 89-83 جفت باز |
| بازدارندگی سنتز اينترلوکینها | ناتوانی گلبولهای سفید در سنتز اینترلوکینهای Iα و Iβ ، تمام سایتوکاینهای TH1/TH2 | ناتوانی گلبولها در سنتز اینترلوکینهای Iα و Iβ در طی ذخیره |
| واکنش گرافت | جلوگیری از واکنش گرافت در مدل موش | جلوگیری از واکنش گرافت در مدل موش |
نور ماوراء بنفش C:
پرتوافشانی کیسههای پلاسما با اشعهی ماوراء بنفش C بدون اضافه کردن مواد دیگر موجب غیرفعالسازی بسیاری از ویروسها میشود ولی در این پروسه ویروس HIV بهطور کامل غیرفعال نمیشود.
گفتنی است که شیوع عفونتهای میکروبی با جمعآوری خون در کیسههای حاوی مسیر انحرافی (diverting pouch) که در آن ۲۰ تا ۳۰ سیسی خون از شروع خونگیری وارد کیسهی انحرافی و سپس وارد کیسهی اصلی میشود، حدود ۵۰ درصد افت داشته است و این به علت جلوگیری از آلوده شده خون با فلورهای پوستی است.
گلبولهای قرمز و پلاکت فاقد هسته بوده و به ژنتیک هسته برای کارآیی نیاز ندارند و ازاینرو هدف قرار دادن اسید نوکلئیک برای کاهش پاتوژنها منطقی به نظر میرسد. کاهش پاتوژنها در سوسپانسیون پلاکتی در پلاسما یا در محلول نگهدارنده پلاکت (PAS) با بکارگیری ریبوفلاوین و آموتوسالن در مجاورت اشعه ماوراء بنفش موفقیتآمیز بوده و کاهش پاتوژنها با استفاده از U.V-C در دست مطالعه است. در پروسهی کاهش پاتوژن با ریبوفلاوین نیازی به برداشت ریبوفلاوین فعال نیست ولی آموتوسالن توسط ماده جاذب از فرآورده خارج میگردد. استفاده از روشهای کاهش پاتوژن موجب کاهش ۱۰ تا ۳۰ درصدی در پارامترCCI (Corrected Count Increment) میگردد که مقدار قابل در تزریق فرآورده پلاکت است. پارامتر CCI مؤثر بودن تزریق فرآورده پلاکت در یک ساعت و ۲۴ ساعت از تزریق را نشان میدهد. در این تکنولوژی با غیرفعالسازی گلبولهای سفید از واکنش گرافت و تحریک سنتز آنتیبادی علیه HLA جلوگیری میشود و امکان پدیده رفراکتوری یا بیپاسخی به تزریق پلاکت را نیز کاهش میدهد.
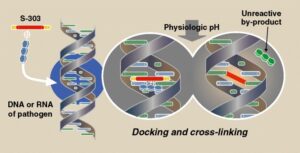
مطالعه تکنولوژی کاهش پاتوژنها در خون کامل و گلبولهای قرمز فشرده به علت جذب اشعه ماوراء بنفش توسط هموگلوبین دشوارتر است. بکارگیری ترکیبات سورالن و ترکیب S-303 که دربردارندهی قسمتهای لنگرگاه (anchor) و افکتور (effector) و پیونددهنده (linker) است تا حد زیادی در کاهش پاتوژنها موفقیتآمیز بوده است. قسمت لنگرگاه ترکیب اکریدین میباشد که در مارپیچ اسیدهای نوکلئیک بهطور قابلبرگشت جای میگیرد، درحالیکه قسمت افکتور مولکول بهطور غیرقابل برگشت ایجاد واکنشهای متقاطع بین بازهای گوانین میکند و ازاینرو مانع تکثیر و نسخهبرداری میشود. با هیدرولیز قسمت پیونددهنده، فرآورده تجزیهشده S-303 بهصورت غیرفعال رها میشود.
سازوکار S-300 در کاهش پاتوژنها از طریق تخریب DNA و RNA
بکارگیری S-303 و گلوتاتیون در غلظت mm 0/2، کاهش6/5 لگاریتمی HIV و کاهش ۷ لگاریتمی میکروب یرسینیا و 7/5 لگاریتمی استاف و 4/2 لگاریتمی سراشیا را نشان داده است.
ساخته شدن آلوآنتیبادی علیه آنتیژنهای جدید (Neoantigen) از مشکلات نسل اول تکنولوژی بوده است ولی در نسل دوم 303-S PRT بسیاری از مشکلات گشوده شده و کیسه خون استانداردهای لازم را برای تزریق کسب کرده است.
تکنولوژی کاهشدهندهی پاتوژنها با توجه به اینکه DNA و RNA را هدف قرار میدهد مورد مطالعه و ارزیابی گسترده از نظر سرطانزایی (Carcinogen)، ژنوتاکسیك (genotoxic) و سمی بودن برای تولیدمثل در سطح سلولهای زایا است. دستیابی به سلامت تکنولوژی نقش مهمی در اهدای خون سالم در مناطق اندمیک HIV و HBV و HCV و مناطقی که امکان دسترسی به کیتهای آزمایش یا تجهیزات آن نیست را دارا است. فرآورده خونی در این تکنولوژی معادل فرآورده اشعهدیده است.
درباره اهدای خون بیشتر بدانیم (قسمت دوم)
پلاسمای غنی از پلاکت (پیآرپی)
برای دانلود فایل pdf بر روی لینک زیر کلیک کنید
ورود / ثبت نام