ارتباط کمخونی فقر آهن با هموگلوبین گلیکوزیله (HbA1C)
نجمه فکری، کارشناس ارشد بیوشیمی، سوپروایزر و مسئول بخش بیوشیمی آزمایشگاه پاسارگاد، کرج، ایمیل pasargadzzma@yahoo.com.
حسین حاجی ابوالحسنی، دکترای علوم آزمایشگاهی، مؤسس و مسئول فنی آزمایشگاه پاسارگاد، کرج، ایمیل pasargadzzma@yahoo.com.
مرضیه حاجی ابوالحسنی، پزشک عمومی، کرج، ایمیل pasargadzzma@yahoo.com.
چکیده:
در این تحقیق ارتباط کمخونی فقر آهن با آزمایش هموگلوبین گلیکوزیله HbA1C بررسی شده است. نمونه آزمایش از افراد در سنین 30 سال و بالاتر در سه گروه آزمایش و سه گروه شاهد تهیه گردید. گروههای آزمایش شامل:
گروه 2 اشخاصی که میزان FBS بین mg/dl(90-70) و سطح HbA1C بین (5.5%-3.0%) و مبتلا به آنمی فقر آهن بودند،
گروه 4 اشخاصی که FBS (100-125) و سطح HBA1C بین (6.4%-5.6%) (پرهدیابتیها) و به آنمی فقر آهن نیز دچار شده بودند
و گروه 6 اشخاصی که میزان FBS بین (150–130) و سطح HbA1C بین (14.5%-%6.5) همراه با آنمی فقر آهن بودند.
گروههای شاهد (1 و 3 و 5) همانند گروههای آزمایش ولی بدون ابتلا به آنمی فقر آهن تعیین گردیدند.
نتایج با تست آماری t بررسی شد و مشخص گردید آنمی فقر آهــــن منجر به افزایـــــش HbA1C بین 20%-18% در افراد طبیعی، پرهدیابتی و دیابتی میگردد و این آزمایش در بیماران دارای کمخونی فقر آهن معیار خوبی برای ارزیابی وضعیت دیابت نیست و در صورت بهرهبرداری از نتایج HbA1C بهتر است کمخونی فقر آهن درمان شود و یا میزان HbA1C بین 18% تا 20% کسر و اصلاح گردد.
کلمات کلیدی: آنمی فقر آهن، هموگلوبین گلیکوزیله، ارتباط هموگلوبین گلیکوزیله با آنمی فقر آهن
مقدمه:
امروزه یکی از شایعترین بیماریها در بین جوامع مختلف دیابت است. دیابت زمانی به وجود میآید که هورمون انسولین عامل تنظیمکننده قند خون به اندازه کافی در بدن تولید نشود و یا بافتهای بدن به آن بهدرستی پاسخ ندهند که به موجب آن سوخت و ساز قند در بدن مختل شده و قند خون از حد طبیعی خود بالاتر میرود (1).
کمخونی فقر آهن IDA یکی از بزرگترین مشکلات سازمان بهداشت جهانی WHO در جهان سوم بوده و محاسبه شده است که حدود 30%-10% جمعیت جهان دچار کمبود آهن هستند. گاهی اختلالات جذبی ناشی از بیماریهای روده کوچک نیز موجب کاهش جذب آهن و نهایتاً فقر آهن میشوند. شایعترین آن بیماری سلیاک است. (4)
تجزیه و تحلیل هموگلوبین گلیکوزیله شده HbA1C در خون شواهدی در مورد میزان قند خون فرد در طی 3 تا 4 ماه گذشته که نیمهعمر پیشبینیشده گلبولهای قرمز RBC است را نشان میدهد. HbA1C اکنون به عنوان یک آزمایش استاندارد جهت بررسی و نظارت دیابت، بهویژه دیابت نوع 2 در نظر گرفته میشود. (3)
در حالت طبیعی قند جذبشده به سیستم گردش خون توسط انسولین وارد سلولهای بدن شده و به مصرف میرسد. قند اضافی باقی مانده در جریان خون با هموگلوبین موجود در گلبولهای قرمز به قسمت آمینی زنجیره گلوبین متصل شده و ایجاد هموگلوبین گلیکوزیله مینماید، این اتصال محکم بوده و تا زمان زنده ماندن گلبولهای قرمز باقی میماند. در بیماران مبتلا به دیابت نوع 1 چون انسولین ندارند و یا در بیماران دیابت نوع 2 به دلیل از دست رفتن کفایت انسولین، قند خون جهت مصرف وارد سلولها نمیشود و هموگلوبینها با میزان بیشتری از گلوکز در تماس بوده و در نتیجه هموگلوبین گلیکوزیله به میزان زیادتری تشکیل میگردد (1).
معیارهای تشخیص دیابت در سال 1985 توسط سازمان جهانی بهداشت WHO معرفی شده و در سال 1997 مورد تأیید WHO نیز قرار گرفت. بر پایه معیارهای جدید، تشخیص دیابت صرفاً بر اساس قند ناشتای پلاسمایی بیشتر یا مساوی 126 mg/dl صورت میگیرد. بررسیها نشان داده که زمینه ارثی در ایجاد دیابت نوع 2 خیلی مؤثر است. این بیماری یکی از پرهزینهترین بیماریها بوده که شیوع جهانی آن با سرعت زیادی رو به افزایش است. این نوع دیابت با مقاومت به انسولین و فقدان نسبی انسولین مشخص میشود و 90 تا 95 درصد موارد دیابت در جهان را به خود اختصاص میدهد. بر اساس تعریف WHO از دیابت، افرادی که قند بین 126-100 داشته باشند بهعنوان پیشدیابت یا پرهدیابت در نظر گرفته میشوند (1).
HbA1C که منعکسکننده غلظت گلوکز خون در طی 4–3 ماه است، یک معیار ارزشمند برای مقایسه گروههای درمانی در یک کارآزمایی تصادفی، برای ارزیابی روندهای گلیسمی در یک جمعیت در گذر زمان با مقایسه کنترل گلیمسی در جمعیتهای مختلف است و تنها معیار کنترل قند خون بوده که به شدت با عوارض عروقی دیابت مزمن مرتبط است. با این حال، بحث شده است که آیا برای یک بیمار، سطح HbA1C بهترین علامت برای خطر عوارض بوده یا اینکه سطح گلیسمی که HbA1C با آن مرتبط است، یک مارکر برابر یا بهتر برای بررسی خطر بروز عوارض خواهد بود (2).
این واقعیت بهخوبی شناخته شده است که HbA1C ممکن است در صورت وجود هموگلوبینوپاتی، کمخونی همولیتیک، سایر شرایطی که بر طول عمر گلبولهای قرمز خون تأثیر میگذارند و یا باعث اختلال در اتصال گلوکز به هموگلوبین میشوند، کنترل دقیق گلیسمی را نشان ندهد. با این حال، چیزی که مورد استقبال قرار نمیگیرد این است که حتی در مواقعی که چنین شرایط تشخیصی وجود نداشته باشد، HbA1C ممکن است به دلیل وجود دامنه وسیع میانگین غلظت گلوکز شکلهای گلوکز که میتوانند با یک HbA1C مرتبط باشند، نشانه خوبی از کنترل قند خون فرد نباشد. فرض بر این است که این عدم تعادل میانگین گلوکز و HbA1C به دلیل تغییرات بین افراد در طول عمر گلبولهای قرمز است (2).
مواد و روشها:
جامعه مورد بررسی شامل افراد 30 سال و بالاتر مراجعه نموده به مراکز بهداشت از مجموعه معاونت بهداشتی دانشگاه علوم پزشکی البرز بودند که طی 10 سال گذشته با این آزمایشگاه طرف قرارداد بودهاند. جامعه آماری با استفاده از نرمافزار SPSS-22 و فرمول کوکران به میزان جمعیت تقریبی کشور ایران N=80.000.000 با ضریب اطمینان 95% 0/05=d، تعداد 384 نمونه تعیین گردید. برای شروع تحقیق 6 گروه آماری به تعداد هر گروه 64 نمونه (64 نفر) مشخص شد.
گروه 1- مراجعین به آزمایشگاه، در سنین 30 سال و بالاتر که میزان FBS آنها بین 95-60 میلیگرم در دسیلیتر بوده، میزان HbA1C بین 5.5-3.0 درصد و دچار کمخونی فقر آهن نیستند و نیز سابقه مصرف داروهای کاهنده قند خون و ترکیبات آهن را ندارند. (گروه غیر دیابتیهای شاهد)
گروه 2- مراجعین به آزمایشگاه در سنین 30 سال و بالاتر که میزان FBS آنها بین 95-60 میلیگرم در دسی لیتر و نیز HbA1C بین 5.5-3.0 درصد بوده و دچار کمخونی فقر آهن هستند و نیز سابقه مصرف داروهای کاهنده قند خون و ترکیبات آهن را ندارند. (گروه غیر دیابتی دچار کمخونی فقر آهن)
گروه 3- مراجعین به آزمایشگاه، در سنین 30 سال و بالاتر که میزان FBS آنها بین 125-100 میلیگرم در دسیلیتر و میزان HbA1C بین 6.4-5.6 و دچار کمخونی فقر آهن نیستند و نیز سابقه مصرف دارهای کاهنده قند خون و ترکیبات آهن را ندارند. (گروه پرهدیابتیهای شاهد)
گروه 4- مراجعین به آزمایشگاه، در سنین 30 سال و بالاتر که میزان FBS آنها بین 125-100 میلیگرم در دسیلیتر و میزان HbA1C بین 6.4-5.6 بوده و دچار کمخونی فقر آهن هستند و نیز سابقه مصرف داروهای کاهنده قند خون و ترکیبات آهن را ندارند. (گروه پرهدیابتی با کمخونی فقر آهن)
گروه 5- مراجعین به آزمایشگاه، در سنین 30 سال و بالاتر که میزان FBS آنها بین 150-130 میلیگرم در دسیلیتر و میزان HbA1C بین 14.0-6.5 بوده و دچار کمخونی فقر آهن نیستند و نیز سابقه مصرف داروهای کاهنده قند خون و ترکیبات آهن را ندارند (گروه دیابتیهای شاهد).
گروه 6- مراجعین به آزمایشگاه در سنین 30 سال و بالاتر که میزان FBS آنها بین 150-130 میلیگرم در دسیلیتر و میزان HbA1C بین 14.0-6.5 بوده و دچار کمخونی فقر آهن هستند و نیز سابقه مصرف داروهای کاهنده قند خون و ترکیبات آهن را ندارند. (گروه دیابتی با کمخونی فقر آهن)
معیار انتخاب بیماران دچار کمخونی فقر آهن مشتمل بر نتایج آزمایش CBC، فریتین، آهن و TIBC به شرح ذیل است:
Hb مساوی یا کمتر از 12 در مردان و مساوی یا کمتر از 11 در زنان.
HCT مساوی یا کمتر از 36 در مردان و مساوی یا کمتر از 33 در زنان.
MCV مساوی یا کمتر از 79.
MCH مساوی یا کمتر از 26.
MCHC مساوی یا کمتر از 31 در مردان و زنان.
فریتین سرم مساوی یا کمتر از 49 در مردان و مساوی یا کمتر از 19 در زنان.
آهن سرم مساوی یا کمتر از 49 در مردان و مساوی یا کمتر از 24 در زنان.
TIBC بیشتر از 455 در مردان و زنان.
نتایج:
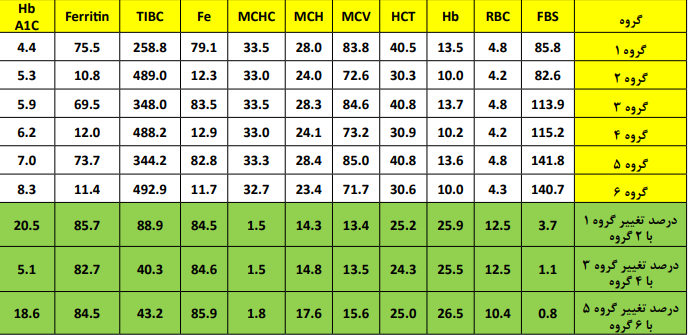
جدول 1- میانگین نتایج آزمایشهای گروههای شاهد و آزمایش
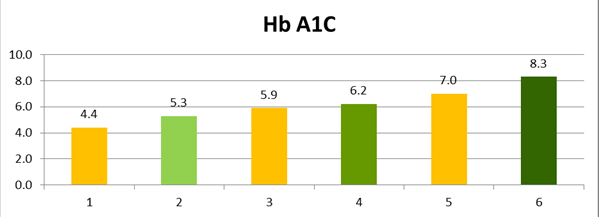
نمودار 1- میانگین نتایج HbA1C گروههای شاهد و آزمایش
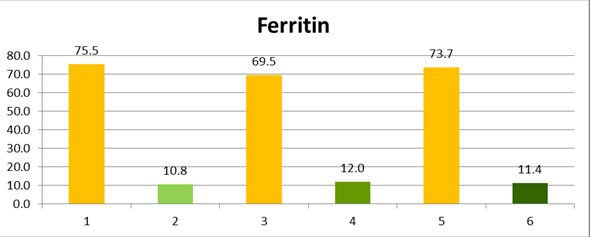
نمودار 2- میانگین نتایج Ferritin گروههای شاهد و آزمایش
بحث و نتیجهگیری کلی:
در مقایسه گروههای آزمایش با گروههای شاهد مشخص گردید که کمخونی فقر آهن باعث افزایش HbA1C بدون تطبیق سیر بیماری و میزان قند خون میشود. میزان افزایش در بیماران دیابتی بیش از 18% و برای بیماران با قند خون طبیعی بیش از 20% است؛ اما در بیماران پرهدیابتی این میزان 5% بود. در بررسی بیشتر مشاهده میشود به علت روش انتخاب نمونههای پرهدیابتی با 2 فاکتور FBS بین 125-100 و HbA1C بین 6.4%-5.6% که منجر به حذف مبتلایان به کمخونی فقر آهن پرهدیابتی با HbA1C بالاتر از محدوده پرهدیابتی شده است، پس میتوان برای بیماران پرهدیابتی مبتلا به کمخونی فقر آهن افزایش HbA1C را بین 18% تا 20% در نظر گرفت.
از آنجا که کمخونی فقر آهن باعث افزایش طول عمر گلبولهای قرمز میشود، در نتیجه مدت زمان بیشتری گلوکز در اختیار Hbهای موجود در جریان خون قرار میگیرد و همچنین میزان بیشتری از این Hbهای گلیکوزیله شده در مدت زمان زیادتری در جریان خون باقی میمانند که باعث افزایش HbA1C به میزان 18%-20% میگردد. پس به منظور ارزیابی گلیسمی در اشخاص، نخست باید ارزیابی آهن و عدم ابتلا به کمخونی فقر آهن بررسی شده و در صورت عدم ابتلا به کمخونی فقر آهن، ارزیابی گلیسمی را بر پایه میزان HbA1C انجام داد؛ و در صورت ابتلا قبل از درمان نتایج HbA1C جهت ارزیابی گلیسمی استفاده نشود و در موارد اضطرار اصلاح 20-18% میزان HbA1C انجام شود. برای ارزیابی ابتلا یا عدم ابتلا به کمخونی فقر آهن انجام آزمایش CBC، Fe و Ferritin ضروری است.
منابع:
1- طیبه محمدی، محمدحسن ابوالحسنی و همکاران، «شیوع دیابت نوع 2 عوامل خطرزای آن و لزوم برنامهریزی جهت پیشگیری از این بیماری در ایران»، ش ص: 14-9 مجله پزشک و آزمایشگاه خرداد 1392.
2- Ray W. Beck, et al, “The Fallacy of Average: How Using HBA1C Alone to ASSESS Glycemic Control Can Be Misleading” Diabetes Care PP: 994-999 Volume 40, August 2014.
3- Shariy I. Shermani, et al., “Significance of Hb AIC Test in Diagnosis and Prognosis of Diabetic Patients, “Biomarker insights, PP: 95-104 11:2016.
4- Smith- Thier, “Pathophysiology of Blood and Blood- Forming Organs” PP: 41-85.1995.
رابطۀ RDW با آنمی فقر آهن و كاهش بار اقتصادی منتج از آزمايشات غير ضروری
مروری بر تشخیص آزمایشگاهی HbA1c
HbA1c: مروری بر جنبههای آنالیتیکی و بالینی
`مروري بر تستهاي ارزيابي پروفايل آهن بدن
برای دانلود فایل pdf بر روی لینک زیر کلیک کنید
ورود / ثبت نام