معصومه رسولینسب1، امیرهوشنگ نژاده2
- دکتری تخصصی باکتریشناسی پزشکی از انستیتو پاستور ایران
- دکتری علوم آزمایشگاهی و عضو انجمن شیمی کلینیکال آمریکا
آزمایشگاه پاتوبیولوژی و ژنتیک آینده
بیماری سل یا توبرکلوزیس[1] (TB) یکی از مهمترین بیماریهای عفونی و بسیار مسری و یکی از مهمترین علل مرگومیر در سراسر جهان بهویژه در کشورهای درحالتوسعه و توسعهیافته به شمار میآید. همچنین سیزدهمین عامل مرگومیر و دومین عامل کشنده عفونی پس از کووید-19 (بالاتر از HIV و ایدز) است. اگرچه این بیماری بهطورمعمول ریهها را تحت تأثیر قرار میدهد (به آن سل ریوی میگویند)، اما میتواند به سایر قسمتهای بدن نیز گسترش یابد (بهعنوان سل خارج ریوی شناخته میشود).
عامل اتیولوژی این بیماری در انسان، مایکوباکتریوم توبرکلوزیس[2](M. tb) (یا باسیل کخ) یک باکتری داخل سلولی اختیاری است و اوليــن بار در سال 1882 توسط كخ بهعنوان عامـــل ایجادکننده سـل معرفـي شد. این باکتری بهصورت باسیل گرم مثبت، غیرمتحرک و بدون اسپور است که به دلیل داشتن مقدار زیادی چربی و اسید مایکولیک فراوان در دیواره سلولی به رنگهای باکتریولوژی نفوذناپذیر است و بهسادگی رنگ نمیگیرد و به رنگآمیزی گرم مقاوم است. برای رنگآمیزی این باکتری از رنگآمیزی زیل-نلسون[3] (رنگآمیزی اسید فاست) استفاده میشود و به همین دلیل به این باکتریها، اسید فاست[4] میگویند. مایکوباکتریوم توبرکلوزیس ازنظر فیزیولوژی، میکروبی هوازی است که برای رشد خود به مقدار زیادی اکسیژن نیاز دارد. مهمترین روشهای تشخیصی بالینی مایکوباکتریوم توبرکلوزیس شامل تست پوستی توبرکولین، رنگآمیزی زیل-نلسون و عکسبرداری اشعه ایکس از قفسه سینه است.
.M.tb میتواند سالها در بدن انسان خاموش بماند و بدون هیچ نشانهای از بیماری در بدن باقی بماند که در آن بسیاری از افراد به ناقل بدون علامت (سل غیرفعال) تبدیل میشوند. تظاهرات بالینی سل ریوی فعال ممکن است شامل درد قفسه سینه پلوریتیک، تب خفیف، سرفه مولد طولانیمدت، هموپتیزی، خستگی، از دست دادن اشتها، تعریق شبانه و کاهش وزن باشد.
سل یا توبرکلوزیس از دیرباز تاکنون بهعنوان یک معضل بهداشتی و بیماریهای عفونی در دنیا مطرح میباشد و تقریباً یکسوم از مردم دنیا به این باکتری آلوده میباشند. در سال 2021، حدود 10/6 میلیون نفر در سراسر جهان به بیماری سل (TB) مبتلا شدند. شش میلیون مرد، 3/4 میلیون زن و 1/2 میلیون کودک. آخرین گزارش WHO در سال 2022، مستند کرد که بیش از یکمیلیون نفر- حدود 1/6 میلیون نفر- در سال 2021 بر اثر سل جان باختند (تقریباً 1/4 میلیون و 0/2 میلیون مرگ در میان گروههای HIV منفی و HIV مثبت به ترتیب) که بالاترین میزان مرگومیر بین سالهای 2000 تا 2010 رخ داده است. درواقع تا زمان همهگیری کورناویروس در 2019 (COVID-19)، مرگومیر ناشی از سل از تعداد مرگومیر ناشی از هر عامل عفونی دیگر، ازجمله HIV/AIDS فراتر میرفت. سالانه 13 میلیارد دلار برای پیشگیری، تشخیص، درمان و مراقبت از سل موردنیاز است تا به هدف جهانی توافق شده در نشست عالی سازمان ملل در سال 2018 در مورد سل برسد.
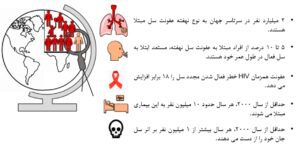
از نظر جغرافیایی در سال 2021، اکثر افرادی که به سل مبتلا شدهاند در منطقه جنوب شرق آسیا (45%) و پسازآن منطقه آفریقا (23%) و منطقه اقیانوس آرام غربی (18٪) قرار داشتند. چهار کشور بیش از نیمی از بار جهانی سل را به خود اختصاص دادهاند: دو کشور در آسیای جنوب شرقی، هند (28%) و اندونزی (9/2%)، علاوه بر این دو کشور در غرب اقیانوس آرام، چین (7/4%) و فیلیپین (7%). بر اساس گزارش 2022 سازمان بهداشت جهانی (WHO[5])، حدود یکچهارم جمعیت جهان (2 میلیارد) بهطور پنهان به M. tb مبتلا هستند (شکل 1). در افراد ناقل عفونت سل نهفته (LTBI[6])، احتمال فعال شدن مجدد سل 5 تا 10 درصد است. درواقع، مایکوباکتریهای خفته را میتوان بیدار کرد (سل فعال)، بهویژه در بیماران نقص ایمنی، مانند افرادی که همزمان با ویروس نقص ایمنی انسانی (HIV) آلوده هستند. در میان افراد مبتلا به HIV (تقریباً 38 میلیون)، خطر ابتلا به سل 18 برابر بیشتر از افراد بدون HIV برآورد شده است. با فعال شدن دوباره سل بار باکتری افزایش مییابد، بنابراین بیماری علامتدار میشود.
شکل 1. آمار کلی توبرکلوزیس
در کشور ایران، سل تقریباً در تمامی استانهای کشور و بیشتر در استانهای سیستان و بلوچستان، گلستان، خراسان رضوی، خوزستان، هرمزگان، قم، کرمانشاه و گیلان گزارش شده است. 35% سل دنیا در 22 کشور گزارش شده است که 2 کشور پاکستان و افغانستان جزء این کشورها هستند.
تشخیص زودهنگام و درمان موفقیتآمیز سل برای جلوگیری از گسترش بیشتر باکتری و جلوگیری از ایجاد سویههای مقاوم بسیار مهم است. روشهای تشخیصی متعددی معمولاً مورداستفاده قرار میگیرند، ازجمله روشهای ایمونولوژیک، رادیوگرافی، میکروسکوپی، کشت باکتریایی و روشهای بالینی. تستهای ایمونولوژیکی مانند QFT[7] و تست پوستی توبرکولین (تست مانتو[8]) عمدتاً برای غربالگری و رد عفونت سل استفاده میشود. بهطور مشابه، رادیوگرافی (اشعه ایکس قفسه سینه) یک ابزار غربالگری است که برای تشخیص سل ریوی فعال استفاده میشود. بااینحال، نمیتواند در تشخیص عفونت نهفته سل کمک کند. آنالیز میکروسکوپی اسمیر خلط یک ابزار بسیار کارآمد و پرکاربرد در تشخیص سل است که در آن باکتری سل با رنگ زیل نلسون رنگآمیزی میشود، اما حساسیت کم و عدم تمایز بین M. tb و سایر باسیلهای اسید فست از نکات مهم این امر است. برخلاف طیفسنجی اسمیر، کشت خلط یک روش تشخیصی سل بسیار خاص و حساس است که در آن از محیط لونشتاين جانسون[9] برای کشت باکتری سل استفاده میشود. از مواردی كه مشكلات و عوارض بيماري ناشي از سل را افزایش میدهد میتوان به روشهاي درمان نادرست، ايجاد باسيلهاي مقاوم به داروهاي موجود (مقاومت دارویی) و نقش پاندمي عفونت HIV بهعنوان عامل مهمي در گسترش سل اشاره کرد. به همين دليل بيماري سل در سال 1393 توسط سازمان بهداشت جهاني بهعنوان يك فوريت بهداشت جهاني اعلام شد.
داروهای مختلفی برای درمان سل در دسترس هستند. داورهای ضد سل شامل دو گروه خط اول و خط دوم درمان است. داروهای خط اول ایزونیازید[10] (INH)، ریفامپین[11] (RIF)، پيرازيناميد [12](PZA) و اتامبوتول[13] (EMB) میباشند که جز, داروهای اصلی درمان سل هستند. رژیم استاندارد درمانی شامل یک فاز اولیه فاز 2 ماهه ایزونیازید، ریفامپین، اتامبوتول و پيرازيناميد و فاز ادامه 4 ماهه با فقط ایزونیازید یا ریفامپین درمان شوند. مقاومت به این داروها مشکلی است که روزبهروز بزرگتر میشود. سل مقاوم به دارو بهصورت یک مشکل جهانی در مبارزه با بیماری سل است.
صنعتی شدن تولید و استفاده از آنتیبیوتیک توسط انسان در 100 سال گذشته منجر به افزایش جهانی در شیوع سویههای باکتریایی مقاوم به آنتیبیوتیک شده است. تجویز نادرست دارو، عدم استفاده از درمان چند دارویی و کاربرد رژیم تکدارویی و قطع مصرف دارو، نبود برنامههای کنترل بیماری سل، میتواند به کاهش اثر داروهای ضد سل کمک کند. افراد مبتلا به سل مقاوم، بهویژه در بیماران مبتلا به سویههای مقاوم به چند دارو، به داروهای خط دوم سل نیاز پیدا میکنند که در مقایسه با داروهای خط اول، برای مدت طولانیتری باید مصرف شوند و احتمال بروز عوارض در آنها بیشتر است. داروهای خط دوم شامل فلوروکینولونها، آمینوگلیکوزیدها، اتیونامید، سیکلوسرین[14] هستند. آفلوکساسین[15](OFX) و سیپروفلوکساسین[16] (CIP) دو داروی مهم فلوروکینولونی و مؤثر بر روی سویههای مایکوباکتریوم توبرکلوزیس هستند. رژیم درمانی خط دوم به علت اثربخشی کمتر و تحملناپذیری و توکسیسیته بیشتر، برای موارد مقاوم به داروهای خط اول تجویز میگردد.
طبق تعریف سازمان جهانی بهداشت، سل مقاوم به چند دارو[17] (MDR-TB) عبارت از مقاومت میکروب سل به ایزونیازید و ریفامپین (دو داروی رایج سل) است که تهدید عمده برنامه کنترل سل است. این داروها برای تمام افراد مبتلا به سل تجویز میشود. البته این میکروب ممکن است نسبت به داروهای دیگر ضدسلی نیز مقاوم باشد. عوامل تزریقی (آمیکاسین یا استرپتومایسین)، دلامانید، پیرازین آمید یا اتامبوتول را ترجیحاً میتوان انتخاب کرد. آزمایش حساسیت برای فلوروکینولونها باید قبل از شروع درمان MDR-TB انجام شود. پیدایش MDR امروزه بهعنوان یک مشکل جدی در برابر برنامه کنترل سل در اغلب کشورها و در سطح جهانی مطرح است و بیمار مبتلا به سل مقاوم به دارو بهجای 6 ماه باید 2 سال تمام تحت درمان باشد. مقاومت XDR نوع نادری از سل مقاوم به چند دارو بهصورت سل بسیار مقاوم به دارو یا سل با مقاومت گسترده[18] (XDR-TB) است با مقاومت به ایزونیازید، ریفامپین، یک فلوروکوئینولون و یک داروی تزریق خط دوم (آمیکاسین، کاپرومایسین و کانامایسین) یا ایزونیاید، ریفامپین، یک فلوروکوئینولون و بداکوئیلین[19] یا لیزنولاید همراه است. داروهای این دسته از بیماران تا زمانی که از دیدگاه پزشک معالج بهبودی کامل نیافته است قطع نمیشود و این بیماران بیشتر از دو سال باید داروهای خود را مصرف نمایند و عوارض دارویی شدیدی را متحمل میشوند. نوع دیگری از سل MDR بهصورت سل مقاوم به چند دارو[20] (PDR-TB) ناشی از ارگانیسمهایی است که به بیش از یک داروی خط اول ضد سل بهجز ایزونیازید و ریفامپین مقاومت نشان میدهند.
مرگومیر ناشی از سل مقاوم به چند دارو حدود 65-45% میباشد و این معادل مرگومیر ناشی از سل درمان نشده است. مقاومت ثانویه یا اکتسابی به پیدایش مقاومت به دنبال مصرف داروی ضد سل گفته میشود و اگر بیماری با مقاومت ثانویه افراد دیگر را آلوده سازد، افراد اخیر در صورت ابتلا به بیماری بهخودیخود و بدون اینکه سابقه قبلی درمان داشته باشند، گرفتار سل مقاوم میشوند که به آن مقاومت اولیه میگویند. از زمان اولین استفاده از داروهای ضد سل در اواخر دهه 1940، موارد عود سل با مقاومت اکتسابی بهطور مکرر برای همه داروهای مؤثر جدید مشاهده شده است. در کشورهایی با درآمد متوسط، با توجه به ناکافی بودن آزمایشگاه، بسیاری از بیماران مبتلا به سل تشخیص داده نشده و مقاوم به درمان میگردند. شیوع خاص منطقهای از مقاومت دارویی در بین ایزولههای بالینی سل وجود دارد.
در حال حاضر سل MDR از تمام کشورهای جهان و از سال 2005 سل XDR از برخی نقاط دنیا بهخصوص مناطقی که با بیماری ایدز درگیر هستند گزارش شده است و شیوع توبرکلوزیس در ایران در سال 2005، حدود 37% و مرگومیر ناشی از آن 3/3 در هر صد هزار نفر در سال بود. شیوع مقاومت اولیه به داروهای ضد سل (فرد قبلاً درمان نشده مبتلا به MDR-TB) در جهان، اداره منطقهای مدیترانه شرقی[21] (EMRO) و ایران به ترتیب 3/4، 4 و 1/3 درصد است. همچنین شیوع مقاومت ثانویه به داروهای ضد سل (تشکیل MDR-TB در طول درمان) در جهان، EMRO و ایران به ترتیب 18، 16 و 8/3 درصد است. شیوع سل مقاوم به دارو در مشهد و تهران به ترتیب 4 درصد و 6 درصد گزارش شده است. پراکندگی سل MDR در تمام نقاط ایران یکسان نیست. گزارش شده است که روند MDR-TB بهویژه در موارد درمان مجدد در دهه گذشته در ایران افزایش یافته است.
سل مقاوم به دارو اعم از MDR و XDR و حتی بروز سل مقاوم به تمام داروها[22] (TDR)، یک معضل بهداشتی در کشور میباشد. ایران، بهعنوان یکی از کشورهای شرق مدیترانه، دارای مرز مشترک با کشورهایی با فراوانی بالای TB -MDR (جمهوری آذربایجان، ارمنستان، افغانستان و پاکستان) در منطقه است. اهمیت سل در ایران به دلیل همسایگی آن با کشورهای آذربایجان و ارمنستان (با فراوانی بالایی با سل مقاوم به دارو هستند) و عراق و كشورهاي غربی ايران (با شيوع بالاي سل) بسیار بالاست. در کشورهایی با درآمد متوسط، با توجه به ناکافی بودن آزمایشگاه، بسیاری از بیماران مبتلا به سل تشخیص داده نشده و مقاوم به درمان میگردند. درمان در این موارد عمدتاً شکستخورده و هزینه قابلتوجهی از منابع مراقبتهای بهداشتی موردنیاز است. سل مقاوم به چند دارو همچنان یک بحران بهداشت عمومی و یک تهدید امنیت بهداشتی است. در سال 2021 تنها حدود 1 نفر از هر 3 نفر مبتلا به سل مقاوم به دارو به درمان دسترسی داشتند. ظهور و گسترش سویههای مقاوم به دارو یک تهدید جدی برای برنامههای کنترل سل است؛ بنابراین برای تشخیص سویههای مقاوم به چند دارو و جلوگیری از گسترش سویههای TB -MDR، آزمایش مقاومت دارویی[23] (DRT) بهمنظور تجویز داروی مناسب در بیماران مبتلا به سل ضروری است. آزمایش مقاومت دارویی تنها در 58% موارد سل قبلاً درمان شده (یا 12% موارد درمان نشده) و بیشتر در کشورهای با درآمد بالا با کمترین میزان مقاومت انجام میشود، چراکه معیارهای مقاومت دارویی در سل در بیماران با شکست درمانی (مقاومت بالینی) تحت عنوان سویههای سل مقاوم تعریف شده بود. آزمایش مقاومت دارویی برای مایکوباکتریوم توبرکلوزیس دارای دو هدف است: (1) مدیریت فردی (درمان و پیشگیری) موارد سل و (2) نظارت بر مقاومت دارویی ضد سل.
تخمین زده میشود که بین سالهای 2000 تا 2021، جان 74 میلیون نفر از طریق تشخیص و درمان سل نجات یافته است. غربالگری اکتیو، تشخیص بهموقع، آزمایش مقاومت دارویی، رژیمهای دارویی زودهنگام، سریع و مؤثر با رعایت مصرف دارو و طول مدت درمان کافی از مهمترین راهکارهای پیشگیری از انتقال و کنترل MDR و XDR هستند؛ بنابراین در مناطق آندمیک سل از جمله در ایران، ارزیابیهای تشخیصی سل در تمامی بیمارانی که تب طولانیمدت همراه با علائم ریوی یا خارج ریوی دارند، توصیه میشود؛ بنابراین آزمایش مقاومت دارویی، تشخیص و جداسازی توبرکلوزیس مقاوم به درمان برای بهبود سلامت، کاهش موارد مرگومیر و کاهش سرعت گسترش توبرکلوزیس مقاوم به درمان دارویی تا زمانی که خطر انتقال از بین برود بسیار حائز اهمیت است. پایان دادن به اپیدمی سل تا سال 2030 ازجمله اهداف بهداشتی اهداف توسعه پایدار سازمان ملل متحد[24] (SDGs) است.
References:
- World Health Organization; https://www.who.int/teams/global-tuberculosis-programme/tb-reports.
- Habibnia, M. Karami-Zarandi, S. Zaker, Z. Ghalavand, F. Doustdar, G. Eslami, H. Kazemian. Molecular Characterization of Resistance to Second-Line Anti-Mycobacterial Drugs among Clinical Isolates of Multidrug-Resistant Mycobacterium tuberculosis. Clin Lab. 2023 Jan 1; 69(1).
- S R Alsayed1, H. Gunosewoyo. Tuberculosis: Pathogenesis, Current Treatment Regimens and New Drug Targets. Int J Mol Sci. 2023 Mar 8; 24(6):5202.
- Ebrahimzadeh, S. Pagheh, T. Mousavi, M. Fathi, and S. Gh. Mortazavi Moghaddam. Serosal membrane tuberculosis in Iran: A comprehensive review of evidences. J Clin Tuberc Other Mycobact Dis.2023 May; 31: 100354.
- B Hall, L. Lima, L. J M Coin, Z. Iqbal. Drug resistance prediction for Mycobacterium tuberculosiswith reference graphs. Microb Genom, 2023 Aug; 9(8):mgen001081.
- Lallungawi Khawbung, D. Nath, S. Chakraborty. Drug resistant Tuberculosis: A review. Comp Immunol Microbiol Infect Dis. 2021 Feb: 74:101574.
[1] Tuberculosis
[2] Mycobacterium tuberculosis
[3] Ziehl–Neelsen
[4] Acid Fast
[5] World Health Organisation
[6] latent TB infections
[7] QuantiFERON-TB Gold
[8] Mantoux
[9] Löwenstein-Jensen
[10] Isoniazid
[11] Rifampin or Rifampicin
[12] Pyrazinamide
[13] Ethambutol
[14] Cycloserine
[15] Ofloxacin
[16] Ciprofloxacin
[17] Multidrug-resistant TB
[18] Extensively drug-resistant TB
[19] Bedaquiline
[20] Polydrug-resistant TB
[21] Eastern Mediterranean Regional Office
[22] Total Drug Resistant
[23] Drug-resistance testing
[24] Sustainable Development Goals