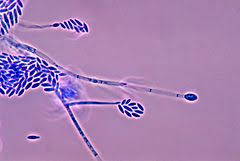
مایکوتوکسینهای شایع قارچ فوزاریوم
مژگان سبزعلیزاده1، عاطفه شجاعیان1، الهام بغدادی1، صادق خداویسی2
1 کارشناسی ارشد میکروبیولوژی، دانشگاه آزاد اسلامی واحد ورامین- پیشوا
2 دانشجوی دکتری تخصصی قارچ شناسی پزشکی، دانشگاه علوم پزشکی تهران
قارچ فوزاریوم نوعی قارچ رشتهای از شاخه آسکومیستها است و از جمله قارچهای ساپروفیت است که موجب فساد مواد غذایی میشود. به عنوان یکی از مهمترین قارچهای خاکزی و همهجازی بوده و در همه مناطق اقلیمی دنیا از جمله در کویر و اقیانوسها یافت میشود. این قارچ بیشتر بر روی برنج، لوبیا و سویا رشد میکند. فوزاريوم يكي از شايعترين قــارچهايی است که ميتواند سبب واكنشهاي آلرژيك تنفسي در انسان شود. مهمترین گونههای بیماریزا در انسان گونههای فوزاریوم سولانی، فوزاریوم اکسیسپوریوم و فوزاریوم ورتیسیلوئیدس میباشد. گونههای سولانی، اکسیسپوریوم و مونیلیفرم قادرند کراتیت، مایستوما و اونیکومایکوزیس ایجاد کنند. برخی گونهها مثل فوزاریوم گرامینهآروم با تولید و ترشح توکسین موجب مسمومیت غذایی میشوند. مایکوتوکسینهای تولید شده به وسیله این قارچها بدون تردید یک تهدید برای سلامت انسان و حیوانات محسوب میشوند.
توکسینهای قارچ فوزاریوم
Fomonisin: به طور کلی این توکسینها مهار کنندههای بالقوه سنتز سرامید وابسته به استیل COA در پستانداران هستند و در متابولیسم اسفنگولیپیدها مداخله میکنند. ابتداییترین تغییر بافتی که در اثر مصرف فومونیسین در ناحیه کبد یا کلیه اتفاق میافتد عبارت است از افزایش آپوپتوز و به دنبال آن تکثیر سلولهای زاینده. اگرچه مسمومیت حاد در مورد فومونیسین کمتر است اما این توکسین عامل دو بیماری است که در حیوانات خانگی با وقوع زودهنگام رخ میدهد:
1) سندرم لوکوآنسفالومالاشیا
2) سندرم ادم ششها
که هر دوی این بیماریها متابولیسم اسفنگولیپید و اختلال در عملکرد قلب و عروق را باعث میشوند. Fomonisin B1 (FB1) یکی از معمولترین اعضای خانواده فومونیسینها میباشد که توسط فوزاریوم ورتیسیلوئیدس تولید میشود. این کپک عمدتاً روی ذرت، گندم و غلات دیگر رشد میکند. FB1 از طریق مصرف غذا به میزان کم جذب میشود، پس از جذب، مقداری از فومونیسین در کبد و کلیه باقی میماند و اغلب به سرعت به شکل اصلی خود دفع میشود. تجمع اسفنگانین و اسفنگوزین دلیل اولیه سمیت FB1 است. به نظر میرسد افزایش آپوپتوز نقش مهمی در ایجاد اثرات سمی شامل القای تومور داشته باشد. اگرچه قابل ذکر است که کاهش غلظت سرامید و افزایش غلظت اسفنگوزین 1- فسفات موجب مهار آپوپتوز و پیشبرد میتوز و بازسازی سلولها میشود. FB1 با اسفنگانین (یا اسفنگوزین) و آسیل COA در سرامید سنتاز واکنش الکترواستاتیک میدهد. بخشی از FB1 که شباهت ساختاری با بازهای اسفنگوئید دارد با محل اتصال اسفنگانین واکنش میدهد در حالی که گروه تریآسیل اسید با بار منفی با محل اتصال آسیل COA واکنش میدهد. چون EB1 نیز فضای آسیلCOA را اشغال میکند پس آسیله نمیشود زیرا برای آسیله شدن نیاز به آسیل COA میباشد. EB1 فقط مانع سرامید سنتاز میشود. زمانی که گروه کربوکسیلیک اسید توسط فرایند هیدرولاز از FB1 جدا میشود محصول حاصل AP (آمینوپنتول) نه تنها به عنوان یک مهار کننده بلکه به عنوان یک سوبسترا برای سرامید سنتاز عمل میکند. AP توسط سرامید سنتاز آسیله میشود و N-Palmitol-AP1 تشکیل میشود که این مولکول مهار کننده قوی سرامید سنتاز بوده و بنابراین در ایجاد سمیت فومونیسینها نقش دارد. بیشترین اثرات سمی ناشی از نغییر متابولیسم اسفنگولیپید توسط مهار سرامید میباشد. تولید گونههای واکنشی فعال (ROS) نیز میتواند اتفاق بیفتد که باعث افزایش تنش اکسیداتیو و القای پراکسیداسیون لیپید میشود که میتواند سلولها را تخریب کند. اثر دیگر تماس با FB1 وقوع آپوپتوز است که در بافتها و سلولهای مختلفی گزارش شده است. مهار سرامید سنتاز مسئول این اثر نمیباشد بلکه مهمترین فاکتورها عبارتند از فراگمانتاسیون DNA و فعالسازی کاسپاز3، همچنین FB1 دارای اثرات ایمونوتوکسیک است. اثر سمی که این توکسین در انسان دارد نقص در لوله عصبی (NTD) است که کمبود آهن یک فاکتور اصلی برای وقوع NTD محسوب میشود. FB1 متابولیسم اسفنگولیپید را مختل کرده و این امر بر جذب آهن اثر گذاشته و موجب NTD میشود. گمان میرود که بین وقوع سرطان مری و فومونیسین ارتباطی وجود داشته باشد. وضعیت اقتصادی نامناسب و بدنبال آن داشتن رژیم غذایی یکنواخت که عمدتاً شامل گندم و ذرت میباشد مرتبط با بروز سرطان مری است. در حیوانات، فومونیسین به طور ضعیف جذب، به سرعت حذف شده و متابولیزه نمیشود. در rat و خوک توزیع FB1 بسیار بوده اما تنها مقدار کمی در کبد و کلیه تجمع مییابد و در میمونها FB1 به میزان جزئی در روده هیدرولیز میگردد.
مهار سرامید سنتاز توسط FB1 برگشت پذیر است زیرا اتصال توسط پیوندهای غیرکووالان ایجاد میشود. فاکتورهایی که این برگشت پذیری را القا میکنند عبارتند از کاهش غلظت FB1 سلولی و افزایش غلظت سلولی سوبستراهای سرامید سنتاز. فعالیت زیستی FB1 را میتوان با تیمار ذرت آلوده به فومونیسین با گلوکوماناز استخراج شده از دیواره سلولی مخمر ساکارومایسزسرویزیه کاهش داد، این پلیساکاریدها قادرند به مایکوتوکسینهای خاصی متصل شوند. کلروفورین مؤثرترین ترکیب در کاهش تولید توکسین است که همراه با کافئیک اسید، فرولیک اسید، واینلیک اسید میزان EB1 را 91-90% کاهش میدهد. ژنهای تنظیمی مسیر بیوسنتز فومونیزین به صورت خوشه ژنی در ژنوم قرار دارند که شامل 16 ژن غیر تنظیمی است. دو ژن غیر مرتبط ZFR1 و FCC1 که خارج از خوشه واقع شدهاند در تولید فومونیزین نقش دارند. اخیراً ژن جدیدی بنام Fum21 کشف شده که مجاور ژن پلیکتاید سنتاز شناسایی شده است. جهش در این ژن باعث کاهش 70% تولید توکسین شده است.
Trichothecene: گونههای فوزاریوم، تریکوتسینهای غیر مایکروسایکلیک تولید میکنند که عبارتند از: DON، DOS، 3-Ace-Don، Verrucarol-T2 Tetraol و توکسین T2. در مورد انسان و حیوان تریکوتسین نوع A مورد توجه است زیرا بیشتر از توکسینهای غذایی دیگر سمی میباشد. تریکوتسینها با اتصال به ریبوزومها و مهار پپتیدیل ترانسفراز باعث جلوگیری از سنتز پروتئین میشوند. تریکوتسینها مهار کننده ایمنی هستند و موجب انواعی از علائم بالینی نورولوزیکی، پوستی، معدهای و رودهای میشوند. تریکوتسین با اتوکلاو مهار نمیشود و برای غیر فعال شدن نیاز به حرارت 900F دارد. همچنین محلول 3% تا 5% سدیم هیپوکلریت نیز یک ماده غیر فعال کننده مؤثر برای آن است. تریکوتسین از سه مسیر متابولیکی کنژوگه شدن، دآپوکسیداسیون و داستیلاسیون عمل میکند که دآپوکسیداسیون برای سمزدایی مهم است که سمزدایی با استفاده از میکروارگانیسمهای موجود در مجرای معدی رودهای انجام میشود. حیواناتی که این باکتری را در سیستم گوارشی خود ندارند به تریکوتسین حساسترند. این میکروارگانیسمها تریکوتسین را به متابولیتهای کم خطرتر تبدیل میکنند. مکانیسم عمل تریکوتسین با مهار مراحل ابتدایی سنتز پروتئین و مهار مرحله طویل سازی و خاتمه میباشد. Deoxynivalenol وارد سلول میشود و به ریبوزومهای فعال متصل و باعث ارسال سیگنال به یک پروتئین کیناز فعال شده با RNA و نیز یک کیناز سلولی هماتوپوئیتیک میشود. سپس فسفریلاسیون پروتئین کیناز فعال شده با میتوزن باعث به را افتادن آپوپتوز و اثرات ایمونوتاکسیک و مزمن میشود. این گروه از مایکوتوکسینها از لحاظ ساختاری اثر شدیدی روی سلامت انسان و حیوان میگذارند. تریکوتسینها مهار کنندههای قوی سنتز پروتئین هستند؛ آنها از طریق واکنش با اجزای ریبوزوم این عمل را انجام میدهند. سنتز پروتئین یک عملکرد اصلی در تمام بافتها میباشد، بافتهایی که سلولهای آنها به طور دائم در حال رشد و تقسیم و فعالیت سریع هستند نسبت به توکسینها بسیار حساس هستند. در مقایسه با برخی از مایکوتوکسینهای دیگر تریکوتسین ظاهرا نیازی به فعالسازی متابولیک برای اعمال فعالیت بیولوژیکی خود ندارد. پس از تماس مستقیم پوستی یا مصرف خوراکی، تریکوتسین به سرعت روی پوست و موکوز روده اثر میگذارد. تماس پوستی باعث نکروز جلدی و التهاب، مصرف خوراکی باعث آسیب به مجرای معدی رودی فوقانی و تماس چشمی باعث آسیب قرنیه میشود. از آنجائی که این مایکوتوکسین خاصیت جلوگیری از تقسیم سلولها در اثر مهار سنتز پروتئین و RNA را دارد، از آن در شیمی درمانی استفاده میشود. مولکولهای تریکوتسین به مولکولهای تریکوتسین با سمیت کمتر قابل تبدیل هستند. این مولکولها مشتقات مولکول تریکوتسین اصلی هستند اما حلقه اپوکسی را ندارند در نتیجه سمیت این مولکول ثانویه کمتر است. برخی از میکروارگانیسمها مانند میکروارگانیسمهای فلور دستگاه گوارش خوک قادرند داکسینیوالنول را در محیط آزمایشگاهی متابولیزه کنند، بنابراین باکتریهای دستگاه گوارش قادرند سمیت تریکوتسین را با داستیلاسیون ساختار تریکوتسین کاهش دهند. با جداسازی ژنهای دخیل در مسیر بیوسنتز تریکوتسین، در مسیر Tri-5 ژن تولید کننده اولین آنزیم یعنی تریکودین سنتاز، 10 ژن بیوسنتز حاوی 2 ژن تنظیمی، 7 ژن مسیر بیوسنتز و 1 ژن ترانسپورتر کشف شدند.
Zearalenone: نوع دیگری از توکسین است که مهار کننده تولیدمثل در انسان و حیوان است. مشخص شده است که زرالینون و الکل آن دارای فعالیت آنابولیکی یا تسریع رشد هستند و به صورت تجاری به عنوان یک عامل آنابولیک در گوسفند و گاو برای درمان علائم سندرم اختلال قاعدگی و نیز به عنوان یک داروی خوراکی برای جلوگیری از بارداری استفاده میشود که اثرات آنابولیکی آن بسته به نوع کاربرد و مقدار آن میتواند برای ارگانیسم میزبان مفید یا مضر باشد و با وجود اینکه کاربرد زرالینون به عنوان عامل تسریع کننده رشد در برخی کشورها ممنوع گردیده اما در برخی کشورها مجاز میباشد. این مسئله میتواند موجب بروز مشکلاتی در تجارت بینالمللی گردد زیرا در گوشت حیواناتی که با رژیمهای غذایی حاوی زرالینون تغذیه شدهاند این ترکیب حضور دارد. این توکسین ساختاری شبیه استروژن دارد و میتواند پاسخ استروژنی را در حیوان ایجاد کند. علائم دیگر ZEA التهاب واژن، ترشحات واژنی و عملکرد ضعیف تولیدمثلی است.
مایکوتوکسینهای آسپرژیلوس پارازیتیکوس
برای دانلود پی دی اف بر روی لینک زیر کلیک کنید
ورود / ثبت نام