مقاله مروری
تأثیر قند خون بالا در پیر شدن پوست
امیرحسین احمدیه یزدی1*
1- دانشجوی کارشناسی ارشد بیوتکنولوژی پزشکی، دانشگاه علوم پزشکی همدان، همدان، ایران
چکیده
گلیکاسیون، واکنش غیرآنزیمی قندهای احیاکننده با پروتئینها، لیپیدها یا اسیدهای نوکلئیک است. این فرآیند بهطور طبیعی در بدن انسان انجام میشود ولی استرس اکسیداتیو و قرارگیری در معرض گونههای فعال اکسیژن، نهایتاً منجر به تشکیل محصولات نهایی گلیکاسیون پیشرفته (AGEها) میشود که ترکیباتی مضر هستند و تجمع آنها در بافتهای مختلف میتواند منجر به آسیب شود. این تجمعات در بیماریهایی مثل دیابت، آلزایمر و بیماریهای قلبی مشاهده میشود، همچنین اخیراً نتایجی در خصوص تأثیر آنها در فرآیند پیری به دست آمده است. در پوست، پروتئینهایی نظیر الاستین و کلاژن میتوانند دچار گلیکاسیون شوند که در نتیجهی آن، انعطافپذیری پوست کاهش یافته و آثار پیری زودرس در پوست مشاهده خواهد شد. با توجه به اثر مخرب تجمع AGEها در بدن، طی سالهای اخیر، تأثیر ترکیبات مختلف برای از بین بردن AGEها و جلوگیری از تولید آنها بررسی شده است که در این مطالعه به تعدادی از این موارد اشاره میکنیم. مقالهی حاضر یک مقالهی مروری است که به بررسی ارتباط گلیکاسیون و پیری پوست میپردازد.
کلیدواژهها: گلیکاسیون، AGE، کلاژن، دیابت، پوست
مقدمه
گلیکاسیون
گلیکاسیون واکنش غیرآنزیمی قندها با پروتئینها است که واکنشی برگشتناپذیر است. این واکنش نباید با گلیکوزیلاسیون که یک واکنش آنزیمیِ اتصال قند به پروتئین است، اشتباه گرفته شود. گلیکاسیون بهصورت عادی و بدون صرف ATP در بدن اتفاق میافتد و به غلظت قند موجود در بدن بستگی دارد (1). اتصال غیرآنزیمی گلوکز به پروتئینها، باعث تغییر شکل آنها میشود و پروتئین را از شکل عملکردی آن خارج میکند. خشکی و عدم انعطاف پوست در پیری حاصل گلیکوزیله شدن غیرآنزیمی پروتئینهای پوست ازجمله کلاژن و الاستین است (2). DNA نیز در اثر افزایش قند در محیط گلایکه میشود. کربوکسی اتیل گوانوزین، اصلیترین محصول این واکنش است. در آزمایشهایی که اخیراً انجام شده، مشخص گردیده است کهAGE ها میتوانند منجر به جهش در DNA، شکست DNA و فعال شدن ترنسپوزونها شوند (3).
گلیکاسیون خارج سلولی و تشکیل AGEها وقتی اتفاق میافتد که قندها با پروتئینها یا چربیها طبخ شوند و به همراه هم در معرض گرما قرار بگیرند. دمای بالای 120 درجه سلسیوس بهشدت این واکنش را تسریع میکند. حدود ده درصد ازAGE ها در بدن جذب میشوند. واکنش قهوهای شدن یا واکنش میلارد، یکی از شواهد گلیکاسیون است که در حضور گرما انجام میگیرد (4). در برخی مواد غذایی، برای بهبود رنگ و طعم غذا، روشهایی مورد استفاده قرار میگیرد که میتواند منجر به ایجاد مقادیر بالایی از AGEها در آن مادهی غذایی شود. مواد غذایی همچون دوناتها، کیکها، نوشابه و گوشت گریلشده به مقدار زیادی حاوی این ترکیبات مضر هستند. گلیکاسیون همچنین ممکن است منجر به تولید آکریل آمید شود که یک کارسینوژن بالقوه است (5).
محصولات نهایی گلیکاسیون پیشرفته (AGEها)
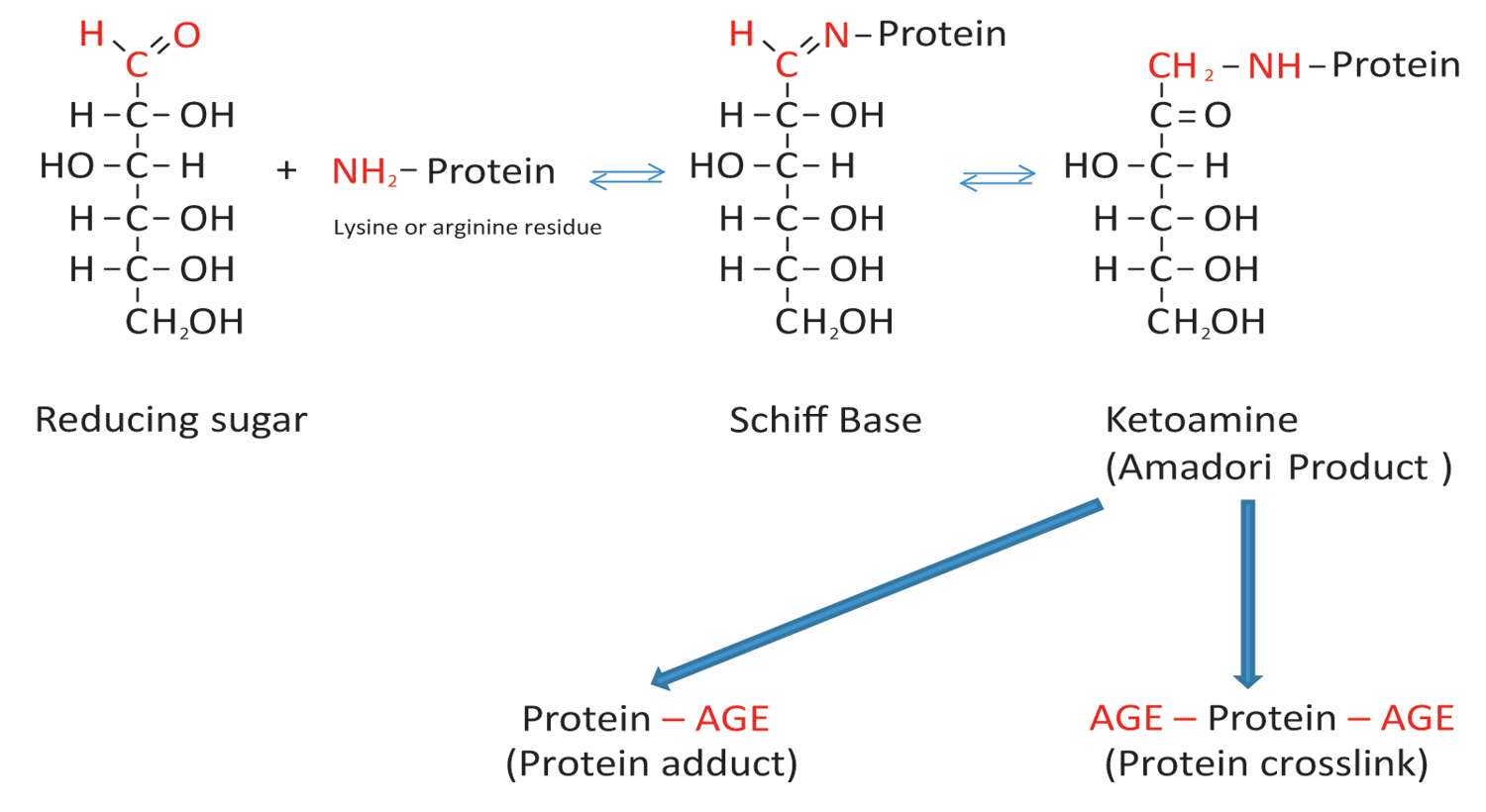
تشکیل AGEها، یک فرآیند پیچیدهی مولکولی است که چندین مرحلهی شیمیایی را دربر میگیرد. در طی واکنش میلارد، گروه کربونیل الکتروفیل گلوکز و یا سایر قندهای واکنشگر، با گروه آمین آزاد آمینواسیدها واکنش میدهد (بهخصوص ریشهی لایزین و آرژنین) و نهایتاً منجر به تشکیل یک ترکیب ناپایدار بنام باز شيف میشود. در ادامه باز شيف به ترکيبات فروکتوزآمين (کتوآمين) پايدار تبديل و با نوآرايي به محصولات آمادوري تبديل ميگردد. اکسيداسيون و نوآراييهاي مولکولي بيشتر موجب تبديل اين محصولات که محصولات ابتدايي گليکاسيون هستند، به AGE ها خواهد شد (6). چون فرآيند گليکاسيون اغلب با اکسيداسيون همراه است، آن را گليکواکسيداسيون نيز مينامند. AGEها محصولات مضری هستند که میتوانند با تجمع در بدن اثرات سوء خود را اعمال کنند. آنزیمها و آنتیاکسیدانها، بهطور طبیعی میتوانند تا حدی اثرات آنها را خنثی کنند. تجمع AGEها در بافتهایی مثل پوست، کلیه و قلب نارساییهای حادی را ایجاد میکند و همچنین میتواند موجب پیری زودرس شود. افرادی که قند خون بالایی دارند، مثل افراد مبتلا به دیابت، بیشتر در معرض خطر هستند (7).
رژیم غذایی بزرگترین منبع AGEها است و مصرف مواد غذایی که در معرض حرارت زیادی قرار گرفتهاند، 10 تا 100 برابر سطح AGEها را در بدن افزایش خواهد داد. در مطالعهای که در سال 2003 بین 559 زن بالای 65 سال آمریکایی، با میزان AGE بالا در خون انجام شد، نتایج نشان داد که این افراد دو برابر بیشتر از سایرین در معرض بیماریهای کبدی، قلبی و آلزایمر قرار میگیرند (8).
استرس اکسیداتیو منجر به تحریک فرآیند گلیکاسیون و اکسیداسیون پروتئین میشود و یکی از عوامل اصلی تخریب سلول طی پیری است. AGEها در واقع میانجیهایی بین استرس اکسیداتیو و مشکلات ناشی از دیابت هستند (7). اثر مخرب گلیکاسیون از آنجا آغاز میشود که تغییراتی در ساختار پروتئینها صورت بگیرد و در فرآیندهای تخریب، جابجایی، تجمع و برقراری پیوند در آنها مشکل ایجاد کند. AGEها همچنین cross-linking را در پروتئینهایی با طول عمر بالا، مثل کلاژن تحریک میکنند و میتوانند باعث عوض شدن شکل بافتها و از بین رفتن ماتریکس خارج سلولی و پیری پوست شوند. آنها از طریق تغییر ساختار رگها، اتصال به گیرندههای خود در بدن و فعالسازی یکسری مسیرهای سیگنالینگ، منجر به ایجاد سایتوکاینهای خاصی شده و فرآیند التهاب را تحریک میکنند (9). مرگ برنامهریزیشدهی سلول، تخریب ساختارهای درون سلولی و در پی آن، تحلیل عضلانی را هم میتوان از جمـله تأثیرات مخـرب AGEها برشمرد. در واقع همهی ساختارها و سلولهای بدن انسان میتوانند تحت تأثیر این ترکیبات قرار بگیرند و AGE ها را میتوان یکی از اصلیترین عوامل پیری و بیماریهای مرتبط با آن مثل بیماریهای قلبی بهحساب آورد (7). AGEها، همچنین با اتصال به برخی از سلولها مثل سلولهای اندوتلیال، ماکروفاژها و سلولهای مزانشیمی، ترشح بعضی سایتوکاینها را القا میکنند که میتواند منجر به تشدید استرس اکسیداتیو شود (8).
برخی ترکیبات میتوانند تولید AGEها را تحریک و آنها را فعال کنند؛ بهعنوان مثال میتوان به پتاسیم سربات اشاره نمود. پتاسیم سربات یک اسید چرب غیراشباع است که بهصورت طبیعی در متابولیسم چربیها در بدن انسان شرکت میکند و به CO2 و آب اکسید میشود. به همین دلیل استفاده از این ماده در محصولات غذایی و بهداشتی بلامانع اعلام شده است. با این وجود، استنشاق این ماده و یا تزریق زیرجلدی آن عوارضی نظیر اسپاسم برونشها و مشکلات تنفسی، درد در قفسهی سینه، ادم ریوی و مشکلات دیگری را به دنبال دارد. در سال 2013، موسوی موحدی و همکاران، تأثیر این ماده را در گلیکاسیون سرم آلبومین انسانی در حضور و عدم حضور گلوکز بررسی کردند که نتایج از تأثیر این ماده در ایجاد AGEها حکایت داشت (10).
شکل 1: تصویر شماتیک واکنش میلارد و تشکیل محصولات نهایی گلیکاسیون پیشرفته
نقش AGEها در پیری پوست
پیری فرآیندی است که به از دست دادن کارایی فرایندهای بیوشیمیایی و فیزیکی در بدن اطلاق میشود و تا مرگ انسان ادامه خواهد داشت. در واقع پیری فرآیند پیچیدهای است که فاکتورهای درونی و محیطی بسیاری میتوانند در آن تأثیرگذار باشند (2). فرضیههای زیادی برای توجیه و چگونگی پروسهی پیری مطرح شده است؛ از جمله کوتاه شدن طول تلومر، تجمع جهشهای میتوکندریایی و غیره که هیچکدام نمیتوانند دلیل جامع و متقاعدکنندهای برای این فرآیند باشند. یکی از فرضیههایی که در سالهای اخیر مطرح شده است، دلیل پیری را تجمع ترکیبات سمی و مضر بیولوژیکی در بدن میداند (11).
پوست بزرگترین اندام بدن و همچنین پیونددهندهی موجود زنده با محیط پیرامون او است، بنابراین پوست نهتنها تحت تأثیر فاکتورهای درونی القاکنندهی پیری، بلکه تحت تأثیر فاکتورهای خارج سلولی و محیطی نیز قرار میگیرد و ظاهر و عملکردهای آن میتواند در طی زمان بهطور مشخصی تغییر کند (12). پیری پوست میتواند منجر به تغییر نفوذپذیری، تغییر در تعریق و تولید چربی، آسیبپذیری نسبت به محرکهای خارجی، آتروفی و آسیبهای دیگر شود. در بخشی از پوست که کمتر در معرض محیط بهخصوص در معرض اشعهی UV قرار میگیرد بیشتر میتوان اثرات پیری در اثر فرایندهای درونی را مشاهده کرد (2). تغییراتی مثل از دست دادن انعطافپذیری، شل شدن پوست و جدایی از بافت زیرین و نازک شدن پوست را میتوان از علائم پیری پوست متأثر از عوامل درونی برشمرد؛ اما در بخشهایی از پوست که تحت تأثیر محیط بیرونی و عوامل مخرب آن بهویژه اشعهی UV قرار میگیرد میتوان علائمی از جمله سفت شدن و ضخیم شدن پوست، تغییر رنگ پوست، افزایش تعداد سلولهای پوستی و هایپرپلاستیا را مشاهده کرد (13).
یک ویژگی بارز در فاکتورهای پیرکنندهی پوست، توانایی آنها در ایجاد التهاب و تحریک ایجاد پاسخ التهابی است که در پی آن و با ایجاد پاسخ ایمنی، فعالسازی متالوپروتئازهای ماتریکسی و ترشح سایتوکاینها، تغییراتی در ساختار پوست اتفاق میافتد (12).
در سالهای اخیر نقش AGEها در پیری پوست بسیار مورد توجه قرار گرفته است و پتانسیل ضدAGE ها برای استفاده در محصولات آرایشی و بهداشتی میتواند شدیداً مورد توجه شرکتهای دارویی قرار بگیرد. در این مقالهی مروری به بررسی تأثیر AGEها در روند پیری پوست و راههای مواجهه با آن پرداخته میشود (14).
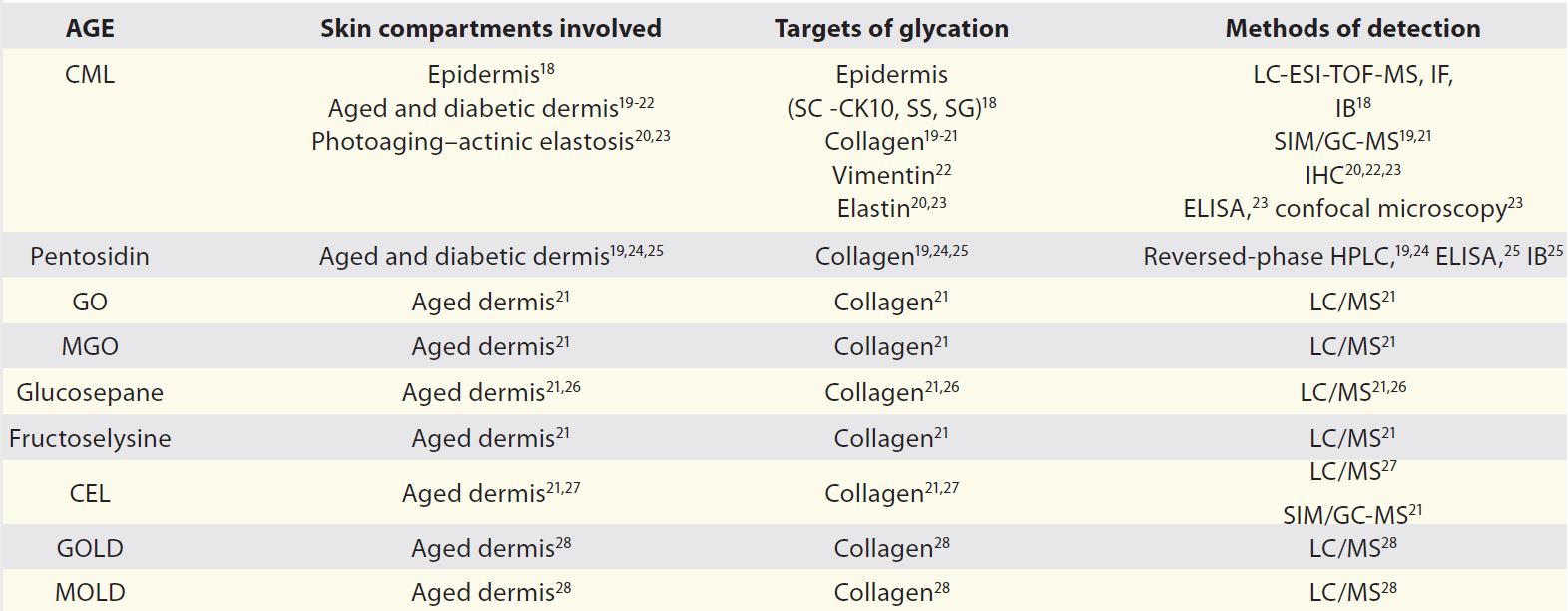
AGEها ترکیبات بسیار ناهمگن و متنوعی هستند. از زمان کشف هموگلوبین گلایکه شده بهعنوان اولین پروتئین گلایکه، چندین AGE دیگر نیز یافت شدهاند. برخی از آنها خواص اتوفلورسنت مشخصی دارند که کمک فراوانی در شناسایی آنها کرده است. در جدول 1 اسامی تعدادی از AGEهای مهم یافتشده در پوست ذکر شده است (15).
جدول 1: AGEهای مهم یافتشده در پوست
یکی از نشانههای پیری پوست، تجمع AGE ها در پوست است. همانطور که قبلاً ذکر شد، AGEها میتوانند در بدن تولید و یا از طریق مصرف مواد غذایی وارد بدن شوند. تجمع AGEها در بافتهای مختلف بدن طی پیری پوست و همچنین دیابت مشاهده شده است؛ از جمله در کلاژن غضروفها، در عضلات صاف دیوارهی رگها و عضلات اسکلتی و بافتهای دیگر (14).
پوست با توجه به امکان دسترسی آسانی که به آن وجود دارد، زمینه بسیار مناسبی برای مطالعه در زمینه AGEها با استفاده از خواص اتوفلورسنت آنها فراهم آورده است. مطالعاتی که روی تجمع AGEها در پوست انجام گرفت نشان داد که نهتنها در بیماری دیابت، بلکه در پروسه پیری پوست هم تجمع AGEها نقش ایفا میکنند. مطالعات نشان داده است که تجمع AGEها تا حد زیادی به نرخ تبدیل و تجزیه پروتئینها بستگی دارد (11)؛ بنابراین میتوان نتیجه گرفت که گلیکاسیون روی پروتئینهایی که طول عمر بالاتری دارند، تأثیر بیشتر و مهمتری خواهد داشت؛ بهعنوان مثال کلاژن تیپ ۱ و تیپ ۴ که طول عمر آنها تقریباً به ۱۰ سال میرسد و پروتئین دیگر مثل فیبرونکتین که طول عمر بالایی دارد بیشتر در معرض گلیکاسیون قرار میگیرند و تغییر میکنند (2). کلاژن گلیکه شده برای اولین بار در بدن حدوداً در سن ۲۰ سالگی ظاهر میشود. میزان تجمع آن سالیانه در حدود 3/7% افزوده میشود و این افزایش تا سن ۸۰ سالگی میتواند به ۳۰ الی ۵۰ درصد نیز برسد. مطالعات پائولی و همکاران در سال ۲۰۰۱، روی پوست افرادی که بیشتر در معرض نور خورشید قرار گرفته بودند، نشان داد که اشعه UV میتواند بهعنوان یکی از عوامل تسریعکننده انباشته شدن AGEها در پوست عمل کند (12). یکی دیگر از شواهدی که میتواند رابطه AGEها و پیری را بیان کند، کاهش فعالیت مکانیسمهای آنزیمی است که در جهت مقابله با گلیکاسیون و از بین بردن AGEها فعالیت میکنند که از جمله آنها میتوان سیستم گلی اکسیلاز وابسته به گلوتاتیون را نام برد (11).
پیامد تجمع AGEها در پوست
همانطور که در بالا گفته شد، AGEها میتوانند بهصورت داخل سلولی یا خارج سلولی تولید شوند. حضور آنها در مولکولهای شیمیایی، ویژگیهای عملکردی و بیوشیمیایی آنها را تغییر میدهد (1). لیپیدها، پروتئینها و اسیدهای نوکلئیک میتوانند تحت گلیکاسیون قرار گرفته و در نتیجهی آن، تغییراتی در برهمکنش پروتئین- پروتئین، لیپید- پروتئین، آنزیم- سوبسترا، -DNA پروتئین، تنظیم ترجمهی DNA و فرآیندهای اپیژنتیکی ایجاد کنند، بنابراین میتوانند عملکردهای فیزیولوژیک فراوانی را تحت تأثیر قرار بدهند (4). AGEها همچنین میتوانند مستقیماً به گیرندههای خود متصل شده و مسیرهای تکثیر سلولی بیان ژنهای خاص و پیامرسانی مختلفی را فعال کنند که منجر به التهاب و پاسخ ایمنی میشود (16).
ماتریکس خارج سلولی
پروتئینهای ماتریکس خارج سلولی، بهعنوان مهمترین هدف گلیکاسیون در نظر گرفته میشوند. فراوانترین نوع کلاژن در پوست، کلاژن تیپ ۱ و فراوانترین نوع در غشای پایه، کلاژن تیپ ۴ است. کلاژن در پوست نهتنها بهعنوان یک داربست مستحکمکننده عمل میکند، بلکه به دلیل توانایی برهمکنش با سایر مولکولها و اجزای سلولی، بسیار حائز اهمیت است (17). همچنین در فرآیندهایی نظیر مهاجرت، تکثیر و تمایز سلولی هم میتواند نقش ایفا کند. گلیکاسیون کلاژن به شیوههای مختلف، عملکرد آن را مختل میسازد. پیوند فیبرهای کلاژن مجاور به یکدیگر، باعث سختی و کاهش انعطافپذیری آن و همچنین آسیبپذیری نسبت به استرسهای فیزیکی میشود (16). همچنین، گلیکه شدن کلاژن میتواند در اتصال آن به سایر مولکولها و برهمکنش آن با سایر اجزای سلولی تأثیر بگذارد، در نتیجه این تغییرات، کلاژن به متالوپروتئازهای ماتریکسی مقاوم میشود و دیگر تخریب و جایگزین نخواهد شد (17).
دیگر پروتئینهای ماتریکس خارج سلولی که میتوانند تحت تأثیر گلیکاسیون قرار بگیرند، الاستین و فیبرونکتین هستند. احتمال گلیکه شدن الاستین با قرارگیری در معرض اشعه فرابنفش بالا میرود. در مطالعهای که توسط بائیک و همکاران در سال ۲۰۰۲ انجام شد، مشخص گردید که پوست مبتلایان به دیابت نسبت به افراد سالم، انعطافپذیری کمتری دارد (18).
پروتئینهای داخل سلولی
پروتئینهای داخل سلولی مثل ویمنتین در فیبروبلاستها و CK10 در کراتینوسیتها هم میتوانند تحت تأثیر AGEها قرار بگیرند، همچنین آنزیمهای درون سلولی و فاکتورهای رشد هم میتوانند تحت تأثیر گلیکه شوند (17). بهعنوان مثال میتوان به آنزیم Cu-Zn سوپراکسید دسموتاز اشاره کرد که ممکن است گلیکه شده و عملکرد آن از دست برود (18).
از آنجایی که AGEها تأثیر بسزایی در روند پیری و همچنین دیابت و دیگر بیماریها دارند، پیدا کردن راهی برای مقابله با آنها میتواند بسیار حائز اهمیت باشد. امروزه ترکیباتی که میتوانند منجر به تخریب AGEها در بدن و یا جلوگیری از ساخت آنها شوند، مورد بررسی قرار گرفته و بسیاری از آنها بهصورت بالینی تحت آزمایش هستند (17).
ترکیباتی که از ساخته شدن AGEها جلوگیری میکنند
آمینوگوانیدین
آمینوگوانیدین یکی از اولین ترکیباتی بود که بهعنوان بازدارنده تولید AGEها مورد بررسی قرار گرفت.
آمینوگوانیدین یک هیدرازین نوکلئوفیل است که قادر است محصولات اولیهی گلیکاسیون را به دام بیاندازد.
هرچند این ماده اثرات ضد AGE اثباتشده و مؤثری دارد، ولی مصرف آن بهصورت بالینی، به دلیل تأثیرات منفی که روی بیماران دیابتی دارد، منع شده است (19).
شکل 2: آمینوگوانیدین
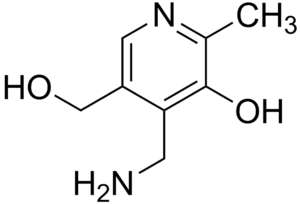
شکل 3: پیرودوکسامین
پیرودوکسامین
این ماده ایزوفرم ویتامین B6 است که با به دام انداختن حدواسطهای فعال کربونیل، ROSها را حذف میکند (19).
کارآزمایی بالینی این ماده، نتایج نویدبخش و مثبتی روی نفروپاتی دیابتی داشته است. در سال 2002، آلدرسون و همکاران، تأثیر این ماده را در گلیکاسیون کلاژن در نوعی موش بررسی کردند. نتایج نشان داد که افزودن این ماده به غذای موشها در بلندمدت، نرخ گلیکه شدن کلاژن را پایین میآورد (20).
تخریبکنندههای AGE
برخی ترکیبات میتوانند پیوندهای AGEها را بشکنند. از جمله این ترکیبات میتوان به دی متیل-3- فنیل تیازولیوم کلراید و N-فناستیل تیازولیوم اشاره کرد. این ترکیبات تحت کارآزمایی بالینی قرار گرفتهاند و نتایج امیدوارکنندهای در ارتباط با تأثیر آنها روی بیماریهای قلبی، دیابت و پیری پوست حاصل شده است (19).
اصلاح رژیم غذایی
از سادهترین راههای مواجهه با AGEها، اصلاح رژیم غذایی است. برخی مواد غذایی به میزان بسیار بالایی حاوی AGEها هستند؛ بهعنوان مثال میتوان به نوشابهها، دوناتها و گوشتهای گریلشده اشاره کرد. همچنین مصرف همزمان قندها با پروتئینها یا چربیها میتواند تولید AGEها را در بدن افزایش دهد (19).
مصرف ویتامین C و آنتیاکسیدانها در رژیم غذایی میتواند تا حدی بدن را از اثرات مخرب AGEها در امان نگه دارد (21).
در مطالعهای که در سال ۲۰۰۹، توسط یوشیکاوا و همکاران، روی ۱۷ زن میانسال انجام گرفت، مشخص شد فعالیت بدنی میتواند تا سی درصد اثرات مخرب AGEها را در بدن کاهش دهد (22).
تغییر روشهای پخت غذا نیز میتواند در کاهش واکنش میلارد و در نتیجه کاهش AGEها مؤثر باشد.
پخت در دمای بالا و یا پخت طولانی مدت در دمای متوسط ایجاد AGE را ۵۰ درصد افزایش میدهد.
استفاده از سایر روشهای پخت غذا، مثل بخارپز کردن میتواند به میزان زیادی در سالم بودن غذا و عاری بودن آن از AGEها، مؤثر واقع شود (21).
نتیجهگیری
شواهد بسیاری تأثیر AGEها در روند پیری و بهخصوص پیری و چروکیدگی پوست را تأیید میکنند، همچنین تحقیقات زیادی درباره ترکیباتی که میتوانند با AGEها مقابله کنند صورت گرفته است که برخی از این تحقیقات نتایج امیدوارکنندهای در خصوص مواجهه با پیری پوست و دیابت داشته است. تحقیقات در زمینه تأثیر AGEها روی پیری پوست و مواجهه با آن، جای کار بسیار دارد و میتواند در آینده مورد تحقیقات گستردهتری قرار بگیرد.
منابع:
- BROWNLEE M, VLASSARA H, CERAMI A. Nonenzymatic Glycosylation and the Pathogenesis of Diabetic Complications. Ann Intern Med. 1984;101:527–537. doi: 10.7326/0003-4819-101-4-527
- Viña J, Borrás C, Miquel J. Theories of ageing. IUBMB Life 2007; 59:249-54; PMID:17505961; http://dx.doi. org/10.1080/15216540601178067
- International Diabetes Federation diabetes atlas. 5th ed. Brussels, Belgium: International Diabetes Federation; 2011.
- Cai, W., Gao, Q. D., Zhu, L., Peppa, M., He, C., & Vlassara, H. (2002).Oxidative stress-inducing carbonyl compounds from common foods: novel mediators of cellular dysfunction. Molecular medicine (Cambridge, Mass.), 8(7), 337–346.
- Uribarri J, Woodruff S, Goodman S, Cai W, Chen X, Pyzik R, Yong A, Striker GE, Vlassara H. Advanced glycation end products in foods and a practical guide to their reduction in the diet. J Am Diet Assoc. 2010 Jun;110(6):911-16.e12. doi: 10.1016/j.jada.2010.03.018. PubMed PMID: 20497781; PubMed Central PMCID: PMC3704564.
- Ahmed N. Advanced glycation endproducts–role in pathology of diabetic complications. Diabetes Res Clin Pract 2005; 67:3-21; PMID:15620429; http://dx.doi. org/10.1016/j.diabres.2004.09.004
- Avery NC, Bailey AJ. The effects of the Maillard reaction on the physical properties and cell interactions of collagen. Pathol Biol (Paris) 2006; 54:387-95;
PMID:16962252; http://dx.doi.org/10.1016/j.patbio.2006.07.005
- Mizutari K, Ono T, Ikeda K, Kayashima K, Horiuchi S. Photo-enhanced modification of human skin elastin in actinic elastosis by N(epsilon)-(carboxymethyl)lysine, one of the glycoxidation products of the Maillard
reaction. J Invest Dermatol 1997; 108:797-802; PMID:9129235; http://dx.doi.org/10.1111/1523- 1747.ep12292244
- Fan X, Sell DR, Zhang J, Nemet I, Theves M, Lu J, et al. Anaerobic vs aerobic pathways of carbonyl and oxidant stress in human lens and skin during aging
and in diabetes: A comparative analysis. Free Radic Biol Med 2010; 49:847-56; PMID:20541005; http:// dx.doi.org/10.1016/j.freeradbiomed.2010.06.003
- Taghavi F, Moosavi-Movahedi AA, Bohlooli M, Alijanvand HH, Salami M, Maghami P, Saboury AA, Farhadi M, Yousefi R, Habibi-Rezaei M, Sheibani N. Potassium sorbate as an AGE activator for human serum albumin in the presence and absence of glucose. International journal of biological macromolecules. 2013 Nov 1;62:146-54.
- Elosta A, Ghous T, Ahmed N. Natural products as anti-glycation agents: possible therapeutic potential for diabetic complications. Curr Diabetes Rev 2012; 8:92-108; PMID:22268395; http://dx.doi.org/10.2174/157339912799424528
- Edelstein D, Brownlee M. Mechanistic studies of advanced glycosylation end product inhibition by aminoguanidine. Diabetes 1992; 41:26-9
- Beisswenger PJ, Howell S, Mackenzie T, Corstjens H, Muizzuddin N, Matsui MS. Two fluorescent wavelengths, 440(ex)/520(em) nm and 370(ex)/440(em)
nm, reflect advanced glycation and oxidation end products in human skin without diabetes. Diabetes Technol Ther 2012; 14:285-92
- Genuth S, Sun W, Cleary P, Sell DR, Dahms W, Malone J, et al.; DCCT Skin Collagen Ancillary Study Group. Glycation and carboxymethyllysine levels in skin collagen predict the risk of future 10-year progression of diabetic retinopathy and nephropathy in the diabetes control and complications trial and epidemiology of diabetes interventions and complications participants with type 1 diabetes. Diabetes 2005; 54:3103-11
- Smit AJ, Gerrits EG. Skin autofluorescence as a measure of advanced glycation endproduct deposition: a novel risk marker in chronic kidney disease. Curr Opin Nephrol Hypertens 2010;
- Pageon H, Técher MP, Asselineau D. Reconstructed skin modified by glycation of the dermal equivalent as a model for skin aging and its potential use to evaluate anti-glycation molecules. Exp Gerontol 2008; 43:584-
8;
- Yoon HS, Baik SH, Oh CH. Quantitative measurement of desquamation and skin elasticity in diabetic patients. Skin Res Technol 2002; 8:250-4; MID:12423544; http://dx.doi.org/10.1034/j.1600-0846.2002.00332.x
- Vasan S, Foiles P, Founds H. Therapeutic potential of breakers of advanced glycation end product-protein crosslinks. Arch Biochem Biophys 2003; 419:89- 96; PMID:14568012; http://dx.doi.org/10.1016/j. abb.2003.08.016
- Degenhardt TP, Alderson NL, Arrington DD, Beattie RJ, Basgen JM, Steffes MW, et al. Pyridoxamine inhibits early renal disease and dyslipidemia in the streptozotocin- diabetic rat. Kidney Int 2002; 61:939-50; PMID:11849448;
- Grzebyk E, Piwowar A. Inhibitory actions of selected natural substances on formation of advanced glycation endproducts and advanced oxidation protein products. BMC Complement Altern Med. 2016 Sep 29;16(1):381. doi: 10.1186/s12906-016-1353-0. PubMed PMID: 27687139; PubMed Central PMCID: PMC5041538.
- Yoshikawa T, Miyazaki A, Fujimoto S. Decrease in serum levels of advanced glycation end-products by short-term lifestyle modification in non-diabetic middle-aged females. Medical Science Monitor. 2009 May 29;15(6):PH65-73.
مروری بر تشخیص آزمایشگاهی HbA1c
سندرم پیری زودرس هاچینسون گیلفورد
برای دانلود فایل pdf بر روی لینک زیر کلیک کنید
ورود / ثبت نام