نویسنده: محمدرضا یزدانی، کارشناس ارشد ایمنیشناسی دانشگاه علوم پزشکی شیراز
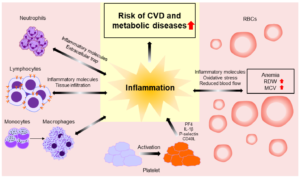
التهاب یک واکنش یکپارچه و یک مکانیسم دفاعی اصلی در برابر اختلال هموستاز در شرایط عفونی و آسیبرسان است. مطالعات اخیر نشان دادهاند که التهاب نقش مهمی در ناتوانیها، سرطان، پیری و بیماریهای مرتبط با سن، مانند تصلب شرایین و بیماریهای قلبی عروقی دارد. بیماری قلبی عروقی (CVD) یک مشکل عمده بهداشتی و علت اصلی مرگ و میر در سراسر جهان است. تخمین زده میشود که CVD در 20 سال آینده 10٪ افزایش مییابد؛ بنابراین، ارزیابی اقدامات پیشگیرانه برای به حداقل رساندن خطر CVD مهم است. چندین نشانگر التهاب به عنوان پیشبینی مورد مطالعه قرار گرفته است (شکل یک).
شکل 1- بیومارکرهای مرتبط با بیماری قلبی و عروقی[1]
شمارش جامع گلبولهای سفید خون (WBC) شامل 5 زیرگروه است: نوتروفیلها، مونوسیتها، لنفوسیتها، بازوفیلها و ائوزینوفیلها. همهWBC ها نقشهای مختلفی در پاسخ التهابی و ایمنی میزبان دارند.
علت اصلی بیماریهای قلبی و عروقی (CVD)
علت اصلی CVD آترواسکلروز است که به عنوان تشکیل مزمن پلاک در رگهای خونی تعریف میشود. التهاب یک فرآیند اصلی در ایجاد CVD است. آترواسکلروز منعکسکننده بستر پاتولوژیک CVD است. بسیاری از واسطهها در تنظیم التهاب متقابل در آترواسکلروز نقش دارند. مونوسیتهای در گردش به اندوتلیوم فعال میچسبند، به دیواره عروق نفوذ میکنند و در معرض عوامل رشد قرار میگیرند و باعث تمایز آنها به ماکروفاژها میشوند که در تمام بافتها وجود دارند و پاتوژنها را فاگوسیت کرده و لیپیدها را میخورند و به سلولهای کف تبدیل میشوند. ماکروفاژها حدود 8 درصد از غیرکاردیومیوسیتها را در قلب جذب میکنند. این درصد میتواند بهطور قابلتوجهی شرایط زمینهای CVD را تغییر دهد. آترواسکلروز زمانی شروع میشود که اندوتلیوم توسط سندرم متابولیک، فشار خون بالا، دیابت، دیس لیپیدمی آسیب ببیند و نیاز به تجمع زیر اندوتلیالی کلسترول لیپوپروتئین با چگالی کم (LDL) داشته باشد. تحت استرس متابولیک، کلسترول LDL اکسید میشود و کلسترول LDL اکسید شده، اختلال عملکرد سلولهای اندوتلیال را بدتر میکند. سلولهای اندوتلیال فعال شده، مولکولهای چسبنده را بیان میکنند و مواد شیمیایی خاصی را افزایش میدهند، مانند اینترلوکین-8 (IL-8) و پروتئین شیمی جذب مونوسیتی-1(MCP-1) . این عمل بر جذب مونوسیتها در اندوتلیوم عروقی تأثیر میگذارد. فعال شدن مونوسیتها و تمایز آنها به ماکروفاژهای مملو از چربی که به سلولهای کف معروفند، واکنشهای ضروری در تشکیل ضایعات آترواسکلروتیک هستند. آترواسکلروز یک بیماری پیشرونده با فاز مزمن بدون علامت است که با التهاب و تجمع چربی در دیواره عروق مشخص میشود و منجر به ایجاد پلاک میگردد؛ بنابراین، اکثر افراد با خطر CVD بالا از وضعیت بحرانی خود آگاه نیستند. همانطور که شرح داده شد، شروع پلاک آترواسکلروتیک، پیشرفت، آسیبپذیری و تشکیل ترومبوز، پدیدههای متوالی شامل تعامل لیپوپروتئینها، اجزای دیواره عروقی، سلولهای خونی و سیستم ایمنی هستند که با ویسکوزیته خون بهویژه در آترواسکلروز اولیه واضحتر میشوند.
WBC count بهعنوان یک بیومارکر برای بیماریهای قلبی و عروقی
افزایش تعداد کل WBC بهطور مثبت باCVD، سکته مغزی و مرگ و میر به هر علت مرتبط است. با این حال، مشخص نیست که کدام جزء از شمارش WBC توانایی پیشبینی CVD را دارد (شکل 2). شمارش WBC بهطور گستردهای به عنوان یک نشانگر زیستی ارزان و ساده برای التهاب سیستمیک استفاده میشود. این یک شاخص یکپارچه شامل چندین زیرگروه WBC مانند نوتروفیلها، مونوسیتها، لنفوسیتها، بازوفیلها و ائوزینوفیلها است. بهطور کلی، تعداد WBC نشاندهنده سطح پاسخ میزبان به استرس، شاخص فرآیندهای التهابی حاد یا مزمن است؛ بنابراین، تعداد WBC با بسیاری از خطرات درازمدت سلامتی ارتباط دارد و نشان داده شده است که خطر مرگ و میر، سرطان و بیماریهای قلبی عروقی را پیشبینی میکند.
شکل 2- ارتباط CBC با بیماریهای قلبی و عروقی[2]
مونوسیت بهعنوان یک بیومارکر جدید برای پیشبینی وقایع قلبی و عروقی
شواهد فزاینده نشان میدهد که آتروژنز جنبههای التهابی مهمی دارد. در مطالعات مقطعی، نشانگرهای مختلف التهاب از جمله گلبولهای سفید، پروتئین واکنشگر C و فیبرینوژن با آترواسکلروز ارزیابیشده با اولتراسوند مرتبط هستند. مونوسیتها از مغز استخوان به داخل رگهای خونی آزاد میشوند. این بخشی از سیستم فاگوسیت تکهستهای است که در التهاب و ایمنی میزبان نقش دارد. فعال شدن مونوسیتها و تمایز به ماکروفاژهای مملو از چربی، رویدادهای اساسی در تشکیل ضایعات آترواسکلروتیک هستند. به نظر میرسد به حاشیه راندن مونوسیتها در امتداد اندوتلیوم و انتقال به فضاهای داخلی بستگی به حضور محلی مقادیر بالای کلسترول لیپوپروتئین کمچگالی اکسید شده دارد و توسط مولکولهای چسبنده (مولکول چسبنده سلول عروقی، مولکول چسبندگی بین سلولی) که توسط مولکول انتخاب شده بیان میشود مطالعات قبلی سطوح بالایی از مولکولهای چسبندگی در گردش را در افراد مبتلا به آترواسکلروز کاروتید نشان دادهاند. در یک مطالعه مبتنی بر جامعه اخیر، تعداد مونوسیتها در خون نشانگر مقطعی بهتری برای حضور پلاک نسبت به IL-6، پروتئین واکنشگر C با حساسیت بالا، فیبرینوژن و گلبولهای سفید خون است. مونوسیتها بخشی از سیستم فاگوسیتی تکهستهای هستند که در توسعه، التهاب و ایمنی میزبان نقش دارند. امتیاز ریسک فرامینگهام (FRS) یک روش ساده و عملی است که برای پیشبینی شدت CVD استفاده میشود FRS، یک ابزار بهطور گسترده پذیرفته شده، از مطالعه قلب فرامینگهام مشتق شده است و برای پیشبینی خطر بیماریهای عروق کرونر، مانند آنژین صدری، انفارکتوس میوکارد، مرگ قلبی عروقی در یک دوره 10 ساله استفاده میشود. این ارزیابی خطر یک روش وابسته به جنس خاص است که با مجموعه متغیرهای زیر تعیین میشود: جنسیت (مرد/زن)، سن (سال)، فشار خون سیستولیک (mmHg)، درمان فشار خون بالا (بله/خیر)، وضعیت دیابت (بله/ خیر)، سیگاری فعلی (بله/خیر)، کلسترول تام (mg/dL) و HDL کلسترول FRS (mg/dL). از هر دو عامل خطر قابل اصلاح (سیگار کشیدن، فشار خون سیستولیک، استفاده از داروهای ضد فشار خون، دیس لیپیدمی، وضعیت دیابت) و غیر قابل تغییر (سن، جنس) تشکیل شده است. نمرات افراد، نماینده خطر 10 ساله ابتلا به CVD و محاسبه بر اساس مجموع امتیازات آنها، معمــــــولاً به عنوان پایین (FRS <10%)، متوسط (FRS=10-20%) و بالا (FRS>20%) طبقهبندی میشود. در این مطالعه، تعداد مونوسیتها با افزایش FRS مورد استفاده برای پیشبینی خطر CVD در یک دوره 10 ساله مرتبط بود[3]. یک مطالعه آیندهنگر اخیر که 1000 نفر کرهای را طی 6 سال مورد بررسی قرار داد، نشان داد که تعداد مونوسیتهای بالا با افزایش تشکیل پلاکهای شریانی در مرحله تحت بالینی در ارتباط است. اهمیت این مطالعه در این است که تعداد مونوسیتها بهطور بالقوه پیشبینی کننده بهتری برای خطر بیماری قلبی عروقی نسبت به کل WBC به تنهایی است.
یک مطالعه 7 ساله نشان داد که تعداد مونوسیتها پیشبینیکننده مستقل تشکیل پلاک جدید در افراد بدون پلاک در ابتدا است. به نظر نمیرسد اثر مونوسیت پاسخی به بیماری قلبی عروقی بالینی باشد. احتمالاً اثر مونوسیتها با تشکیل پلاک و نه ضخیم شدن منتشر لایه انتیما مدیا مرتبط است. در یک جمعیت سالم، شمارش مونوسیتها ممکن است برای پیشبینی خطر تشکیل پلاک در آینده استفاده شود [6]، همچنین در مطالعه دیگری که توسط نزاوا و همکارانش انجام شد، ایشان پیشنهاد کردند که مونوسیتهای در گردش نقش مهمی در پیشرفت پلاک کرونر در انفارکتوس حاد میوکارد (AMI) دارند، در حالی که اوج تعداد مونوسیتها ممکن است پیشبینیکننده پیشرفت پلاک باشد. مونوسیتوز محیطی با اختلال عملکرد بطن چپ همراه است که نشاندهنده نقش احتمالی مونوسیتها در ایجاد بازسازی بطن چپ پس از reperfused AMI است [4].
زیرگروههای مونوسیت در بیماریهای قلبی و عروقی
مونوسیتهای نفوذی منبع کلیدی ماکروفاژهای پلاکی هستند. آنها از پیشسازهای موجود در مغز استخوان به وجود میآیند و در گردش خون آزاد میشوند، جایی که 3 تا 8 درصد از گلبولهای سفید خون را تشکیل میدهند. مطالعات بر روی موش نشان داده است که مسدود کردن هجوم مونوسیتها به پلاک میتواند پیشرفت آترواسکلروز را کاهش دهد. در انسان، سطوح بالایی از مونوسیتها با ایجاد CVD دیده میشود و تعداد آنها به عنوان شاخصی از شدت CVD ظاهر میشود. با توجه به اینکه ماکروفاژهای مشتق شده از مونوسیت نقش اساسی در فرآیندهای التهابی ایفا میکنند که پیشرفت و بیثباتی پلاک را تعیین میکنند، تغییرات در جمعیت مونوسیت ممکن است بر عملکردهای التهابی ماکروفاژها تأثیر بگذارد و در نتیجه پیشرفت پلاک آترواسکلروتیک ناپایدار را افزایش دهد. بزرگترین مطالعه کوهورت در میان افراد ظاهراً سالم، مطالعه I LIKE HOME است که بهصورت سونوگرافیک بیماری عروقی آترواسکلروتیک تحت بالینی را با اندازهگیری ضخامت میانی داخلی کاروتید (IMT) ارزیابی کرد. در میان 569 شرکتکننده، مطالعه I LIKE HOME ارتباط معنیداری بین تعداد سلولهای مونوسیت CD16 مثبت و IMT یافت. هنگام تقسیم مونوسیتهای CD16 مثبت به مونوسیتهای متوسط و غیرکلاسیک، تنها دومی بهطور قابلتوجهی با IMT مرتبط باقی ماند [7]. در CVD، نسبت مونوسیتهای متوسط و/یا غیرکلاسیک اغلب افزایش یافته است. همچنین به نظر میرسد افزایش بیشتری در این زیرمجموعهها با افزایش شدت بیماری وجود دارد. بیماران مبتلا به آترواسکلروز در رگهای متعدد، مونوسیتهایCD16+ (متوسط + غیرکلاسیک) بهطور قابلتوجهی بیشتری نسبت به بیماران مبتلا به بیماری یک رگ داشتند. [7]. نتایج حاصل از مطالعات دیگر نشان داد که در بیماریهای قلبی عروقی و التهابی انسان، مونوسیت +CD14++CD16 افزایش مییابد. همچنین زیرمجموعه +CD14++CD16، بهطور مستقل وقایع قلبی عروقی را در بیمارانی که برای آنژیوگرافی اورژانسی کرونر مراجعه میکنند، پیشبینی میکنند [4]. با این حال، تغییر تعداد ++CD14 + CD16 غیر کلاسیک مونوسیت متناقض است. تعداد مونوسیتهای ++CD14+CD16 در بیماری مزمن کلیه، آنوریسم آئورت شکمی، سپسیس، هپاتیت B، عفونت ویروس نقص ایمنی انسانی و سل افزایش مییابد، اما در نارسایی احتقانی قلب، سکته مغزی و سپسیس کاهش مییابد[5]. مونوسیتهای التهابی ممکن است نه تنها با تولید سیتوکینهای التهابی، بلکه از طریق فعالسازی سلولهای T با واسطه CD40، به التهاب عروقی کمک کنند. گزارش شده است که سیگنالینگ CD40- CD40L نقش مهمی در تصلب شرایین ایفا میکند [6].
شکل 3: زیرگروههای مختلف مونوسیتی در انسان
بهبود عملکرد مونوسیت
ممکن است بتوانید عملکرد مونوسیت خود را با یک شیوه زندگی سالم بهبود بخشید. برای مثال:
- از یک رژیم غذایی متعادل استفاده کنید.
- بهطور منظم تمرین کنید.
- استرس خود را کاهش دهید یا مدیریت کنید.
- سیگار نکشید.
- از مصرف الکل اجتناب کنید.
- با شستن مرتب دستها و اجتناب از تماس با افراد بیمار، از خود در برابر عفونت محافظت کنید.
- اگر تعداد مونوسیتهای شما به دلیل بیماری یا دارو کم یا زیاد است، دستورالعملهای پزشک خود را دنبال کنید.
منابع:
- Stătescu C, Anghel L, Tudurachi B-S, Leonte A, Benchea L-C, Sascău R-A. From Classic to Modern Prognostic Biomarkers in Patients with Acute Myocardial Infarction. International Journal of Molecular Sciences. 2022;23(16):9168.
- Seo I-H, Lee Y-J. Usefulness of Complete Blood Count (CBC) to Assess Cardiovascular and Metabolic Diseases in Clinical Settings: A Comprehensive Literature Review. Biomedicines. 2022;10(11):2697.
- Kim JH, Lee YJ, Park B. Higher monocyte count with normal white blood cell count is positively associated with 10-year cardiovascular disease risk determined by Framingham risk score among community-dwelling Korean individuals. Medicine (Baltimore). 2019;98(17):e15340.
- Khan HA, Alhomida AS, Sobki SH, Al Moghairi A. Significant increases in monocyte counts and serum creatine kinase in acute myocardial infarction versus general infections. Indian Journal of Pathology and Microbiology. 2012;55(4).
- Stansfield BK, Ingram DA. Clinical significance of monocyte heterogeneity. Clinical and Translational Medicine. 2015;4(1):5.
- Mach F, Schönbeck U, Sukhova GK, Atkinson E, Libby P. Reduction of atherosclerosis in mice by inhibition of CD40 signalling. Nature. 1998;394(6689):200-3.
ورود / ثبت نام