مهندس هانیه جعفری
شرکت گیتانیک طب
هموگلوبین چیست
هر سلولی برای داشتن عملکرد طبیعی بهطور مداوم به اکسیژن نیاز دارد. در طول متابولیسم سلولی، اکسیژن مصرف شده و به جای آن کربن دی اکسید تولید میشود. یکی از عملکردهای اصلی خون، رساندن اکسیژن (O2) از طریق ریهها به سلولهای بدن و انتقال کربن دیاکسید (CO2) از سلولها به ریهها است. انتقال این گازها به کمک پروتئین هموگلوبین (Hb) موجود در گلبولهای قرمز انجام میگیرد. بهطور معمول در یک میلیلیتر خون، ۲۸۰ میلیون مولکول هموگلوبین وجود دارد.
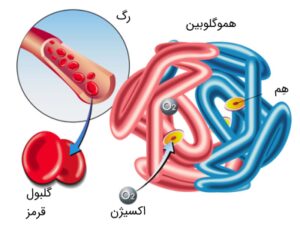
در هموگلوبین یک مولکول حاوی آهن که هِم (Heme) نامیده میشود با پروتئینهای گلوبین ترکیب میشود و هموگلوبین را تشکیل میدهد. هموگلوبین یک پروتئین کروی است که از ۴ زنجیره پلیپپتیدی تشکیل شده است. در مرکز این زنجیرهها یک گروه هِم شامل اتم آهن در حالت (۲+Fe) قرار دارد (شکل ۱). اتم آهن محل اتصال اکسیژن در هموگلوبین محسوب میشود. میل ترکیبی هموگلوبین با مونوکسید کربن بیشتر از اکسیژن است. در واقع اگر کسی در معرض مونوکسیدکربن قرار بگیرد، هموگلوبینهای او به جای اکسیژن با مونوکسیدکربن ترکیب شده و در نتیجه اکسیژن به سلولها نمیرسد و شخص دچار خفگی میشود. اتفاقی که در گازگرفتگیها میافتد دقیقاً همین است.
شکل ۱: ساختار هموگلوبین
به هموگلوبینی که به اکسیژن متصل میشود اکسی هموگلوبین گفته میشود. هر اتم آهن با یک مولکول اکسیژن واکنش میدهد؛ بنابراین یک هموگلوبین ۴ مولکول اکسیژن را به سلولها منتقل میکند. از طرفی دیگر به هموگلوبینی که با دی اکسید کربن متصل میشود، کربو آمینو هموگلوبین (carbaminohemoglobin)گفته میشود.
روشهای اندازهگیری غلظت هموگلوبین
روشهای متعددی برای اندازهگیری غلظت هموگلوبین وجود دارد؛ اما روشی که سازمان بهداشت جهانی به استفاده از آن تأکید میکند، روش اسپکتروفتومتری است. این روش با توجه به مزیتهایی که دارد بهطور گسترده در سراسر دنیا برای اندازهگیری غلظت هموگلوبین مورد استفاده قرار میگیرد. از مزیتهای استفاده از هموگلوبینمتر یا اسپکتروفتومتر میتوان به موارد زیر اشاره کرد:
- همه اشکال هموگلوبین (بهجز سولفهموگلوبین) به سیانمتهموگلوبین تبدیل میشود.
- خطای بصری در این روش وجود ندارد؛ زیرا نیازی به تطبیق رنگ خون نیست.
- محلول سیانمتهموگلوبین پایدار است و با گذشت زمان تغییر نمیکند. به همین دلیل به راحتی میتوان آزمایش را انجام داد.
- میزان جذب سریعاً به دست میآید.
- یک استاندارد مرجع و معتبر برای مقایسه نتایج وجود دارد.
اندازهگیری غلظت هموگلوبین خون (ctHb) به روش اسپکتروفتومتری
برای اندازهگیری هموگلوبین خون ابتدا نمونه خون با محلولی حاوی پتاسیم فریسیانید K3Fe(CN)6 و پتاسیم سیانید (KCN) ترکیب میشود. در اثر این ترکیب پتاسیم فریسیانید آهن موجود در خون را اکسید میکند و متهموگلوبین تشکیل میشود. سپس پتاسیم سیانید با متهموگلوبین ترکیب میشود و سیانمتهموگلوبین (HiCN) را تشکیل میدهد. در طی این فرآیند بیشتر مشتقات هموگلوبین (اکسی هموگلوبین، متهموگلوبین و کربوکسی هموگلوبین) به HiCN تبدیل میشوند. سپس این محلول به دست آمده را در اسپکتروفتومتر قرار میدهند. HiCN در طولموج ۵۴۰ نانومتر دارای بیشترین جذب است؛ بنابراین مقدار جذب را در این طولموج اندازهگیری میکنند.
همان طور که میدانید میزان جذب با غلظت نمونه طبق قانون بیر لامبرت رابطه مستقیم دارد. برای تعیین غلظت هموگلوبین (به روش اسپکتروفتومتری)، منحنی استاندارد رسم میشود و از این طریق غلظت مجهول به دست میآید.
اسپکتروفتومتر
روشهای جذب سنجی یکی از قدرتمندترین و رایجترین روشهای اندازهگیری طیف وسیعی از آنالیتها محسوب میشود. بسیاری از دستگاههای مورد استفاده بر پایه اندازهگیری میزان جذب با عبور انرژی تشعشعی ساخته شدهاند. دستگاههایی که برای جذب سنجی به کار میروند فتومترها و اسپکتروفتومترها هستند که در دهه 1940 ابداع شدند. در فتومترها ابزاری برای تهیه طیف وجود ندارد و تنها در طول موج مشخصی کار میکنند و از روی شدت نور جذب شده توسط ماده، آنالیز صورت میگیرد. این دستگاه میتواند از فیلتر نوری استفاده کند اما در دستگاه اسپکتروفتومتر امکان تهیه طیف و اندازهگیری جذب در طول موجهای مختلف وجود دارد. دستگاههای اسپکتروفتومتر به جداسازی و اندازهگیری تغییرات انرژی هستهها، یونها و یا مولکولها میپردازند که این تغییرات ناشی از برهمکنش اشعه الکترومغناطیس با ماده است. روشهای اسپکتروفتومتر شامل انواع مختلفی از جمله اسپکتروفتومتری مرئی (vis)، فرابنفش (uv/vis)، فرابنفش، نزدیک مادون قرمز (NIR/Vis/Uv)، نشر شعله (Flame) و جذب اتمی(Atomic Absorption) است که با این روشها میتوان نمونه را مورد تجزیه و تحلیل کمی و کیفی قرار داد. در این جا به مطالعه روشهای اسپکتروفتومتری مرئی – فرابنفش (UV/Vis) میپردازیم.
روشهای اسپکتروفتومتری در ناحیه مرئی – فرابنفش (UV/Visible)
روش رنگ سنجی (Colorimetry) در ناحیه مرئی تابش
در ناحیه مرئی (700-400)، جذب یا انتقال ماده میتواند به رنگ آنالیت مربوط باشد. در این روش اگر محلولی هیچ طول موج مرئی را از خود عبور ندهد بهطور تئوری به رنگ سیاه است. اگر همه طول موج مرئی را عبور دهد و هیچ نوری را جذب نکند نمونه محلول بیرنگ است و اگر محلول رنگی داشته باشیم و نوری از آن عبور دهیم که مقداری از این نور جذب شود، در این صورت این نور جذب شده دارای رنگ مکمل رنگ محلول است، برای مثال اگر نمونه محلول رنگ زرد را جذب کند برابر 595 نانومتر به رنگ آبی ظاهر میشود، چون آبی رنگ مکمل زرد است. در واقع در اسپکتروفتومتری مرئی باید طول موجی را انتخاب نمود که رنگ آن، مکمل رنگ محلول باشد. با توجه به اینکه محلولهای رنگی در رنگ مکمل خود حداکثر جذب نور را دارند، بر اساس همین ویژگی مواد را در طول موجهای مربوط به خود مورد بررسی قرار میدهند و شدت و ضعف این رنگ بستگی به مقدار ماده موجود در محلول دارد؛ بنابراین در دستگاه اسپکتروفتومتری مرئی به وسیله تجزیهگرها از جمله فیلتر، شبکه یا منشور، نور تک رنگ ایجاد مینمایند تا بتوان غلظت یک محلول رنگی را محاسبه کرد. در این دستگاه از فیلتر به عنوان مونوکروماتور استفاده میشود؛ بنابراین بخش محدودی از طول موج قابل دسترسی است.
روش اسپکتروفتومتری در ناحیه UV- Visible
در دستگاههای اسپکتروفتومتری مرئی – فرابنفش، اساس اندازهگیری بر پایه تابش نور به آنالیت مورد آنالیز در طول موجهای مختلف و بررسی میزان جذب و عبور آن است. محدوده جذب در این ناحیه از 190 تا 1000 نانومتر است. در این روش با استفاده از قانون بیر – لامبرت میتوان غلظت نمونه مورد آنالیز را اندازهگیری نمود.
قانون بیر بیان میکند هنگامی که نور تکرنگی از داخل محلول عبور نماید، میزان نور جذب شده متناسب با غلظت مولکولهایی است که در مسیر اشعه نورانی قرار گرفته و نور را جذب میکنند و طبق قانون لامبرت، تحت شرایط مساوی شدت نور خارج شده با افزایش طول مسیری که نور از محلول عبور میکند کاهش مییابد، بنابراین بر اساس قوانین بیر و لامبرت رابطه بین غلظت محلول و نور جذب شده به صورت خطی است و معمولاً در محدودهای که جذب با غلظت رابطه خطی دارد تعیین غلظت مواد انجام میشود. این دستگاه شدت نور عبوری (I) از نمونه را با شدت اولیه (I0) مقایسه میکند. نسبت I/I0، «عبور» نامیده میشود که معمولاً آن را با T% نشان میدهند. تعداد مولکولهای جاذب نور در یک نمونه متناسب با میزان جذب آن در نمونه است و به صورت رابطه زیر بیان میشود:
A= جذب قابل اندازهگیری نور
ɛ= ضریب جذب مولی
b= ضخامت سل (طول مسیر عبور نور در نمونه)
c = غلظت
در نتیجه میتوان نوشت:
A = log(l/T) = log I0/It = log ١٠ ɛ x b x c = ɛ x b x c
عوامل انحراف از قانون بیر ولامبرت شامل انحرافات فیزیکی، انحرافات دستگاهی و انحرافات شیمیایی است. انحرافات فیزیکی مربوط به محدودیت در غلظت ماده جاذب و وابستگی ضریب جذب مولی (ɛ) به ضریب شکست (n) است. انحرافات دستگاهی به دلیل تک رنگ نبودن نور، آلودگی سلها، خطی نبودن جریان حاصل در دتکتور با شدت نورتابشی، تغییر در مقدار برق و حرارت ایجاد میشود و انحرافات شیمیایی نیز ناشی از اثرات تفکیک، تجمع، تشکیل کمپلکس و یا حلال کافت و همچنین ناشی از اثرات فلورسانس و واکنش های فتوشیمیایی است.
انواع اسپکتروفتومتر
در اصل دو نوع اسپکتروفتومتر وجود دارد: اسپکتروفتومتر معمولی و آرایه دیودی
اسپکتروفتومتر معمولی
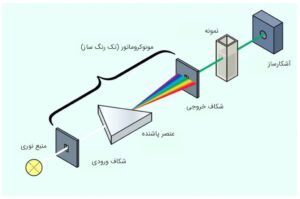
شکل 2 شماتیکی از اسپکتروفتومتر تک پرتو معمولی را نشان میدهد. نور چند رنگ از شکاف ورودی رد شده و به باریکه نور تبدیل میشود. سپس باریکه نور توسط یک المان پاشنده (بهطور مثال منشور)، پراکنده میشود. طول موج مورد نظر توسط شکاف خروجی تعیین شده و نور تک رنگ از نمونه عبور میکند و در نهایت به سمت آشکارساز هدایت میشود.
شکل 2: اسپکتروفتومتر تک پرتوی پلیکروماتیک
از این مدل برای اندازهگیری میزان جذب در یک نقطه از طیف استفاده میشود ولی برای اندازهگیری ترکیبات مختلف در طول موجهای مختلف یا به دست آوردن طیف نمونهها باید به دنبال یک روش جایگزین بود؛ زیرا برای چنین اندازهگیریهایی باید قسمتهایی از مونوکروماتور چرخانده شود که این مسئله به دلیل غیرقابل تکرار بودن، مناسب نیست.
اسپکتروفتومتر آرایه دیودی
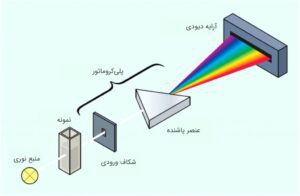
شکل 3 شماتیک اسپکتروفتومتر آرایه دیودی را نشان میدهد. نور پلیکروماتیک از نمونه عبور کرده و به سمت شکاف ورودی هدایت میشود. بخش پلیکروماتور، نور عبوری از نمونه را بر روی آرایه دیودی پراکنده میکند. هر دیود یک باند باریک از طیف را اندازهگیری میکند. بخش پلیکروماتور شامل شکاف ورودی و المان پاشنده است. از آنجا که موقعیت نسبی نمونه و المان پاشنده در مقایسه با اسپکتروفتومتر معمولی، معکوس میشود؛ اغلب از این مدل به عنوان اپتیک معکوس یاد میشود.
شکل 3: اسپکتروفتومتر تک پرتوی آرایه دیودی
پیکربندی اسپکتروفتومتر
اسپکتروفتومتر به دو صورت تک پرتو و دو پرتو ساخته میشود که در زیر به هر یک از این پیکربندیها به صورت جداگانه پرداخته شده است.
اسپکتروفتومتر تک پرتو
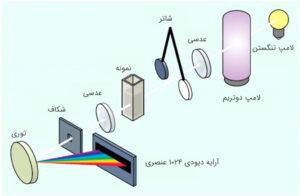
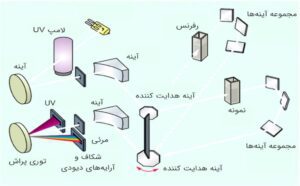
هر دو اسپکتروفتومتر معمولی و آرایه دیودی به صورت تک پرتو طراحی میشوند. البته باید در نظر داشت که آرایه دیودی برای این طراحی مناسبتر است؛ زیرا طیفها خیلی سریع به دست میآیند و فاصله زمانی که نمونه و رفرنس جابهجا میشود، به حداقل میرسد. شکل 4 سیستم نوری اسپکتروفتومتر تک پرتو را نشان میدهد. این سیستم شامل یک آرایه دیودی ۱۰۲۴ عنصری است. از شاتر برای به حداقل رساندن واکنشهای فتوشیمیایی و برای جلوگیری از ورود نور به دستگاه حین تعویض رفرنس با نمونه استفاده میشود. با شروع اندازهگیری، شاتر بهطور خودکار باز میشود و نور از رفرنس عبور میکند. زمانی که شخص رفرنس را با نمونه جابهجا میکند، شاتر بسته شده و بدین ترتیب از رسیدن نور به آشکارساز جلوگیری میکند.
شکل 4: چیدمان اپتیکی اسپکتروفتومتر تک پرتوی آرایه دیودی
اسپکتروفتومتر دو پرتو
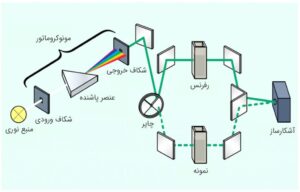
شکل 5 ساختار دستگاه اسپکتروفتومتر دو پرتو را نشان میدهد. در این طراحی نور ابتدا وارد مونوکروماتور شده و سپس به سمت چاپر هدایت میشود. چاپر مسیر نوری را بین نمونه و رفرنس سوئیچ میکند و با سرعتی میچرخد که اندازهگیریهای بین نمونه و رفرنس چندین بار در ثانیه اتفاق میافتد.
شکل 5: چیدمان اپتیکی اسپکتروفتومتر دو پرتو معمولی
نوعی دیگر از طیفسنج UV-VIS دو پرتوی معمولی وجود دارد که به آن طرح پرتو-اسپلیت گفته میشود. این مدل همانند اسپکتروفتومتر دو پرتو است با این تفاوت که به جای چاپر از اسپلیتر استفاده شده است. وقتی پرتو به اسپلیتر میرسد به دو باریکه تقسیم میشود. این باریکهها همزمان به نمونه و رفرنس میرسند (شکل 6).
شکل 6: اسپکتروفتومتر طرح پرتو- اسلیت
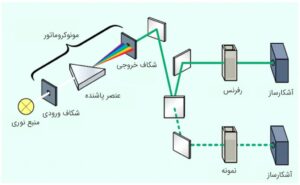
در شکل 7 طراحی اسپکتروفتومتر دو پرتوی آرایه دیودی نشان داده شده است. دلیل اینکه در این مدل از دو عدد آشکارساز استفاده شده این است که هر یک از آشکارسازها بتوانند بازه وسیعی از طول موجها را شناسایی کنند.
شکل 7: اسپکتروفتومتر دو پرتو آرایه دیودی