تاریخچه بالینی، تشخیص و بحث
(قسمت 5)
مراد رستمی: کارشناس ارشد بیوشیمی بالینی
معصومه جرفی: کارشناس ارشد میکروبشناسی
با سلام و احترام
مطالب زیر برگرفته از ویرایش ششم (2018) کتاب Tietz textbook of clinical chemistry and molecular diagnostics میباشد. در برخی موارد، به نظر میرسد که برای رسیدن به تشخیص قطعی، بررسیها و انجام آزمایشهای تأییدی بیشتری لازم باشد. با این وصف، هدف کتاب حاضر و سایر کتابهای مشابه، آموزش بیشتر، سادهتر و مؤثرتر از طریق مطرح کردن مورد (Case) بوده و بهمنظور سادهتر کردن روند آموزش و جلوگیری از هجوم یکباره و سنگین مطالب به ذهن خواننده، در هر بار، ممکن است تنها بر روی یک و یا تعداد محدودی نکته تأکید شده باشد.
لطفاً پیشنهادها و انتقادهای سازنده خود را از طریق رایانامه morad_r56@yahoo.com با ما در میان بگذارید.
با تشکر
مراد رستمی – معصومه جرفی
مورد (Case) 17
تاریخچه بالینی:
یک دختربچه 8 ساله مبتلا به صرع، در حال درمان با کاربامازپین، نیترازپام و سدیم والپروآت بود. برای ارزیابی اثر سمیت این داروها بر کبد، تستهای کبدی برای این بیمار انجام شد که نتایج بهصورت زیر بود:
|
محدوده رفرانس |
نتیجه | |
|
< 0.6 |
< 0.6 | Total Bilirubin (mg/dl) |
|
10-45 |
30 |
Aspartate aminotransferase (AST) (U/L) |
|
0-37 |
122 |
γ-Glutamyl transpeptidase (GGT) (U/L) |
| 34-52 | 46 |
Albumin (g/L) |
تشخیص و بحث:
- فعالیت GGT بهویژه توسط داروهای ضدتشنج کاربامازپین، فنوباربیتون و فنیتوئین قابل القا است.
- سایر تستهای کبدی اغلب تحت تأثیر این داروها قرار نمیگیرند، اما ممکن است فعالیت ALT یا ALP مختصری افزایش یابد.
- میزان تحت تأثیر قرار گرفتن فعالیت GGT، در افراد مختلف، بسیار متفاوت میباشد (به عبارتی دیگر، تغییرات بین فردی، در القای فعالیت GGT بسیار زیاد است)؛ در برخی از افراد پس از تجویز طولانیمدت داروهای ضدتشنج، سطح GGT بسیار زیاد افزایش مییابد؛ درحالیکه در سایر افراد پس از مصرف طولانیمدت داروهای ضدتشنج، فعالیت GGT در محدوده طبیعی باقی میماند.
مورد (Case) 18
تاریخچه بالینی:
یک دختربچه 6 ساله مبتلا به لوسمی لنفوبلاستیک حاد (Acute lymphoblastic leukemia; ALL) پس از شروع شیمیدرمانی، دارای تهوع و استفراغ بود. او همچنین دارای درد شکمی و زردی (یرقان) بود. رژیم درمانی او شامل داروهای آسپاراژیناز و وینکریستین بود. کلیشه رادیوگرافی (فیلمی که عکس رادیولوژی بر روی آن ظاهر میگردد) شکم این بیمار، نشاندهنده سطوح مایع- هوا (Air-fluid levels) متعدد بود که احتمالاً بیانگر ایلئوس پارالیتیک (انسداد روده به علت از بین رفتن حرکات رو به جـلوی روده که به آن فلج روده نیز میگویند Paralytic ileus;)، ثانویه به مصرف داروی وینکریستین میباشد. نتیجه آزمایش آمیلاز پلاسما در این زمان، در محدوده مرجع بود. این بیمار، 3 روز بعد از پذیرش وی در بیمارستان، علائمی از اریتم (قرمزی) دیواره شکم، رنگپریدگی اطراف ناف (Circumumbilical pallor) [رنگ آبی- خاکستری اطراف ناف] و کبودی پهلوی چپ (Left flank bruising) نشان داد که نشانههای کلاسیک پانکراتیت حاد خونریزیدهنـــــــــــــــده (Acute hemorrhagic pancreatitis) هستند. این تشخیص، بهوسیله توموگــــرافی کامپیوتری (Computer tomography ;CT) شکم که نشاندهنده وجود تورم در پانکراس بود، تأیید گردید. پانکراتیت این بیمار به مصرف داروی آسپاراژیناز نسبت داده شد. پس از مشخص شدن تشخیص، لیپاز پلاسما نیز اندازهگیری گردید. نتایج هم آمیلاز و هم لیپاز این بیمار در نمونههای مختلف پلاسما (اندازهگیری هر دو در شروع و در پایان پانکراتیت حاد) در تصاویر زیر نشان داده شده است:
[توضیح: بهطور طبیعی، انتظار میرود که مقداری گاز در معده و روده بزرگ مشاهده گردد؛ بنابراین وجود گاز در روده کوچک، نشانه وجود نوعی اختلال در سیستم گوارشی میباشد. در انسداد روده کوچک، مایع و گاز در روده کوچک تجمع یافته که تولید یک الگوی ویژه موسوم به سطح مایع- هوا (Air-fluid level) مینماید. گاز بر روی مایع قرار گرفته و تولید یک سطح صاف در محل تلاقی مایع- هوا مینماید. از بیمار در وضعیتهای خوابیده و ایستاده، کلیشههای رادیوگرافی تهیه شده و با بررسی وجود و یا عدم وجود سطح مایع- هوا در آنها، وضعیت بیمار ارزیابی میگردد].
[توضیح: در نشانههای کلاسیک پانکراتیت حاد خونریزیدهنده (Acute hemorrhagic pancreatitis)، کبودی پهلوی چپ (Left flank bruising) به نشانه Gray Turner᾽s و رنگپریدگی اطراف ناف (Circumumbilical pallor) یا رنگ آبی- خاکستری اطراف ناف (Gray-blue discoloration around the umbilicus) به نشانه Cullen᾽s موسوم است].
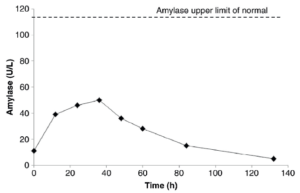
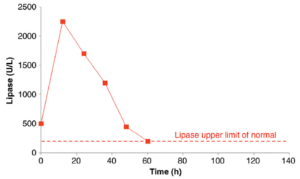
تصویر: تغییرات سطوح پلاسمایی آمیلاز و لیپاز با گذشت زمان در پانکراتیت حاد
[توضیح: پانکراتیت حاد اغلب یک بیماری خفیف (Mild) بوده و بهطور خودبخودی برطرف میگردد؛ اما در حدود 20 درصد موارد آن، بیمار نیاز به بستری شدن در بیمارستان پیدا مینماید. میزان شیوع آن 17 مورد در هر 100000 نفر در ایالات متحده میباشد. شیوع در مردان و زنان تقریباً برابر بوده و بیشتر در سنین 60-50 سالگی رخ میدهد.
در اثر انسداد مجاری و یا آسیب سلولهای آسینار (Acinar cells) صفراوی، تریپسین از حالت زیموژن به فرم فعال تبدیل شده که این تریپسین فعالشده، بهنوبه خود موجب فعال شدن سایر آنزیمهای پانکراسی (کیموتریپسین، فسفولیپاز، لیپاز و الاستاز) در داخل سلولهای آسینار میشود. این آنزیمهای فعالشده موجب خودهضمی (Autodigestion) بافت پانکراس و ایجاد التهاب، آسیب عروقی، نکروز و تشکیل کیستهای کاذب (فضای غیرطبیعی مشابه یک کیست که توسط اپیتلیوم پوشیده نشده و در آن مایعات و قطعات نکروزه تجمع مییابند،Pseudocysts ) و خونریزی داخــل بافـــــــت پانکـــــــراس (پانکراتیت حاد خونریزیدهنده، Acute hemorrhagic pancreatitis) میشوند. این پروسهها ممکن است محدود به بافت پانکراس نبوده و گاهی حتی بافتهای اطراف پانکراس (Peripancreatic tissues) و یا حتی بافتهای دورتر را نیز درگیر نمایند.
از ریسکفاکتورهای ایجاد پانکراتیت حاد به مصرف الکل، بیماریهای انسدادی مجاری صفراوی (بهویژه وجود و یا ایجاد سنگ صفراوی، Cholelithiasis)، اولسر پپتیک، ترومای شکمی، ترومای ناشی از جراحی، هیپرلیپیدمی (افزایش سطح لیپیدهای خون)، هیپرکلسمی (افزایش سطح کلسیم خون)، عفونتها (بهویژه عفونتهای ویروسی)، فاکتورهای ژنتیکی (پانکراتیت ارثی و سیستیک فیبروزیس)، برخی داروها (از قبیل دیورتیکهای تیازیدی) و … میتوان اشاره نمود. در 25-15 درصد موارد، علت آن ناشناخته است].
تشخیص و بحث:
- نتایج این بیمار نشان میدهند که افزایش سطح لیپاز پلاسما زودتر و بیشتر از سطح پلاسمایی آمیلاز رخ میدهد.
- در این مورد (Case)، اندازهگیری لیپاز پلاسما، تشخیص پانکراتیت را زودتر مشخص مینماید.
- نشان داده شد که سطح آمیلاز پلاسما در این بیمار افزایش و سپس کاهش یافته، اما از سطح بالای محدوده طبیعی عبور نکرده است.
- این مورد (Case)، نشان میدهد که سطح آمیلاز پلاسما در پانکراتیت حاد ممکن است طبیعی باشد.
- بنابراین، اندازهگیری لیپاز پلاسما در تشخیص پانکراتیت حاد توصیه میگردد.
مورد (Case) 19
تاریخچه بالینی:
یک پسربچه 3 ساله با سندرم روده کوتاه (Short bowel syndrome ;SBS)، اســـهال فـــــراوان (Profuse diarrhea) داشت. نتایج الکترولیتها و اسمولالیته مدفوع بهصورت زیر بود:
[توضیح: سندرم روده کوتاه (Short bowel syndrome)، یک حالت اختلال جذب در اثر برداشتن بخشی از روده کوچک بهوسیله جراحی و یا ناشی از کوتاه بودن شدید روده کوچک به علل مادرزادی است. در سندرم روده کوتاه، طول روده کوچک اغلب کمتر از 200 سانتیمتر میباشد. در این سندرم، ظرفیت جذبی روده کوچک، ناکافی بوده و سبب ایجاد علائم بالینی از قبیل اسهال، دهیدراسیون و سوء جذب میشود].
|
محدوده رفرانس |
نتیجه |
|
|
* |
80 | Sodium (mmol/L) |
|
* |
11 |
Potassium (mmol/L) |
| * | 308 |
Osmolality (mmol/kg) |
[*توضیح: در این کتاب، محدوده رفرانس در این مورد ذکر نشده بود. محدوده رفرانس سدیم در مــــدفوع، 9.8-5.8 mmol/day و محدوده رفرانس پتاسیم در مدفوع، 20.7-15.7 mmol/day است].
شکاف اسموتیک مدفوع (Fecal osmotic gap; FOG) ممکن است بهصورت زیر محاسبه شود:
FOG = 308 – 2 × (مدفوع Na+ +مدفوع K+)
FOG = 308 – 2 × (80 + 11)
FOG = 126 mmol/kg
تشخیص و بحث:
- در اسهال اسموتیک، شکاف اسموتیک مدفوع (FOG)، بیشتر از 50 میلیمول در کیلوگرم میباشد، درحالیکه در اسهال ترشحی، میزان FOG اغلب پایین است.
- بهنظر میرسد که این بیمار دارای اسهال اسموتیک ناشی از سوءجذب کربوهیدراتها باشد، اگرچه شاید غلظت بالای سدیم مدفوع غیرمنتظره است.
- بهجای اندازهگیری اسمولالیته مدفوع، استفاده از مقدار تئوری 290 میلیمول در کیلوگرم برای اسمولالیته مدفوع نیز پیشنهاد شده است که با در نظر گرفتن مقدار تئوری 290 میلیمول در کیلوگرم برای اسمولالیته مدفوع (بهجای میزان اسمولالیته 308 میلیمول در کیلوگرم بهدستآمده در اندازهگیری مستقیم اسمولالیته مدفوع این بیمار)، میزان FOG در این بیمار، 108 میلیمول بر کیلوگرم به دست خواهد آمد.
FOG = 290 – 2 × (مدفوع Na+ + K+)
FOG = 290 – 2 × (80 + 11)
FOG = 108 mmol/kg
[توضیح: اسهال ممکن است از نظر فیزیوپاتولوژیکی به انواع ترشحی (Secretory) و اسموتیک (Osmotic) تقسیمبندی شود. اسهال ترشحی یک اسهال حجیم آبکی ناشی از افزایش تحریک ترشح آب و الکترولیتها، توقف جذب آنها و یا هر دو مکانیسم است. از انواع اسهال ترشحی میتوان به برخی عفونتهای معدی- رودهای از قبیل انتاموبا کلی و وبا، برخی علل هورمونی از قبیل سندرم کارسینوئید و … اشاره نمود. اسهال اسموتیک یک اسهال ناشی از وجود مواد غیرمحلول مثل سولفات منیزیوم در روده میباشد. از انواع اسهال اسموتیک میتوان به لاکتولوز و سوءهضم/ جذب کربوهیدراتها از قبیل عدم تحمل لاکتوز و … اشاره کرد].
مورد (Case) 20
تاریخچه بالینی:
یک کودک 21 ماهه با علائم لتارژی (افت سطح هوشیاری همراه با خوابآلودگی، بیتوجهی و بیاحساسی، Lethargy) و تب خفیف (Mild fever) مراجعه نمود. معاینه شکم، یک توده بزرگ را نشان داد. در اسکن اولتراسوند، یک تومور با منشأ غده آدرنال سمت راست، تشخیص داده شد. نمونه ادرار راندوم (تصادفی) بهمنظور اندازهگیری کاتکولامینها و متابولیتهای آن جمعآوری و نتایج زیر حاصل گردید:
|
محدوده رفرانس |
نتیجه |
|
|
|
0.03 | Norepinephrine (mol/mmol creatinine) |
|
|
0.01 |
Epinephrine (mol/mmol creatinine) |
|
2-15 |
13.7 |
Vanillylmandelic acid (VMA) (mol/mmol creatinine) |
|
2-19 |
104.8 |
Homovanilic acid (HVA) (mol/mmol creatinine) |
| 2.7 > | 28.7 |
Dopamine (mol/mmol creatinine) |
تشخیص و بحث:
- این نتایج نشاندهنده افزایش قابلملاحظه دوپامین و متابولیت آن، هومووانیلیک اسید (HVA) هستند که با تشخیص نوروبلاستوما (Neuroblastoma) مطابقت دارد.
- نوروبلاستوما شایعترین سرطان توپر (Solid cancer) در بچههای کم سن است که تقریباً 90 درصد موارد آن در بچههای کمتر از 5 سال رخ میدهد.
- اندازهگیری کاتکولامینها و متابولیتهای آنها، یک جزء ضروری در تشخیص بیماران مشکوک به نوروبلاستوما میباشد.
- غلظتهای ادراری VMA، HVA و یا هر دو، در بیش از 90 درصد موارد افزایش مییابد.
- در این جمعآوری ادرار، VMA بهطور قابلتوجهی افزایش نیافت.
- در این بیمار، سطح نوراپینفرین و اپینفرین افزایش نداشت، درحالیکه افزایش آنها در مورد نوروبلاستوما اغلب رخ میدهد.
- این بیمار دارای افزایش سطح دوپامین بود که بهطور کلی، با نتایج نامطلوب در نوروبلاستوما همراه است.
[توضیح: نوروبلاستوما یک تومور بدخیم بافت عصبی غده آدرنال، گردن و طناب عصبی است که تقریباً 8-10 درصد سرطانهای کودکان را شامل شده و 80 درصد موارد آن در سنین قبل از 4 سالگی رخ میدهد. نوروبلاستوما پس از لوکمی و سرطان سیستم عصبی مرکزی، سومین عامل شایع سرطان در کودکان میباشد. شیوع نوروبلاستوما تقریباً 10 مورد در هر 1 میلیون کودک است که سالانه منجر به حدود 10000 مورد جدید در کل دنیا میشود. رفتار کلینیکی نوروبلاستوما متفاوت است؛ برخی تومورها بهطور خودبخودی پسرفت (Regression) نموده و برخی دیگر یک رفتار بسیار بدخیم را از خود بروز میدهند. درمان شامل جراحی، شیمیدرمانی و رادیوتراپی میباشد.
از تومورمارکر “انولاز اختصاصی نرون” (Neuron-specific enolase ;NSE) نیز ممکن است در بررسی کارسینومای سلول کوچک ریه (Small cell lung carcinoma)، نوروبلاستوما و تومورهای نورواندوکراین استفاده شود].
تاریخچه بالینی، تشخیص و بحث (3)
تاریخچه بالینی، تشخیص و بحث ( 4)
مقدمهای بر عفونتهای ویروسی دستگاه گوارش
تاریخچه بالینی، تشخیص و بحث ( 1)
برای دانلود فایل pdf بر روی لینک زیر کلیک کنید
ورود / ثبت نام


دیدگاه برای این مطلب بسته شده است.