سندرم کمبود تستوسترون
دکتر سید مهدی زرگریان
خلاصه
هدف: بازبینی مقالات مرتبط با Testostrone Deficiency Syndrome (TDS) با تأکید بر ملاحظات تشخیصی
طراحی و روشها: مقالات مرتبط با تأکید بر تظاهرات بالینی سندرم، ضرورت بررسی بیوشیمیایی و سؤالات مربوط به نوسانات بیولوژیک و آنالیتیکال مورد بازبینی قرار گرفت. در این بررسیها گزینههای درمانی نیز مورد توجه بود.
یافتهها: به دلیل کمبود ویژگی (specifity) و نیز نامحسوس بودن تظاهرات بالینی در مواردی که کمبود تستوسترون شدید نیست، مشکلات متعددی در تشخیص بالینی TDS وجود دارد. تأئید حدس بالینی محتاج ارزیابی آزمایشگاهی میباشد، گرچه درخصوص اینکه تستوسترون آزاد و تستوسترون Bioavailable هر دو میزان هورمونهای مردانه را بهتر منعکس میکنند، اجماع وجود دارد اما انتخاب روش اندازهگیری همچنان محل بحث است.
تشخیص آزمایشگاهی در میان پزشکان از مقبولیت برخوردار است اما نقاط ضعف در تفسیر آن باید مورد تأکید قرار گیرد و اینکه همکاری و ارتباط نزدیک بین آزمایشگاه و پزشک معالج در افزایش دقت تشخیص حائز اهمیت میباشد. حتی زمانی که تابلوی بالینی بیمار متقاعدکننده است، نتایج آزمایش ممکن است مبهم باشد و در این شرایط باید یک دوره درمان مدنظر باشد. گزینههای درمانی بین پزشک و بیمار باید با توجه به دسترسی، تحمل بیمار، کارآیی و هزینه درمان مورد بررسی قرار گیرد.
نتیجهگیری: TDS یک اتفاق شایع است اما بهواسطه تعارضهای بالینی و آزمایشگاهی همیشه محل جروبحث بوده است. مردانی که علائم کمبود تستوسترون را دارند و کمبود آنها مورد تأئید آزمایشگاه بوده است، باید مورد درمان قرار گیرند.
مقدمه:
با افزایش سن میزان تستوسترون در مردان کاهش مییابد. این کاهش در مردان بالای 40 سال معمول است. میزان تستوسترون توتال سالانه هشتدهم درصد و مقدار تستوسترون آزاد و تستوسترون زیست فراهم Bioavailable سالانه 2% کاهش مییابند (1). مطالعات بالتیمور نشان میدهد که 20% افراد بین 60 تا 69 سال دچار کمبود تستوسترون هستند (2). مطالعات ماساچوست میزان کمبود تستوسترون را تا 12/3% تخمین میزند که به عبارتی 2/4 میلیون نفر از مردان 40 تا 60 ساله آمریکایی دچار کمبود تستوسترون هستند (3). البته همه این افراد علائم بالینی کمبود را ندارند و علائم بالینی در 5/6% افراد دیده میشود (4). مطالعات سالمندی در اروپا میزان کلی کمبود تستوسترون را 2/1% و کمبود آن را در افراد بین 70 تا 79 سال بالغ بر 5/1% برآورد میکند (5).
علیرغم اینکه TDS بهطور وسیع شناختهشده و مورد پذیرش میباشد، اما در مورد مواجهه و درمان آن اختلاف نظر بسیاری وجود دارد.
تظاهرات بالینی کمبود تستوسترون معمولاً تا زمانی که کمبود آن شدید نباشد غیراختصاصی و مبهم است، لذا پزشک معالج تأکید خود را بر نتیجه آزمایش میگذارد. این مقالهی مروری، به خطاهای تشخیص و TDS و راههای فائق آمدن بر آنها تمرکز مینماید.
بررسی اجمالی هیپوگنادیسم
تعریف
TDS یک سندرم بالینی و آزمایشگاهی است که با افزایش سن، تستوسترون کاهش مییابد ولی حساسیت به آندروژنها در بافتها ممکن است ثابت باشد و یا کاهش پیدا کند. این اتفاق میتواند منجر به تغییرات اساسی در کیفیت زندگی شده و اثرات مضر بر اعضای مختلف بدن داشته باشد (8).
البته TDS را نباید با یائسگی مقایسه کرد چرا که اثرات آن جزئی و تدریجی بوده و در همه افراد هم دیده نمیشود. متأسفانه اغلب این پذیرش وجود ندارد که عملکرد ژنومیک و غیرژنومیک تستوسترون در مردان و زنان متفاوت است. در اکثر موارد TDS در نتیجه پیر شدن بیضهها بوجود میآید و لذا در این گونه موارد میتوان برچسب هیپوگنادیسم اولیه بر آن زد که ویژگی آن کاهش تستوسترون و افزایش FSH و LH میباشد.
در هیپوگنادیسم ثانویه که ناشی از اختلال در محور هیپوتالاموس- هیپوفیز است مقدار تستوسترون کاهش مییابد اما بطور همزمان FSH و LH افزایش نمییابند. محور هیپوتالاموس– هیپوفیز هم نسبت به سالخوردگی آسیبپذیر نیستند، لذا هیپوگنادیسم بزرگسالان میتواند ناشی از عوارض پیری در این محور باشد. اثرات تغییرات مرکزی در کنترل عملکرد سلولهای leydig در مردان مسن از دیرباز مشخص شده بود که در نتیجه ریتم شبانهروزی تولید تستوسترون کند شده و تعداد و دامنه پالسهای LH کاهش مییابد. این وقایع در نتیجه کاهش تحریک توسط GnRH میباشد (5). این موضوع بسیار مهم است چرا که مردان مسن را بهراحتی نمیتوان تحت عناوین هیپوگنادیسم اولیه و یا ثانویه طبقهبندی نمود، بلکه هیپوگنادیسم در این افراد حالت مختلط داشته که در آن تستوسترون کم شده اما مقدار گنادوتروپینها کاملاً متغیر (طبیعی، بالا یا کمتر از نرمال) میباشند (9).
واژه آندروپوز andropause لغت مناسبی نیست اما در فرهنگ عامه وارد شده است. به نظر نگارنده این واژه باید فقط برای افرادی در نظر گرفته شود که توقف فعالیت هردو گناد در آنها تحقق یافته است که این توقف به خاطر شرایطی همچون پیچش بیضه، اورکیت و یا جراحی و برداشتن هردو بیضه میباشد. در این چنین شرایطی تابلوی واضح بالینی و آزمایشگاهیِ توقف تولید هورمون جنسی مشاهده میگردد.
تظاهرات TDS
گرچه ارتباط مستقیمی بین شدت کاهش تستوسترون و تظاهرات بالینی وجود دارد اما تفاوتهای زیادی بین افراد در نمایش این تظاهرات مشاهده میشود. این باور وجود دارد که بین شدت کاهش تستوسترون و بروز علائم و نشانههای بالینی رابطه مستقیمی هست (جدول 1)، بنابراین اولین نشانه ممکن است کاهش میل جنسی باشد اما اختلال در نعوظ درصورتیکه سایر عوامل مانند اختلال خونرسانی مطرح نباشند نشانگر هیپوگنادیسم شدید خواهد بود. الزاماً همه تظاهرات با هم بروز نخواهند کرد و میزان شدت بروز آنها به عواملی همچون سن، سلامت عمومی و داروهای مصرفی نیز بستگی دارد.
تشخیص
تاریخچه و معاینه فیزیکی
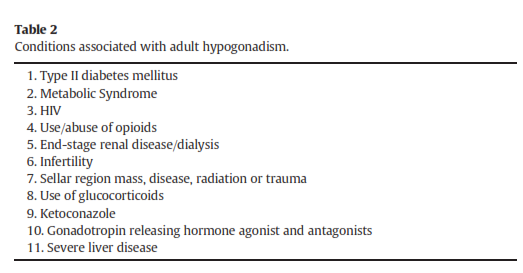
علائم و نشانههای TDS متنوع و غیراختصاصی میباشند، بنابراین اخذ تاریخچه و معاینات فیزیکی نقش محدودی در تشخیص این سندرم دارند. تنها درصورتیکه میزان تستوسترون بسیار کم باشد تظاهرات مشخص در آن ظاهر میگردد. شرححال بیمار میتواند شک به هیپوگنادیسم را برانگیزد (جدول 2). مردانی که چنین شرایطی را دارند (به شرح جدول 2) ریسک بالاتری برای کمبود آندروژن دارند و باید از نظر هورمونی ارزیابی شوند.
پرسشنامه تشخیصی
برای تسهیل تشخیص بالینی، پرسشـــــــنامههای خاصـــــی طراحی شدهاند؛ مهمترین این پرسشنامهها
Androgen Deficiency in Aging Male (ADAM) (10) وAging Male Symptom (AMS) Rating Scale (11) میباشند. ADAM یک پرسشنامه خودارزیابی است که 10 سؤال دارد که جواب آنها بله یا خیر میباشد. اخیراً برای پاسخهای این پرسشنامه برحسب شدت و دفعات تظاهرات هیپوگنادیسم ضریب و اهمیت تعیین شده است (12). از آنجا که پاسخها کمیتر میشوند لذا انتظار میرود که در ارزیابی نتایج درمان در طی زمان مفیدتر باشند.
AMS هم یک پرسشنامه خودارزیابی است که برای ارزیابی علائم سالخوردگی در مردان، کیفیت زندگی در طول زمان و اثرات درمان با آندروژنها طراحی شده است (3). پاسخ سؤالات از صفر (هیچ) تا 5 (بینهایت شدید) میباشد و سؤالات در سه زمینه روانی (5 سؤال)، جسمی (7 سؤال) و جنسی (5 سؤال) میباشند. نمره نهایی بین 17 تا 85 میباشد. برای غربالگری هیپوگنادیسم در مردانی که اختلال عملکرد جنسی دارند متعاقب پرسشنامه یک مصاحبه هم انجام میشود (13). گرچه این پرسشنامه معتبر است اما مقبولیت عام نیافته است.
به لحاظ سادگی، ADAM در کاردرمانی استفاده بیشتری دارد و AMS بیشتر در کارهای تحقیقاتی استفاده میشود. هردوی این پرسشنامهها از حساسیت بالایی برخوردارند اما از نظر ویژگی ضعیف هستند، بنابراین وسیله تشخیصی مناسبی نیستند. پرسشنامهها بیشتر برای شکستن یخ فضای اولیهی مصاحبه با بیمار کاربرد دارند. در ارزیابی درمان با تستوسترون این پرسشنامهها کاملاً مفید هستند.
تشخیص آزمایشگاهی
با توجه به کاستیهای شرححال و معاینه فیزیکی، تشخیص آزمایشگاهی کمبود تستوسترون مهمترین رکن تشخیص میباشد. گرچه اندازهگیری مقدار تستوسترون یک اقدام ضروری و حیاتی میباشد، اما اعتماد کامل به نتیجه آزمایش نباید صورت پذیرد. مشکل عمده در نبود صحت (Accuracy)نتایج ایمونواسی و فقدان استانداردهای مرجع میباشد. بیشتر گایدلاینها بر سنجش تستوسترون کل سرم تأکید دارند (14)، اما بعضی از آنها هم سنجش تستوسترون زیست فراهم Bioavailable (BAT) را توصیه میکنند (15). جدا از اینکه چه آزمایشی انجام میشود تبادلنظر پزشک و آزمایشگاه در خصوص تفسیر، قابل اعتماد بودن، تکرارپذیری و هزینه آزمایش ضروری میباشد.
اگرچه این اتفاقنظر وجود دارد که تستوسترون آزاد و تستوسترون زیست فراهم (BAT) انعکاس دقیقتری از مقدار آندروژنها میباشند، اما انجام این آزمایشها چندان متداول نیست و قیمت آنها نیز گرانتر میباشد. با توجه به اینکه نقش آنها در فرایند تشخیص، اساسی میباشد لذا در ادامه به شرح آنها خواهیم پرداخت. علاوه بر آن برای نشان دادن ویژگیهای تشخیصی آنها، برخی موضوعات مرتبط با نوسان بیولوژیک و آنالیتیک آنها بیان خواهد شد.
آزمایش انتخابی
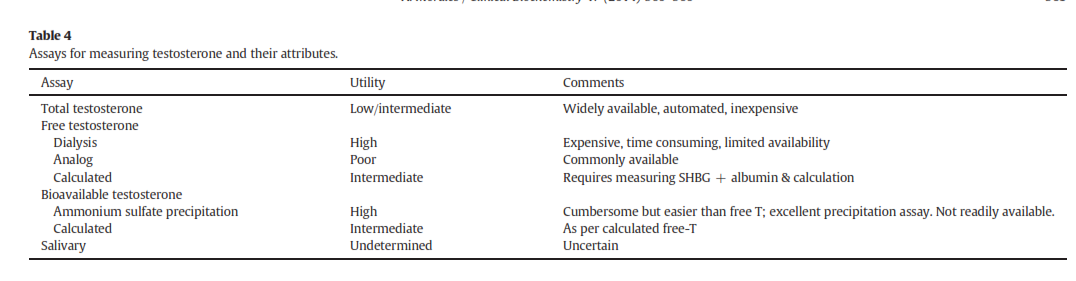
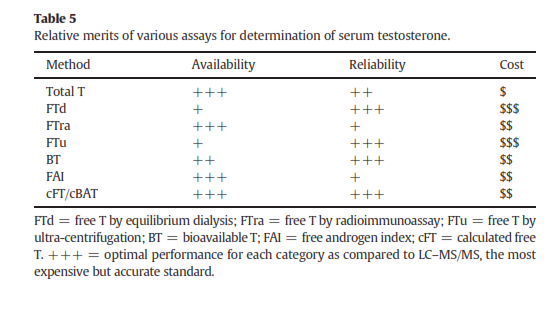
متداولترین آزمایشاتِ در دسترس در جدول 3 نمایش داده شدهاند که هرکدام مزایا و معایب خاص خود را دارند (جدول 4). در تفسیر میزان تستوسترون توتال باید عواملی همچون سن، هیپرتیروئیدیسم و بیماری کبدی را مدنظر داشت چرا که این عوامل موجب تغییر در میزان Sex Hormone-Binding Globulin (SHBG) میشوند. معالوصف آزمایش تستوسترون توتال یک آزمایش قابلاعتماد، باارزش و در دسترس میباشد. تستوسترون آزاد (FT) و تستوسترون زیست فراهم (BAT) دقیقتر هستند اما گرانتر بوده و در آزمایشگاههای کمتری انجام میشوند. انتخاب یک آزمایش به عوامل مختلفی همچون در دسترس بودن و قیمت بستگی دارد (جدول 5). اگرچه توسط تعدادی از شرکتهای تجهیزاتی و آزمایشگاههای تحقیقاتی جهت استاندارد کردن روشها اقداماتی بعمل آمده است اما ظاهراً دست یافتن به این هدف آسان نیست (17).
تستوسترون توتال
تستوسترون توتال را بهوسیله رادیوایمونواسی یا ردیابهای غیررادیواکتیو میتوان اندازه گرفت. ردیابهای غیررادیواکتیو مزایای زیادی دارند از جمله اینکه بهوفور در دسترس هستند، با نمونه کم قابل ا نجام میباشند و تناسب آنها با اسپکترومتری جرمی بالا میباشد. این آزمایش برای ارزیابی هیپوگنادیسم در مردان مسن به لحاظ بالینی کفایت میکند. درصورتیکه مقدار SHBG بالا باشد نتیجه گمراهکننده خواهد بود چرا که SHBG به تستوسترون متصل گردیده و مانع شرکت آن در انجام واکنش با معرف میگردد. بیثباتی و تباین آنالیتیکال در این آزمایش وجود دارد و باید مدنظر باشد.
Bioavailable T
تستوسترون در جریان خون به سه صورت دیده میشود؛ آزاد، متصل به آلبومین و متصل بهSHBG. فرم آزاد و متصل به آلبومین از نظر متابولیکی فعال بوده و مجموعه آنها را تستوسترون زیست فراهم BAT مینامند. در مردان از 25 تا 75 سالگی بیش از 50% در مقدار BAT کاهش ایجاد میشود (18).
برای اندازهگیری BAT بهوسیله سولفات آمونیم SHBG را به همراه هورمونهای متصل به آن رسوب میدهند. پس از سانتریفوژ کردن آنچه در مایع رویی باقی میماند BAT است که میتوان آن را بهطور مستقیم با روشهای ایمونواسی اندازهگیری نمود. راه دیگر استفاده از فرمول Vermeulen (16) برای محاسبه BAT است که آن فرمول را میتوان در آدرس www.Issam.ch مشاهده نمود.
تستوسترون آزاد (FT)
تستوسترون آزاد برای تشخیص اولیه یا بهعنوان تست تأئیدی در هنگام مواجهه با موارد دوپهلو و متناقض هیپوگنادیسم انجام میشود. اطلاعات مهارتسنجی کالج پاتولوژیستهای آمریکا نشان میدهد که سنجش تستوسترون آزاد در بیشتر مناطق آمریکای شمالی متداول است. درواقع فقط 5 روش مجزا برای سنجش FT وجود دارد (19). متأسفانه مقالاتی که کاربرد تشخیصی FT را توصیه میکنند همیشه تفاوت این روشها را مشخص نمیسازند و لذا برای پزشکان بالینی درخصوص تفاوت روشها ابهام بوجود میآید.
الف- دیالیز تعادلی Equilibrium dialysis روش مرجع سنجش FT میباشد. تستوسترون آزاد از غشاء دیالیز عبور میکند اما تستوسترون متصل به پروتئین در پشت غشاء باقی میماند. FT منتقل شده به پشت غشاء توسط روش ایزوتوپ رادیواکتیو اندازهگیری میشود. نتایج توسط دمای محیط، PH و رقت نمونه تحت تأثیر قرار میگیرند. دیالیز تعادلی یک روش زمانبر و گران است که در تعداد محدودی از آزمایشگاهای آمریکای شمالی انجام میشود و لذا بهطور روتین در دسترس اکثر پزشکان نیست.
ب- از اولتراسانتریفوژ هم بهعنوان یک روش مرجع یاد میشود. تستوسترون آزاد تحت تأثیر فشار اولتراسانتریفوژ از غشاء انتخابی رد شده و سپس توسط روش ایزوتوپ رادیواکتیو اندازهگیری میشود.
ج-analog FT. به لحاظ گران بودن انجام آزمایش FT با روشهای مرجع، روش سنجش مستقیم RIA بهصورت کیتهای تجاری عرضه شده است. در این روش که تکمرحلهای است و نیاز به استخراج وجود ندارد، یک آنالوگ تستوسترون که متصل به ماده رادیواکتیو است با تستوسترون آزاد سرم بر سر اتصال به یک آنتیبادی که بر سطح لوله آزمایش فیکس شده است رقابت میکند.
پیشفرض این آزمایش این است که آنالوگ تستوسترون میل ترکیبی اندکی برای ترکیب با SHBG و آلبومین دارد و در طی یک آزمایش به این پروتئینها متصل نمیشود، اما نکته قابلتوجه در اینجاست که مقدار FT بدست آمده با این روش در مقایسه با روش مرجع برای مردان سالم 10 برابر کوچکتر میباشد و این یافته بدان معنی است که باید محدوده مرجع را بر اساس روش اصلاح نمود و نیز ملاحظات و نگرانیهای جدی نسبت به صحت این روش داشت. این پیشفرض که آنالوگ تستوسترون نباید به سایر پروتئینهای نمونه متصل شود هم ضرورتی است که در اکثر کیتهای تجاری تحقق نمییابد. روشهای ایمونواسی متعددی بهطور تجاری برای سنجش تستوسترون آزاد وجود دارد.
Rosner (20) یکی از اولین کسانی بود که نسبت به صحت روش آنالوگ تستوسترون در سنجش FT هشدار داد. وی اظهار داشت که شواهد بیشماری نشان میدهد که روش RIA مستقیم (مبتنی بر آنالوگ) در سنجش تستوسترون آزاد بشدت خطا داشته و غلظت تستوسترون را بهمراتب کمتر از روش مرجع برآورد میکند. مطالعات مقایسهای بعدی با روش دیالیز تعادلی توسط Winters (21) این عدم یکنواختی را تأیید کرد و در سال دوهزاروهشت Fritz و همکارانش (22) مجدداً نتیجهگیری کردند که روش مبتنی بر آنالوگ قادر به سنجش FT نیست و نباید مورد استفاده قرار گیرد.
د- تستوسترون آزاد محاسبه شده. روش چهارم برای تخمین تستوسترون آزاد استفاده از فرمولی است که بهطور آنلاین در دسترس میباشد www.Issam.ch و با در اختیار داشتن تستوسترون توتال، SHBG و آلبومین میتوان مقدار تستوسترون آزاد را محاسبه نمود. در مقایسه با روش مرجع، نتایج این روش قابلقبول است (10،11). براساس نوع کیتها و روشهای مورد استفاده برای سنجش تستوسترون توتال، SHBG و آلبومین توسط آزمایشگاههای مختلف عدد بدست آمده از طریق محاسبه ممکن است متفاوت باشد. بر همین اساس لازم است که آزمایشگاهها مقدار FT محاسبهشده خود را از نظر محدوده مرجع صحهگذاری نمایند
ه- .Free Androgen Index (FAI) براساس نسبت تستوسترون توتال و SHBG محاسبه میشود. این اندکس معتبر نیست و نباید مورد استفاده قرار گیرد.
در مقایسه روشهای سنجش تستوسترون این اجماع وجود دارد که روش LC-MS/MS برتری قابلتوجهی در خصوص حساسیت و ویژگی نسبت به روشهای ایمونواسی دارد (23). متأسفانه LC-MS/MS در بیشتر مناطق به سهولت در دسترس نمیباشد.
تفسیر نتایج آزمایشگاهی
صحت روشهای آزمایش (26،25) و زمان مناسب برای نمونهگیری مهمترین عوامل فقدان اجماع در خصوص روش مناسب اثبات TDS میباشند (27). در این خصوص توجه کمتری به موضوع تغییرات بیولوژیک شده است که خود اهمیت خاصی در بررسی اختلالات استروئیدهای گنادها دارد (29،28).
تغییرات بیولوژیک
موضوع تغییرات بیولوژیک بطور مفصل در گذشته مورد تحقیق و بررسی قرار گرفته است (31،30). در اینجا کافی است اشاره کنیم که تفسیر نتایج بهطور سنتی مبتنی بر مقایسه آنها با محدوده نرمال یا فواصل مرجع بوده است. نتایج خارج از این محدودهها غیرطبیعی تلقی شده و هدف درمان این است که نتیجه را به محدوده طبیعی بازگرداند، اما باید توجه داشت که یک نتیجه ممکن است در محدوده طبیعی قرار داشته باشد اما با توجه به سابقه و شرایط بیمار طبیعی نباشد؛ بهعنوان مثال کراتینین در افراد سالم محدوده خاصی دارد اما برای یک فرد خاص در یک محدوده بسیار باریک نوسان میکند، لذا مهم است که در تفسیر نتایج یک بیمار به نوسان بیولوژیک آن تست توجه شود.
در مورد تستوسترون بندرت نتیجه اولیه آزمایش در دسترس است (نتیجه تستوسترون در زمانی که فرد سالم بود) و تکرار آزمایش در فواصل زمانی، هم به لحاظ اقتصادی و هم به لحاظ تأخیر در درمان قابلقبول نیست. دلایل مختلف نوسانات بیولوژیک در جدول 6 آمده است.
تجربیات خود ما نشان میدهد که مقدار تستوسترون در مردان سالم نهتنها بین افراد مختلف نوسانات زیادی دارد بلکه در یک فرد نیز تستوسترون صبحگاهی بیشتر از مقدار تستوسترون بعدازظهر است (22). از طرف دیگر انجام آزمایش در دو نمونه صبحگاهی (بین 7 تا 10 صبح) کفایت میکند مگر آنکه اختلاف آنها بیش از 20% باشد. درصورتیکه مقدار تستوسترون در منتهیالیه محدوده مرجع (کمتر از ng/L7 یا بالاتر از ng/L 14) باشد میتوان آن را معتبر در نظر گرفت چرا که مقادیر بالاتر یا پایینتر تغییری در تفسیر آزمایش ایجاد نمیکنند. در برخی افراد که نتیجه در حد مرز واقع شده تکرار آزمایش در همان آزمایشگاه پس از یک مدت ضرورت دارد. آزمایشگاهها باید مقادیر کاتآف یا مرزی borderline خود را با همکاری پزشکان محلی مشخص نمایند. علاوه بر این خصوصیات روش اندازهگیری در صورت درخواست پزشک باید در دسترس باشد.
علاوه بر نوسانات روزانه و نوسانات در طی زمان طولانیتر در مقدار تستوسترون، نوسان وابسته به آزمایشگاه هم موضوعی است که باید موردتوجه بیشتر پزشکان واقع گردد. روشهای اندازهگیری تستوسترون بهطور وسیع مورد بررسی و مقایسه قرار گرفتهاند. موضوع کنترل کیفی هم همیشه مورد توجه بوده و مقالات زیادی درخصوص آن نوشته شده است. پرسنل آزمایشگاهی از وجود نگرانیها در این خصوص بهخوبی آگاه هستند و اعتبار آنها در گرو توجه به این ملاحظات میباشد.
نوسانات آنالیتیکال
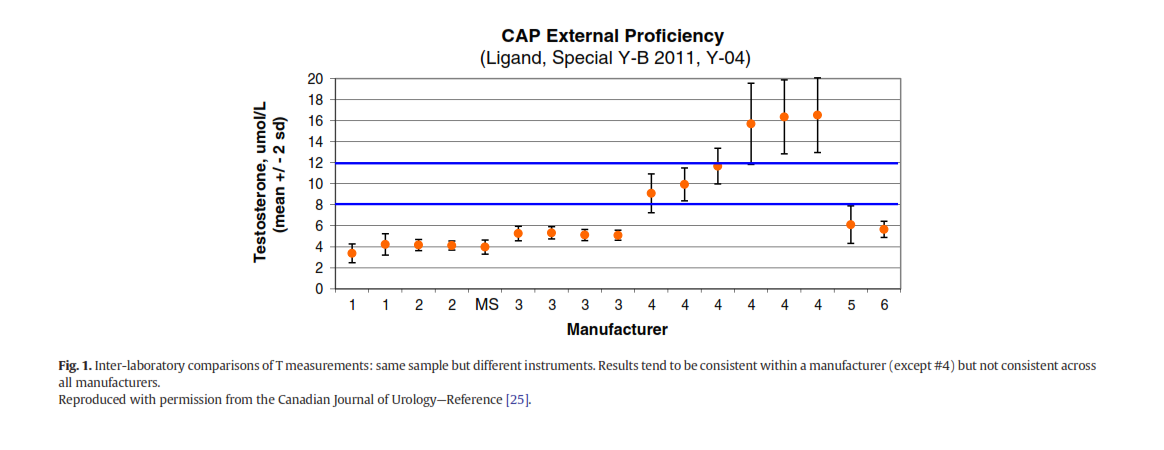
موضوع دیگری که تفسیر نتایج تستوسترون را تحت تأثیر قرار میدهد اختلافات ذاتی روشهای اندازهگیری میباشد. این اختلافات ذاتی را میتوانیم در نتایجی که کالج پاتولوژیستهای آمریکا بر اساس برنامه آزمایش مهارتسنجی خارجی خود منتشر کرده است مشاهده کنیم. در این برنامه سه نمونه با غلظتهای مختلف دو بار در طی سال بین آزمایشگاههای شرکتکننده توزیع شد. نتایجی را که در شکل 1 ملاحظه میکنید با 17 دستگاه از شش سازنده مختلف انجام شدهاند. سازندهها را فقط با شماره نشان دادهاند. بهجز سازنده شماره 4، نتایج تستوسترون در هر سازنده پایداری نشان میدهد اما الزاماً بین سازندههای مختلف همخوانی وجود ندارد (33).
معذلک محدوده مرجع جمعیت تقریباً همیشه هماهنگ میباشد، بنابراین حتی در روشهای کاملاً اتوماتیک امکان مشاهده نوسانات اندازهگیری در سنجش تستوسترون وجود دارد.
مسئله پیچیده لب مرز borderline
علیرغم تأکید بر اهمیت ارزیابی بالینی و آزمایشگاهی باید یادآور شویم که سردرگمی در تشخیص اغلب غیرقابل اجتناب است. درواقع نتایج آزمایشگاهی قاطع نظیر افزایش گنادوتروپینها بهطور همزمان با هیپوگنادیسم واضح همیشه مشاهده نمیگردد (9). گروهی از مردان با علائم کاهش تستوسترون مشاهده میشوند که مقدار تستوسترون در آنها (با دو بار تکرار یا بیشتر) (ng/dL320-230) nmol/L 8-11 میباشد که این افراد را در گروه لب مرز طبقهبندی میکنند (5). در این افراد پیشنهاد میشود که بهطور آزمایشی به مدت سه ماه تحت درمان با مکملهای تستوسترون قرار بگیرند. درصورتیکه علائم تغییر نکرد درمان با تستوسترون نباید ادامه یابد.
درمان
درمان با تستوسترون
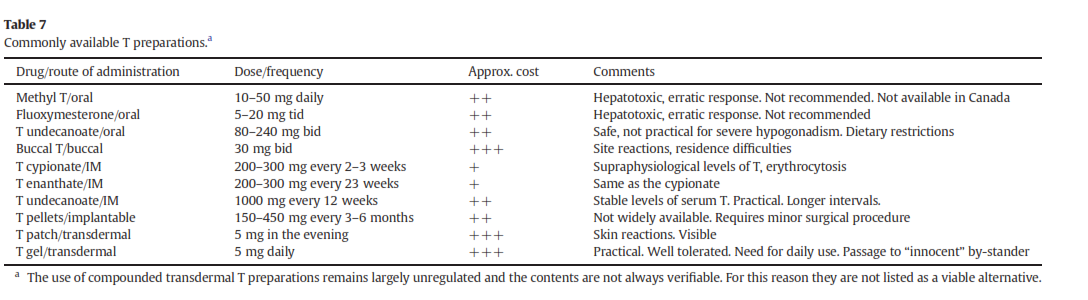
درصورتیکه تشخیص هیپوگنادیسم در فرد علامتدار مشخص شد، چنانچه موارد منع مصرف وجود نداشته باشد درمان با مکملهای تستوسترون باید آغاز شود (جدول 7).
برای انتخاب شکل دارو و طریق مصرف آن باید بین پزشک و بیمار مذاکره گردد. اشکال داروی قابلمصرف در حال حاضر شامل فرم تزریقی (طولانیمدت 3 ماهه)، خوراکی و ژلها و چسبهای جلدی میباشند. تحقیقات برای ساختن اسپری استنشاقی در حال انجام است.
هر کدام از این روشهای مصرف مزایا و معایبی دارند که پزشک معالج باید از آنها آگاهی داشته باشد. عواملی همچون ضرورت (آیا فرد واقعاً دچار کمبود تستوسترون است)، ایمنی، قیمت و موارد منع مصرف باید مدنظر باشند.
جانشین درمان با تستوسترون
همه مردانی که هیپوگنادیسم دارند الزاماً نباید با تستوسترون درمان شوند، در برخی از آنها روشهای درمانی دیگر هم مفید واقع میشوند و در برخی نیز بهطور کلی منع مصرف تستوسترون وجود دارد. تغییر شیوه زندگی بسیار مؤثر میتواند باشد (38). عدم مصرف داروهای اپوئید یک اقدام مهم است (39).
کاهش وزن و افزایش عضله را به کمک رژیم غذایی و ورزش میتوان انجام داد. اگر به هنگام خواب آپنه وجود دارد باید درمان شود.
در مردانی که هیپوگنادیسم هیپوآندروتروپیک دارند مصرف Clomiphene citrate میتواند جایگزینی برای مصرف تستوسترون باشد. گزارش شده که این دارو در افزایش تحرک اسپرم و افزایش تولید تستوسترون تأثیر داشته است (41). اخیراً ادعا شده که یک ترانــــــــسایزومر Clomiphene یعنی enclomiphene citrate واکنش بهتری نسبت به مصرف تستوسترون داشته و عوارض آن نیز کمتر بوده است (42).
نتیجهگیری
TDS یک بیماری است که همانند بیماریهای دیگر در مردان مسن همچون آب مروارید، هیپوتیروئیدیسم و آرتریت باید مورد بررسی و درمان قرار گیرد. بخاطر پیچیدگی تشخیص، تظاهرات بالینی و سنجش مقدار تستوسترون، مشکلاتی در این مسیر بروز میکند. در این خصوص باید اصل را بر سلامت گذاشت و غربالگری افراد بالای 40 سال از نظر کمبود تستوسترون و یا درمان کردن موارد کمبود تستوسترون در حالی که علامتی وجود ندارد، نباید انجام شود. گاهی ملاحظه میشود که جراید غیرتخصصی هیپوگنادیسم مردان را با یائسگی مقایسه میکنند که بههیچوجه صحیح نیست.
این مقاله ترجمهای است از:
Testosterone Deficiency Syndrome: An overview with emphasis on the
diagnostic conundrum
Alvaro Morales ⁎
Queen’s University, Kingston, Ontario, Canada
Clinical Biochemistry 47 (2014) 960–966
https://pubmed.ncbi.nlm.nih.gov/26924592/
https://medlabnews.ir/%d8%aa%d8%b3%d8%aa%d9%88%d8%b3%d8%aa%d8%b1%d9%88%d9%86/
برای دانلود پی دی اف بر روی لینک زیر کلیک کنید
ورود / ثبت نام