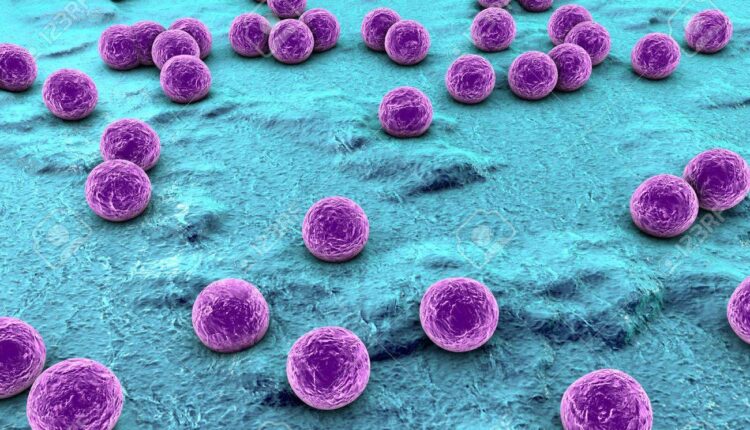
مروری تازه بر خانواده استافیلوکوکها
(یک عامل مهم ایجادکننده عفونت بیمارستانی)
دکتر رضا میرنژاد (استاد دانشگاه)
مقدمه:
خانواده استافیلوکوکاسه در سال 2010 از خانواده میکروکوکاسه که قبلاً دارای جنسهای مهم پلانوکوک، استوماتوکوک، میکروکوک، استافیلوکوک و کوکوریا (یک باکتری پاتوژن) بود، جدا گردید. این خانواده دارای جنسهای Jeotgalicoccus Macrococcus ,Nosocomiicoccus ,Salinicoccus ,Staphylococcus میباشد که تنها جنس استافیلوکوک در انسان بیماریزا میباشد.
جنس Jeotgalicoccus از ماهیها جدا شده و هالوفیل و بیهوازی اختیاری میباشد.
جنس Macrococcus کوکسی گرم مثبت بدون حرکت، بدون اسپور، بدون تیکوئیک اسید در دیواره سلولی، بدون کپسول، کاتالاز مثبت و کوآگولاز منفی میباشد. این باکتری از استافیلوکوکوس اورئوس 2 تا 4 برابر بزرگتر میباشد و مقاوم به باسیتراسین و لیزوزیم و حساس به فورازلیدون است. گونه شاخص این جنس Macrococcus equipercicus است. برای انسان بیماریزا نیست، ولی مقاومت به متیسیلین در بعضی گونههای این جنس مشاهده شده است.
جنس Nosocomiicoccus، باکتری گرم مثبت و اسموفیلیک و هالوفیل بوده و در شرایط نمکی بالا قادر به رشد میباشد. از محیط بیمارستان جدا شده، ولی برای انسان بیماریزا نمیباشد.
جنس Salinicoccus که در سال 1990 توصیف شده یک باکتری گرم مثبت میباشد که تاکنون ژنوم آن سکانس نگردیده است.
جنس پلانوکوک، کوکسی گرم مثبت، متحرک، کاتالاز مثبت است که تکتک، دوبهدو، سهتایی و چهارتایی کنار همدیگر قرار میگیرند. گونههای پلانوکوک که کوکسی موجود در دریا میباشند قادر به رشد در محیط کشت حاوی 5% NaCl میباشند. این باکتریها در انسان بندرت بیماریزا میباشند.
استوماتوکوک، کوکسی گرم مثبت، کپسولدار میباشند که بخشی از فلور نرمال دستگاه تنفسی فوقانی بوده و در افراد دچار ضعف سیستم ایمنی سبب عفونتهایی مانند اندوکاردیت، سپتیسمی و عفونتهای وابسته به کاتتر میشود. این باکتری بیهوازی اختیاری و کاتالاز منفی یا مثبت میباشد و برخلاف سایر اعضای خانواده میکروکوکاسه قادر به رشد در محیط حاوی 5% NaCl نیست و کلنیهای موکوئیدی و چسبیده به سطح آگار ایجاد میکند.
میکروکوکها کوکسیهای گرم مثبت میباشند که از باکتریهای استافیلوکوک کمی بزرگتر هستند و بهصورت جفت، تتراد و خوشههای نامنظم قرار میگیرند. میکروکوکها اغلب بهعنوان فلور نرمال پوست، پاتوژن فرصتطلب بوده و میتوانند سبب اندوکاردیت و سایر عفونتهایی که بهوسیله استافیلوکوک اپیدرمیدیس ایجاد میگردد، باشند. این باکتریها مانند استافیلوکوک کاتالاز مثبت و بدون حرکت هستند و قدرت رشد در حضور 5% NaCl را دارا میباشند. برای افتراق استافیلوکوکها از میکروکوکها و کوکوریا از جدول زیر استفاده میگردد.
جدول 1: تشخیص افتراقی جنس میکرکوک و کوکوریا از استافیلوکوکها
| ویژگی | استافیلوکوک | میکروکوک | کوکوریا |
| اکسیداز | – | + | + |
| حساسیت به باسیتراسین g/ml μ0/4 | مقاوم | حساس | حساس |
| حساسیت به gr/ml µ 200 لیزواستافین | حساس | مقاوم | مقاوم |
| حساسیت به دیسکgrµ 100 فورازولیدون | حساس | مقاوم | مقاوم |
| تولید اسید از گلیسرول در شرایط هوازی | + | – | + |
| تولید اسید از کلوگز در شرایط بیهوازی | +/- | – | + (با تأخیر) |
جنس استافیلوکوک:
استافیلوکوکها کوکسی گرم مثبت 1/5-0/5میکرومتر، بدون حرکت و بدون اسپور، بیهوازی اختیاری، کاتالاز مثبت و اکسیداز منفی میباشند که قدرت رشد در حضور 5% تا 10 درصد NaCl را دارند و معمولاً بهصورت خوشههای نامنظمی شبیه به انگور مشاهده میشوند. این باکتریها بهراحتی روی انواع محیطهای کشت رشد میکنند و از نظر متابولیکی فعال هستند، کربوهیدراتها را تخمیر کرده و رنگدانه تولید میکنند که از سفید تا زرد پررنگ متغیر است. گروهی، جزء فلور طبیعی پوست و مخاط انسان هستند و گروهی چرک، آبسه و عفونتهای چرکزای گوناگون را ایجاد میکنند و حتی منجر به بروز سپتیسمی کشنده میشوند.
استافیلوکوکهای بیماریزا اغلب خون را همولیز میکنند و پلاسما را منعقد میسازند و انواع سموم و آنزیمهای خارج سلولی را تولید میکنند. شایعترین مسمومیت غذایی توسط یک انتروتوکسین استافیلوکوکی پایدار در برابر حرارت ایجاد میشود. استافیلوکوکها بهسرعت نسبت به اغلب آنتیبیوتیکها مقاومت پیدا میکنند و مشکلات درمانی متعددی را پدید میآورند. جنس استافیلوکوک حداقل 30 گونه دارد؛ سه گونه مهم از نظر بالینی عبارتند از: استافیلوکوکوس اورئوس (طلایی)، استافیلوکوکوس اپیدرمیدیس و استافیلوکوکوس ساپروفیتیکوس.
استافیلوکوکوس اورئوس:
استافیلوکوکوس طلایی کوآگولاز مثبت است که آن را از سایر گونهها متمایز میسازد. استافیلوکوکوس طلایی (اورئوس)، عامل بیماریزای اصلی انسان و یکی از عوامل اصلی عفونتهای بیمارستانی میباشد. ساختمان آنتیژنی استافیلوکوکوس اورئوس از پپتیدوگلیکان، تیکوئیک اسید، پروتئین A، کپسول و فاکتورهای تودهایکننده یا جمعکننده یا کوآگولاز تشکیل شده است و کپسول و میکروکپسول، انواع همولیزینها، لکوسیدین پانتون والنتین، هیالورونیداز، توکسین اکسفولیاتیو و توکسین ایجادکننده شوک سمی، انتروتوکسین، استافیلوکیناز (فیبرینولیزین)، نوکلئاز، بتالاکتاماز از عوامل مؤثر در بیماریزایی (عوامل ویرولانس) این باکتری میباشند.
این باکتری انگل منحصر به فرد انسان بوده و فلور نرمال پوست، چشم، دستگاه تنفسی فوقانی، دستگاه گوارش، مجاری ادراری و بندرت واژن میباشد، به همین دلیل عفونتهای استافیلوکوکی میتواند اندوجنوس یا اگزوجنوس باشد. منابع اصلی عفونت، انتشار از ضایعات انسان، وسایل آلوده به چنین ضایعاتی و پوست و دستگاه تنفسی انسان میباشد. فاکتورهایی که در ایجاد عفونتهای استافیلوکوکی نقش دارند عبارتند از: آسیب به پوست و مخاطات، وجود اجسام خارجی در بدن مانند ایمپلنتها، ابتلا به بیماریهای ویروسی مانند سرخک و سرخجه، بیماریهای زمینهای با نقص ایمنی سلولی یا هومورال.
انتشار تماسی عفونت در بیمارستانها اهمیت بیشتری دارد؛ جایی که تعداد زیادی از کارکنان، استافیلوکوکهای مقاوم به آنتیبیوتیک را در بینی یا روی پوست خود حمل میکنند. اگرچه نظافت، بهداشت و درمان ضایعات میتواند جلوی انتشار استافیلوکوکها را بگیرد، ولی روشهای معدودی برای جلوگیری از گسترش استافیلوکوکها از حاملین در دسترس است. آئروسلها (مثل گلیکول) و پرتوی فرابنفش اثر کمی دارند. در بیمارستانها، بخشهایی که بیشترین خطر ابتلا به عفونتهای استافیلوکوکی شدید را دارند، بخش نوزادان، ICU، اتاقهای عمل و بخش شیمیدرمانی بیماران سرطانی میباشند.
ورود نژادهای بیماریزا به این بخشها به همهگیری بیماریهای بالینی جدی میانجامد. کارکنان دارای ضایعات فعال استافیلوکوکوس طلایی و حاملین آن، نباید وارد این بخشها شوند، برای چنین افرادی، به کار بردن ضدعفونیکنندههای موضعی (مثل کلروهگزدین یا کرم باسیتراسین) در بینی یا اطراف مقعد از انتشار ارگانیسمهای خطرناک میکاهد. ریفامپین همراه با یک داروی خوراکی ضداستافیلوکوکی در مدت طولانی میتواند حالت حامل بودن (در بینی) را برطرف کند. این نحوه درمان را فقط برای مواردی که مشکلات عمدهای از حامل باکتری بودن پدید آمده است، نگه میداریم، زیرا استافیلوکوکها میتوانند سریعاً به ریفامپین مقاوم شوند. ضدعفونیکنندههایی مثل هگزاکلروفن برای کاهش کلونیزاسیون استافیلوکوکها بر پوست نوزادان بهکار میروند، ولی سمیت این مواد، استفاده گسترده از آنها را محدود کرده است.
بیماری:
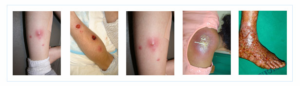
تقریباً همه انسانها در طول زندگی خود نوعی عفونت استافیلوکوکوس اورئوس را تجربه میکنند که شدت آن از یک مسمومیت غذایی یا عفونت پوستی خفیف تا عفونتهای تهدیدکننده زندگی متغیر است. اغلب بیماریهای استافیلوکوکی از پوست منشأ میگیرند. استافیلوکوک طلائی سبب عفونتهای پوستی، آبسههای زیرجلدی و زیرمخاطی، استئومیلیت، پنومونی، سپتیسمی، عفونت مجاری ادراری، اندوکاردیت، مسمومیت غذائی و انتروکولیت استافیلوکوکی، سندرم شوک سمی و غیره میشود.
شکل 1: نمایی از عفونتهای ناشی از استافیلوکوکوس اورئوس
10 تا 15 سال گذشته عفونت کسبشده از اجتماع ناشی از سویههای استافیلوکوکوس اورئوس مقاوم به متیسیلین[1] (CA-MRSA) که اغلب آنها تولیدکننده لکوسیدین پانتون والنتین (PVL) بودند نسبت به سویههای کسبشده از بیمارستان (بندرت سم لکوسیدین پانتون والنتین تولید میکنند) رایجتر بودند. سم لکوسیدین پانتون والنتین عامل نکروز شدن پوست، عفونتهای بافت نرم و گاهی اوقات پنومونی کشنده میباشند.
CA-MRSA برخلاف سویههای MRSA کسبشده از بیمارستان یا مراکز بهداشتی [2] (HA-MRSA)، اغلب به بیشتر کلاسهای غیر بتا-لاکتام آنتیبیوتیکها حساس هستند و در مقابل HA-MRSA معمولاً به تمام آنتیبیوتیکها بهجز گلیکوپپتیدها مانند وانکومایسین مقاوم میباشند. هر دوی این سویهها به دلیل داشتن ژن MecA به متیسیلین مقاوم شدند. هرچند که کاست کروموزومی ژن mecA در CA-MRSA کوچکتر از کاست کروموزومی ژن mecA در HA-MRSA میباشد و تنها با روشهای تایپینگ مولکولی میتوان اینها را از هم افتراق داد. مطالعات نشان داده است که سویه غالب CA-MRSA در ایالات متحده آمریکا USA300 است.
باکتریمی ناشی از CA-MRSA اغلب در افراد دچار دیابت، بیماری مزمن کبدی و عفونت اچآیوی شایع است، درحالیکه باکتریمی ناشی از سویههای HCA-MRSA اغلب در افراد بستری در بیمارستان که کاتتر داخل عروقی دارند، مبتلا به تومورهای جامد، نارسایی مزمن کلیوی میباشند یا قبل از بستری شدن درمان آنتیبیوتیکی شدند، شایع میباشد.
تشخیص آزمایشگاهی:
چرک آبسه، زخم، خلط، خون، ادرار، مدفوع یا مواد استفراغ شده و سوآب از بینی نمونههای ارسالی به آزمایشگاه میباشند. برای تشخیص استافیلوککها از روشهای زیر استفاده میشود:
اسمیر مستقیم: در رنگآمیزی گرم در زیر میکروسکوپ، کوکسیهای گرم مثبت بهصورت منفرد، زنجیرههای کوتاه و خوشهای مشاهده میشود. زنجیرههای استافیلوکوک بیش از پنج کوکسی نیست.
کشت: استافیلوکوکوس اورئوس روی اکثر محیطهای عمومی رشد میکند، ولی برای جداسازی از محیط بلادآگار حاوی 7/5% تا 10% NaCl و محیط تیوگلیکولات براث، TSB، کلمبیا کلستین نالیدیکسیک اسید آگار (CNA)؛ فنیل اتیل الکل (PEA) و تلوریت سستئین آگار استفاده میشود. استافیلوکوکوس اورئوس برخلاف سایر استافیلوکوکها تلوریت را مصرف و کلنی سیاه رنگ میدهد. چون این باکتری مانیتول را تخمیر میکند و مقاوم به نمک میباشد، میتوان نمونهها را مستقیماً روی محیط مانیتول سالت آگار (MSA) یا چاپمن کشت داد. این باکتری قدرت رشد روی محیط مکانکی را هم دارد.
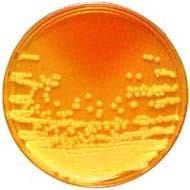
کلنی روی محیط بلادآگار بعد از 24 ساعت انکوباسیون در شرایط هوازی، بیهوازی به شکل مدور، بزرگ با سطح نرم، صاف، مرطوب، محدب به قطر 4-2 میلیمتر و با همولیز بتا میباشد (شکل 2).
شکل 2: نمای کلنیهای استافیلوکوکوس اورئوس روی محیط بلاد آگار
هنگامی که استافیلوکوکوس اورئوس در شرایط اتاق، روی محیط جامد و در شرایط هوازی کشت انکوبه میشود، کلنیهای زردرنگی ایجاد میکند که تنها در 40 درصد از آنها مشاهده میشود. نداشتن پیگمان وجود استافیلوکوکوس اورئوس را رد نمیکند.
| كليد تشخيصي استافيلوكوكوس اورئوس: كوكسي گرم مثبت، كاتالاز مثبت، اكسيداز منفي و كوآگولاز مثبت |
سؤال: در صورتی که کلنی بزرگ مخاطی با تست کاتالاز مثبت داشته باشیم، آیا قاطعانه میتوانیم آن را از استافیلوکوکها بدانیم؟
جواب: خیر چون خصوصیات کلنی مخمرها معمولاً میتواند این چنین باشد و آنها کاتالاز مثبت هم هستند.
تستهای تشخیص افتراقی:
تست کوآگولاز:
یکی از تستهای قابل اعتماد در شناسایی استافیلوکوکوس اورئوس تست کوآگولاز میباشد که به دو روش لولهای یا اسلایدی قابل اجرا است.
کوآگولاز استافیلوکوکی یک پروتئین با ترکیبات ناشناخته میباشد که فعالیت مشابه پروترومبین داشته که فیبرینوژن را به فیبرین تبدیل میکند و لخته ایجاد میشود. برای انجام تست کواگولاز از پلاسمای خرگوش یا انسان که با EDTA تهیه شده (بهصورت تجاری در فرم لئوفیلیزه قابل دسترسی میباشد) استفاده میشود. میتوان از خون تاریخ گذشته بانک خون و پلاسمای فریز شده تا دو هفته برای انجام آزمایش استفاده کرد. باید توجه داشت که در پلاسمای سیتراته بعضاً واکنش مثبت کاذب توسط برخی باکتریها از جمله استرپتوکوک فکالیس ایجاد میشود.
بیش از 95٪ از جدایههای S. aureus تست اسلایدی کواگولاز مثبت هستند که clumping factor را شناسایی میکنند و تقریباً 100٪ از همه جدایهها تست لولهای کوآگولاز که کوآگولاز آزاد را شناسایی میکند، مثبت میباشند. تست اسلایدی کواگولاز در استافیلوکوکوس لگدنسیس، استافیلوکوکوس شلفری مثبت است. در هر آزمون اسلاید باید یک کنترل از امولسیون کلنیهای مشکوک در نمک استفاده شود تا اطمینان حاصل گردد که autoagglutination رخ نداده است. اگر اتوآگلوتیناسیون رخ داد، نتایج آزمون اسلاید برای تعیین ماهیت کواگولاز طبیعی در ایزولهها نامناسب است.
استافیلوکوکوس اینترمدیوس و استافیلوکوکوس هیکوس در تست لولهای کواگولاز مثبت هستند، این دو گونه عمدتاً پاتوژن حیوانات هستند و در نمونههای انسانی بهندرت دیده میشوند.
| برای کنترل کیفی تست باید از سوشهای استاندارد استافیلوکوکوس اورئوس (کنترل مثبت) و استافیلوکوکوس اپیدرمیدیس (کنترل منفی) استفاده کرد. |
برای انجام تست لولهای چندین کلنی از باکتری را در لوله حاوی cc0/5 پلاسما که به نسبت 1/5 با سرم فیزیولوژی رقیق شده است حل کرده و در 37-35 درجه سلسیوس انکوبه نمایید. بعد از 4-1 ساعت از نظر ایجاد لخته بررسی نموده و در صورت منفی بودن آن را در حرارت اتاق انکوبه نمایید و مجدداً بعد از 18 ساعت آن را بررسی نمایید.
در روش اسلایدی بر روی لام یک یا دو کلنی را در آب مقطر یا سرم فیزیولوژی حل نمایید تا سوسپانسیون یکنواختی حاصل شود (در صورتی که سوسپانسیون یکنواختی بدست نیاید از این روش در مورد آن سوش نمیتوان استفاده کرد). در مرحله بعد یک قطره پلاسما را به کمک لوپ به سوسپانسیون افزوده و بهم بزنید. در طرف دیگر اسلاید یک قطره آب مقطر با سرم فیزیولوژی را که فقط به آن پلاسما اضافه شده بهعنوان کنترل قرار دهید. بعد از 10-5 ثانیه ایجاد تودههای لخته مانند، بیانگر مثبت بودن تست کوآگولاز اسلایدی میباشد. روش اسلایدی در بیش از 95% موارد با روش لولهای مطابقت دارد. در صورتی که تست کوآگولاز با روش اسلایدی منفی شد، باید با روش لولهای تکرار گردد.
شکل 3: نتایج مثبت و منفی تست کواگولاز لولهای
میتوان از تستهای لاتکس آگلوتیناسیون و هماگلوتیناسیون غیرفعال (پسیو) بهعنوان تست جایگزین تست کوآگولاز استفاده کرد. برای تشخیص سریع S. aureus، چندین آزمایش آگلوتیناسیون لاتکس تجاری وجود دارد. این آزمایشها پروتئین A و فاکتور clumping را تشخیص میدهند. برخی نیز پلیساکارید کپسولی را شناسایی میکنند.S. saprophyticus و S. sciuri دو گونه از گونههای استافیلوکوکی هستند که تست لاتکس آنها نیز مثبت میشود. همچنین در برخی از میکروکوکهای نادر، این تست مثبت میشود. لازم به ذکر است که در این میکروکوک ها تست اسلایدی کواگولاز منفی است.
تست کاتالاز:
بر روی لام، کلنیهای مشکوک را با لوپ پلاتینی یا شیشهای (پیپت پاستور) یا اپلیکاتور چوبی در یک قطره آب اکسیژنه 3% حل کنید. ایجاد گاز دلیل بر مثبت بودن تست است. این تست در مورد میکروکوکاسه (بهجز پلانوکوک) مثبت و در مورد استرپتوکوکاسه منفی میباشد.
شکل 3: نتایج مثبت و منفی تست کاتالاز
| نکته:
1- تشکیل حبابهای کوچک 20 تا 30 ثانیه بعد از مخلوط کردن مثبت در نظر گرفته نشود. 2- حتیالامکان برای انجام تست کاتالاز بایستی کلنیها از روی محیط بلادآگار برداشته نشود چرا که سلولهای خون دارای آنزیم کاتالاز میباشند و سبب ایجاد نتایج مثبت کاذب میگردند. |
تست تخمیر مانیتول:
استافیلوکوکوس اورئوس برخلاف استافیلوکوک کوآگولاز منفی قدرت تخمیر مانیتول را دارد. برای اجرای تست، نمونههای مشکوک را روی محیط چاپمن یا مانیتول سالت آگار (MSA) که حاوی مانیتول (1%)، 7/5% NaCl معرف فنل رد و پپتون میباشد، کشت دهید. بعد از 24-18 ساعت انکوباسیون در شرایط 37 درجه سلسیوس وجود هاله زرد رنگ اطراف کلنیها نشانه تخمیر مانیتول و تأئید استافیلوکوکوس اورئوس میباشد. باید توجه داشت که استافیلوکوکوس اورئوس جداسازیشده بایستی با تست کوآگولاز تأئید قطعی شود.
شکل 4: کلنیهای با هاله زرد رنگ استافیلوکوکوس اورئوس روی محیط مانیتول سالت آگار
تست DNase:
بعضی از استافیلوکوکوس اورئوسها در تست کوآگولاز دارای واکنش ضعیف یا منفی هستند، لذا برای شناسایی این سویهها از تستDNase استفاده میشود. برای اجرای این تست، کلنی استافیلوکوکوس اورئوس را روی محیطDNase که به دلیل داشتن معرف تولوئیدین بلو آبی رنگ میباشد، کشت داده و بعد از 24 ساعت انکوباسیون، هاله شفاف اطراف کلنی را بررسی نمایید. اگر هاله اطراف کلنی مشاهده گردید، تست مثبت میباشد که به دلیل تجزیه DNA توسط آنزیم DNase استافیکوکوک اورئوس است.
تست حساسیت به باسیتراسین و فورازولیدون:
تمام استافیلوکوکها برخلاف میکروکوکها نسبت به باسیتراسین 4% واحد مقاوم هستند و تمام استافیلوکوکها برخلاف میکروکوکها نسبت به فورازولیدون (FX) 100 میکروگرم واحد حساس میباشند. برای انجام این تست ابتدا کلنیهای مشکوک را به یک میلیلیتر محیط تریپتیکاز سوی براث منتقل کرده و کدورتی معادل 0/5 مک فارلند ایجاد نمایید. با استفاده از سوآب پنبهای از محلول قبلی روی محیط مولر هینتون یا تریپتیکاز سوی آگار یا بلادآگار مانند انجام تست آنتیبیوگرام در سه جهت کشت داده شود. یک دیسک TaxoA باسیتراسین 4% واحد و یک دیسک فورازولیدون (FX) 100 میکروگرم را در سطح پلیت قرار دهید.
بعد از 18 ساعت انکوباسیون در شرایط 35 درجه سلسیوس، هرگونه وجود هاله را مورد بررسی قرار دهید. استافیلوکوکها در اطراف دیسک باسیتراسین رشد میکنند ولی میکروکوکها رشد نمیکنند و معمولاً هالهای به قطر بیش از 10 میلیلیتر ایجاد مینمایند. برعکس میکروکوکها در اطراف دیسک فورازولیدون رشد میکنند و یا هالهای عدم رشد کمتر از 9 میلیمتر ایجاد مینمایند ولی استافیلوکوکها حساس به فورازولیدون میباشند و هالهای به قطر بیش از 15 میلیمتر ایجاد میکنند.
سایر تستهای تأئیدی استافیلوکوکوس اورئوس:
تکنیکهای مولکولی مانند DNA پروب و PCR با حساسیت و اختصاصیت بالای 95 درصد برای شناسایی استافیلوکوکوس اورئوس در بعضی از آزمایشگاههای پیشرفته انجام میشود.
آنتیبیوگرام:
به علت شیوع بالای نژادهای مقاوم، باید تمام نمونههای اسافیلوکوکی مشکوک را حتماً از نظر حساسیت آنتیبیوتیکی بررسی کرد تا به یافتن درمان انتخابی کمک شود. آنتیبیوتیکهای مورد استفاده جهت آنتیبیوگرام:
- Penicillin (10 unit/disk): بیش از 80% از استافیلوکوکهای طلائی به پنیسیلین مقاومند.
- Oxacillin (30 μg)
- Erythromycin (15 μg)
- Sulfamethoxazole (23.75 μg), Trimethoprim (1.25 μg)
- Clindamycin(2 μg)
- Augmentin (30 μg)
- Fusidic acid (10 μg). در آنتیبیوگرام ادرار بجای آن باید از Novobiocin (5 μg) استفاده نمود.
در عفونتهای موضعی (جلدی، چشمی و غیره) بجای Erythromycin ,Cotrimoxazole از Neomycin(30 μg) ,Chloramphenicol(30 μg) استفاده میشود.
استافیلوکوکهای تولیدکننده بتالاکتاماز ممکن است هاله نسبتاً بزرگی اطراف دیسک پنیسیلین یا آمپیسیلین ایجاد نمایند، ولی رشد باکتری در مرز تلاقی آنها با هاله عدم رشد بهصورت کپهای و برجسته میباشد، درحالیکه در سوشهای حساس این حالت وجود ندارد و مرز رشد بهصورت لبه نازکی مشاهده میشود. باکتریهایی که رشد آنها به فرم اول میباشد علیرغم وجود هاله عدم رشد باید مقاوم تلقی شوند.
استافیلوکوکهای مقاوم به متیسیلین اغلب در روش معمول آنتیبیوگرام حساس تلقی میشوند، برای تعیین حساسیت به متیسیلین باید از محیط کشت نوترینت آگار به اضافه 6% NaCl استفاده نمود یا اگر متیسیلین را در محیط معمول آنتیبیوگرام به همراه سایر آنتیبیوتیکها بررسی میکنید، پلیت در 34-32 درجه سانتیگراد انکوبه شود. نتیجه حساسیت به متیسیلین را میتوان به گلوکزاسیلین، فلوگلوکزاسیلین، اگزاسیلین و بیشتر سفالوسپورینها تعمیم داد. بیشتر استافیلوکوکها به وانکومایسین، ریفامپین و موپیرویسن حساس میباشند.
مطالعات مختلف نشان میدهد، بیش از 90٪ از استافیلوکوکها به دلیل داشتنβ-lactamase القائی کدکننده پلاسمیدی به پنیسیلین مقاوم هستند، به همین دلیل تست -βلاکتامازهای کروموژنیک (مانند آزمون دیسک نیتروسیفن) یا تست دیسک دیفیوژن پنیسیلین طراحی شدهاند. استافیلوکوکها حساسیت بالایی به دیسک نیتروسفین دارند. هنگامی که β-lactamase مثبت باشد، حتی اگر در تست دیسک نیتروسفین منفی شده باشند، جدایهها باید بهعنوان مقاوم به پنیسیلین گزارش شوند. اگر پنیسیلین در درمان عفونتهای شديد S. aureus مورد توجه قرار میگیرد، بايد يک تست دیسک دیفیوژن و یا تعیین MIC براي تأييد انجام شود؛ MIC پنیسیلین از 0/12 یا کمتر بهعنوان حساس تعریف میشود (CLSI 2014).
مقاومت به پنیسیلینهای مقاوم به پنیسیلیناز (متیسیلین، اگزاسیلین و نفیسیلین) در بیش از 80٪ از استافیلوکوکهای منفی کواگولاز منفی و در بیش از 50٪ از جدایههای S. aureus کسبشده از بیمارستان بهدست میآید. مقاومت به این گروه از عوامل ضدمیکروبی ناشی از وجود ژن mecA که کدکننده PBP-2a میباشد، است. مقاومت معمولاً هترجنوس است؛ به این معنی که یک سلول در 104 تا 108 سلول مقاومت نشان میدهد. امروزه برای شناسایی این گونه مقاومت، دیسک اگزاسیلین توصیه نمیشود و بهجای آن تست دیسک سفوکستین 30 میکروگرم بایستی استفاده گردد. برای پیشگویی وجود ژن mec A در استافیلوکوکوس اورئوس یا استافیلوکوکوس لگدنسیس CLSI توصیه میکند که ایزولههای با قطر 22 میلیمتر یا بزرگتر بهعنوان حساس (S) و با قطر 21 میلیمتر یا کمتر مقاوم در نظر گرفته شوند.
در استافیلوکوکهای کواگولاز منفی، قطر 25 یا بالاتر حساس و کمتر از 24 میلیمتر مقاوم میباشند (CLSI 2014). در تست میکرودایلوشن اگزاسیلین در محیط مولر هینتون براث کاتیوندار (حاوی 2٪ NaCl) استفاده میگردد و باید 24 ساعت کامل در 35 درجه سلسیوس انکوبه گردد. در گزارشدهی بایستی برای اگزاسیلین نه سفوکستین نتایج ارائه گردد. هرگونه رشد در محيط غربالگري، MRSA را نشان میدهد و براي تأييد بايد تستهای مولکولی بيشتري مانند بررسی وجود ژن mec A انجام شود. ژن mec C با روشهای شناسایی ژن mec A شناسایی نمیگردد و باید با روشهای شناسایی PBP2a ارزیابی گردند.
جهت استافیلوکوکهای کواگولاز منفی (CNS) به غیر از S. lugdenensis، یک تست میکرودایلوشن برای اگزاسیلین بکار میرود که در این تست رقت کمتر از 0/25 میکروگرم در میلیلیتر حساس در نظر گرفته میشود. اگر تست دیسک دیفیوژن استفاده میشود قطر بیشتر از 25 میلیمتر حساس در نظر گرفته میشود. اگر گونههای کواگولاز منفی غیر از استافیلوکوکوس اپیدرمیدیس دارای MIC0/5 تا 2 میکروگرم در میلیلیتر برای اگزاسیلین بودند، بایستی تستهای شناسایی mecA یا PBP2a برای تأئید مقاومت انجام شود.
امروزه چند روش سریع برای شناسایی مقاومت به اگزاسیلین استفاده میشود مانند PCR، پروب اسی برای ژن mec A و لاتکس آگلوتیناسیون برای PBP2a و PBP2. برای تشخیص مستقیم MRSA در سوآب بینی، از دو روش میتوان استفاده کرد: استفاده از محیط کروموژنیک اختصاصی و انکوباسیون 24 ساعته و استفاده از کلنیهای اختصاصی رنگشده. این روشها نسبت به روشهای مولکولی حساسیت کمتری دارند، ولی ارزانتر میباشند.
امروزه میتوان از روشهای مولکولی مختلف زیر، MRSA را بهطور مستقیم در نمونههای بالینی (سوآبهای بینی، کشت خون و دیگر موارد) در طی 90 دقیقه شناسایی کرد:
Gene-Ohm (Becton Dickinson Microbiology Systems، Sparks،
MD)، Xpert MRSA (Cepheid و Sunnyvale. هر دوی Gene-OHM و Cepheid برای تشخیص S. aureus و MRSA در نمونههای بالینی و از کشت خون مثبت استفاده میشوند. مطالعات نشان میدهد که استافیلوکوکهای مقاوم به اگزاسیلین ممکن است ظاهراً حساس به سفالوسپورینها باشند که در این صورت باید نسبت به تمام عوامل بتا-لاکتام (پنیسیلین، سفالوسپورینها و کرباپنمها) مقاوم در نظر گرفته شوند. اصولاً سویههای کسبشده از بیمارستان معمولاً مقاوم به بسیاری از آنتیبیوتیکهای غیربتا-لاکتام نیز میباشند و تعدادی از سویههای CA-MRSA همچنان برای بسیاری از آنتیبیوتیکهای غیربتا-لاکتام حساس باقی ماندهاند.
کلیندامایسین ممکن است برای درمان عفونت استافیلوکوکی استفاده شود. مقاومت به این آنتیبیوتیک ناشی از وجود ژن erm میباشد که آنزیمهای غیرفعالکننده این آنتیبیوتیک را کد میکند. این مقاومت توسط تستهای روتین حساسیت شناسایی نمیشود. این ژن erm مقاومت متقاطع به ماکرولیدها (بهعنوان مثال، اریترومایسین) و استرپتوگرامینها (Quinupristin-dalfopristin) را نیز کد میکند. اگر جدایـــــهای از S. aureus به اریترومایسین مقاوم، اما حساس به کلیندامایسین هستند بایستی با تست D-zone مقاومت القائی به کلیندامایسین در آنها بررسی شود.
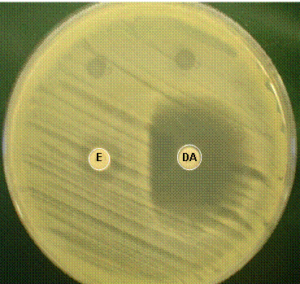
در این تست از دیسکهای اریترومایسین 15 میکروگرمی و کلیندامایسین 2 میکروگرمی با فاصله 15 میلیمتر از یکدیگر روی بلاد اگار استفاده میگردد. پس از انکوباسیون شبانه، اگر مقاومت القاشده به کلیندامایسین وجود داشته باشد، هاله عدم رشد در اطراف دیسک کلیندامایسین در کنار دیسک اریترومایسین با ظاهر D مشاهده میگردد. استافیلوکوکوس اورئوس در 20-5 درصد موارد به اریترومایسین، لینکومایسین و کلیندامایسین مقاوم است (شکل 5).
هرچند مقاومت به وانکومایسین بهندرت در S. aureus دیده میشود، ولی یک مسئله جدی است که آزمایشگاهها باید از آن آگاهی داشته باشند و بایستی آن را بررسی نمایند. سویههای با حساسیت واسط به وانکومایسین VISA)) دارای MICs بین 8-4 میکروگرم در میلیلیتر میباشند، ولی تعدادی از سویههای مقاوم به وانکومایسین با MIC بالای 1024 میکروگرم در میلیلیتر گزارش شده است. برای جداسازی سویههای مقاوم به وانکومایسین باید 100 میکرولیتر سوسپانسیون 0/5 مکفارلندS. aureus روی محیط BHI آگار حاوی 6 میکروگرم بر میلیلیتر وانکومایسین کشت داده شده و به مدت یک شبانهروز در 35 درجه سلسیوس انکوبه گردد.
اگر حتی یک کلنی هم رشد کرد این نشاندهنده کاهش حساسیت باکتری به وانکومایسین میباشد و باید MIC آن تعیین گردد. اگر MIC 4 میکروگرم در میلیلیتر مشاهده شد بایستی توسط تستهای میکرودایلوشن تأئید شود، ولی اگر MIC بالای 8 میکروگرم در میلیلیتر یک ارگانیسم هم مشاهده شد بایستی ایزوله به آزمایشگاه مرجع ارسال گردد.
جداسازی و تشخیص hVISA (سویههای از S. aureusکه در داخل جمعيت يا کلنیهای مقاوم به وانکومايسين مشاهده میشوند) بهصورت روزمره در آزمایشگاه ميکروبيولوژي کاری دشوار است. اگر یک سویه با MIC2 میکروگرم بر میلیلیتر به وانکومایسین در نظر گرفته میشود، بایستی برای آن سوسپانسیون 2 مکفارلند بهجای 0/5 مکفارلند انجام داد و کلنیهای موجود در مرکز هاله عدم رشد بیشتر ارزیابی شوند. برای جداسازی hVISA باید غلظت آنتیبیوتیک وانکومایسین را افزایش داد.
عوامل آنتیبیوتیکی جدیدی که برای درمان عفونتهای ناشی از استافیلوکوکهای مقاوم بکار میروند عبارتند از: Quinupristin /Dalfopristin، Streptogramin؛ لیپوپپتید Daptomycin؛ لینزولید؛ Televancin و سفترولین. سفترولین تنها سفالوسپورین است که جدایههای MRSA به آن حساس هستند. برای جداسازی VISAیا VRSA و یا زمانی که پزشکان نیازمند تجویز غیر از وانکومایسین هستند باید آزمایشگاهها این آنتیبیوتیک را مدنظر داشته باشند یا اینکه نمونهها را به آزمایشگاههای مرجع که میتوانند این تستها را انجام دهند، ارسال نمایند.
شکل 5: شمای کلی از نتیجه تست D-zone
آزمایشهای سرولوژیک و تعیین تیپ
ارزیابی آنتیبادی ضد اسیدتیکوئیک در عفونتهای شدید طولانی مدت (مانند اندوکاردیت) مفید میباشد.
امروزه از تکنیکهای تعیین تیپ مولکولی (Molecular Typing) برای اثبات انتشار دودمانهای ایجادکننده بیماری استافیلوکوکوس اورئوس استفاده میشود. در آزمایشگاههای مرجع برای اهداف اپیدمیولوژیکی و تعیین منشأ آلودگی از تستهای حساسیت به باکتریوفاژهای مختلف، پروفایل پلاسمیدی، اسیدهای چرب سلولی، الکتروفورز آنزیم چند لوکوسی و یا تایپینگ مولکولی کروموزومی (پالس فیلد ژل الکتروفورزیس یا Rep-PCR) استفاده میگردد.
استافیلوکوکوس کوآگولاز منفی (CoNS)
عفونتهای ناشی از گونههای استافیلوکوکوس کوآگولاز منفی (CoNS) معمولاً در افرادی که ایمپلنت دریچه قلبی، مفاصل و شانت دارند مشاهده میگردد. تشکیل بیوفیلم و مقاومت به آنتیبیوتیک در ایجاد باکتریمی و ادهسینهای خاص در ایجاد عفونتهای مفاصل نقش دارند. ارتباط با اجسام خارجی، دریچه مصنوعی بهویژه کاشت مفاصل و شنت رخ میدهد.CoNS ها یکی از عوامل شایع مرتبط با عفونت شنت CSF میباشند. این عوامل بندرت سبب عفونت ادراری، پنومونی و نکروز پوستی میشوند. استافیلوکوکوس همولیتیکوس برخلاف سایرCoNS ها مقاوم به وانکومایسین میباشد. S. lugdunensis از نظر مورفولوژیکی شبیه به استافیلوکوکوس اورئوس بوده (همولیز β با قطر کم ایجاد میکند) و گاهی اوقات کوآگولاز مثبت میباشد. این باکتری سبب آندوکاردیت و استئومیلیت میگردد و نسبت به سایر CoNSها تهاجمیتر است. در آزمایشگاه برای افتراق آن از سایر CoNSها بایستی تست حساسیت به اگزاسیلین (سفوکسیتین) که برای استافیلوکوکوس اورئوس استفاده میشود نه برای سایر CoNSها، انجام شود.
استافیلوکوک اپیدرمیدیس:
این باکتری بخشی از فلور طبیعی بدن انسان (اغلب در پوست) میباشد و در بیماران بستری، افرادی که قطعات مصنوعی (مانند دریچه قلبی) در بدن خود دارند و در افرادی که دچار نقص ایمنی هستند، ایجاد سپتیسمی، اندوکاردیت، عفونت مجاری ادراری، استئومیلیت، عفونت چشمی، عفونت در نوزادان، عفونت جلدی و مننژیت مینمایند.
به دلیل تشکیل بیوفیلم، مقاومت دارویی در سوشهای مختلف آن بهخصوص سوشهای بیمارستانی بیشتر است. بیشتر سوشها به پنیسیلین، آمپیسیلین، متیسیلین و گلوکزاسیلین مقاومند. حساسیت نسبت به سفالوسپورینها، جنتامایسین، فوزیدیک اسید و بهویژه وانکومایسین، ریفامپین و سیپروفلوکساسین زیاد است هرچند که نسبت به وانکوماسین مقاومت مشاهده شده است. سوشهایی که نسبت به اگزاسیلینها مقاومت نشان میدهند (با همان روشی که برای استافیلوکوکوس اورئوس ذکر شد) میبایست در برابر کلیه سفالوسپورینها مقاوم تلقی شوند.
استافیلوکوکوس اپیدرمیدیس یا استافیلوکوک با کلنیهای سفید کوآگولاز منفی بوده و بندرت همولیز بتا تولید میکند. در شناسایی آن از دیسکهای پلیمیکسین B و نووبیوسین استفاده میشود که این باکتری مانند استافیلوکوکوس اورئوس به پلیمیکسن مقاوم و به نووبیوسین حساس میباشد (جدول 2).
استافیلوکوک ساپروفیتیکوس:
استافیلوکوکوس ساپروفیتیکوس فلور طبیعی موقت پوست و اطراف مجاری ادراری میباشد و یکی از عوامل اصلی ایجادکننده عفونتهای ادراری (سیستیت و پیلونفریت) در خانمهای جوان با فعالیت جنسی بالا میباشد. این باکتری کوآگولاز منفی بوده و همانند استافیلوکوکوس اپیدرمیدیس همولیز بتا تولید نمیکند و برخلاف استافیلوکوکوس اورئوس و اپیدرمیدیس حساس به پلیمیکسین B و مقاوم به نووبیوسین میباشد، همچنین این باکتری به فلورکینولونها و تریمتوپریم- سولفومتاکسازول حساس میباشد (جدول 2).
تست سریع حساسیت به نووبیوسین:
به دو لوله حاوی 3 میلیلیتر تریپتیکاز سوی براث از سوش مشکوک تلقیح کنید، بهنحوی که هیچ کدورت محسوسی ایجاد نشود، سپس در یکی از لولهها یک دیسک نووبیوسین (μg5) انداخته و ده ثانیه بهم بزنید. لوله را به مدت 5 ساعت (یا تا زمانی که لوله کنترل کدورتی معادل 0/5 مکفارلند بیابد) انکوبه نمایید. در صورتی که کدورت هر دو لوله یکسان بود، باکتری مورد آزمایش استافیلوکوکوس ساپروفیتیکوس است و اگر در لوله محتوی آنتیبیوتیک رشدی مشاهده نشود، استافیلوکوکوس اپیدرمیدیس میباشــــــد. لازم به ذکر است که S. lugdenensis هم مقاوم به نووبیوسین میباشد.
جدول 2: تشخیص افتراقی استافیلوکوکهای بیماریزا در انسان
| صفات بیوشیمیایی | استافیلوکوکوس اورئوس | استافیلوکوکوس اپیدرمیدیس | استافیلوکوکوس ساپروفیتیکوس |
| حساسیت به نووبیوسین | + | + | _ |
| حساسیت به پلیمیکسین | + | + | _ |
| تست کوآگولاز | + | _ | _ |
| هیدرولیز قند مانیتول | + | _ | +_ |
| DNase | + | _ |
[1] Community-Associated Methicillin-Resistant Staphylococcus aureus (CA–MRSA)
[2] Healthcare-acquired methicillin-resistant Staphylococcus aureus(HA-MRSA)
استافیلوکوکوس مقاوم به متیسیلین (MRSA)
نکات مهم کاربردی در میکروبشناسی بالینی (1)
برای دانلود پی دی اف برروی لینک زیر کلیک کنید
ورود / ثبت نام