کاهش 70 درصدی خطاهای آزمایشگاهی با دانستنیهای قبل از آنالیز
دکتر حبیب اله گل افشان، عضو هیئت علمی دانشگاه علوم پزشکی شیراز
قسمت دوم
خونگیری ویژه:
ناشتا بودن بیمار و اینکه آیا بیمار در متابلیزم پایه است بایستی توسط خونگیر تشخیص داده شود. به این مفهوم که بیمار در 12 ساعت گذشته از خوردن و نوشیدن بجز آب خودداری کرده و ورزش نداشته است. نبودن ناشتا روی آزمایشهای چربی و آزمایشهای تعيين ریسک قلبی اثر فراوان دارد. ناشتا بودن طولانی مدت موجب افزایش بیليروبین، تریگلیسرید و کاهش شدید قند میشود.
برای آزمایش GTT (تست تحمل گلوکز) بیمار بایستی 12 ساعت و نه بیش از 16 ساعت از خوردن و نوشیدن بجز آب خودداری کند، نوشیدن قهوه و چای تلخ و آدامس بدون شکر و سیگار موجب تحریک گوارش و غیر مطمئن شدن تست میشود، از این رو قبل و در حین آزمایش از خوردن این مواد اجتناب کند.
آزمایش قند دو ساعته برای مقایسه قند ناشتا با قند خون بعد از 2 ساعت از خوردن ماده قندی است که معادل 100 گرم گلوکز داشته باشد.
در حالت ایدهآل مقدار قند 2 ساعته به حدود قند ناشتا میرسد و در هر حال کمتر از 140 mg/dl نرمال است. برای انجام تست بیمار بایستی از دو روز قبل غذای سرشار از کربوهیدارت مصرف كرده باشد.
تست تحمل گلوکز برای تشخیص دیابت (هیپرگلیسمی) و یا برای تشخیص علت کاهش قند خون (هیپوگلیسمی) در بیماری که علائم کاهش قند خون را نشان میدهد بکار میرود. جمعآوری نمونه خون در فواصل زمانی 1 و 2 و 3 ساعت و گاهي هر ساعت تا 6 ساعت بعد از خوردن مقدار مشخص گلوکز برای مثال 100 گرم گلوکز طعمدار (گلوکولا) یا یک گرم به ازای هر کیلوگرم در بچهها انجام میگیرد. نوشیدنی گلوکز را بایستی حداکثر در ظرف 5 دقیقه نوشید و پس از پایان نوشیدن زمان یادداشت میگردد. قبل از نوشيدن، یک آزمايش قند خون ناشتا از بیمار گرفته میشود و سفارش میگردد که قبل از نوشیدن محلول گلوکز مقدار قند ناشتا اندازهگیری شود که آیا بیمار تحمل گلوکز خوراکی برای تست دارد یا خیر؟
استفراغ به ویژه در اوایل نوشیدن ميتواند تست را غیر قابل قبول کند و چنانچه مدتی بعد از نوشیدن رخ دهد بایستی پزشک را در جریان قرار داد که آیا روند آزمایش ادامه یابد یا خیر.
نمونهها بایستی بر مبنای زمان نمونهگیری برای مثال ناشتا یا نیم ساعت بعد از نوشیدن گلوکز يا یک ساعت، 2 ساعت و … علامت گذاری شود و چنانچه تأخیر در انجام آزمایشها باشد از لوله با سرپوش رنگی خاکستری برای نمونهگیری استفاده شود که حاوی فلوراید سدیم بوده و تا 3 روز از مصرف گلوکز توسط باکتریها و گلبولها جلوگیری کرده و مانع افت قند میگردد.
به بیمار بایستی آموزش داده شود که از سه روز قبل از انجام تست از غذای پر کربوهیدرات که حداقل حاوی 150 گرم کربوهیدرات باشد استفاده کند. سفارش میشود که در فواصل بین نمونهگیری بیمار در اتاق انتظار باشد و از خوردن و نوشیدن بجز مقداری آب در صورت نیاز خودداری کند. سیگار و چای تلخ محرک گوارش بوده و تست را غیر قابل اطمینان میکنند. برخی از داروها موجب تداخل در تست تحمل گلوکز شده که در صورت مصرف بایستی پزشک مطلع گردد که در این میان میتوان به الکل، داروهای ضد تشنج، آسپرین، قرصهای ضد حاملگی، داروهای ضد پرفشاری، استروئیدها و مدرها اشاره کرد.
تغییرات روزانه (Diurnal variation)
پارامترهای خونی مانند گلوکز، کرتیزول، تستسترون، پروژسترون، رنین، هورمون محرک تیروئید (TSH)، آهن سرم و گلبولهای سفید خون به ویژه ائوزینوفیل دارای نوسان مقدار در طول روز هستند و برخی از این تغییرات بسیار چشمگیر است؛ برای مثال کرتیزول نمونه خون که در ساعت 8 تا 10 صبح جمع آوری شده دو برابر مقداری است که در ساعت 4 عصر جمعآوری شده باشد و یا آهن سرم در صبح 30% بیشتر از غروب است. تعداد ائوزینوفیلهای خون نسبت عکس با میزان کرتیزول دارد.
پیگیری سطح دارویی (Therapeutic drug monitoring)
سطح بعضی از داروها برای مؤثر بودن دوزاژ درمانی و حفظ سلامتی بیمار اندازهگیری میشود که برای مثال میتوان به داروهایی مانند دیجوکسین، پروکائین آمید، والپوریک اسید، دیلانتین و تئوفیلین اشاره کرد. گرچه برای پیگیری سطح دارویی در غالب موارد نمونه اتفاقی گرفته میشود ولی پایش سطح در 30 دقیقه قبل از دریافت دوزاژ بعدی (Trough level) و زمان رسیدن سطح دارو به اوج خود (peak level) ارزیابی بهتری بدست میدهد.
کشت خون
از کشت خون برای تشخیص سپتيسمی در بیمار تبدار استفاده میشود. نمونه خون برای کشت معمولا ًبه صورت 2تایی (Two set) به فاصله نیم تا یکساعت یا قبل از اوج تب در بیمار گرفته میشود. چنانچه شروع درمان با آنتی بیوتیک فوری باشد میتوان نمونه 2تایی را همزمان از دو محل جداگانه تهیه کرد. با تهیه نمونه خون از محلهای مختلف در یک زمان و کشت آنها میتوان میکروب عامل بیماری (پاتوژن واقعی) را از آلوده کنندههای پوستی (Contaminant) افتراق داد. میکروبهای فلور پوستی زمانی به عنوان پاتوژن قلمداد میگردد که کشت مثبت از دو محل نمونهگیری جداگانه مشاهده شود.
نمونه خون را میتوان مستقیماً به بطری کشت خون اضافه کرد و یا اینکه نخست خون را در لوله مخصوص با سرپوش زرد که حاوی ضد انعقاد است ریخت و سپس در آزمایشگاه به محیط کشت اضافه کرد. ضد انعقاد (Sodium polyanethol sulfonate) با خواص ضد فاگوسیتوز، ضد کمپلمــان و بازدارنده برخی از آنتیبیوتیکها نه تنها ویژگی ضد لختگی دارد بلکه کمک به رشد میکروبها میکند. لخته شدن خون با به دام انداختن میکروبها مانع از رشد آنها میگردد. برخی از محیطهای کشت دارای رزينهایی جهت جذب آنتیبیوتیکها میباشند. ابتدا نمونه خون را به بطری کشت غیرهوازی اضافه کنید. قبل از نمونهگیری بایستی محل خونگیری را کاملاً استریل کرد تا فلورهای پوستی نمونه را آلوده نکنند.
برای این منظور محل خونگیری را با الکل ایزوپروپیل برای 60 ثانیه با مالش محکم ضدعفونی کنید. سپس محل را از مرکز خونگیری به طرف خارج دایرهوار تا 3 الی 4 اینچی با یک لایه از پوویدون ایدوین (Povidone- Iodine) یا 2 درصد ایودین (Iodine) بپوشانيد و اجازه دهید تا یک دقیقه روی محل باقی بماند. برای جلوگیری از تحریک پوستی لایه ید را با استفاده از الکل بعد از اتمام نمونهگیری پاک کنید. در موارد حساسیت به ید میتوان از ضد عفونی کنندههای کلرهگزیدین ایزوپروپیل الکل استفاده کرد. چنانچه احتیاج به حس کردن رگ ناحیه باشد بایستی انگشت را مطابق روش فوق ضدعفونی کرد. سر بطری کشت را قبل از اضافه کردن نمونه خون بایستی ضد عفونی کرد و برای این منظور استفاده از ایزوپروپیل الکل 70% کافی است. محلول ید نبایستی روی سر بطری باقی بماند چون امکان ورود به محیط کشت در هنگام اضافه کردن نمونه دارد.
برای کشت خون معمولاً یک ست نمونه به بطری کشت هوازی و دیگری به بطری کشت غیرهوازی اضافه میشود. وقتی که با سرنگ نمونه را به بطری کشت اضافه میکنید نخست نمونه را به بطری غیرهوازی اضافه کنید و چنانچه در روش نمونهگیری حبابهای هوا وجود دارد اول نمونه را به بطری هوازی اضافه کنید. رعایت کردن نسبت یک به ده (حجم خون به محیط کشت) اساسي است. حجم کم موجب منفی کاذب و حجم بیش از حد خون موجب مثبت کاذب در برخی از سیستمهای اتوماتیک تشخیصی میشود. بطری کشت را قبل از اضافه کردن نمونه برای حجم مورد نیاز مطالعه کنید. برای نوزادان بطریهای مخصوص وجود دارد و در غالب موارد یک سیسی خون برای اطفال کمتر از 5 کیلو به محیط کشت اضافه میشود.
نمونههای حساس به نور
تابش نور به لوله آزمایش موجب کاهش بیلیروبین، بتاکاروتین، اسید فولیک، ویتامینهای B6 ,B12 ,A و پورفیرینها میگردد. لولههای آزمایش در پوشش یک ورق آلومینيوم یا در کیسه کهربایی رنگ به آزمایشگاه منتقل میشود.
انتقال نمونه با پوششی از ورقه آلومینوم
تهیه نمونه خون در شرایط گرم (رعایت زنجیره گرم)
آزمایشهای تعیین عیار آگلوتینین سرد (Cold agglutinin) و کرایوگلوبولین و کرایو فیبرینوژن نیاز به خونگیری در شرایط گرم دارند؛ بدین مفهوم که لولههای آزمایش را از قبل بمدت 30 دقیقه در 37 درجه گذاشته و در حوله گرم به اتاق بیمار منتقل میكنند. بهتر است که دست بیمار هم با حوله گرم داغ شود.
به محض خونگیری، لوله آزمایش در حوله گرم یا در دست مشت بسته سریع به آزمایشگاه منتقل میشود. آزمایشگاه لولهها را در 37 درجه گذاشته تا خون لخته شود، سپس در سانتریفوژ گرم شده، با حوله داغ سرم از سلول جدا و در لوله دیگری ریخته میشود و سپس مورد آزمایش قرار میگیرد.
برای آزمایشهای فوق چنانچه شرایط زیر 37 درجه برسد آگلوتینینهای سرد یا کرایوگلوبولین روی گلبولهای قرمز رسوب کرده و تست منفی کاذب میشود. از لولههای ژلدار نیز نبایستی برای آزمایشهای فوق استفاده شود.
قرار دادن نمونه خون در سرما (رعایت زنجیره سرد)
آزمایش گازهای خونی، آمونیاک، استون، اسیدهای چرب، اسید لاکتیک، پیرووات، گلوکاگون، گاسترین، هورمون محرک آدرنال (ACTH)، هورمون پاراتیروئید، رنین، آنزیم تبدیل کننده آنژیوتانسین (ACE)، کاتکول آمینها، هموسیستین و اندازهگیری برخی از فاکتورهای انعقادی مانند 5 و 8 نیاز به رعایت زنجیره سرد دارند؛ بدین مفهوم لوله حاوی نمونه در ظرف حاوی یخ خرد شده همراه با آب قرار میگیرد. قرار دادن لوله آزمایش در تکههای یخ به علت اینکه سرما یکنواخت پخش نمیشود قابل قبول نیست.
انتقال نمونه با رعایت زنجیره سرد
تهیه نمونه در ارتباط با جرایم (Legal specimen)
اندازهگیری مواد مخدر، الکل، داروها و آنالیز DNA چنانچه در ارتباط با جرایم باشد را بایستی به طور مستند در حضور شاهد و مأمور قانون نمونهگیری کرد. مستنداتی مانند عکس و اثر انگشت به منظور شناسایی ممکن است لازم باشد. هیچگاه نمونهها بیتوجه روی میز رها نشود و افرادی که نمونه را حمل یا مورد آزمایش قرار میدهند مشخص باشند.
در تهیه نمونه خون برای الکل از ضد عفونی الکلی استفاده نشود چون ممکن است موجب آلودگی محل و هوای اطراف شود. در این حالت میتوان با یک ضد عفونی کننده غیر الکلی مانند بنزال کونیوم کلراید محل خونگیری را ضد عفونی کرد.
لوله آزمایش را بایستی کاملاً از خون پرکرده و در ضمن سرپوشدار باشد.
خونگیری از پوست (Dermal puncture)
پیشرفت تکنولوژی در آزمایشگاه امکان تهیه میکروسمپل (نمونه کوچک) را از نوزادان و کودکان زیر 2 سال فراهم ساخته است.
آنالیز خون سرانگشتی در بیمارانی که یافتن رگ مشکل است از قبیل بیماران بخش سوختگی با پوست سفت و اسکار شده و بیمارانی که شیمیدرمانی میشوند و همچنین برای استفاده از دستگاههای اندازهگیری خانگی دارای اهمیت است.
خون سرانگشتی ترکیبی از خون کاپیلاری، آرتریولی و وریدهای کوچک و مایع میان بافتی است. از خون سرانگشتی برای اندازهگیری مکرر بیلیروبین در نوزادان استفاده میشود و در هنگام تهیه نمونه بایستی لامپ فتوتراپی را خاموش کرد تا کاهش کاذب بیلیروبین رخ ندهد. چنانچه خون سرانگشتی آزاد جریان یابد مقادیر آنالیتهای آن تقریباً مشابه خون وریدی است. خشک نشدن الکل ضدعفونی و ماساژ شدید موجب همولیز میشود.
غلظت گلوکز در خون سرانگشتی بیشتر از خون وریدی است و غلظت پتاسیم، پروتئین توتال و کلسیم آن کمتر است. چنانچه قصد مقایسه تغییرات جوابها باشد بايستي آزمایش با یک روش باشد مثلاًً نمیتوان گلوكز خون وریدی را با خون سرانگشتی مقایسه کرد.
ابزار لازم نمونهگیری از پوست (Dermal puncture)
1- لانست
2- لوله میکرو
3- الکل ایزوپروپانول 70%
4- گاز
5- اسلاید
6- پنبه الکلی
7- گرم کننده پاشنه پا
8- بانداژ
نکته مهم: لانستها بایستی از سوی کمیته OSHA مورد تأیید باشند.
به منظور جلوگیری از ورود لانست به استخوان، عمق برش پوستی بایستی در بالغین 2 تا 2/5 ميليمتر و در نوزادان و کودکان کمتر از 2 میلیمتر باشد.
لانست در انواع مختلف جهت نمونه گیری از پاشنه پا در نوزادان رسیده و نارس از سرانگشت وجود دارد. در نوع اتوماتیک آن عمق خارج شدن لانست و ایجاد برش توسط یک فنر تنظیم میگردد. هرگز یک تیغ جراحی را جایگزین لانست نکنید.
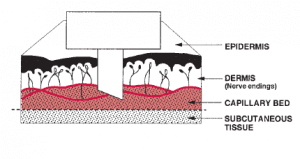
گفتنی است که برای خروج بهتر خون اهمیت پهنای برش بیشتر از عمق آن است. چنانچه در شکل مشاهده میشود بیشترین عروق پوست در مرزdermal- subcutaneous بوده و این عمق در نوزادان 0/35 تا 1/6 میلیمتر و حداکثر تا 3 میلیمتر در یک فرد بزرگ بالغ است. برشی به پهنای 2/5 میلیمتر نه بیشتر، خون کافی را از خود خارج میکند.
برش آناتومیک پوست
لانست با پوششهای رنگی مختلف (Color coded) برای ایجاد برشهای مختلف با توجه به مقدار مورد نیاز خون در دسترس میباشد.
لانستهای لیزری با رخنه دادن نور لیزر در عمق یک تا 2 میلیمتری پوست سوراخی را توسط تبخیر آب در شبکه مویرگی پوست ایجاد کرده که میتوان 100 میکرولیتر خون بدون احساس درد را تهیه کرد.
خونگیری با سیستم لانست نیاز به لولههای میکرو از قبیل لولههای میکروهماتوکریت، میکروتیوب و سیستمهای رقیق سازی خون دارد.
لولههای میکروهماتوکریت با نوار قرمز حاوی 2 واحد هپارین بوده كه برای اندازهگیری هماتوکریت به کار میروند. نوار آبی به مفهوم لوله کاپیلاری ساده و بدون هپارین است. اندازهگیری بیلیروبین نیز با لولههای کاپیلاری انجام میشود. میکروپیپت و میکروتیوبها در حجمهای مختلف با سرپوشهای مختلف رنگی ژلدار و بدون ژل فراهم است. امکان رقیق سازی خون برای حجم بیشتر جهت آزمایش CBC با استفاده از سیستم رقیق سازی میکروتیوب نیز میسر است. لولههای میکرو با رنگ کهربایی جهت اندازهگیری آنالیتهای حساس به نور فراهم است.
شیوه نمونهگیری از پوست
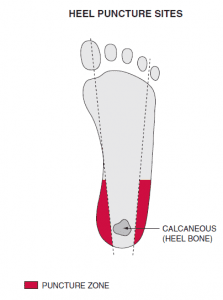
برای افزایش جریان خون پوست مانند پاشنه پا میتوان از حوله گرم با دمای 42 درجه یا از دستگاه گرم کننده استفاده کرد. منطقه خونگیری بایستی دور از استخوان باشد. پاشنه پا یا انگشتان 3 و 4 از محلهای انتخابی است. هرگز از محل قبلی لانست زده استفاده نکنید چون احتمال انتقال میکرو ارگانیسم به بافت مطرح است. از لانست زدن در نواحی سرد، کبود و اسکار شده خودداری کنید. محل خونگیری از پاشنه پا در شکل نشان داده شده است.
از لانست زدن به قسمت انحنای خلفی به علت آسیب به کارتیلاژ و عصب و تاندون خودداری کنید. پاشنه پا محل مناسب خونگیری در کودکان زیر یکسال است.
از نواحی قرمز رنگ برای لانست زدن به پاشنه پای نوزاد استفاده میشود
خون سرانگشتی
در کودکان بالای یک سال میتوان با لانست زدن به قسمت مرکزی و گوشتی بند آخر انگشتان 3 و 4 خونگیری کرد. قسمت نوک و جدار به علت جرم بافتی کمتر، آسیب پذیرتر بوده و احتمال عفونت استخوان وجود دارد. از انگشت کوچک به علت توده بافتی کمتر و انگشت اشاره به علت وفور شبکه عصبی استفاده نمیشود.
ضد عفونی کردن پوست
محل خونگیری را دایرهوار توسط گاز آغشته به الکل ایزوپروپیل 70% ضد عفونی کنید و اجازه دهید تا الکل خشک شود. خشک نشدن الکل دارای معایب زیر است:
- تماس الکل با لبههای زخم احساس دردي شبیه نیش زنبور میدهد.
- آلوده شدن نمونه
- همولیز شدن گلبولهای قرمز
- از تشکیل قطرات گرد خون جلوگیری میکند.
از ضد عفونی كننده پویدون – ایودین برای ضد عفونی پوست استفاده نمیشود، چون ممکن است در اندازهگیری پتاسیم، بیلیروبین، اسید اوریک و فسفر دخالت کرده و افزایش کاذب بدهد.
ضربه زدن
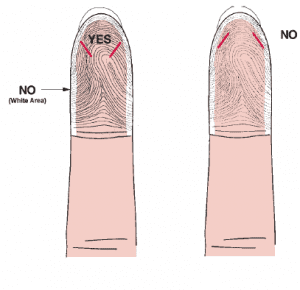
پاشنه پا یا انگشت بیمار بایستی بین انگشت شست و انگشت نشانه نمونهگیر ثابت گردد. در هنگام لانست زدن پوست را کمی کشیده و سعی کنید لانست به قسمت تا خورده پوست وارد نشود. جهت زدن لانست بایستی عمود بر شیارهای پوست باشد تا از روان شدن خون در شیارهای پوست جلوگیری شود.
برای تهیه نمونه خون سرانگشتی ضربه لانست باید عمود بر خطوط انگشتان باشد. ضربه افقی موجب روان شدن خون در شیارهای خطوط و جلوگیری از تشکیل قطرات گرد میگردد
جمعآوری نمونه
اولین قطره خون پوست که آلودگی با مایع میان بافتی و الکل دارد را با گاز استریل پاک کرده و از آن به بعد در لولههای کاپیلاری و میکروتیوب جمعآوري کنید. برای جلوگیری از ورود حباب میکروتیوبها را در حالت افقي و در لبه قطرات خون كه خارج ميشوند قرار دهيد تا خون جذب لولهها گردد. با وارد كردن فشار متناوب در یک تا یک و نیم سانتیمتری ضربه لانست سرعت خارج شدن خون را افزایش دهید. چنانچه خونگیری بیش از 2 دقیقه طول کشید لولههای حاوی ضد انعقاد را در حین نمونهگیری مخلوط کنید. از فشار ممتد و چلانیدن محکم محل خونگیری خودداری کنید. لولههای حاوی ضد انعقاد را حداقل با 10 تا 20 بار عمل واژگون ساختن مخلوط کنید. به علت چسبندگی پلاکتها به لبههای زخم و کاهش کاذب شمارش آن اولین لولهای که خونگیری میشود مربوط به آزمایش CBC است.
بعد از اتمام خونگیری با گاز استریل به ناحیه فشار آورید. بانداژ محل خونگیری در کودکان زیر 2 سال سفارش نمیشود چون ممکن است آنرا باز کرده و در دهان گذاشته و سبب آسپیره گردد. چسبهای زخم نیز ممکن است باعث آزردگی پوست ترد و ظریف نوزاد گردد.
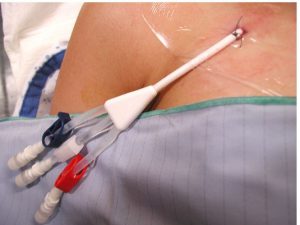
خونگیری از طریق کاتترها
کاتترها با جایگیری در وریدها راه را بسهولت به گردش خون بیمار باز میکنند. کاتترهای مرکزی توسط جراح در عروق بزرگ مانند ورید سفالیک، ژوگولار یا ورید فمورال جای میگیرند.
برای باز نگه داشتن راه کاتترها از هپارین استفاده میشود و از این رو آلودگی نمونه خون با هپارین آزمایشهای انعقادی را بیاعتبار میکند؛ مگر اینکه هپارین نمونه خون خنثی شود یا حدود 5 تا 10 سیسی خون را که وارد سرنگ میشود کنار گذاشته و با سرنگ دیگر نمونه گیری شود.
ترتیب خونگیری از کاتترها بشرح زیر است:
- 3 تا 5 سیسی خون گرفته و دور بریزید.
- نمونه مربوط به کشت خون گرفته شود.
- لولههای ضد انعقاددار نمونهگیری شود.
- لولههای مربوط به نمونه لخته خونگیری شود.
کاتتر ورید مرکزی
خطاهای شایع در جمعآوری نمونه
- برچسب اشتباه روی لوله
- نمونه با حجم کم (short draw)
- ضد انعقاد اشتباهی
- مخلوط کردن ناکافی نمونههایی که احتیاج به مخلوط کردن كامل دارند.
- گرفتن نمونه در لوله اشتباهی و ضد انعقاد اشتباهی
- بستن طولانی مدت تورنیکت و غلیظ شدن مصنوعی خون
- قرار دادن نمونه در معرض تابش نور و حرارت نامناسب
- تأخیر در ارسال نمونه، گرفتن نمونه در زمان نامناسب
- ایجاد همولیز در نمونه
- ورود سرسوزن به رگ قبل از خشک شدن الکل
- نمونه گیری بدون آگاهی از رژیم غذایی و مفهوم ناشتایی
- تنظیم نکردن ضد انعقاد سیترات سدیم در بیماران با هماتوکریت بیشتراز 55% برای آزمایشهای PT و PTT (آزمایش های انعقادی)
مدت زمان ناشتایی
به طور ایدهال بیمار بایستی 12 ساعت ناشتا بماند و انتخاب 12 ساعت بر این مبناست که بعد از خوردن یک غذای چرب افزایش تریگلیسرید تا 9 ساعت ادامه دارد اما دارای اثرات کمتری روی سطح کلسترول توتال است.
ناشتایی طولانی مدت برای مثال برای 48 ساعت موجب افزایش بیلیروبین، کاهش سطح آلبومین و پرهآلبومین و جزء سوم کمپلمان میشود. قند خون بعد از 72 ساعت ناشتا به 45 mg% در خانمها میرسد.
نوع تغذیه ممکن است یک سری آنالیتها را تحت تأثیر قرار دهد. اثرات موقتی و قابل کنترل هستند. خوردن غذا اثر فوری روی افزایش چربیها، قند خون، آهن، فسفاتاز قلیایی و پتاسیم دارد. آزمایش خون در مدفوع وابسته به تغذیه است چنانچه آزمایش خون در مدفوع بر پایه آنزیم پروکسیداز صورت میگیرد، خوردن تربچه و سایر مواد پروکسیدازدار آزمایش خون را به طور کاذب مثبت میکنند و چنانچه آزمایش بر پایه ترکیبات هم (Heme) باشد خوردن گوشت، آزمایش را مثبت میکند. گیاهخواری طولانی مدت موجب کاهش چربیها و ویتامین B12 میگردد. غذای سرشار از پروتئین مقدار اوره و دفع آمونیاک را افزایش میدهد. غذای سرشار از پروتئین و تهی از کربوهیدارت مانند تغذیه آتکین (Atkins) موجب افزایش BUN و اجسام کتونی در ادرار میگردد.
تغذیه با نسبت زیاد اسیدهای چرب غیر اشباع به اشباع ممکن است کلسترول را کاهش دهد. موز، آناناس، گوجه فرنگی و آواکادو سرشار از سروتونین بوده و موجب افزایش سطح ادراری 5 – هیدروکسی ایندول استیک میشود. کافئین موجب تحریک در رها شدن کاتکولآمینها از مدولای فوق کلیه و مغز شده و اسیدهای چرب را افزايش ميدهد. الکلیسم مزمن حجم متوسط گلبولی (MCV) را افزایش داده و فعالیت آنزیمی(γ- glutamyl transferase) GGT را افزايش ميدهد. افزايش GGT در ارتباط با ادامه مصرف الکل ميباشد. سطح لاکتات، اورات و تریگلیسرید و HDL کلسترول در افراد الکلی بالاتر است.
چاقی ارتباط مستقیمی با افزایش کلسترول، تریگلیسرید و اپولیپو پروتئین B دارد. فعالیت آنزیم LD، تولید کرتیزول و سطح گلوکز در افراد چاق بیشتر است، هر چند سطح انسولین هم دراین افراد بالا میرود ولی تحمل گلوکز آسیب میبیند. در مردان چاق غلظت تستسترون کاهش مییابد.
استرسهای فیزیکی و مغزی با افزایش ترشح ACTH، کرتیزول و کاتکول آمینها همراه هستند. استرس، کلسترول توتال را افزایش داده و سطح HDLکلسترول تا 15% افت میکند.
افرادی که در طول روز به دفعات زیاد غذای کم میخورند دارای سطح کمتری از توتال LDL و HDL کلسترول نسبت به افرادی هستند که همان مقدار غذا را سه وعده میخورند.
آزمایشهایی که تحت اثر تغییرات روزانه و استرس قرار میگیرند
- کرتیزول: اوج افزایش در 6-4 AM و کمترین مقدار در 8 PM تا 12 AM و حدود 50 درصد کاهش در 8 PM نسبت به 8 AM، افزایش با استرس
- هورمون محرک غده فوق کلیوی (ACTH): کاهش در شب، افزایش با استرس
- فعالیت رنین: کاهش در شب، افزایش در وضعیت ایستاده تا درازکش
- آلدوسترون: کاهش در شب
- انسولین: کاهش در شب
- هورمون رشد: افزایش در عصر و غروب
- فسفاتاز اسیدی: افزایش در عصر و غروب
- تیروکسین: افزایش با ورزش
- پرولاکتین: افزایش در 4 و 8 AM و در 8 تا 10 PM، افزایش با استرس، خواب، خوردن غذا، درد، حاملگی، تحریک سینه، تشنج
- آهن: اوج افزایش در اوایل تا آخر صبح، کاهش 30 درصدی در طی روز
- کلسیم: کاهش 4 درصدی در وضعیت درازکش
- ائوزینوفیل: نسبت عکس با کرتیزول (صبحها کمتر از غروب)
ضد انعقاد (Ethylene Diamine Tetra Acetic Acid) EDTA
ضد انعقاد EDTA در لوله با سرپوش ارغوانی (Lavender) ویژه آزمایش CBC موجود است. املاح EDTA به صورت نمک Na2 EDTA ,K2EDTA و K3EDTA در آزمایشگاه هماتولوژی در مقدار ایدهآل 1.5 mg به ازای هر سیسی خون بکار میروند. توجه داشته باشید که EDTA یک اسید است و پیوند یون به آن موجب کاهش اسیدیته آن میشود؛ برای مثال K3EDTA دارای pH بیشتری نسبت به K2 یا Na2EDTA است.
نمک K3EDTA بسیار حلال بوده ولی بایستی توجه کرد که تمام املاح EDTA هاپیراسمولار بوده و موجب چروک خوردگی گلبولهای قرمز و کاهش میکروهماتوکریت میگردد. این پدیده در مورد K3EDTA چشمگیر است. ولی در مورد K2EDTA و Na2EDTA کمتر رخ میدهد چون pH اسیدیتر آنها موجب تورم گلبول قرمز و نمک بودن آنها موجب چروکیدگی گلبولها میشوند که روی هم رفته این دو پدیده متعادل شده و از چروکیدگی گلبول جلوگیری میکند.
توجه داشته باشید که این تغییرات با زمان رخ میدهد و EDTA در غلظت 1.5 mg/cc تغییرات زیادی بین یک تا 4 ساعت از خونگیری در نتايج آنالیزورها نمیدهد، ولی برای کالیبراسیون دستگاهها استفاده از نمك K2EDTA سفارش میشود.
با مانده شدن خون در حرارت اتاق تورم گلبولها به ویژه در K2EDTA و Na2EDTA رخ میدهد. گستره محیطی تا 3 ساعت از خونگیری بایستی تهیه شود و حداکثر تا 6 ساعت از خونگيري مورد آنالیز دستگاهی قرار گيرد.
تورم پلاکتها در خون مانده ایجاد پلاکتهای بزرگ كرده و پاره شدن آنها موجب افزایش کاذب پلاکت میگردد. لولههای حاوی ژل و EDTA با سرپوش سفید جهت مطالعات مولکولی و استخراج DNA نیز بکار میروند.
سیترات سدیم
از سیترات سدیم برای آزمایشهای انعقادی مانند PT و PTT استفاده میشود. سیترات سدیم فاکتورهای انعقادی به ویژه فاکتور 5 را بهتر حفظ کرده و کمپلکس سریع آن با کلسیم آن را ضد انعقاد مناسب جهت تستهای انعقادی کرده است.
سیترات تری سدیم با 2 مولکول آب (Dihydrate Trisodium Citrate) درغلظت 3/2 درصد در آب مقطر معادل 0/109 مول در لیتر، ضد انعقاد سفارش شده برای تستهای انعقادی است. سیترات سدیم در غلظت3/8% معادل 0/129 مول در لیتر میباشد. گرچه آزمایشگاه میتواند از هر دو غلظت فوق برای آزمایش انعقادی استفاده کند، (نکته مهم: غلظت 3/2 و 3/8 از سیترات تری سدیم دو آبه تهیه میشود) ولی برای محاسبه INR فقط بایستی از یک غلظت استفاده شود. برای مثال چنانچه یک آزمایشگاه PT بیماران را برحسب INR با سیترات سدیم 3/2 درصد آزمایش میکند، چنانچه نمونهای در سیترات سدیم 3/8 درصد تهیه شده باشد نمیتواند از میانگین جبری PT پلاسماي نرمال در سیترات 3/2% در فرمول محاسبه INR استفاده كند، به ویژه زمانی که معرف ترومبوپلاستین با تکنولوژی نوترکیبی تهیه شده باشد که شبيه معرف WHO است.
ضد انعقاد هپارین
ضد انعقاد هپارین به صورت لیتیوم هپارین (LI Hep) و سدیم هپارین (Na Hep) در لوله با سرپوش سبز بکار میرود. پلاسمای جدا شده از ضد انعقاد لیتیوم هپارین برای اکثر آزمایشهای شیمی بجز اندازهگیری لیتیوم و اسید فولیک کاربرد دارد. گفتنی است که اندازهگیری پتاسیم در پلاسمای هپارینه میزان دقیقتری نسبت به سرم بدست میدهد و این به علت رها کردن پتاسیم از پلاکتها در حین پروسه انعقاد است. در حالت ترومبوسیتوز اندازهگیری پتاسیم خون هپارینه ترجیح داده میشود. استفاده از هپارین در طیف 12 تا 30 واحد در سیسی رضایت بخش است. از خون حاوی سدیم هپارین برای اندازهگیری سدیم نمیتوان استفاده کرد. ضد انعقاد هپارین برای آزمایشهای گازهای خون و آزمایش شکنندگی اسمزی بکار میرود.
هپارین بازدارنده آنزیم پلیمراز است و از این رو در آزمایشهای واکنش زنجيرهاي پلیمراز (PCR) به عنوان ضد انعقاد بکار نمیرود. استفاده از هپارین در آزمایش CBC ایجاد زمینه آبی رنگ در اسلاید رنگآمیزی شده مثل رنگ رایت میکند. گزارش شده که هپارین بازدارنده آنزیم فسفاتاز اسیدی است. در روشهایی که برای اندازهگیری کلسیم از EDTA استفاده میشود، هپارين با ایجاد کمپلکس با EDTA در سنجش کلسیم دخالت میکند. هپارین با ممانعت از پیوند هورمون T3 و T4 به پروتئین حامل موجب افزایش بخش آزاد این هورمونها میگردد.
هپارین با پیوند به آنتی ترومبین موجب خنثی کردن فاکتورهای فعال انعقادی به ویژه ترومبین گردیده و از این رو خاصیت ضدانعقادی خود را بازی میکند.
کاهش 70 درصدی خطاهای آزمایشگاهی با دانستنیهای قبل از آنالیز
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5896195/
برای دانلود پی دی اف بر روی لینک زیر کلیک کنید
ورود / ثبت نام



عالی
مفید و کوتاه و کاربردی