هایپرکلسترولمی خانوادگی؛ اساس مولکولی، تشخیص و درمان
دکتر نجمه آهنگری دکترای تخصصی پزشکی مولکولی (کلینیک چند تخصصی ژنتیک نسل فردا مشهد)
هایپرکلسترولمیای خانوادگی یا FH یکی از شایع ترین و شناخته شده ترین اختلالات ژنتیکی است. جهش در ژن گیرنده لیپوپروتئین با چگالی کم یا LDLR در بیش از 90٪ موارد علت اصلی بیماری است. FH با ریسک بالای بیماری عروق کرونر قلب زودرس یا PCAD همراه است. شیوع FH از 1 در 200 تا 1 در 500 نفر جمعیت تخمین زده میشود. با این حال بر اساس برخی مطالعات، گزارش شده که بیش از 80٪ افراد مبتلا به FH تشخیص داده نشده باقی می مانند. سازمان بهداشت جهانی، غربالگری در مقیاس وسیع را برای شناسایی بیمارانی که میتوانند از مزایای اولیه درمان کاهنده چربی بهره مند شوند پیشنهاد میکند. در صورت کاهش غلظت LDL کلسترول یا LDL-C در طول زندگی، شناسایی و درمان به موقع این بیماران، میتواند ریسک بالای قلبی عروقی آنها را کاهش یا حتی برطرف نماید. در حال حاضر شناسایی بیماران بر اساس معاینات بالینی صورت می گیرد، اما در بیشتر موارد برای شناسایی افراد مبتلا کافی نیست. بنابراین، دستورالعملهای اخیر اختلال چربیهای خون، آزمایش مبتنی بر DNA را در هر زمان که امکان پذیر باشد توصیه میکنند. درک اساس مولکولی هایپرکلسترولمی خانوادگی برای تشخیص صحیح این بیماری بسیار مهم است. حدود 5٪ از بیمارانی که قبل از 60 سالگی از سکته قلبی را تجربه می کنند، مبتلا به FH هتروزیگوت هستند. ریسک متفاوت مرگ در بیماران FH نشان دهنده تعامل بین عوامل ژنتیکی و محیطی است. فرم هموزیگوت FH یا HoFH نادر است، یعنی 1 در 1 میلیون نفر گزارش شده است، اگرچه مطالعات اخیر نشان داده اند که شیوع ممکن است به میزان 1 در 300،000 نیز رخ دهد. به دلیل اثر بنیانگذار یا founder effect، شیوع این بیماری در جمعیتهای خاصی بیشتر است. در یک دوره 2 ساله (2011–2009)، بانک اطلاعاتی بسیار گسترده محققان لیپید، نشان داد که 0/3 درصد افراد (1 نفر از 340 نفر یا بعبارتی 3829 نفر از 1320581 نفر) را که مطابق با انجمن ملی لیپید (NLA ) بودند – غربالگری LDL-C مبتنی بر سن را جهت آستانه FH مشخص کرد.
ویژگیهای بالینی هایپرکلسترولمی خانوادگی
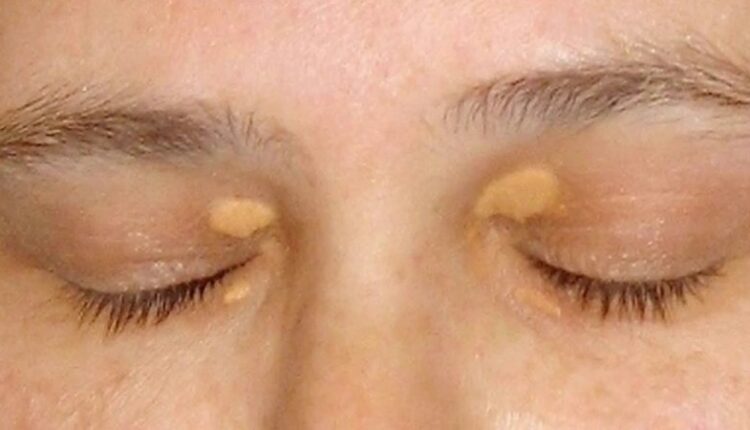
تظاهرات اصلی FH شامل افزایش قابل توجه سطح سرمیLDL-C ، بیماری عروق کرونر زودرس یا ASCVD و رسوب کلسترول در زیر پوست (زانتوما ) و قوس قرنیه میباشد. سطح LDL-C به طور معمول برای سن و جنس به بیش از صدک 90 افزایش می یابد، در حالی که سطح لیپوپروتئین با چگالی سنگین یا HDL-C و تری گلیسیرید معمولاً طبیعی است یا به مقدار کمی تغییر میکند. دلایل ثانویههایپرکلسترولمی، مانند اختلال عملکرد کبدی، کلیوی و تیروئید، باید کنار گذاشته شود. برخی از داروها ممکن است منجر به افزایش ثانویه سطح LDL-C شود .
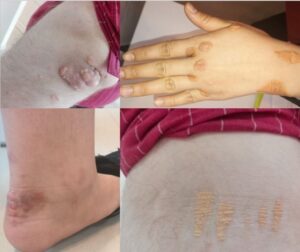
زانتوما در دست، آرنج و پاشنه پا
پاتوفیزیولوژی آترواسکلروز
آترواسکلروز یک بیماری التهابی است. از آنجا که غلظت بالای کلسترول در پلاسما، به ویژه میزانLDL-C ، یکی از عوامل اصلی خطر ابتلا به آترواسکلروز است، بسیاری تصور میکنند که این فرآیند بیشتر به دلیل تجمع چربیها رخ میدهد. با این حال، مکانیسمهای بیشتری در این فرآیند دخیل هستند. در حقیقت، ضایعات آترواسکلروز نمایانگر مجموعه ای از پاسخهای سلولی و مولکولی بسیار خاصی است که به بهترین وجه میتوان به طور کلی، به عنوان یک بیماری التهابی توصیف کرد. ضایعات آترواسکلروز اساساً در عروق بزرگ و متوسط الاستیک و عضلانی رخ میدهد و میتواند سبب ایسکمی قلب، مغز یا اندامها شود و در نهایت منجر به انفارکتوس میوکارد شود. این ضایعات ممکن است در طول زندگی فرد وجود داشته باشند. در واقع، اولین شکل ضایعه- اصطلاحاً رگه چربی -که در نوزادان و کودکان خردسال رخ میدهد، یک ضایعه التهابی خالص است که فقط از ماکروفاژهای مشتق شده از مونوسیتها و لنفوسیتهای T تشکیل شده است .
در افراد مبتلا به هایپرکلسترولمی، هجوم سلولهای التهابی با رسوب خارج سلولی لیپیدهای بی شکل و غشایی اتفاق می افتد. با توجه به افزایش سطح LDL-C در پلاسما از بدو تولد، بیماران مبتلا به FH در معرض خطر زیادی برای ASCVD، به ویژه انفارکتوس میوکارد و مرگ ناگهانی هستند. خطر ASCVD در بیماران مبتلا به FH نیز تحت تأثیر عوامل خطر معمول مانند جنس )مرد(، سیگار کشیدن، چاقی، دیابت، فشار خون بالا و سطح پایین HDL-C سرم قرار دارد. با این حال، الگوریتمهای طبقه بندی خطر معمولی در افراد مبتلا به FH در معرض افزایش سطح LDL-C از بدو تولد را در نظر نمی گیرند و بنابراین ممکن است خطر ASCVD را دست کم بگیرند. در صورت عدم درمان، بیماران مبتلا به فرم هموزیگوت بیماری دچار ASCVD میشوند و می تواند منجر به فوت قبل از 20 سالگی شود. درفرم هتروزیگوت FH، در صورت عدم درمان در اوایل میانسالی بیماری قلبی عروقی تقریباً در حدود 35 سالگی اتفاق می افتد. با این حال، اگر از سن 18 سالگی درمان شود، این آستانه به 48 سالگی تغییر میکند و درمان از سن 10 سالگی بروز بیماری قلبی را تا 53 سالگی به تأخیر می اندازد.
اساس ژنتیکی هایپرکلسترولمی خانوادگی
پاتوفیزیولوژی اصلی FH به طور کلی بعلت جهش در ژن LDLR و به میزان کمتر در ژنهای آپولیپوپروتئین B (APOB) و PCSK9 رخ میدهد. ژن LDLR روی کروموزوم 19 قرار دارد و دارای 18 اگزون با طول 45 کیلوباز است. تاکنون بیش از 1288 جهش منحصر به فرد و واریانتهای اللی در ژن LDLR شناسایی شده است. جهش در ژنهایی که پروتئینهای درگیر در جذب LDL و کاتابولیسم را رمزگذاری میکنند، یعنی LDLR، APOB، پروتئین آداپتور گیرنده LDL یا LDLRAP1 و PCSK9 شناخته شدهاند که باعث ابتلا به FH میشوند، ناشی از برداشت و تنظیم معیوب LDL میباشند.
تشخیص بالینی
معیارهای بالینی مختلفی برای تشخیص FH ارائه شده است. در عمل، دو گروه از معیارهای بالینی معتبر، به عنوان مثال، سیستم DLCN و سیستم Simon Broome (SBR) بر اساس سابقه بالینی خانوادگی و فردی، معاینه فیزیکی و نتایج پروفایل لیپیدی، به طور گسترده ای برای شناسایی افراد مبتلا استفاده میشود. در جمعیتهای آسیایی، معیارهای فوق الذکر با تغییراتی مورد قبول قرار گرفته اند. این مجموعه معیارها ممکن است سبب عدم تشخیص برخی از بیماران هتروزیگوت مبتلا به نوع فنوتیپ خفیف گردد و برای جمعیت کودکان نیز قابل استفاده نیستند. با اینحال، هر دو معیار فوق الذکر در بالین برای تشخیص FH کاربرد دارند.
غربالگری آبشاری : بررسی خطر در خانواده
یک روش مقرون به صرفه برای شناسایی موارد جدیدهایپرکلسترولمی خانوادگی، غربالگری آبشاری خانوادگی در خویشاوندان یک پروباند با تشخیص احتمالی FH است که مبتنی بر یک استراتژی فنوتیپی با/ یا بدون ارزیابی ژنوتیپی انجام می گردد. با توجه به دو شرط مهم غربالگری یعنی دسترسی عموم و مقرون به صرفه بودن، و از طرفی شرایط اقتصادی متفاوت کشورهای درحال توسعه، ممکن است ویژگیهای فوق برای همگان فراهم نگردد. با این حال، در کنار غربالگری آبشاری، آزمایش ژنتیک آبشاری که تشخیص بر اساس جهش بیماریزا در همه اعضای در معرض خطر خانواده است، دقیق تر از غربالگری با فنوتیپ به تنهایی میباشد. اگر آزمایشات مبتنی بر DNA در دسترس نباشد، غربالگری آبشاری باید فقط با استفاده از سطح کلسترول LDL پلاسما بر اساس سن، جنس و کشور انجام شود. به دلیل احتمال بیشتر قبل از آزمایش، از ابزارهای تشخیصی بالینی برای موارد شاخص نباید برای بستگان استفاده شود. ترسیم شجره نامه خانوادگی میتواند در برنامه ریزی روند غربالگری ارزشمند باشد.
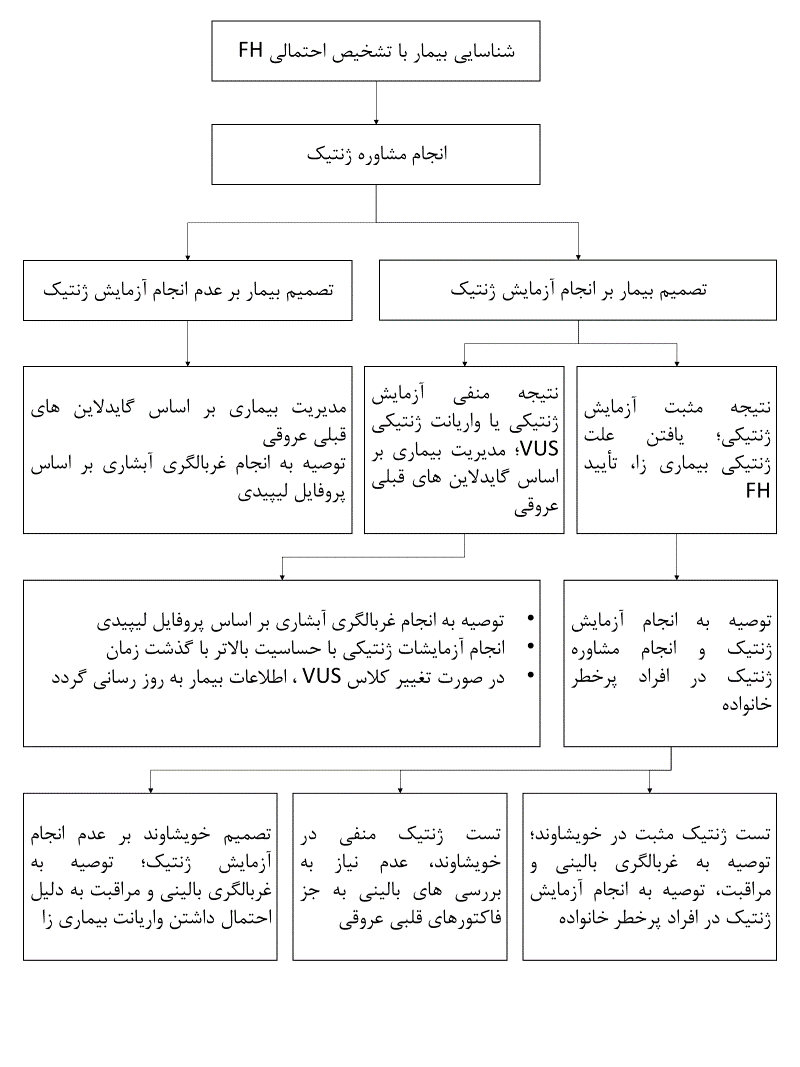
روند پیگیری بیماران و خانوادههای مبتلا بر اساس پیشنهاد کالج آمریکایی قلب JACC
تشخیص ژنتیکی
اکثر موارد FH به علت جهش در ژنهای LDLR ، APOB و PCSK9 ایجاد میشود. جهش بیماریزا در یکی از این ژنها در حدود 70 درصد موارد قطعی FH با فنوتیپ مشخص و 20 درصد موارد با تشخیص احتمالی FH شناسایی شده است. تکنیکهای جدید مولکولی، مانند تعیین توالی اگزوم ، میتواند منجر به کشف جهشهای جدید شود. این تکنیک به ویژه در مورد جمعیتهای چند قومی میتواند مورد مطالعه قرار گیرد. حدود 95 درصد جهشهای شناسایی شده در ژن LDLR ، 4-5 درصد در ژن APOB و 1 درصد در ژن PCSK9 قرار دارند. تشخیص جهش در یکی از اعضای خانواده کمک میکند تا تشخیص قطعی FH انجام شود. با این حال، عدم تشخیص جهش، تشخیص FH را نفی نمیکند، به ویژه اگر فنوتیپ بالینی به احتمال زیاد بیانگر وجود FH باشد. خدمات غربالگری متمرکز ژنتیکی همراه با رهنمودهایی برای بازپرداخت بیمهها میتواند میزان انجام آزمایش ژنتیکی و غربالگری آبشاری را بهبود بخشد. تلاشها برای توسعه برنامههای آموزشی برای مشاوران ژنتیک و محققان لیپید در مورد ژنتیک FH ادامه دارد.
درمان هایپرکلسترولمی خانوادگی
در حال حاضر، استاتینها، ازتیمایب، گیرندههای اسید صفراوی و مهار کنندههای PCSK9 اصلی ترین روشهای درمانی برای درمان هایپرکلسترولمی هستند. علاوه بر این، درمانهای جدید مبتنی بر RNA نظیر Inclisiran تأثیر بسیار زیادی در استراتژیهای درمانی دهههای اخیر داشته است. درمان باید به محض تشخیص آغاز شود و در طول زندگی ادامه یابد. در حالی که هایپرکلسترولمی ممکن است در اثر تغییرات خاص ژنتیکی ایجاد شود، بیشتر موارد هایپرکلسترولمی تحت تأثیر عوامل دیگری مانند بیماریهای غدد درون ریز یا متابولیک، سبک زندگی (ورزش و رژیم) و داروها قرار دارند. این داروها از طریق افزایش فعالیت گیرنده LDL و پاکسازی LDL-C عمل میکنند. علاوه بر این، با پیشرفت چشمگیر تکنیکهای مولکولی، رویکردهای درمانی مبتنی بر RNA برای مداخله درمانی تأثیر زیادی بر استراتژیهای درمانی دهههای اخیر داشته است.
کلسترول LDL: زمانه در تغییر است!
متابولیسم کلسترول و اختلالات آن
دیدگاههایی در مورد تغییر چشمانداز اندازهگیری ریسک قلبی عروقی مرتبط با LDL
پیشرفتها در اندازهگیری لیپید
اهميت و اندازهگيري ليپيدهاي سرم
برای دانلود پی دی اف بر روی لینک زیر کلیک کنید
ورود / ثبت نام