سرولوژی SARS-Cov2
تبلیغات فراوان، اطلاعات اندک
دکتر حسن بیات، دکترای علوم آزمایشگاهی
سندرم حاد تنفسی کروناویروس 2 (SARS-CoV-2)، عامل بیماری کروناویروسی 2019 (COVID-19)، سبب مرگومیر فراوانی در سراسر دنیا شده است (1). FDA در واکنش به کمبود آزمایشCOVID-19 ، سند راهنمایی برای روشهای سرولوژی منتشر کرد که در آن گفته شده است اگرچه سازندگان میتوانند از «تأییدیه کاربرد اضطراری» (Emergency Use Authorization, EUA) استفاده کنند، اما روشهای سرولوژی میتوانند بدون اخذ این تأییدیه به بازار عرضه شوند (2). این امر سبب شده است آزمایشهای سرولوژی بهطور گستردهای در دسترس قرار بگیرند، در حالی که سازندگان بیشتر آنها دارای سابقه اندک یا فاقد سابقه در بازار فرآوردههای تشخیصی هستند. تا زمان نوشتن این مطلب، بیش از 100 سازنده به FDA اطلاع دادهاند که در حال فروش یا برنامهریزی برای فروشِ آزمایشهای سرولوژی در امریکا هستند و از بین آنها تنها 4 سازنده EUA دارند (3). این نشاندهنده عرضه شمار بیسابقهای از روشهای آزمایشگاهی ساخت شرکتهاست که توسط FDA بررسی نشدهاند. مقالاتی درباره برخی از این روشها، بدون مرور توسط همکاران در سرورهای پیش از چاپ منتشر شده است و سبب جلب توجه و نیز انتقاداتی در رسانههای جمعی گردیده است. بهرغم این، تقاضا برای آزمایشهای سرولوژیCOVID-19 به رشد ادامه داده است.
سه نقش برای سرولوژی در پاندمی COVID-19 پیشنهاد شده است:
(الف) تشخیص،
(ب) شناسایی اهداکنندگان پلاسمای بهبودی یافته،
(پ) غربالگری جمعیتها با هدف تعیین مواجهه و مصونیت.
تشخیص
یکی از پرسشهای رایج پزشکان این است که آیا میتوان از سرولوژی برای تشخیص استفاده کرد. سودمند بودن سنجشهای سرولوژی در تشخیص نامحتمل است. گزارشهای اولیه حاکی از این هستند که بیماران تقریباً 7 تا 14 روز پس از بروز علائم از نظر anti-SARS-CoV-2 IgG مثبت میشوند (4). در بیمارستان ما، زمان میانه از شروع علائم تا مراجعه بیمار 3 روز است (میانگین تقریباً 5 روز)، که تشخیص سرولوژی را در زمان بررسی اولیه بیمار نامحتمل میکند. استفاده از anti-SARS-CoV-2 IgM برای شناسایی عفونت ابتدایی پیشنهاد شده است؛ با وجود این، بیشتر روشهای مبتنی بر IgM نسبت به روشهای مبتنی بر IgG از میزان مثبت کاذب بالاتری رنج میبرند (5). نظر به این محدودیتها، تکنیکهای مولکولی برای تشخیص COVID-19 ترجیح داده میشوند. با وجود این، محدودیتهای موجود در حساسیت روشهای مولکولی مورد توجه قرار گرفته و درمانـــگران را بهسوی روشهای جایگزین برای آزمایش بیماران PCR منفی که دارای علائم سازگار با کووید-19 هستند، سوق داده است. البته هنوز تا کارآمدی آزمایش سرولوژی در تشخیص فاصله داریم. در تجربه ما، آزمایش بیمارانی که COVID-19 PCR ایشان منفی شده بود، فقط درصد کوچکی از بیماران سرولوژی مثبت را تشکیل داد (تقریباً 1% بیماران علامتدار که PCR منفی بودند)، در حالی که قضاوت درباره وضعیت بیماری چنین بیمارانی سخت است، این یافتهها جایگاه محدودی را برای آزمایش سرولوژیک تشخیصی مطرح میکنند. این یافتهها با توصیــــــــــــــــههای اخیر «انجمن بیماریهای عفونی امریکا» (Infectious Disease Society of America, IDSA) همخوانی دارد (6).
اهدای پلاسمای بهبودی یافته
پلاسمای بهبودی یافته ممکن است درمان مؤثری باشد (7). شناسایی اهداکنندگان پلاسمای بهبودی یافته یکی از کاربردهایی است که برای آزمایش سرولوژی پیشنهاد شده است. اخیراً، بیمارانی که از COVID-19 بهبودی یافتهاند اگر با روشهای مولکولی منفی شده باشند، میتوانند پلاسمایشان را اهدا کنند. فرض بر این است که بیمارانی که تیتر anti-SARS-CoV-2 بالایی دارند میتوانند جمعیت اهداگر ایدهآل باشند. البته مطالعات بیشتری لازم است برای اینکه معلوم شود آیا آنتیبادیهای anti-SARS-CoV-2 خنثی کننده هستند و اینکه چه تیتری برای مصونیتبخشی لازم است. علاوه بر این، چون بیشتر سنجشهای سرولوژی نتایج را بهصورت کمّی ارائه نمیکنند، مکانیسمهای محدودی برای تفکیک اهداکنندگان دارای تیتر بالا از اهداکنندگان دارای تیتر پایین وجود دارد. اگر قصد تبدیل روشهای کیفی به روشهای کمّی وجود دارد، باید آنها را از این منظر ارزشیابی کرد (شامل بررسی دقت در طول محدوده گزارش).
غربالگری جمعیت
غربالگری جمعیت پیشنهاد شده است برای شناسایی بیمارانی که مواجهه داشتهاند و بهطور فرضی نسبت به SARS-CoV-2 ایمن شدهاند و نیز برای تعیین شیوع مواجهه در یک جمعیت برای مقاصد همهگیرشناسی. در حالی که راهکارنماهای اختصاصی درباره اینکه چگونه میتوان “مصونیت فرضی” را تعیین و بهکار برد وجود ندارد، این کاربرد بالقوه هیجان زیادی را در فضای عمومی برانگیخته است. اعضای «کارگروه کروناویروس کاخ سفید» از سنجشهای سرولوژی بهعنوان مجوز بازگشت آمریکائیان به کار تمجید کردهاند (8). متأسفانه، در حال حاضر مشخص نیست که آیا آنتیبادیهای anti-SARS-CoV-2 مصونیتزا هستند یا خیر. بر اساس آنچه درباره دیگر ویروسهای تنفسی (یعنی آنفلوانزا) میدانیم، ممکن است وجود آنتیبادیها، نوعی از مصونیت را فراهم کند.
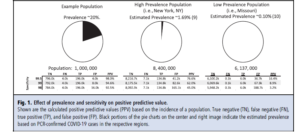
چالش موجود با تعیین سرولوژیک مصونیت این است که شیوع سرولوژیک احتمالاً پائین است؛ حتا در مناطقی که گسترش وسیعی از COVID-19 گزارش شده است. در وضعیتهای شیوع-پایین، حتا یک روش آزمایشگاهی دارای حساسیت و اختصاصیت بالا معمولاً سودمند نیست. اختصاصیت و بروز نتایج مثبت کاذب باید بهدرستی تعیین شود. اگر شیوع COVID-19 در یک جمعیت ۲۰% باشد، آزمایشی با حساسیت و اختصاصیت ۹۸%، ارزش یک نتیجه مثبت (value of a positive result, PPV) را ۹۲٫۵% میکند (شکل 1). در نیویورک، شیوع ۱٫۶۹% برآورد شده است (۹)، بنابراین اگر اختصاصیت یک آزمایش سرولوژی ۹۹٫۵% باشد، PPV برابر ۷۶٫۶% خواهد بود. با وجود این اگر اختصاصیت به ۹۸% کاهش یابد، PPV به ۴۵% سقوط میکند؛ یعنی تقریباً از هر ۲ نتیجه مثبت، یکی مثبت کاذب است. در چنین سناریویی، نیمی از کسانی که مجوز بازگشت به کار گرفتهاند، آنتیبادیهای اختصاصی علیه SARS-CoV-2 را نخواهند داشت و در خطر کسب و انتقال عفونت خواهند بود. در شهرها و ایالاتی با شیوع کمتر مانند میسوری (شیوع ۰٫۱%) (منبع ۱۰)، حتا یک اختصاصیت ۹۹٫۵% به PPV برابر ۱۶٫۴% منجر خواهد شد. پیش از راهاندازی آزمایش سرولوژیک برای غربالگری، درک ارتباطات بین شیوع، اختصاصیت و PPV ضروری است.
اهمیت اختصاصیت آزمایشهای سرولوژی در غربالگری جمعیتهای شیوع-پایین اخیراً در یک مقاله مرورنشده ارائه شده است (۱۱). ۳۳۰۰ نفر از ساکنان کالیفرنیا با روشی که تأییدیه EUA نداشت از نظر آنتیبادیهای SARS-CoV-2 غربال شده بودند. ۱٫۵% از افراد غربالشده از نظر آنتیبادیهای SARS-CoV-2 مثبت بودند و نویسندگان پس از تجزیه و تحلیل، شیوع را ۲٫۴% برآورد کردند. نویسندگان مقاله با استــفاده از ۳۰ نمونه پیش-کووید-19 در ترکیب با ادعای سازنده، حساسیت را برابر ۸۰٫۳% و اختصاصیت را برابر ۹۹٫۵% را تعیین کردند. با وجود این، محدوده اطمینان ۹۵% برای اختصاصیت ۹۸٫۲% تا ۹۹٫۹% بود. نویسندگان تصریح کردهاند که اگر اختصاصیت ۹۸% باشد، شیوع برآوردشده از ۲٫۴% به کمتر از ۱% کاهش خواهد یافت و محدوده اطمینان ۹۵% به ۰% خواهد رسید.
علت نتایج مثبت کاذب چیست؟ نظر به شباهت SARS-CoV-2 به سایر کروناویروسها، این احتمال هست که در کیتهایی که ضعیف طراحی شدهاند، آنتیژنهایی که بهعنوان هدف بهکار برده شدهاند واکنش متقاطع بدهند. در جمعیت سالمندان که احتمالاً با طیف متنوعتری از کروناویروسهای اندمیک مواجهه داشتهاند، این خطر تشدید میشود (۱۲). بسیاری از روشهای سرولوژیک همچنین با ویروس اپشتین-بار، فاکتور روماتوئید و آنتیبادیهای هتروفیل واکنش متقاطع میدهند. بهمنظور پرهیز از واکنش متقاطع با آنتیبادیهای کروناویروسهای اندمیک، ضروری است در انتخاب آنتیژن در روشهای سرولوژیک دقت شود. اگر مطالعات ارزشیابی بهدرستی طراحی نشوند (یعنی فقط نمونههای پیش از پاندمی از افراد جوان و بدون علائم، بهعنوان جمعیت منفی استفاده شود)، آنگاه ممکن است این محدودیتها بهطور کامل بررسی نشود و حساسیت روش ممکن است بهطور فاحشی بیشبرآورد شود.
چگونه باید روشهای سرولوژیک COVID-19 را ارزشیابی کرد؟
نظر به فقدان مبنای مستحکم علمی برای ارزیابی روشهای سرولوژیک در دسترس، جامعه آزمایشگاه بالینی باید این روشها را بهطور کامل بررسی کند و کاربرد آنها را به روشنی با کاربران نتایج در میان بگذارد. این امر بهویژه در مورد روشهای فاقد EUA که ساخت و عملکردشان ممکن است متغیر باشد اهمیت دارد. «مؤسسه معیارهای بالینی و آزمایشگاهی» (Clinical and Laboratory Standards Institute, CLSI) توصیه میکند که حساسیت با آزمایش حداقل ۵۰ نمونه مثبت از بیماران تأییدشده بررسی شود (۱۳). بهطور ایدهآل، این بررسی بهصورت متوالی [با گرفتن نمونه در روزهای مختلف از هر بیمار] انجام میشود تا حساسیت در روزهای مختلف متعاقب بروز علائم معلوم شود. CLSI همچنین استفاده از ۵۰ نمونه را برای تعیین اختصاصیت توصیه میکند. در حالی که این توصیهها مفید هستند، میزان سختگیری در ارزشیابی نهایتاً به جمعیت مورد نظر برای آزمایش بستگی خواهد داشت (۱۳). برای غربالگری جمعیت-بنیان با شیوع سرمی پائین، لازم است اختصاصیت بیش از ۹۹% باشد (یعنی بین ۹۹ تا ۹۹٫۹) تا PPV بالایی را تضمین کند. این امر، بسته به مدل آماری مورد استفاده، مستلزم استفاده از یک جمعیت کنترل با منفی بیش از ۷۵۰ نفر (۱۴) یا بیش از ۲۰۰۰ نفر (۱۵) خواهد بود. در مقابل، هنگام آزمایش گروههای دارای احتمالات پیشآزمونی بالاتر (یعنی اهداکنندگان پلاسمای بهبودی یافته)، لازم نیست اختصاصیت آنچنان بالا باشد. برای تعیین میزان مثبت کاذب، نمونههایی از چندین منبع باید آزمایش شود شامل بیماران علامتدار که آزمایش مولکولی ایشان برای COVID-19 منفی شده است و نمونههایی که پیش از فراگیری COVID-19 گرفته شدهاند. همچنین نمونههای هر ارزشیابی/گواهی کردن باید شامل زیرمجموعهای از بیماران تأییدشده از نظر کروناویروسهای اندمیک مانند NL633، HKU1، OC43 و 229E باشد. نهایتاً اینکه سایر نمونههایی که بهطور بالقوه دارای واکنش متقاطع هستند باید آزمایش شوند، شامل نمونههای حاوی آنتیبادیهای هتروفیل و فاکتور روماتوئید.
در نتیجه، در حالی که روشهای سرولوژیک سبب تبلیغات زیادی شدهاند، برای پشتیانی از کارآمدی بالینی آنها نیازمند اطلاعات هستیم. در صورتی که این روشها بهدرستی ارزیابی نشوند، ممکن است سبب تشخیص نادرست یا گمراهی شوند. همچنین ضروری است که آزمایشگاهها برای اطمینان از اینکه این روشها برای استفاده نهاییشان مناسب هستند، آنها را سختگیرانه ارزیابی کنند. علاوه بر این، همچنان که مردم نسبت به امیدی که روشهای سرولوژیک برانگیختهاند دلبسته میشوند، این مسئولیت صاحبحرفهگان آزمایشگاهی است که خطرات بالقوه را به هر کسی گوشزد کنند.
برگردان از:
SARS-CoV-2 Serology: Much Hype, Little Data
Clinical Chemistry 66:7 (2020)
کارآیی بالینی دو ارزیابی سرولوژیک SARS-CoV-2
برای دانلود پی دی اف بر روی لینک زیر کلیک کنید
ورود / ثبت نام