تازههایی از عامل طاعون
دكتر رضا ميرنژاد (استاد تمام دانشگاه)
طايفه یرسینیائه (Yersinieae Tribe)
يرسينيا قبلاً جزء پاستورلاها طبقهبندي شده بود و ظاهرش بر روي محيط تريپل شوگر آيرون آگار (TSI) همانند گونههاي پاستورلاست، اما برخلاف پاستورلاها، طایفه يرسينيائه اکسیداز منفی هستند. این تیره یا طایفه در خانواده انتروباکتریاسه طبقهبندی میشوند. در طايفه يرسينيائه فقط جنس يرسينيا قرار دارد که دارای 11 گونه يرسينيای شناختهشده است كه فقط 3 گونه آن در انسان بيماريزاست. يكي از آنها يرسينيا پستيس (Yersinia pestis) عامل طاعون است و از نظر اپيدميولوژيك بيماري مشترك بين دام و انسان است. دو گونه بیماریزای ديگر يرسينيا سودوتوبركلوزيس (Y.pseudotuberculosis) و يرسينيا انترکولیتيكا (Y.enterocolitica) هستند.
يرسينيا پستيس
يرسينيا پستيس عامل بيماري وحشتناك و وهمآلود طاعون است كه هميشه نامش با ترس همراه بوده و بنابراين در ادبيات و تاريخ از آن به بدي ياد شده است. قدیمیترین مداركي كه از طاعون در دسترس است مربوط به وصیتنامهی كهني است كه یک اپيدمي بهصورت تورم غدد خياركي را در بين فلسطينيان بعد از گرفتن كشتي ميثاق از اسرائیلیها توصيف كرده است. اولين پاندمي طاعون در سال 547 قبل از ميلاد در دوران سلطنت جاستينيان اول، امپراطور روم، از آفريقاي جنوبي آغاز و سريعاً در سرتاسر اروپا منتشر گرديد.
اين اپيدمي 60 سال طول كشيد و بالغ بر 100 ميليون نفر را كشت و بسياري از مناطق را خالي از سكنه كرد. پاندمي دوم از آسيا آغاز شد و آتش خشم آن سرتاسر آسيا و اروپا را در طي قرن 14 درنورديد و فقط در اروپا 25 ميليون نفر را كه معادل يك چهارم جمعيت بودند، كشت. سومين پاندمي از برمه آغاز شد و به چين و هنگکنگ كشيده شد و سپس به بنادر سراسر دنيا توسط موشهای كشتي پخش شد. اين اولين پاندمي بود كه به سواحل آمريكاي شمالي رسيد و در شهرهاي ساحلي نظير سانفرانسيسكو تلفات بسياري گرفت. هند بيشترين صدمه را با حدود 10 ميليون نفر كشته متحمل شد.
به طاعون در شعر كودكانه “حلقهی اطراف يك قرمزي[1]” و كتاب داستان ادگار آلنپو بنام “بالماسكهي مرگ سرخ[2]” اشاره شده است. اين بيماري بههمراه تيفوس عامل ايجاد نظريه مالتوسيان [توماس مالتوس] گرديد كه در آن بيان میشد هرگاه جمعيت جهان بهاندازهی غير قابل كنترلي برسد، توسط اين بیماریها يا جنگ كاهش مییابد.
امروزه موارد تكگير طاعون از طريق گزش كك جوندگان آلوده به انسان منتقل ميشود. سالانه در سراسر جهان هزاران مورد ابتلا گزارش ميشود كه 90 درصدشان در آسياي جنوب شرقي بهخصوص هند و ویتنام است. در ایالات متحده آمريكا سالانه دهها مورد روي میدهد كه بيشتر آنها در ایالتهای جنوب غربي كه جوندگاني نظير موش صحرايي و سگهای چمنزار زندگي میکنند و گاهي حامل باسيل هستند، گزارش میشود. اغلب سگها و گربهها از طريق آوردن جوندگان آلوده به نزد انسان، به انتشار بيماري كمك ميكنند. جمعيت بوميان اين مناطق بدليل تماس با جوندگان، بيشتر در معرض خطر هستند.
حدود 200 گونه حيوان كوچك يافت شده است كه حامل طاعون هستند. بعضي از گونهها در اثر آلودگي سريعاً ميميرند، اما بقيه كمي بيمار ميشوند و يا اصلاً بيمار نميشوند. انتقال حيوان به حيوان يرسينيا از طريق تماس مستقيم يا گزش كك است. اين چرخه كاملاً زئونوتيك، انتشار طاعون روستايي[3] (يا طاعون جنگلي) ناميده ميشود. گاهي اولين علامت طاعون، مرگ دستهجمعي موشهاست. اگر موشها بيماري را از جوندگان وحشي گرفته و از طريق ککها به انسان منتقل كنند، چرخة انتشار طاعون شهري[4] ناميده ميشود.
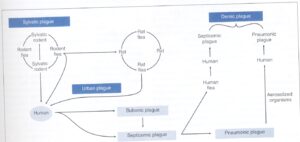
همانطوركه در شکل 1 نشان داده شده است، انسان وقتي وارد چرخة طاعون ميشود كه با حيوانات آلوده يا ككهايشان تماس پيدا كند. در ایالات متحده آمریکا معمولاً بيماري از طريق سنجابهاي كوچك تا انواع موشها و خرگوشها ميتواند به انسان منتقل شود. از آنجايي كه مردان و بچهها بيشتر در تماس با اين حيوانات هستند، حدود دو سوم بيماران آلوده مرد هستند و سه چهارم آنها زير 25 سال سن دارند.
انتشار انسان به انسان طاعون از طريق كك انسان يا قطرات تنفسي آلوده را طاعون Demic ميگويند.
شكل 1: انتقال يرسينيا پستيس، عامل طاعون در حيوانات و انسانها (برگرفته از کتاب میکروبشناسی پزشکی واکر)
خصوصيات يرسينيا پستیس
يرسينيا پستيس باسيل پليمورف گرم منفي است که در رنگآميزي وايسون (Wayson) يا گيمسا شبيه سنجاققفلی است و بهصورت دوقطبي رنگ ميگيرد. يرسينيا پستيس از اعضاء فاميل انتروباكترياسیه است و بر روی محیطهای كشت استاندارد انتخابي براي باسيلهاي رودهاي، مثل مكانكي آگار و سالمونلا- شيگلا آگار قادر به رشد است و در حرارت اتاق، بهصورت كلنيهاي لاكتوز منفي رشد میکند. حرارت رشد اپتيمال براي يرسينياها برخلاف ساير باكتريهاي رودهاي 25 تا 35 درجه سلسیوس است. هنگام كشت، سويههاي بیماریزای يرسينيا پستيس بر روي محیطهای كشت حاوي همين يا كنگو رد، كلنيهاي رنگي توليد ميکنند.
يرسينيا سودوتوبركلوزيس و يرسينيا انتروکولیتيكا بهواسطه متحرك بودنشان و داشتن فلاژل قطبي يا پريتريش، با يرسینيا پستيس متفاوتند. برخلاف يرسينيا انتروکولیتيكا، يرسينيا پستيس همانند یرسینیا سودتوبرکلوزیس، اورنیتين دكربوكسيلاز منفي بوده و قندهاي سوكروز، سلوبيوز يا سوربيتول را تخمير نميكند. يرسينيا پستيس برخلاف يرسينيا سودوتوبركلوزيس، رامنوز را تخمير نميكند (جدول 1).
مكانيسم بیماریزایی
(1) آنتيژنها و شاخصهاي بیماریزایی يرسينيا:
همه یرسینیاها دارای LPS میباشند که همانند سایر انتروباکتریاسه هنگامی که آزاد میشوند دارای فعالیت اندوتوکسین هستند. در یرسینیاها سیستم ترشحی تیپ 3 باعث میشود که پروتئینهای ترشحی از باکتری مستقیماً وارد سیتوپلاسم سلول میزبان گردد. بهطورکلی بیماریزایی يرسينيا پستيس فرآيند پيچيدهاي است كه عوامل بسياري در آن دخالت دارند كه توسط سه پلاسميد بیماریزا ,Tox) Lcr و Pst) و كروموزوم كد ميشوند.
(الف) فاكتورهايي كه بر روي پلاسميد پستيسين[5] (Pst) كد ميشوند. پلاسميد Pst، يك پلاسميد با وزن مولکولی kb10 است كه سنتز سه عامل را كد ميكند: يك آنزيم كه تنظیمکننده تغييرات بعد از ترجمة پروتئینهای غشاي خارجي يرسينياست؛ پستیسين كه پروتئين شبه باكتريوسيني[6] است كه ربطي به بیماریزایی ندارد؛ فعالکننده پلاسمينوژن[7] يرسينيا كه مادهاي براي انتشار يرسينيا از محل اوليه عفونت است. بنظر میرسد كه فعاليت فيبرينولايتيك فعالکننده پلاسمينوژن، نقش كليدي در انتشار عفونت دارد. همچنين فعاليت كوآگولازي فعالکننده پلاسمينوژن ممكن است سبب انعقاد خون در معده كك آلوده شده و سبب ميشود كه كك طي خونخواري از ميزبان پستاندار با استفراغ باكتري را به انسان منتقل كند.
(ب) فاكتورهايي كه بر روي پلاسميد (Lcr)Low-Calcium-response كد ميشوند. پلاسميد Lcr كه فقط در هنگام كم بودن سطح كلسيم فعال ميشود، تنها پلاسميدي است كه علاوه بر يرسينيا پستيس در ساير گونههاي يرسينيا نيز يافت ميگردد.
پلاسميد Lcr، يك پلاسميد با وزن مولکولی kb 70 است كه گروهي از پروتئینهای غشا خارجي يرسينيا[8] (YOPs) را كد میکند.EYop ، YopK، YopM ,YopL در رشد سريع يرسينيا در بافت نقش دارند و YopN سنسور حرارتي است. YopM از نظر ايمونولوژيكي شبيه آنتیژن پلاكتي GPIba است و از تجمع پلاكت جلوگيري ميكند. ظاهراًYopK و YopL با پيشرفت CMIR نسبت به يرسينيا پستيس تداخل كنند. YOPH يك پروتئين تيروزينكيناز[9] است كه يرسينيا را از فاگوسيته شدن توسط لكوسيتها حفظ ميكند. بنظر میرسد كه يرسينياها كپيهاي بسياري از Yopها را ترشح ميكنند كه عمدتاً اثر اولیهشان در ناحيهاي دور از باكتري است.
پلاسميد Lcr ژنی با اندازه 70 کیلو جفت باز را کد میکند که آنتیژنهای Vو W را بیان میكند. V يك مونومر با وزن مولکولی 38 کیلودالتون است كه تمايل به تجمع دارد و W پروتئين 40 کیلودالتوني است. بنظر میرسد كه V و W بهصورت كمپلكس با پروتئين چاپرون GroEL ترشح ميشوند. در موارد متعددي گزارش شده است كه V و W داراي خاصيت سرکوبکننده ايمني، ضد فاگوسيتي و آنتیژن محافظتکننده بوده و داراي پروموتورهاي وابسته به مقدار +Ca2 هستند.
در غلظت بالاتر از +mmol2/5 Ca2 و دماي 37 درجه سلسیوس، يرسينيا بهسرعت تكثير يافته و فاقد V و W است. در غلظت زير +mmol2/5 Ca2، مثل آنچه در سلول ميزبان رخ میدهد، يرسينيا از تكثير باز ايستاده و شارژ انرژي آدنيلات متوقف و توليد محصولات پلاسميد Lcr (يعني V و W و Yop) به بيشترين ميزان خود میرسد.
(ج) فاكتورهايي كه بر روي پلاسميد اگزوتوكسين (Tox) كد ميشوند. پلاسميد Tox، يك پلاسميد با وزن مولکولی kb100 است كه خصوصيات آن بهطور واضح مشخص نيست. بنظر میرسد كه مهمترين محصولات آن، كپسول يرسينيا پستيس و اگزوتوكسين موشی[10] يرسينيا پستيس است.
كپسول كه فراكشن[11]1 (F1) نامیده میشود توسط یک پلاسمید بنامpFra/pMT کد میگردد که يك كپسول گليكوپروتئين ضدفاگوسيتي است كه در حرارت پايين توليد نمیشود و در 37 درجه سلسیوس بیان میگردد. همچنین روی این پلاسمید ژن کدکننده فسفولیپاز D هم وجود دارد که برای بقای باکتری در پیشمعده کک لازم است.
اگر اگزوتوكسيني كه اگزوتوكسين موشی ناميده ميشود به موش تزريق شود، سريعاً سبب مرگ حيوان ميگردد. گزارش شده است كه اگزوتوكسين موشی با شكستن NAD به ADP -ريبوز و نيكوتين آميد سبب مصرف NAD ميشود. همچنین گزارش شده است كه این سم سبب بلوكه شدن بتا رسپتورهاي كاتكولامينها ميگردد و بنظر میرسد كه با توانايي تنظيم حرارت بدن توسط سيستم اعصاب سمپاتيك تداخل كرده و سبب ميشود بيمار تا سرحد مرگ احساس سرما كند.
(د) محصولات كروموزومي. تعداد زيادي از محصولات كروموزومي در بیماریزایی شركت دارند. ليپوپليساكاريد يرسينيا مشابه ساير انتروباكترياسه بوده و داراي فعاليت اندوتوكسيك است. پپتيد پيگمانتاسيون[12]F پروتئين ذخیرهكننده هِمين است كه به يرسينيا پستيس اجازة كسب آهن را میدهد. پروتئینهای Inv و Ail موادي هستند كه تهاجم يرسينيائه به فاگوسيتکنندههای غيرتخصصي (سلولهايي بهجز لكوسيت) را امکانپذیر ميسازند. آنتيژن pH6، كه آنتيژن 4 نيز ناميده میشود، پروتئين رشتهاي[13] است كه تشكيل يك لايه فيمبريه چسبنده در سطح يرسينيا را میدهد. آنتيژن 5 كاتالاز است كه بقای يرسينيا درون فاكوئلهاي فاگوسيتيك را امكانپذير ميسازد.
(2) چرخة عفونت يرسينيا:
يرسينيا پستيس پاتوژن داخل سلولي اختياري است كه درون ماكروفاژها و نوتروفيل زنده ميماند، اما در فضاي خارج سلولي بهتر تكثير ميكند. در حقيقت، عدهاي از محققين عقيده دارند كه به يرسينيا بايد به چشم يك باكتري خارج سلولي نگاه كرد كه توانايي تهاجم به سلول ميزبان را دارد. يرسينيائه با سه محيط متفاوت مواجه ميشوند: مجاري دستگاه گوارش كك، درون سلول ميزبان پستاندار، بافت و خون ميزبان پستاندار.
درون بدن كك بيشتر فاكتورهاي بیماریزای يرسينيا بيان نميشود، زيرا دما پايين است و +Ca2 در اين محيط وجود ندارد. فعاليت كوآگولازي يرسينيا خون را منعقد كرده و سبب انسداد معده كك ميگردد. در نتيجه وقتي كك ميزبان جديدي را نيش ميزند، يرسينيا را به محل گزش منتقل ميكند. از آنجايي كه يرسينيايي كه وارد بدن ميزبان شده فاقد Fx1، V و W و ساير شاخصهاي كليدي بیماریزایی است توسط ماكروفاژها فاگوسيته ميگردد.
در دماي 37 درجه سلسیوس و ميزان كم كلسيم درون ماكروفاژها، يرسينياها از تكثير باز میایستند، اما به سنتز محصولات پلاسميد Lcr ادامه میدهند. ماكروفاژها كشته ميشوند و يرسينياي كاملاً بیماریزا به جريان خون رها ميشود. حال اين يرسينيا نسبت به فاگوسيتوز مقاومت ميكند، سريعاً در بافتها و خون تكثير مييابد، به فاگوسيت کنندههای غيرتخصصي حمله ميكند و توكسينهايي توليد كرده و بافت ميزبان را تخريب مينمايد.
فعالكنندههاي پلاسمينوژن سبب تقويت انتشار يرسينيا در سراسر بدن ميشوند. سپسيس و انعقاد داخل عروقي منتشر[14] (DIC) در انگشتان دست و پا و گوشها سبب نكروز و سياه شدن–نشانه كلاسيك مرگ سياه– ميشود. انتشار ارگانيسمها به ريه سبب پنوموني بدخيم ميگردد. طاعون سپتيسميك توسط كك انساني پولكس ايريتانس[15] از انسان به انسان قابل انتقال است. فرم پنوموني طاعون، از طريق ذرات آئروسل عفوني قابل انتقال است.
تظاهر بالینی
طاعون سه تظاهر باليني عمده دارد كه بهصورت طاعون خياركي[16]، طاعون سپتيسميك و طاعون ريوي شناخته میشوند.
(الف) طاعون خياركي. با علائم سهگانه تب بالا، تورم خياركي (لنفاوي) و کونژنکتیویت بايد قوياً به طاعون خياركي مشكوك شد. از 2 تا 6 روز بعد از گزش كك آلوده، در محل گزش يك زخم وزيکولی ايجاد ميگردد. قبل از ظهور تورم غدد لنفاوي خياركي، بيشتر بيماران علائم سيستميك نظير تب، لرز، گيجي، بيحالي، تهوع و درد در پشت و پاها را نشان میدهند. يرسينيا سريعاً به غدد لنفاوي انتشار يافته و سبب تورم و بزرگي آنها (خيارك) ميگردد. پرخون شدن عروق خوني در چشم سبب کونژنکتیویت ميگردد. بيشتر خياركها در كشاله ران و بعضي در زير بغل و گردن هستند. حضور بيش از يك خيارك غيرمعمول است. پوست اطراف خيارك قرمز شده و ممكن است زخم شود. در اين هنگام، كشت خون حضور يرسينيا را نشان میدهد. اگر درمان شروع نشود، باكتريمي منجر به سپسيس سراسري، پنوموني هموراژيك يا مننژيت ميگردد.
(ب) طاعون سپتيسميك. اگرچه طاعون سپتيسميك معمولاً در اثر انتشار طاعون خياركي روي میدهد، اما حدود 20 درصد از موارد طاعون در ایالات متحده آمريكا بدون تظاهرات خياركي و با سپتيسمي آغاز ميگردد. اين شكل از بيماري كه بهراحتی از طريق ککها به سايرين قابل انتقال است، سبب بيماري بدخيم برقآسايي ميشود كه با DIC و كولاپس عروق همراه است.
(ج) طاعون ريوي. مبتلايان به طاعون ريوي دچار پنوموني تنفسي و اختلالات تنفسياند. در بعضي بيماران، اين شكل از طاعون متعاقب پيشرفت شكل سپتيسميك طاعون حاصل ميشود. در سايرين، عفونت يرسينيا بهصورت طاعون ريوي آغاز شده و در اثر تنفس آئروسلهای آلوده به طاعون بیمار ديگري است. طاعوني كه از طريق تنفسي حاصل شده است، 2 تا 3 روز قبل از ظهور علائم دوره كمون دارد. زمان متوسط بين بروز علائم و مرگومیر در اين طاعون 2 روز است و حتي بسياري 24 ساعت بعد از اولين علائم میمیرند.
تشخيص آزمایشگاهی
در بیماران تبدار در مناطق آندمیک که در تماس با جوندگان بودهاند، تشخیص سریع و تأیید آزمایشگاهی بیماری اهمیت زیادی در شروع درمان و حفظ جان فرد دارد. باسیل یرسینیا پستیس در طاعون خیارکی از چرک غدد متورم لنفاوی، در طاعون ریوی از خلط و در طاعون سپتیسمیک از خون ایزوله میگردند. باید دقت شود که مواد حاوی این باکتری در هوا منتشر نشود زیرا بهشدت آلودهکننده بوده و سبب عفونت ریوی میگردد. زمانی که مننژیت رخ میدهد، مایع مغزی و نخاعی و سرم، نمونه مناسب برای تشخیص است. سرم فاز حاد و مزمن برای ارزیابی سطح آنتیبادی میتواند استفاده گردد.
آزمایش مستقیم:
نكته مهم: به خاطر بسيار مسري بودن يرسينيا پستيس، پرسنل آزمايشگاه در مواردي كه نمونههاي كلينيكي مشكوك به طاعون هستند بايد نكات ايمني را رعايت نمايند.
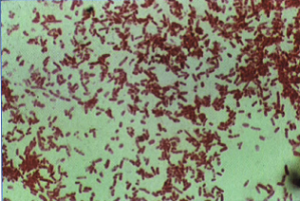
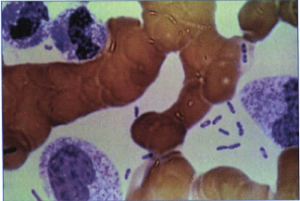
پس از تهیه گسترش از چرک خیارک، خلط، گوارش و دیگر اندامهای آلوده با رنگآمیزی به روش گیمسا و یا به روش ایمونوفلوئورسانس اختصاصی (هدف آنتیژن جز F1 است) بررسی میشود. در رنگآمیزی رایت، گیمسا و وایسون باکتری بهصورت دوقطبی (Bipolar appearance) یا بهصورت سنــجاق قفلی (Safety pin shape) مشاهده میگردد (شکل 2 و 3). در این رنگآمیزیها بهآسانی میتوان باکتری یرسینیا را از روی شکل (گرم منفی و کلفت بودن و بهتر رنگ گرفتن انتهای آنها) تشخیص داد. لازم به ذکر است که بایستي برای جلوگیری از اشتباه با دیگر باکتریها از کشت و تستهای بیوشیمیایی برای تشخیص قطعی استفاده نمود (جدول 1). یرسینیا پستیس غیرمتحرک، کاتالاز مثبت، اکسیداز، اندول، لاکتوز و اورهآز منفی است.
شکل 2: اسمیر رنگآمیزیشده به روش گرم (رنگآمیزي دوقطبی)
شکل 3: اسمیر خون رنگآمیزیشده به روش رایت (بهظاهر سنجاق قفلی دقت شود)
کشت:
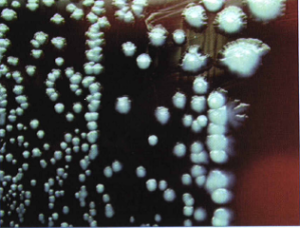
نمونههای برداشتشده را در محیط بلاد آگار، شکلات آگار، مککانکی آگار، آبگوشت براث و BHI براث کشت داده و پس از انکوباسیون 48 ساعته در حرارت 30-28 درجه سلسیوس به بررسی مشخصات کلنی و خصوصیات بیوشیمیایی آن میپردازند. نتیجه کشت خون پس از 24 ساعت قابل بررسی است. با توجه به اینکه این باکتری لاکتوز منفی است روی محیط مککانکی پس از انکوباسیون در 25 درجه کلنیهای سفیدی ایجاد میکند. این باکتری در زیر میکروسکوپ دارای ظاهری شبیه مس چکشخورده است نتیجه کشت مثبت باید توسط روش ایمنوفلورسانس و لیز توسط فاژ که در آزمایشگاههای مرجع انجام میشود، تأیید گردد.
شکل 4: نمای کلنیهای یرسینیا پستیس روی بلادآگار بعد از 24 ساعت
تلقیح به حیوان حساس:
از کشت خالص باکتری به زیر پوست و داخل صفاق موش سفید آزمایشگاهی و یا خوکچه هندی تلقیح میگردد و سپس آسیبهای ایجادشده مورد بررسی و مشاهده قرار میگیرد. چنانچه مقدار کمی از نمونه بر روی پوست مالش داده شود، فقط باسیل طاعون میتواند از پوست عبور نموده و حیوان را مبتلا نماید.
تست وارنر (test Warner):
برای تشخیص بیماری طاعون از لاشه حیوانات و حتی از مواد گندیده آنها میتوان استفاده نمود. قسمت کمی از اجزای لاشه حیوان را در سرم فیزیولوژی حل نموده و پس از جوشاندن، آن را صاف نموده و مقدار کمی از آن را در لوله باریکی ریخته و بر روی آن سرم ضد طاعون میریزند. چنانچه لاشه حاوی باسیل طاعون باشد، در فصل برخورد آنتیژن با آنتیبادی صفحه سفید رنگی حاصل میگردد که نشانه مثبت بودن تست وارنر است.
تستهاي سرولوژی:
در بیمارانی که سابقه واکسیناسیون قبلی نداشتهاند، اندازهگیری تیتر آنتیبادی با میزان 1:16 و بالاتر دلیل احتمالی بر عفونت یرسینیا پستیس است. افزایش تیتر سرمی در دو نمونه مجزا با فاصله زمانی یک یا دو هفته ناشی از ابتلا است. در آزمایشگاههای رفرانس براي تشخيص اوليه يرسينيا پستيس از تستهاي آنتيبادي فلورسنت استفاده ميگردد.
جدول 1: واکنشهای بیوشیمیایی گونههای مختلف جنس یرسینیا
درمان و پیشگیری:
هرچه زودتر درمان آنتیبیوتیکی بايد آغاز شود يعني حداكثر 12 تا 15 ساعت بعد از آغاز علائم طاعون. استرپتومايسين يا جنتامايسين داروي انتخابي است اما بيماران با كلرامفنيكل يا تتراسايكلين نيز درمان ميشوند. داكسيسايكلين و سیپروفلوکسازین داروهای جایگزین میتوانند مدنظر باشند. آمپيسيلين توصيه نميشود، زيرا اين آنتیبیوتیک اثر يكنواختي ندارد. مقاومت دارویی بندرت در یرسینیا پستیس رخ میدهد. به دليل همراهي طاعون با DIC، مراقبتهاي ويژه لازم است.
در بعضي بيماران در طي درمان آنتيبيوتيكي واكنش شديد و گذرايي به نام واكنش جاريس- هرگزهايمر[17] رخ میدهد كه بهنظر میرسد به دليل كشته شدن سريع تعداد زيادي از باكتريها و رها شدن مواد توكسيك داخل سلولی در طي ليز باكتري باشد. بعضي پزشكان براي جلوگيري از اين واكنش كورتيكواستروئيد را همزمان تجويز ميكنند.
طاعون خياركي در صورت عدم درمان آنتیبیوتیکی 50 تا 80 درصد و در صورت درمان 18 تا 19 درصد منجر به مرگ ميشود. تمام بيماران مبتلا به طاعون سپتيسميك و ريوي در صورت عدم درمان بهموقع و مراقبت ويژه خواهند مرد.
بيماران مبتلا به طاعون در سراسر جهان بايد قرنطينه مطلق شوند. كساني كه با بيماران تماس دارند میتوانند از تتراسايكلين جهت پيشگيري استفاده كنند. واكسن غيرفعالي كه حاوي Fx1 فرمالينهشده است به تمام سربازان آمريكايي تزريق ميشود. اگرچه واكسن گاهي سبب تب موقت و تهوع ميشود اما به مسافران مناطق اندميك طاعون نيز توصيه ميگردد. واكسن براي حدود 90 درصد از موارد پيشگيري طاعون خياركي مؤثر است، اما تأثیر آن در مورد طاعون ريوي مشخص نيست. بوستر واكسن[18] طاعون بطورسالانه تجویز میشود.
در مورد سایر یرسینیاها در مقاله قبلی با عنوان مروری تازه بر باسیلهای گرم منفی (یرسینیا، کامپیلوباکتر و هلیکوباکتر- قسمت ششم) بحث شده است که خوانندگان محترم را به آن مقاله ارجاع میدهم.
[1]– Ring Around a Rosie
[2] -The Masque of the Red Death
[3]– Sylvatic plague
[4] – Urban plague
[5] -Pesticin
[6]-Bacteriocinlike protein
[7] -Plasminogen activator
[8] -Yersinis outer membrane proteins
[9]– Tyrosine kinase
[10]– Murine exotoxin
[11] -Fraction 1
[12] -Pigmentation peptide F
[13] -Fibrilar protein
[14]– Disseminated intravascular coagulation
[15]– Pulex irritans
[16] – Bubonic plague
[17] – Jarisch-Herxheimer
[18]– Booster injection
https://en.wikipedia.org/wiki/Plague_(disease)
برای دانلود فایل pdf بر روی لینک زیر کلیک کنید
ورود / ثبت نام